溶液表面吸附量的测定PPT课件
- 格式:ppt
- 大小:573.00 KB
- 文档页数:7

溶液表面吸附量的测定(3学时)一、目的要求1、了解溶液表面吸附量的物理意义及其测定原理。
2、了解最大气泡法测定溶液表面张力的基本原理和方法。
3、了解弯曲液面的附加压力与液面弯曲度、溶液表面张力之间的关系。
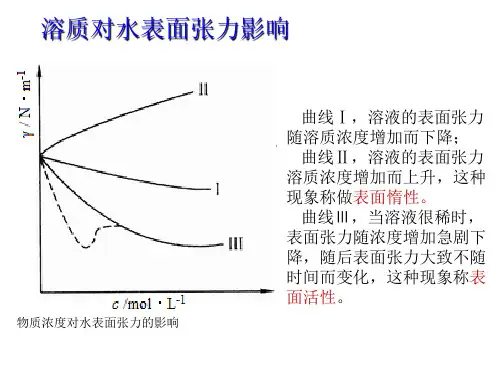
二、实验原理当一种溶质溶于水形成溶液时,溶质在溶液表面的浓度与其在溶液本体中的浓度存在着差别,这种现象称为溶液的表面吸附。
理论上,可用“表面吸附量”(或称表面超量)表示溶液的表面吸附程度大小,表面吸附量的物理化学意义是指溶质在溶液表面处的浓度与其在溶液本体中浓度的差值,通常用符号表示,其SI 单位为mol.m -2。
Γ在恒温、恒压条件下,表面吸附量(mol m -2)、溶液中溶质的活度和溶液表面张力Γa 三者之间的关系可用式(8.1)中的Gibbs 等温式进行描述:()1N m γ−(8.1)a d RT da γΓ=−在浓度不太大时,可以采用浓度代替活度,因此Gibbs 等温式可写成:()1mol L c −a (8.2)c d RT dc γΓ=−可见,只要通过实验测得溶液的表面张力与溶质浓度的关系曲线,即可利用公式γc (8.2)计算得到某一个浓度条件下的表面吸附量。
c Γ例如,图8.1为溶液表面张力随溶质浓度的变化曲线,若要求溶质浓度为时溶液的表1c 面吸附量,可在浓度轴上点作浓度轴的垂线,该垂线与关系曲线相交于A 点,1Γ1c ~c γ则曲线在A 点处切线AB 的斜率即为,由图8.1可知,AD 为纵轴的垂线,则有d dc γ。
又因为,则得到,代入到式(8.2)中即可DB AD d dc γ=1AD c =()1DB c d dc γ=求出浓度为时溶液的表面吸附量。
1c对于溶液表面吸附,可以采用Langmuir 理想吸附模型描述表面吸附量与溶液浓度Γc 之间的关系,即:(8.3)1kc kc θ∞Γ==Γ+γBD 1图8.1表面张力随浓度的变化关系曲线式(8.3)中,为溶质分子对溶液表面的覆盖百分率;为溶液的最大吸附量,对于θ∞Γ给定的体系,一定条件下是常数;为吸附常数∞Γk 可以将式(8.3)重排为直线形式:(8.4)1c c k ∞∞=+ΓΓΓ以对作图可得到一条直线,根据直线的截距和斜率可以求得最大吸c Γc 1k ∞Γ1∞Γ附量和吸附常数。

溶液表面吸附量的测定(3学时)一、目的要求1、了解溶液表面吸附量的物理意义及其测定原理。
2、了解最大气泡法测定溶液表面张力的基本原理和方法。
3、了解弯曲液面的附加压力与液面弯曲度、溶液表面张力之间的关系。
二、实验原理当一种溶质溶于水形成溶液时,溶质在溶液表面的浓度与其在溶液本体中的浓度存在着差别,这种现象称为溶液的表面吸附。
理论上,可用“表面吸附量”(或称表面超量)表示溶液的表面吸附程度大小,表面吸附量的物理化学意义是指溶质在溶液表面处的浓度与其在溶液本体中浓度的差值,通常用符号表示,其SI 单位为mol.m -2。
Γ在恒温、恒压条件下,表面吸附量(mol m -2)、溶液中溶质的活度和溶液表面张力Γa 三者之间的关系可用式(8.1)中的Gibbs 等温式进行描述:()1N m γ−(8.1)a d RT da γΓ=−在浓度不太大时,可以采用浓度代替活度,因此Gibbs 等温式可写成:()1mol L c −a (8.2)c d RT dc γΓ=−可见,只要通过实验测得溶液的表面张力与溶质浓度的关系曲线,即可利用公式γc (8.2)计算得到某一个浓度条件下的表面吸附量。
c Γ例如,图8.1为溶液表面张力随溶质浓度的变化曲线,若要求溶质浓度为时溶液的表1c 面吸附量,可在浓度轴上点作浓度轴的垂线,该垂线与关系曲线相交于A 点,1Γ1c ~c γ则曲线在A 点处切线AB 的斜率即为,由图8.1可知,AD 为纵轴的垂线,则有d dc γ。
又因为,则得到,代入到式(8.2)中即可DB AD d dc γ=1AD c =()1DB c d dc γ=求出浓度为时溶液的表面吸附量。
1c对于溶液表面吸附,可以采用Langmuir 理想吸附模型描述表面吸附量与溶液浓度Γc 之间的关系,即:(8.3)1kc kc θ∞Γ==Γ+γBD 1图8.1表面张力随浓度的变化关系曲线式(8.3)中,为溶质分子对溶液表面的覆盖百分率;为溶液的最大吸附量,对于θ∞Γ给定的体系,一定条件下是常数;为吸附常数∞Γk 可以将式(8.3)重排为直线形式:(8.4)1c c k ∞∞=+ΓΓΓ以对作图可得到一条直线,根据直线的截距和斜率可以求得最大吸c Γc 1k ∞Γ1∞Γ附量和吸附常数。

溶液表面吸附的测定一、实验目的1、采用最大泡压法测定不同浓度的乙醇水溶液的表面张力2、根据吉布斯吸附公式计算溶液表面的吸附量和乙醇分子的横截面积二、实验原理1、表面自由能 从热力学观点看,液体表面缩小是一个自发过程,这是使体系总的自由能减小的过程。
如欲使液体产生新的表面△A ,则需要对其作功。
功的大小应与△A 成正比:A W ∆=σ-式中σ为液体的表面自由能,亦称表面张力。
它表示了液体表面自动缩小趋势的大小,其量值与液体的成分、溶质的浓度、温度及表面气氛等因素有关。
2、溶液的表面吸附 纯物质表面层的组成与内部的组成相同,因此纯液体降低表面自由能的唯一途径是尽可能缩小其表面积。
对于溶液,由于溶质能使溶剂表面张力发生变化,因此可以调节溶质在表面层的浓度来降低表面自由能。
根据能量最低原则,溶质能降低溶剂的表面张力时,表面层溶质的浓度比溶液内部大;反之,溶质使溶剂的表面张力升高时,表面层中的浓度比内部的浓度低。
这种表面浓度与溶液内部浓度不同的现象叫做溶液的表面吸附。
显然,在指定的温度和压力下,溶质的吸附量与溶液的表面张力及溶液的浓度有关,从热力学方法可知它们之间的关系遵守吉布斯(Gibbs)吸附方程:Tdc dσRTc-Γ⎪⎪⎭⎫ ⎝⎛= 式中:Γ为表面吸附量(单位:mol·m -2);T 为热力学温度(单位:K);c 为稀溶液浓度(单位:mol·dm -3);R 为气体常数。
T dc dσ⎪⎪⎭⎫ ⎝⎛<0,则Γ>0,称为正吸附;Tdc dσ⎪⎪⎭⎫⎝⎛>0,则Γ<0,称为负吸附。
以表面张力对浓度作图,即得到c -σ曲线,在c -σ曲线上任选一点作切线,如图12.1所示,即可得该点所对应浓度c i 的斜率:()T i c d /d σ,图12.1 表面张力与浓度的关系其中: ()T i i c c MN d /d σ-= 则: RT MN /=Γ,根据此式可求得不同浓度下各个溶液的Γ值。



实验十九表面吸附量的测定预习题1 •为什么表面活性物质水溶液的表面张力随溶液浓度的变化而变化?2 •用气泡最大压力法测表面张力时,为什么气泡必须均匀缓慢冒出?3 •为什么毛细管端要刚好与液面接触?若毛细管端浸入溶液,则使最大压力差变大还使变小? 为什么?4 •毛细管常数如何测定?5 •表面吸附量r的物理意义是什么?6 .浓度为4.00 TO-4 mol L・-1时的溶液表面吸附量如何得到?此表面吸附量的单位是什么?7 •分析影响本实验结果的因素有哪些?一.实验目的1 •用气泡最大压力法测定十六烷基三甲基溴化铵水溶液的表面张力。
从而计算溶液在某一浓度时表面吸附量r2 •熟悉斜管压力计的使用方法。
二•实验原理1 •在指定的温度下,纯液体的表面张力是一定的,一旦在液体中加入溶质成溶液时情况就不同了,溶液的表面张力不仅与温度有关,而且也与溶质的种类,溶液浓度有关。
这是由于溶液中部分分子进入到溶液表面,使表面层的分子组成也发生了改变,分子间引力起了变化,因此表面张力也随着改变,根据实验结果,加入溶质以后在表面张力发生改变的同时还发现溶液表面层的浓度与内部浓度有所差别,有些溶液表面层浓度大于溶液内部浓度,有些恰恰相反,这种现象称为溶液的表面吸附作用。
根据吉布斯吸附等温式一如一1代(1)RTdc 2.303RT d lg c式中,r代表溶液浓度为c时的表面上溶质的吸附量(mol m-2), c代表平衡时溶液浓度(mol L-1), R为理想气体常数(8.314 J mol-1 K-1) , T为吸附时的温度(K)。
从(1)式可看出,在一定温度时,溶液表面吸附量与平衡时溶液浓度c和表面张力随浓度变化d -率——成正比关系。
dcd -当0时,r> 0表示溶液表面张力随浓度增加而降低,则溶液表面发生正吸附,此时溶液dc表面层浓度大于溶液内部浓度。
d :二当0时,r < 0表示溶液表面张力随浓度增加而增加,则溶液表面发生正吸附,此时溶dc液表面层浓度小于溶液内部浓度。

北京理工大学物理化学实验报告溶液表面吸附的测量班级:09111101实验日期:2013-6-4一、实验目的1、掌握最大气泡压力法测定溶液表面张力的原理和方法。
2、根据吉布斯(Gibbs )吸附方程式,计算溶质(乙醇)在单位溶液表面的吸附量Γ,并作Γ 图。
二、实验原理在定温下,纯物质液体的表面层与本体(内部)组成相同,根据能量最低原理,为降低体系的表面吉布斯自由能,将尽可能地收缩液体表面。
对溶液则不同,加入溶质后,溶剂表面张力发生变化。
根据能量最低原理,若溶质降低溶剂表面张力,c (表面层)> c (本体);反之,若溶质升高表面张力,c (表面层)<c (本体)。
溶质在溶液表面层与在溶液本体中浓度不同的现象称为溶液的表面吸附,即溶液借助于表面吸附来降低表面吉布斯自由能。
溶液表面吸附溶质的量Γ与表面张力σ、浓度c 有关,其关系符合Gibbs 吸附方程T cRT c )(∂∂-=Γσ① 式中:Γ吸附量;c 溶液浓度;T 温度;R 气体常数;σ表面张力或表面吉布斯自由能。
T c)(∂∂σ表示在一定温度下,表面张力随浓度的变化率。
Γ>0,称为正吸附。
Γ<0,称为负吸附。
在一定温度下,测定不同浓度溶液的表面张力σ,以σ对c 作图,求不同浓度时的T c)(∂∂σ值。
由Gibbs 吸附方程求各浓度下的吸附量Γ。
本实验采用最大气泡压力法测定液体表面张力。
将待测液体装入表面张力仪中,使玻璃毛细管下端与液面相切,若液体能润湿管壁,则液体沿毛细管上升形成凹液面,其液面所受压力P '为大气压力P 0和附加压力ΔP 。
根据拉普拉斯(Laplace )方程:rP σ2=∆ ②式中:r 为弯曲液面曲率半径;σ为液体与气体表面(界面)张力。
因是凹液面,弯曲液面的曲率半径 ,Δ (指向大气)。
图1 实验装置示意图当打开漏斗的活塞,让水缓慢滴入下面密封的加压瓶中,当此压力差在毛细管上面产生的作用稍大于毛细管口液体的表面张力所能产生的最大作用时,气泡就从毛细管口逸出。