电子转移的表示方法
- 格式:ppt
- 大小:127.00 KB
- 文档页数:11




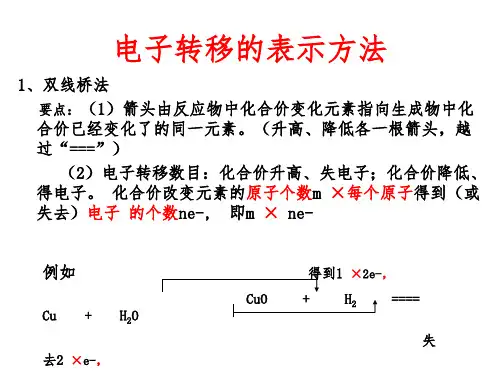
电子转移的表示方法1.双线桥法(1)表示方法写出Cu与稀硝酸反应的化学方程式并用双线桥标出电子转移的方向和数目:(2)注意事项①箭头指向反应前后有元素化合价变化的同种元素的原子,且需注明“得到”或“失去”。
②箭头的方向不代表电子转移的方向,仅表示电子转移前后的变化。
③失去电子的总数等于得到电子的总数。
2.单线桥法(1)表示方法写出Cu与稀硝酸反应的化学方程式并用单线桥标出电子转移的方向和数目:(2)注意事项①箭头从失电子元素的原子指向得电子元素的原子。
②不标“得到”或“失去”,只标明电子转移的总数。
③线桥只出现在反应物中。
[细练过关]1.下列化学反应中电子转移方向、数目表示正确的是()A.B.C.D.解析:选D A项中转移电子数目错误,应为e-;B项中Zn失电子H得电子;C项中用单线桥表示电子转移时不标“得失”。
2.(1)用双线桥法表示下列反应的电子转移的方向和数目①3FeO+10HNO3===3Fe(NO3)3+NO↑+5H2O②3NF3+5H2O===2NO+HNO3+9HF③KClO3+6HCl(浓)===KCl+3Cl2↑+3H2O(2)用单线桥法表示下列反应的电子转移的方向和数目①CaH2+2H2O===Ca(OH)2+2H2↑②FeS2+8HNO3===Fe(NO3)3+2H2SO4+5NO↑+2H2O答案:(1)①②③(2)①②3.(1)对于反应:14CuSO 4+5FeS 2+12H 2O===7Cu 2S +5FeSO 4+12H 2SO 4,当有1 mol FeS 2发生反应,转移电子的物质的量为________。
(2)对于NaNO 2+NH 4Cl===NaCl +N 2↑+2H 2O 反应,生成0.5 mol N 2,转移电子物质的量为________。
解析:(1)根据反应当5 mol FeS 2反应时,CuSO 4→Cu 2S 时得14 mol e -,FeS 2→Cu 2S 时得7 mol e -,共得到21 mol e -,所以当有1 mol FeS 2反应时,转移4.2 mol e -。

第2课时氧化剂和还原剂核心微网络素养新要求1.学会电子转移的表示方法。
2.知道常见的氧化剂和还原剂。
3.能从化学反应中元素化合价的变化认识氧化剂和还原剂、氧化产物和还原产物。
学业基础——自学·思记·尝试一、电子转移的表示方法1.双线桥法表明反应前后同一元素原子的电子转移情况。
(1)双线桥法的基本步骤(2)一般模型(m×n=a×b)(3)注意事项①箭头、箭尾对应化合价变化的同种元素;②必须注明“得到”或“失去”;③还原剂失去的电子总数与氧化剂得到的电子总数相等。
2.单线桥法表明反应前后不同元素原子间的电子转移情况。
(1)单线桥法的基本步骤(2)一般模型(3)注意事项箭头已标明电子转移的方向,因此不需再标明“得到”或“失去”,只需标明电子转移的数目。
二、氧化剂和还原剂1.基本概念(1)氧化剂和还原剂氧化剂:在反应时,所含元素的化合价降低,即得到电子(或电子对偏向)的反应物。
还原剂:在反应时,所含元素的化合价升高,即失去电子(或电子对偏离)的反应物。
模型:(2)氧化产物和还原产物氧化产物:还原剂在反应中失去电子(或电子对偏离)后被氧化成的生成物。
还原产物:氧化剂在反应中得到电子(或电子对偏向)后被还原成的生成物。
(3)氧化性和还原性氧化性:物质得到电子的能力。
在氧化还原反应中,氧化剂具有氧化性,得到电子后,化合价降低,被还原。
还原性:物质失去电子的能力。
在氧化还原反应中,还原剂具有还原性,失去电子后,化合价升高,被氧化。
(4)氧化还原反应中基本概念之间的关系2.常见的氧化剂和还原剂3.氧化还原反应的应用(1)积极作用①汽车尾气的处理汽车尾气的主要成分是氮氧化物(NO、NO2)和碳氧化物(CO、CO2)。
在一定条件下,利用氧化还原反应原理,使NO x与CO发生反应,转化成无毒的N2和CO2,从而减少或消除汽车尾气对大气的污染。
2NO+2CO N2+2CO22NO2+4CO N2+4CO22NO x+2x CO N2+2x CO2②从矿石中冶炼金属。

反映氧化还原反应中电子转移情况有两种表示法:单线桥和双线桥。
(1)单线桥(也叫单箭号)意义:表示电子转移的方向和总数(或:表示不同元素原子或离子间电子得失情况).它体现了“谁给谁”.表示法:箭号一定在等式左边,箭头上只标明电子转移总数。
如:该表示法的特点是:箭头指向的物质为氧化剂。
(对于自身氧化还原反应,则箭头指向的元素起氧化作用)(2)双线桥(也叫双箭号)意义:表示同一元素原子或离子间电子得失情况(或:表示电子得与失及氧化、还原过程)。
它体现了“谁变谁”。
表示法:箭号一定横跨等式两边,且不少于两根箭号.在箭号上要标上“得到”或“失去”,也可以用“+”或“-”来表示,然后写出具体的电子数目.对于分子内的氧化还原反应,特别是歧化反应,使用单线桥不方便,用双线桥好.双线桥易画,但麻烦;单线桥简单,能看出氧化剂。
双线桥可用在氧化还原反应方程式配平上。
在考试评分中,回答表示氧化还原反应的电子转移方向和数目(或总数)时,使用任一种表示法都算正确。
其实,单线桥和双线桥并不以线桥的多少来划分,有两根或三根线桥的不一定是单线桥,但双线桥却不可能只有一根线桥.因此,要判断是哪种线桥,关键是看线桥是在等式的左边,还是横跨了等式的两边。
如:双线桥单线桥双线桥单线桥两种表示法也有多种形式,如硫铁矿燃烧的氧化还原反应方程式:以上分析可以看出,双线桥是分析法,可理解为是微观的;单线桥是综合法,可理解为宏观的。
要注意,以下容易标错的氧化还原反应方程式。
如铝与NaOH溶液反应,把NaOH当成氧化剂,且标示如下是错的:因为该化学方程式是总反应方程式,反应过程是铝先与水反应生成氢氧化铝和氢气,然后氢氧化铝和碱反应生成偏铝酸钠和水,前者是置换反应,水是氧化剂;后者是复分解反应,NaOH作为碱与酸反应,并不是氧化剂。
正确的应是如下表示法:又如浓硫酸与硫化氢反应,如下表示是错的:因为氧化还原反应是逐步氧化和逐步还原的,即-2价的S首先变成0价的S,再氧化才升高到+4价的S,直到氧化为+6价的S;同理,+6价的S首先被还原,变成+4价的S,再还原降到0价的S,直至还原到-2价的S.故应如下表示才正确:再如HCl和KClO3反应,如下表示也是错的:因为氧化还原反应有条规律是:只有同一种元素发生的氧化还原反应时,该元素的化合价变化是“只相撞,不相交”。

反映氧化还原反应中电子转移情况有两种表示法:单线桥和双线桥。
(1) 单线桥(也叫单箭号)意义:表示电子转移的方向和总数(或:表示不同元素原子或离子间电子得失情况)。
它体现了“谁给谁”。
表示法:箭号一定在等式左边,箭头上只标明电子转移总数。
如:该表示法的特点是:箭头指向的物质为氧化剂。
(对于自身氧化还原反应,则箭头指向的元素起氧化作用)(2) 双线桥(也叫双箭号)意义:表示同一元素原子或离子间电子得失情况(或:表示电子得与失及氧化、还原过程)。
它体现了“谁变谁”。
表示法:箭号一定横跨等式两边,且不少于两根箭号。
在箭号上要标上“得到”或“失去”,也可以用“+”或“-”来表示,然后写出具体的电子数目。
对于分子内的氧化还原反应,特别是歧化反应,使用单线桥不方便,用双线桥好。
双线桥易画,但麻烦;单线桥简单,能看出氧化剂。
双线桥可用在氧化还原反应方程式配平上。
在考试评分中,回答表示氧化还原反应的电子转移方向和数目(或总数)时,使用任一种表示法都算正确。
其实,单线桥和双线桥并不以线桥的多少来划分,有两根或三根线桥的不一定是单线桥,但双线桥却不可能只有一根线桥。
因此,要判断是哪种线桥,关键是看线桥是在等式的左边,还是横跨了等式的两边。
如:双线桥单线桥双线桥单线桥两种表示法也有多种形式,如硫铁矿燃烧的氧化还原反应方程式:以上分析可以看出,双线桥是分析法,可理解为是微观的;单线桥是综合法,可理解为宏观的。
要注意,以下容易标错的氧化还原反应方程式。
如铝与NaOH溶液反应,把NaOH当成氧化剂,且标示如下是错的:因为该化学方程式是总反应方程式,反应过程是铝先与水反应生成氢氧化铝和氢气,然后氢氧化铝和碱反应生成偏铝酸钠和水,前者是置换反应,水是氧化剂;后者是复分解反应,NaOH作为碱与酸反应,并不是氧化剂。
正确的应是如下表示法:又如浓硫酸与硫化氢反应,如下表示是错的:因为氧化还原反应是逐步氧化和逐步还原的,即-2价的S首先变成0价的S,再氧化才升高到+4价的S,直到氧化为+6价的S;同理,+6价的S首先被还原,变成+4价的S,再还原降到0价的S,直至还原到-2价的S。

氧化还原反应中电子转移数目的判断1.对于双箭桥表示法电子转移数表示为 :AxBe-形式。
其中A为反应前后化合价变化的原子个数;B=高价态-低价态,A=1 或B=1将1省略。
2.对于单箭桥表示法电子转移数表示为 Me 形式。
M=A×B,当 M=1 时,将1省略,A、B 的意义与双箭桥表示法中的相同。
3.电子守恒法配平原理:发生氧化还原反应时,还原剂失去电子、氧化剂得到电子.因为整个过程的本质好比是还原剂把电子给了氧化剂,在这一失一得之间,电子守恒.故根据还原剂失去电子的数目和氧化剂得到电子的数目相等,结合二者化合价的改变情况,可以分别把氧化剂、还原剂的计量数计算出来,这样整个氧化还原反应就顺利配平了.方法和步骤:①标出发生变化的元素的化合价,并确定氧化还原反应的配平方向.在配平时,需要确定先写方程式那边物质的计量数.有时先写出方程式左边反应物的计量数,有时先写出方程式右边生成物的计量数.一般遵循这样的原则:自身氧化还原反应→先配平生成物的计量数;部分氧化还原反应→先配平生成物的计量数;一般的氧化还原反应→既可先配平生成物的计量数,也可先配平反应物的计量数.②列出化合价升降的变化情况.当升高或降低的元素不止一种时,需要根据不同元素的原子个数比,将化合价变化的数值进行叠加.③根据电子守恒配平化合价变化的物质的计量数.④根据质量守恒配平剩余物质的计量数.最终并根据质量守恒检查配平无误.4.待定系数法配平原理:质量守恒定律告诉我们,在发生化学反应时,反应体系的各个物质的每一种元素的原子在反应前后个数相等.通过设出未知数(如x、y、z等均大于零)把所有物质的计量数配平,再根据每一种元素的原子个数前后相等列出方程式,解方程式(组).计量数有相同的未知数,可以通过约分约掉.方法和步骤:对于氧化还原反应,先把元素化合价变化较多的物质的计量数用未知数表示出来,再利用质量守恒吧其他物质的计量数也配平出来,最终每一个物质的计量数都配平出来后,根据某些元素的守恒,列方程解答.。


氧化还原反应中电子转移的表示方法1 双线桥法表明反应前后同一元素原子或离子间的电子转移情况。
(1)双线桥法的基本步骤(2)一般模型如:2 单线桥法表明反应前后元素原子间的电子转移情况。
(1)单线桥法的基本步骤(2)一般模型如:辨析比较双线桥法与单线桥法的比较1.双线桥法的“线桥”从反应物到产物,单线桥法的“线桥”只连反应物。
2.表示氧化还原反应中电子转移、化合价升降、物质被氧化或被还原等关系时,用双线桥法较方便;表示电子转移的方向和数目时,用单线桥法较方便。
典例详析例3-16(四川成都七中期中)下列氧化还原反应方程式中所标电子转移方向与数目错误的是()A.B.C.D.解析◆A反应中,铁元素的化合价升高(0→+2),失去2e-;氢元素的化合价降低(+1→0),得到2×e-,电子转移方向和数目均符合反应事实,A项正确。
B反应中,氮元素的化合价升高(+2→+5),失去4×3e-;氧元素的化合价降低(0→-2),得到6×2e-,电子转移方向和数目均符合反应事实,B项正确。
C反应中,氯元素的化合价由Cl2中的0价变为反应后Ca(ClO)2中的+1价,化合价升高,失去2×e-;氯元素的化合价由Cl2中的0价变为反应后CaCl2中的-1价,化合价降低,得到2×e-,电子转移方向和数目均符合反应事实,C项正确。
D反应中,氯元素的化合价由HCl中的-1价变为反应后Cl2中的0价,化合价升高,失去5×e-;氯元素的化合价由KClO3中的+5价变为反应后Cl2中的0价,化合价降低,得到5e-,题目中电子转移数目不符合反应事实,D项错误。
答案◆D例3-17(河南中原名校期中联考)工业上常用氨气为原料制备硝酸,其中有一步非常重要的反应为4NH3+5O24NO+6H2O,该反应的氧化剂为________,还原剂为________。
用单线桥法表示该氧化还原反应中电子转移的方向和数目:________________。
重难点10 氧化还原反应电子转移的表示方法1.双线桥法(1)表示意义:表示反应前后同一元素原子间电子转移情况。
(2)基本步骤:(3)注意事项:①箭头、箭尾必须对应化合价变化的同种元素的原子;②必须注明“得”或“失”;③氧化剂和还原剂得、失电子总数要相等。
2.单线桥法(1)表示意义:表示反应前后不同元素原子间电子转移情况。
(2)基本步骤:(3)注意事项:①单线桥表示反应物中变价元素原子得失电子的情况;②不需标明“得”或“失”,只标明电子转移数目;③箭头标明电子转移的方向;④单线桥箭头从失电子的元素原子指向得电子的元素原子。
【特别提醒】电子转移表示方法的注意事项(1)氧化还原反应中转移电子总数是得到电子数或失去电子数,而不是二者的加和。
(2)双线桥法标电子转移时,电子转移数用a×b e-形式表示,a表示发生氧化或还原反应的原子个数,b表示每个原子得到或失去的电子数,当a或b等于1时,要省略。
★★★★【重难点考向一】双线桥分析氧化还原反应【例1】用双线桥分析下列氧化还原反应,并指出氧化剂还原剂.Cu+4HNO3(浓)═Cu(NO3)2+2NO2+2H2O【答案】;氧化剂HNO3;还原剂Cu【解析】反应方程式Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,中化合价变化为:Cu→Cu(NO3)2,Cu 元素由0价→+2价,一个Cu原子失2个电子,所以Cu是还原剂;HNO3→NO2,N元素由+5价→+4价,一个HNO3分子得一个电子,所以HNO3是氧化剂;其得失电子数为2,所以其转移电子数为2,即;【重难点考向二】单线桥分析氧化还原反应【例2】用单线桥法分析下列氧化还原反应,标出电子转移方向和数目。MnO2+4HCl(浓)=MnCl2+Cl2↑+2H2O【答案】【重难点考向三】氧化还原反应的分析【例3】下列化学反应中电子转移的表示方法正确的是( )【答案】 C【解析】A.Si元素化合价由+4价降低为0价,得到电子,C元素失去电子,化合价从0价升高为+2价,最小公倍数为4,转移电子为4e-,故A错误;B.H元素化合价由+1降低为0价,总共降低2价,得到2个电子,Na元素从0价升高为+1价,共失去2个电子,最小公倍数为2,转移电子为2e-,故B错误;C.I元素化合价由-1价升高为0价,失去电子,Mn元素化合价从+7价降低为+2价,得到电子,最小公倍数为10,转移电子10e-,故C正确;D.Cu元素化合价由0价升高为+2价,失去电子,S元素化合价由+6价降低为+4价,得到电子,最小公倍数为2,转移电子2e-,故D 错误;故选C。
化学反应中的电子转移反应电子转移反应是化学反应中常见的一种反应类型,它涉及到原子、离子或分子之间的电子的转移和重新组合。
这类反应在生活和工业中都具有重要的意义,如燃烧、氧化还原反应和电池等。
本文将介绍电子转移反应的基本概念、分类和实际应用。
一、电子转移反应的基本概念电子转移反应是指在化学反应中,电子从一个物质转移到另一个物质的过程。
在这类反应中,通常涉及到氧化剂和还原剂。
氧化剂是一种能够接受电子的物质,它在反应中发生还原;而还原剂是一种能够提供电子的物质,它在反应中发生氧化。
电子转移反应可以通过化学方程式表示,例如:A +B → A+ + B-在上述方程式中,A失去一个电子成为A+(氧化),而B获得该电子成为B-(还原)。
这种电子转移反应也被称为氧化还原反应。
二、电子转移反应的分类根据电子转移的方式,电子转移反应可以分为几个不同的类型。
其中最常见的是电子转移反应涉及到金属和非金属之间的电子转移。
1. 金属与非金属的电子转移反应金属通常具有较低的电离能和较高的电子亲和能,因此它们倾向于失去电子成为阳离子。
而非金属通常具有较高的电离能和较低的电子亲和能,因此它们倾向于获得电子成为阴离子。
例如,钠和氯可以发生电子转移反应形成氯化钠:Na + Cl → Na+ + Cl-在这个反应中,钠失去一个电子成为钠离子,氯获得该电子成为氯离子。
2. 氧化还原反应氧化还原反应是一种特殊的电子转移反应。
在这类反应中,氧化剂接受电子,而还原剂提供电子。
氧化还原反应在生活和工业中广泛应用,如燃烧反应、电池和腐蚀等。
三、电子转移反应的实际应用1. 燃烧反应燃烧是一种常见的电子转移反应,它涉及到氧化剂与可燃物质之间的反应。
在燃烧过程中,氧气作为氧化剂接受可燃物质释放出的电子,从而发生氧化反应。
燃烧反应广泛应用于发电、取暖和烹饪等领域。
2. 电化学反应电化学反应是建立在电子转移反应基础上的一类反应。
其中最常见的是电池反应,它涉及到在电解质溶液中发生的氧化还原反应。
氧化还原反应中电子转移的观念一、基本概念1.氧化还原反应:化学反应中,电子的转移导致物质氧化和还原的过程。
2.氧化:物质失去电子,氧化态增加,称为氧化反应。
3.还原:物质获得电子,还原态增加,称为还原反应。
4.电子转移:氧化剂接受电子,还原剂失去电子,实现电子的转移。
二、基本原理1.电子转移的方向:电子从还原剂转移到氧化剂。
2.电子转移的数目:根据反应物的氧化态变化确定。
3.电子转移的规律:遵循电荷守恒定律和质量守恒定律。
三、氧化还原反应的表示方法1.离子方程式:用离子的形式表示氧化还原反应。
2.半反应式:将氧化反应和还原反应分别表示为两个半反应式。
3.电池符号:用电池符号表示电子转移的过程。
四、氧化还原反应的分类1.单一置换反应:一个元素被另一个元素替换。
2.双重置换反应:两种元素互相替换。
3.合成反应:两种或多种物质生成一种新物质。
4.分解反应:一种物质分解为两种或多种物质。
五、氧化还原反应的应用1.电化学:电池、电镀、腐蚀等现象都与氧化还原反应有关。
2.化学反应:许多化学反应都涉及到电子的转移。
3.生物体内:生物体内的代谢过程涉及到氧化还原反应。
六、氧化还原反应的判断1.升降法:通过观察元素氧化态的变化判断氧化还原反应。
2.电荷法:通过观察反应物和产物电荷的变化判断氧化还原反应。
七、氧化还原反应的计算1.电子数的计算:根据氧化态变化计算电子的转移数目。
2.反应热的计算:根据反应物和产物的能量变化计算反应热。
八、实例分析1.钢铁生锈:铁的氧化反应,电子从铁转移到氧。
2.烧碱制氯气:氯的还原反应,电子从氢氧化钠转移到氯。
以上是关于氧化还原反应中电子转移观念的知识点介绍,希望对您有所帮助。
习题及方法:知识点:基本概念题目:下列哪个物质在反应中发生了氧化?A. Na2O + H2O → 2NaOHB. Fe + CuSO4 → FeSO4 + CuC. H2 + O2 → 2H2OD. Mg(OH)2 → MgO + H2O方法:观察每个反应中元素的氧化态变化。