器械临床试验受试者筛选入选表
- 格式:doc
- 大小:27.00 KB
- 文档页数:2

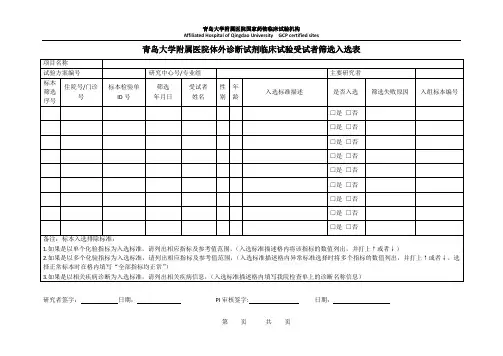
受试者筛选入选表
研究题目:
研究中心编号及名称:
●每个签署知情同意书的患者都需要登记;
●受试者编号为中心号2位+筛选顺序号3位,根据患者签署知情同意书的先后顺序,顺序号依次从小到大;
如01中心,受试者编号为01001 、01002、01003,依次往下;
●患者姓名缩写与CRF填写要求一致;四格需填满,两字姓名填写两字拼音前两个字母;三字姓名填写三字首字母及第三字第二字母;
四字姓名填写每一个字首字母;
举例:张红
李淑明
欧阳小惠
●;
●结束日期是指患者结束试验的日期。
若患者筛选失败,则结束日期为确定筛选失败的日期,并应在“筛选失败的原因”栏予以记录;
若患者完成整个试验,则结束日期为该患者完成试验的日期;若患者提前中止研究(无论是因为失访、不可耐受的不良事件、疗效不佳等任何原因),结束日期应为该患者中止研究的日期,并应在“脱落原因”栏予以记录
受试者筛选入选表
注:受试者编号格式:中心号(2位)+筛选顺序号(3位),例如:01001 ,入组日期请记录获取随机号日期。

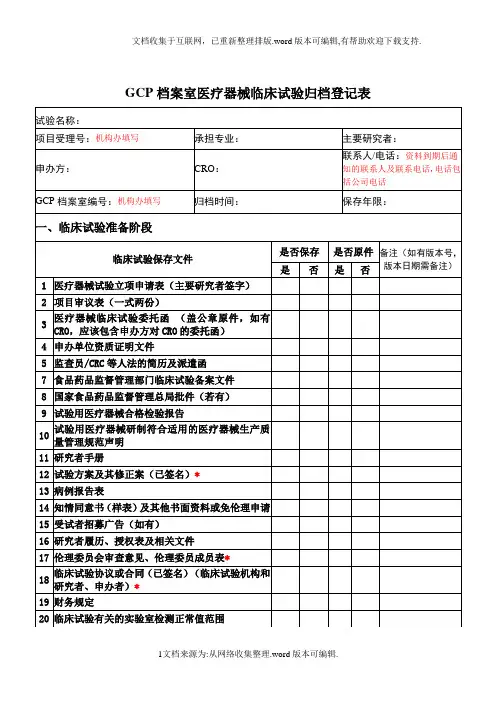
临床试验申请表306PLA-JG-T-001-01研究者履历表306PLA-JG-T-002-01项目名称: CFDA批件号:研究中心名称:研究中心代号:方案编号:参加负责项目分工:研究者声明临床试验协调会签到表306PLA-JG-T-003-01项目名称:申办单位:方案编号:_ _ 主要研究者:_ 会议时间:_ 年月日会议地点:临床试验协调会记录表306PLA-JG-T-004-01项目名称:申办单位:方案编号:_ _ 主要研究者:_ 会议时间:_ 年月日会议地点:日期:__________________ _ 主要研究者:临床试验提交伦理审议申请表306PLA-JG-T-005-01中国人民解放军第306医院国家药物临床试验机构管理文件临床试验启动会签到表306PLA-JG-T-006-01项目名称:方案编号:申办单位:_ _ 主要研究者:_ 会议时间:_ 年月日会议地点:中国人民解放军第306医院国家药物临床试验机构管理文件临床试验启动会记录表306PLA-JG-T-007-01项目名称:方案编号:申办单位:_ _ 主要研究者:_ 会议时间:_ 年月日会议地点:_________日期:主要研究者:_________ _中国人民解放军第306医院国家药物临床试验机构管理文件研究人员分工表306PLA-JG-T-008-01项目名称:方案编号:申办单位:专业科室:主要研究者:主要研究者签字:日期:中国人民解放军第306医院国家药物临床试验机构管理文件受试者筛选/入选表306PLA-JG-T-009-01页第页___共___中国人民解放军第306医院国家药物临床试验机构管理文件受试者签认代码表306PLA-JG-T-010-01 项目名称:方案编号:___第共页___页中国人民解放军第306医院国家药物临床试验机构管理文件严重不良事件报告表306PLA-JG-T-011-01项目名称:CFDA批件号:方案编号:中国人民解放军第306医院国家药物临床试验机构管理文件/ 报告者(研究医生)/报告日期:确认者(主要研究者/日期: /时间:/ / 发送者/日期者送是CFDA注册司否发伦理委员会申办至:□是□否□是□否□是□否中国人民解放军第306医院国家药物临床试验机构管理文件完成试验受试者编码目录306PLA-JG-T-012-01项目名称:方案编号:___第共页___页中国人民解放军第306医院国家药物临床试验机构管理文件临床试验总结会签到表306PLA-JG-T-013-01项目名称:申办单位:方案编号:_ _ 主要研究者:_ 会议时间:_ 年月日会议地点:中国人民解放军第306医院国家药物临床试验机构管理文件临床试验总结会记录表306PLA-JG-T-014-01项目名称:申办单位:方案编号:_ _ 主要研究者:_ 会议时间:_ 年月日会议地点:________日期:主要研究者:_________ _中国人民解放军第306医院国家药物临床试验机构管理文件临床试验用药物(物资)签收记录单306PLA-JG-T-015-01 项目名称: CFDA批件号:方案编号:研究中心名称:研究中心代号:发送单位名称:___第页___共页中国人民解放军第306医院国家药物临床试验机构管理文件试验用药物保存记录表306PLA-JG-T-016-01方案编号:项目名称:药物编号:药物名称:药物批号:药物规格:中国人民解放军第306医院国家药物临床试验机构管理文件试验用药物分发回收记录表306PLA-JG-T-017-01中国人民解放军第306医院国家药物临床试验机构管理文件临床试验剩余药物(物资)退回/销毁记录单306PLA-JG-T-018-01中国人民解放军第306医院国家药物临床试验机构管理文件文件接收、保管记录表306PLA-JG-T-019-01项目名称:方案编号:发送方:接收方:送交人:_________________ 日期:_________________注:本记录一式两份,本份由_____________(研究中心名称)保存。
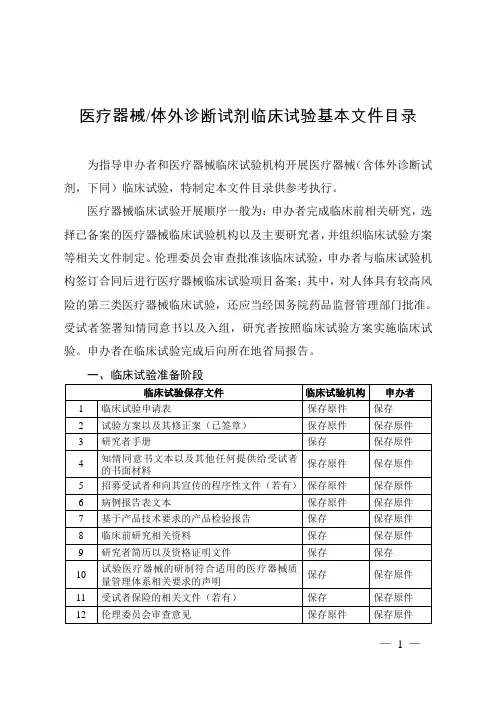
医疗器械/体外诊断试剂临床试验基本文件目录
为指导申办者和医疗器械临床试验机构开展医疗器械(含体外诊断试剂,下同)临床试验,特制定本文件目录供参考执行。
医疗器械临床试验开展顺序一般为:申办者完成临床前相关研究,选择已备案的医疗器械临床试验机构以及主要研究者,并组织临床试验方案等相关文件制定。
伦理委员会审查批准该临床试验,申办者与临床试验机构签订合同后进行医疗器械临床试验项目备案;其中,对人体具有较高风险的第三类医疗器械临床试验,还应当经国务院药品监督管理部门批准。
受试者签署知情同意书以及入组,研究者按照临床试验方案实施临床试验。
申办者在临床试验完成后向所在地省局报告。
一、临床试验准备阶段
—1 —
二、临床试验进行阶段
—2 —
三、临床试验完成或者终止后
—3 —。
受试者筛选、入选SOP
一、目的:建立受试者筛选、入选的操作规程,确保试验的顺利进行。
二、范围:适用于所有临床试验。
三、规程:
1.受试者是药物临床试验的客观对象,试验方案的设计应满足科学和伦理的要求,保护受试者权益。
2.根据药物临床试验方案的要求,从不同人群中(健康志愿者、门诊患者、住院患者等)招募受试者。
可以通过张贴招募广告、社区宣传、电视广播等方式招募受试者。
3.药物临床试验的研究人员在熟悉试验方案后,向受试者进行知情同意,待对方充分考虑、理解并充分咨询同意后,签署知情同意书。
知情同意的过程遵照受试者知情同意SOP。
4.受试者签署知情同意书后,按照各项药物临床试验的入组和排除标准对受试者进行筛选,并填写《受试者筛选与入选表》。
必须满足所有入选标准,并不能符合任一排除标准的受试者方可进入药物临床试验。
5.符合方案要求的受试者按照方案既定的标准随机分组,并进行相应的观察治疗。