金属材料的点腐蚀和缝隙腐蚀
- 格式:docx
- 大小:11.53 KB
- 文档页数:4

露点腐蚀、孔蚀(点蚀)、缝隙腐蚀:
1.露点腐蚀
广义地讲就是在工艺气体在降温过程达到相变点产生液态结露即露点。
反之,由液态升温达到汽化——沸腾就称为沸点。
二者温度是一样的,但是能温位水平就差个汽化潜热。
此时,介质中若存在一些酸性物质(如:
SOx,HCl,NOx等)就会在结露的水份
中富集形成酸。
比如最常见的露点腐蚀
产生于锅炉排放的烟气,主要酸性物质
为硫化物——硫酸,亚硫酸(当然也会
存在少量氯化物,氮化物),它的浓度可
高达85%,对金属特别是对不锈钢产生
强烈的腐蚀(有时甚至包括应力腐蚀)。
2.孔蚀(点蚀)和缝隙腐蚀
点蚀又称小孔腐蚀,是一种极端的局部腐蚀形态。
蚀点从金属表面发生后,向纵深发展的速度大于或等于横向发展的速度,腐蚀的结果是在金属上形成蚀点或小孔,而大部分金属则未受到腐蚀或仅是轻微腐蚀。
这种腐蚀形态称点蚀或小孔腐蚀。
孔
蚀(点蚀)的机理、缝隙腐蚀的机理实质上
是相同的,但是两者却是有区别的。
孔蚀不需要客观存在的缝隙,它可以
自发产生蚀孔。
一般来说在某些介质中,
易发生孔蚀的金属,也同样容易发生缝隙
腐蚀,但是发生缝隙腐蚀的体系(包括金属和介质)却并不一定产生孔蚀。
影响因素:(1)溶液的成分:大多数孔蚀是由Cl-引起的。
(2)介质的流速:由于静滞的液体是孔蚀的必要条件,由此在有流速的介质中或提高介质的流速常使孔蚀减轻。
(3)金属本身的因素:具有自。


不锈钢的腐蚀方式与腐蚀性能⑴不锈钢的腐蚀方式简介在众多的工业用途中,不锈钢能提供令人满意的耐蚀性能。
根据使用的经验来看,除机械失效外,不锈钢的腐蚀主要表现在:不锈钢的一种严重的腐蚀形式是局部腐蚀(亦即应力腐蚀开裂,点腐蚀,晶间腐蚀,腐蚀疲劳以及缝隙腐蚀)。
①应力腐蚀开裂(SCC)应力腐蚀开裂是指承受应力的合金在腐蚀性环境中由于裂纹的扩展而产生失效的一种形式。
应力腐蚀开裂具有脆性断口形貌,但它也可能发生于韧性高的材料中。
发生应力腐蚀开裂的必要条件是要有拉应力(不论是参与应力还是外加应力,或者两者兼而有之)和特定的腐蚀介质存在。
裂纹的形成和扩展大致与拉应力方向垂直。
这个导致应力腐蚀开裂的应力值,要比没有腐蚀介质存在时材料断裂所需要的应力值小得多。
在微观上,穿过晶粒的裂纹称为穿晶裂纹,而沿晶界扩展的裂纹称为沿晶裂纹,当应力腐蚀开裂扩展至一定的深度时(此处,承受荷载的材料断面上的应力达到它在空气中的断裂应力),则材料就按正常的裂纹(在韧性材料中,通常是通过显微缺陷的聚合)而断开。
因此,由于应力腐蚀开裂而失效的零件的断面,将包含有应力腐蚀开裂的特征区域以及与显微缺陷的聚合想联系的“韧窝”区域。
通常是应力腐蚀开裂的基本条件是:弱的腐蚀介质,一定的拉应力和特定的金属材料构成的特定腐蚀系统。
下面将详细介绍这方面的内容。
a 仅当弱的腐蚀在金属表面形成不稳定的保护膜时,才可能发生应力腐蚀开裂。
实验结果表明:pH值降低将减弱奥氏体不锈钢的应力腐蚀开裂敏感性。
一般的结构用钢在中性pH 值和高pH值介质中,将发生不同机制的应力腐蚀开裂。
b 在一定的拉应力的应变条件下易产生腐蚀。
对Cr-Ni不锈钢的应力腐蚀开裂,应力(σ)和开裂时间(t s)关系一般认为符合1gt s=a+bσ方程,式中a,b为常数。
这表明所受应力越大,不锈钢产生应力腐蚀开裂的时间越短。
对不锈钢应力腐蚀开裂研究表明,存在产生应力腐蚀的临界应力值,常用σSCC表示。

不锈钢的腐蚀反应通常包括以下几种:
1. 应力腐蚀开裂(SCC):这是一种由金属材料内部拉应力和腐蚀介质共同作
用导致的腐蚀形式。
在某些情况下,如使用含有氯化物的介质,不锈钢的耐蚀性可能会受到影响,导致SCC的发生。
2. 孔蚀:孔蚀是一种局部腐蚀形式,通常发生在金属表面的缺陷处。
在氯化物或其他腐蚀介质的存在下,不锈钢的表面可能会形成蚀孔。
3. 缝隙腐蚀:这种腐蚀形式通常发生在金属材料存在缝隙或夹杂物的地方。
在某些腐蚀介质中,不锈钢的缝隙腐蚀可能会加速。
4. 均匀腐蚀:这种腐蚀形式发生在整个金属表面,通常是由于不锈钢表面存在
划痕、凹坑或其他缺陷造成的。
在某些情况下,均匀腐蚀可能会加速金属材料的破坏。
不锈钢的腐蚀反应可能会受到多种因素的影响,包括材料成分、表面状态、环境条件(如温度、湿度、压力、介质类型和浓度等),以及应力作用等。
为了减缓不锈钢的腐蚀反应,可以采取一些防护措施,如选择合适的材料和表面处理方法、改善环境条件、降低应力作用等。

ASTM G48-2011(R2015)使用三氯化铁溶液做不锈钢及其合金的耐点腐蚀和抗缝隙腐蚀性试验的标准方法(中文翻译版)本标准以固定名称G48发布;紧跟在名称后面的数字表示最初采用的年份,如果是修订,则表示最后修订的年份。
括号中的数字表示上次重新批准的年份。
上标(ε)表示自上次修订或重新批准以来的编辑性更改。
1.范围1.1本试验方法包括若干测定规程,用于测定不锈钢及其台金暴露于氯-氧化环境时的耐麻点和缝隙腐蚀性(见术语G15)。
介绍六种规程,命名为方法A、B、C、D、E和F。
1.1.1方法A——三氯化铁点腐蚀试验。
1.1.2方法B——三氯化铁缝隙腐蚀试验。
1.1.3方法C——镍基和铬包复合金的临界点腐蚀温度试验。
1.1.4方法D——镍基和铬包复合金的临界缝隙腐蚀温度试验。
1.1.5方法E——不锈钢的临界点腐蚀温度试验。
1.1.6方法F——不锈钢的临界缝隙腐蚀温度试验。
1.2方法A用于测定不锈钢和镍基、铬包复合金的相对耐点腐蚀性,方法B可用于侧定这些合金的耐麻点和缝隙腐蚀性。
方法C、D、E 和F可在标准三氯化铁溶液中,按导致不锈钢、镍基和铬包复合金各自开始点腐蚀和缝隙腐蚀的最低(临界)温度,为这些合金划分等级。
1.3这些试验可用于测定合金填加剂、热处理和表面光洁度对耐点腐蚀性和耐缝隙腐蚀性的影响。
1.4以SI单位表示的值被认为标准。
在括号中给出其它单位,仅供参考。
1.5本标准并不意味已提及与其使用相关的所有安全事项。
制定合适的安全和健康规范,确定规章限制的适用性,是本标准用户的职责。
2.引用文件2.1 ASTM标准A262检测奥氏体不锈钢晶间腐蚀敏感性规范D1193试剂水技术规范E691进行实验室间研究以测定试验方法精度的规范E1338计算机化材料性能数据库中金属与合金识别指南G1制备、清洗和评估腐蚀拭验试样的规范G15与腐蚀和腐蚀试验相关的术语(2010年撤回)33该历史标准的最新批准版本在上引用。

金属腐蚀的种类什么是金属腐蚀?金属腐蚀是指金属物质受到环境中的化学或电化学作用而发生不可逆转的破坏过程。
金属腐蚀可能导致金属材料的强度降低、形状变化、外观损坏甚至完全失效。
金属腐蚀是一个普遍存在的问题,涉及到许多不同的腐蚀类型和机制。
金属腐蚀的种类金属腐蚀可以分为许多不同的种类,下面将介绍几种常见的金属腐蚀:1.电化学腐蚀:电化学腐蚀是最常见的金属腐蚀类型之一。
它是由金属材料与周围环境中的电解质之间的化学反应引起的。
在一个电化学腐蚀过程中,金属材料的一部分被氧化成阳极,而另一部分被还原成阴极。
这种腐蚀类型可以通过控制电解质浓度、温度和电压来减轻。
2.化学腐蚀:化学腐蚀是指金属材料与化学物质(如酸、碱等)发生直接的化学反应。
这种腐蚀类型通常发生在金属表面,会导致金属材料的质量损失和外观改变。
化学腐蚀是由于与金属表面接触的化学物质具有一定的腐蚀性。
3.晶粒腐蚀:晶粒腐蚀是一种特殊的金属腐蚀类型,发生在金属晶粒的界面处。
这种腐蚀类型通常由局部电池效应引起,导致晶粒边界处的金属发生腐蚀。
晶粒腐蚀可能会导致金属材料的强度降低和应力腐蚀开裂等问题。
4.微生物腐蚀:微生物腐蚀是由微生物(如细菌、真菌等)引起的金属腐蚀过程。
微生物通过代谢产物(如酸性物质)或电化学反应来腐蚀金属材料。
微生物腐蚀通常发生在潮湿的环境中,常见于海洋、土壤和水处理等领域。
5.应力腐蚀开裂:应力腐蚀开裂是金属在受到应力作用时发生的腐蚀现象。
当金属材料处于应力状态下,并且受到腐蚀介质的影响时,可能发生应力腐蚀开裂。
这种腐蚀类型可能导致金属材料的断裂和失效,对工程结构的安全性有重大影响。
6.间隙腐蚀:间隙腐蚀是一种在金属材料相对密封的小缝隙或间隙中发生的腐蚀类型。
当缝隙中的腐蚀介质滞留,并且缝隙处的氧气供应不足时,金属材料容易受到间隙腐蚀的影响。
这种腐蚀类型通常发生在连接处、焊缝等地方。
以上仅是金属腐蚀的几种常见种类,实际上金属腐蚀还存在其他许多类型。


金属材料腐蚀的分类一般将腐蚀形态分为八类,分别是:①均匀腐蚀或全面腐蚀:腐蚀均匀分布在整个金属表面上。
镁合金牺牲阳极从重量上来看,均匀腐蚀代表金属的最大破坏。
但从技术观点来看,这类腐蚀形态并不重要。
因为如果知道了腐蚀速度,便可估算出材料的腐蚀公差,并在设计时将此因素考虑在内。
②电偶腐蚀或双金属腐蚀:凡具有不同电极电位的金属相互接触,并在一定介质中所发生的电化学腐蚀称为电偶腐蚀或双金属腐蚀。
③缝隙腐蚀:浸在腐蚀介质中的金属表面,在缝隙和其它隐蔽的区域内常常发生强烈的局部腐蚀.这种腐蚀常和空穴、垫片底面、措接缝、表面沉积物以及螺帽和铆钉下的缝隙内积存的步量静止溶液有关。
④小孔腐蚀(简称孔蚀):这种腐蚀的破坏主要集中在某些活性结点上,并向金属内部深处发展。
通常其腐蚀深度大于孔径,严重时可穿透设备。
⑤晶间腐蚀:这种腐蚀首先在晶粒边界上发生,并沿着晶界向纵深发展。
测试桩虽然外观没有明显的变化,但其机械性能大为降低。
⑥选择性腐蚀:合金中的某一组分由于腐蚀优先地溶解到电解质溶液中,铝热焊接从而造成另一组分富集于金属表面上。
⑦磨损腐蚀:腐蚀性流体和金属表面间的相对运动,引起金属的加速磨损和破坏。
一般这种运动的速度很高,同时还包括机械磨耗和磨损作用。
⑧应力腐蚀:应力腐蚀破坏是指在拉应力和一种给定腐蚀介质共存而引起的破坏。
金属或合金发生应力腐蚀破坏时,大部分表面实际不遭受腐蚀,只有一些细裂纹穿透内部,破坏现象能在常用的设计应力范围内发生,因此,后果很严重。
金属腐蚀又根据其发生的部位,可分为全面金属腐蚀和局部金属腐蚀两大类。
金属腐蚀还可按腐蚀环境分类,即分为化学介质腐蚀、大气介质腐蚀、海水介质腐蚀和土壤腐蚀等。
也可按腐蚀过程的特点,分为化学腐蚀、电化学腐蚀和物理腐蚀三大类。
上述腐蚀分类方法虽。
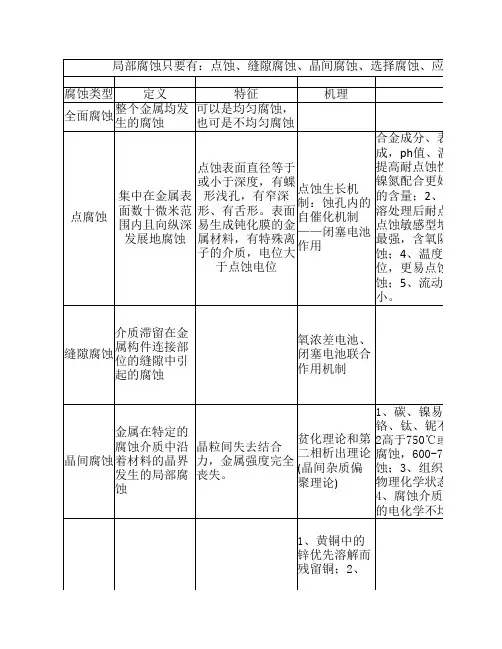

金属材料的点腐蚀和缝隙腐蚀点腐蚀和缝隙腐蚀(pitting and crevice corrosion)金属材料接触某些溶液,表面上产生点状局部腐蚀,蚀孔随时间的延续不断地加深,甚至穿孔,称为点腐蚀(点蚀),也称孔蚀。
通常点蚀的蚀孔很小,直径比深度小得多。
蚀孔的最大深度与平均腐蚀深度的比值称为点蚀系数。
此值越大,点蚀越严重。
一般蚀孔常被腐蚀产物覆盖,不易发现,因此往往由于腐蚀穿孔,造成突然性事故(见金属腐蚀)。
缝隙腐蚀是两个连接物之间的缝隙处发生的腐蚀,金属和金属间的连接(如铆接、螺栓连接)缝隙、金属和非金属间的连接缝隙,以及金属表面上的沉积物和金属表面之间构成的缝隙,都会出现这种局部腐蚀。
许多金属材料都能产生点蚀和缝隙腐蚀。
不锈钢、铝合金等靠钝化来增强耐蚀性的金属材料,也易产生点蚀和缝隙腐蚀。
许多环境介质都能引起金属材料的点蚀和缝隙腐蚀,尤其是含氯离子的溶液。
点腐蚀金属表面的电化学不均匀性是导致点蚀的重要原因。
金属材料的表面或钝化膜等保护层中常显露出某些缺陷或薄弱点(如夹杂物、晶界、位错等处),这些地方容易形成点蚀核心。
金属浸入含有某些活化阴离子(特别是氯离子)的溶液中,只要腐蚀电位达到或超过点蚀电位(或称击穿电位),就能产生点蚀。
这是由于钝化膜在溶液中处于溶解以及可再度形成的动平衡状态,而溶液中的活化阴离子(氯离子)会破坏这种平衡,导致金属的局部表面形成微小蚀点,并发展为点蚀源。
例如不锈钢表面的硫化物夹杂的溶解,暴露出钢的新鲜表面,就会形成点蚀源。
点蚀的发展是一个在闭塞区内的自催化过程。
在有一定闭塞性的蚀孔内,溶解的金属离子浓度大大增加,为保持电荷平衡,氯离子不断迁入蚀孔,导致氯离子富集。
高浓度的金属氯化物水解,产生氢离子,由此造成蚀孔内的强酸性环境,又会进一步加速蚀孔内金属的溶解和溶液氯离子浓度的增高和酸化。
蚀孔内壁处于活化状态(构成腐蚀原电池的阳极),而蚀孔外的金属表面仍呈钝态(构成阴极),由此形成了小阳极/大阴极的活化-钝化电池体系,使点蚀急速发展。
不锈钢的腐蚀类型一种不锈钢有可能在许多介质中具有良好的耐蚀性,但在另外某种介质中,却可能因化学稳定性低而发生腐蚀。
也就是说,一种不锈钢不可能对所有介质都耐腐蚀。
金属的腐蚀,按机理可分为物理腐蚀、化学腐蚀与电化学腐蚀三种。
金属的物理溶解属于物理腐蚀。
化学腐蚀是指在介质中直接发生的化学作用,即金属同介质中离子直接交换电荷。
早先认为金属遭受高温而引起氧化属于纯化学腐蚀,其实多数的高温氧化属于电化学腐蚀。
钝化防护薄膜之所以能阻止金属再受腐蚀,其重要的一个方面即为阻碍其离子交换和电荷交换的速度。
电化学腐蚀是金属在电介质中,由于电极反应而发生的腐蚀。
在许多电化学腐蚀过程中,有一种金属与另一种金属共同参与,或者金属内部各不同相的组成物共同参与,即形成所谓电偶腐蚀。
此种情况下,一种金属构成阳极受腐蚀而发生溶解,另一种金属构成阴极而发生还原反应,这是电化学腐蚀的特点。
在生活实际、工程实际中的金属腐蚀,绝大多数都属于电化学腐蚀。
不锈钢的主要腐蚀形态有均匀腐蚀(表面腐蚀)、点腐蚀、缝隙腐蚀、晶间腐蚀和应力腐蚀等。
一、均匀腐蚀均匀腐蚀是指接触腐蚀介质的金属表面全面产生腐蚀的现象。
均匀腐蚀使金属截面不断减少,对于被腐蚀的受力零件而言,会使其承受的真实应力逐渐增加,最终达到材料的断裂强度而发生断裂。
评定均匀腐蚀的方法是在试验条件下,测出单位面积上经一定时间腐蚀以后所损失的重量(g/m2·年),即为腐蚀速率,若以被腐蚀的深度(mm/年)计,则更便于计算设备的耐蚀寿命。
根据腐蚀速率不同,可将金属材料的耐蚀性分为10级。
根据不同的使用情况对耐蚀性一般分为两大等级:腐蚀速率小于0.01mm/年的,认为是“完全耐蚀”;腐蚀速率小于0.1mm/年的,认为是“耐蚀”。
这里显然意味着,腐蚀速率超过0.1mm/年,属于不耐蚀或不太耐蚀。
此外,还有别的分级方法,在此仅举此一种。
根据其耐蚀性优良程度,钢材又有不锈钢和耐蚀钢之分。
1.不锈钢指在大气及弱腐蚀介质中耐蚀的钢。
金属常见的几种腐蚀简介一、垢下腐蚀1、定义垢下腐蚀under-deposit corrosion:金属表面沉积物产生的腐蚀2、腐蚀机理一种特殊的局部腐蚀形态,其机理是由于受设备几何形状和腐蚀产物、沉积物的影响,使得介质在金属表面的流动和电介质的扩散受到限制,造成被阻塞的的空腔内介质化学成分与整体介质有很大差别,空腔内介质pH值发生较大变化,形成阻塞电池腐蚀(Occude cell corrosion),尖端的电极电位下降,造成电池腐蚀。
按其腐蚀原理可分为酸性腐蚀和碱性腐蚀两种,通常循环冷却系统的垢下腐蚀为酸性腐蚀。
结垢是指在冷却水中所含成垢组分在水侧金属表面的结垢过程,污垢是包括水垢在内的固形物的集合体。
常见的污垢物有:泥渣及粉尘砂粒,腐蚀产物,天然有机物群生物群体,一般有碎屑、氧化铝、磷酸铝、磷酸铁和污垢的沉积,冷却塔的污垢来自于以下几个方面:①来自补充水的污垢。
②来自空气污垢。
③来自系统本身的污垢。
微生物是一些细小多为肉眼看不见的生物,微生物的种类有细菌、藻类、真菌和原生动物,微生物在冷却水系统中大量繁殖,会使冷却水颜色变黑,发生恶臭。
破坏环境,同时会形成大量粘泥使冷却塔的冷却效率降低,使效率迅速降低的水头损失增加,沉积在金属表面的菌类,会引起严重的垢下腐蚀所有这些总是导致冷却水系统不能长期安全运转影响生产,造成经济损失。
因此,微生物危害与水垢腐蚀对冷却水的危害是一样的重要三者比较起来控制微生物的危害应是首要的。
冷却水的微生物有以下种类:有真菌、硫酸菌、还原菌、自养菌、异样菌、硫细菌、铁细菌、硝化菌、藻类,藻类是低级的绿色植物,没有要茎叶的分化固然又叫原植体植物,藻类与菌类的主要区别在于具有色素体的色素,能进行光合作用。
制造营养物质是光合自养型生物,在循环冷却水系统,常出现的有蓝绿藻、绿藻、硅藻三大类,在循环冷却水池,冷却塔受光照的部分生长繁殖枯死的藻类进入循环冷却系统成为沉积物的一种成份,金属的垢下腐蚀是由于其本身电化学腐蚀存在自催化作用,酸腐蚀是氢的去极化作用(2H++2e→H2),腐蚀产物主要是可溶性盐,这些盐类的水解使介质的酸性进一步增强,加速了金属的腐蚀。
点腐蚀和晶间腐蚀
点腐蚀这是一种腐蚀集中于金属表面很小范围、深入金属内部迅速发展的小孔状腐蚀形态,又称为孔蚀。
通常蚀孔深度比孔径要大得多。
这是一种隐蔽性强、破坏性大的局部腐蚀。
点腐蚀多发生与表面形成钝化膜或者具有阴极性镀层的金属上,含特种阴离子溶液中易于引发点腐蚀,钝性材料高于临界点电位将引发点腐蚀。
缝隙腐蚀这是金属与其他材料构成表面间隙而且在电解质中发生了缝隙内金属严重腐蚀的一种局部腐蚀形态。
其特点是:缝隙腐蚀可以发生在所有金属和合金上;可能发生在任何侵蚀性溶液中;缝隙腐蚀临界电位比电视电位更低;缝隙宽度必须使侵蚀性溶液能浸入缝隙内,同时又窄到能使液体停滞在缝内,才能发生缝隙腐蚀,一般的敏感宽度为0.0025-0.1mm。
晶间腐蚀这是腐蚀沿着金属晶粒边界或者其临近区域向材料内部迅速发展,而晶粒本体则腐蚀很轻微的一种局部腐蚀类型。
这种腐蚀使晶粒之间失去结合力,金属强度丧失,导致构件过早失效。
电偶腐蚀两种具有不同电位的金属材料在同一电解质中接触或者通过电子导体连接,其中电位较负金属的腐蚀速度增大,电位较正金属腐蚀速度减缓而受到保护,此所谓电偶腐蚀,又称为接触腐蚀、异种金属或者双金属腐蚀。
实质上它是两种不同金属构成的宏观原电池腐蚀,相互接触的异种金属间电位差为电偶腐蚀的原动力。
因此可以利用电偶序判断在某种介质中异金属接触时的电偶腐蚀倾向,但不能定量表征其腐蚀速
度。
金属材料的点腐蚀和缝
隙腐蚀
文档编制序号:[KKIDT-LLE0828-LLETD298-POI08]
金属材料的点腐蚀和缝隙腐蚀
点腐蚀和缝隙腐蚀(pitting and crevice corrosion)金属材料接触某些溶液,表面上产生点状局部腐蚀,蚀孔随时间的延续不断地加深,甚至穿孔,称为点腐蚀(点蚀),也称孔蚀。
通常点蚀的蚀孔很小,直径比深度小得多。
蚀孔的最大深度与平均腐蚀深度的比值称为点蚀系数。
此值越大,点蚀越严重。
一般蚀孔常被腐蚀产物覆盖,不易发现,因此往往由于腐蚀穿孔,造成突然性事故(见金属腐蚀)。
缝隙腐蚀是两个连接物之间的缝隙处发生的腐蚀,金属和金属间的连接(如铆接、螺栓连接)缝隙、金属和非金属间的连接缝隙,以及金属表面上的沉积物和金属表面之间构成的缝隙,都会出现这种局部腐蚀。
许多金属材料都能产生点蚀和缝隙腐蚀。
不锈钢、铝合金等靠钝化来增强耐蚀性的金属材料,也易产生点蚀和缝隙腐蚀。
许多环境介质都能引起金属材料的点蚀和缝隙腐蚀,尤其是含氯离子的溶液。
点腐蚀
金属表面的电化学不均匀性是导致点蚀的重要原因。
金属材料的表面或钝化膜等保护层中常显露出某些缺陷或薄弱点(如夹杂物、晶界、位错等处),这些地方容易形成点蚀核心。
金属浸入含有某些活化阴离子(特别是氯离子)的溶液中,只要腐蚀电位达到或超过点蚀电位(或称击穿电位),就能产生点蚀。
这是由于钝化膜在溶液中处于溶解以及可再度形成的动平衡状态,而溶液中的活化阴离子(氯离子)会破坏这种平衡,导致金属的局部表面形成微小蚀点,并发展为点蚀源。
例如不锈钢表面的硫化物夹杂的溶解,暴露出钢的新鲜表面,就会形成点蚀源。
点蚀的发展是一个在闭塞区内的自催化过程。
在有一定闭塞性的蚀孔内,溶解的金属离子浓度大大增加,为保持电荷平衡,氯离子不断迁入蚀孔,导致氯离子富集。
高浓
度的金属氯化物水解,产生氢离子,由此造成蚀孔内的强酸性环境,又会进一步加速蚀孔内金属的溶解和溶液氯离子浓度的增高和酸化。
蚀孔内壁处于活化状态(构成腐蚀原电池的阳极),而蚀孔外的金属表面仍呈钝态(构成阴极),由此形成了小阳极/大阴极的活化-钝化电池体系,使点蚀急速发展。
缝隙腐蚀
是由缝隙内外介质间物质移动困难所引起的。
为此,缝隙的宽度应足够狭小。
它的发展也是一个闭塞区内的自催化过程。
例如处在海水等介质中的钢制零部件,在缝隙腐蚀的起始阶段,缝隙内外的金属表面都发生以氧还原作为阴极反应的腐蚀过程。
由于缝隙内的溶氧很快被消耗掉,而靠扩散补充又十分困难,缝隙内氧还原的阴极反应逐渐停止,缝隙内外建立了氧浓差电池。
缝隙外大面积上进行的氧还原阴极反应,则促进缝隙内金属阳极溶解。
缝隙内金属溶解产生过剩的金属阳离子(Me+),又使缝隙外的氯离子迁入缝隙内以保持电平衡。
随之而发生的金属离子水解,使缝隙内酸度增高,又加速了金属的阳极溶解(见图)。
点腐蚀和缝隙腐蚀的比较
点腐蚀和缝隙腐蚀两者的发展阶段的机理是一致的,但是它们的诱发机理和发生过程则有所不同。
前者是由于材料的钝态或保护层的局部破坏所引起,通过形成点蚀源而发展起来的;后者则是因介质的电化学不均匀性所引起,腐蚀一开始就在缝隙条件下受闭塞电池的作用。
从电极电位来看,发生和发展缝隙腐蚀的电极电位比点蚀更低。
从介质来看,缝隙腐蚀在不含氯离子的溶液中也会发生,而点蚀则多在含有特殊的活性阴离子条件下才会发生。
溶液中的氯离子浓度对两种腐蚀有很大的影响
通常是氯离子浓度愈高,点蚀和缝隙腐蚀发生的可能性也愈大,而且发展的速度也愈快。
其他卤族离子也有类似的影响。
一般溶液的温度愈高,产生点蚀和缝隙腐蚀的危险性也愈大。
防止措施
提高材料耐点蚀性的重要措施是添加适当的合金元素(如在不锈钢中添加钼),采取钝化处理及适当的热处理,降低金属材料中的夹杂物含量。
防止缝隙腐蚀的主要措施是在结构中要避免缝隙和能造成表面沉积的几何形状,要尽量用焊接代替铆接,采用非吸湿性材料做垫圈。
电化学保护对防止点蚀和缝隙腐蚀都有效。
采用合适的耐点蚀和耐缝隙腐蚀的金属材料也是防止点蚀与缝隙腐蚀的有效措施。