肠道线虫
- 格式:docx
- 大小:35.16 KB
- 文档页数:5
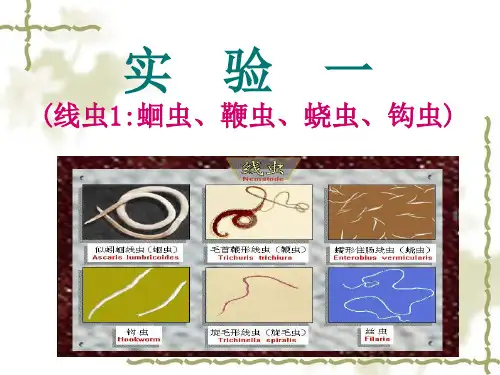



(一)羊体内寄生虫病1、肠道线虫(1)病因寄生于羊消化道线虫种类多,常见的3-5种,一般10多种。
当羊体内寄生虫种类少,虫数不多,膘力在中等以上时,羊表现临床症状不明显,当种类数量增多时,临床症状才明显。
因此,定期驱虫是养羊必须进行的主要工作。
(2)症状病羊食欲不振,消化不良,拉稀,便秘,粪便带血,顽固性或周期性拉稀,羔羊、幼羊生长缓慢,被毛干枯,不光亮,成年羊消瘦,肥育困难,母羊少孕或不孕。
若饲养管理差的情况下,病势加重,极度衰弱,贫血、颌下、胸腹部水肿,最终卧地死亡。
尸检,可见消化道各部有大量虫体。
(3)防治①每年四季季末,给整体羊群各驱1次虫。
②羊粪全部堆积发酵或在侧所,沼气池内、注入相关杀虫卵消毒化学药品,草场定期轮牧,不在低洼潮湿脏水处放牧,阴雨天和露水季节稍迟放牧。
③治疗:采用广谱驱虫药或选择性地用抗蠕敏,敌百虫,左旋咪唑灌服或注射。
2、绦虫病(1)病因含虫地螨被羊采食后而发病。
(2)症状食欲下降,饮欲上升,贫血,拉稀,粪便常有白色节片,有时出现痉挛或回旋运动或头部后仰。
病末期,常因衰弱而卧地不起,多将头折向后方,常作咀嚼运动,口周围有许多泡沫,然后死亡。
羔羊受害最为严重。
(3)防治:① 避免在早晨、黄昏、雨天、低湿地放牧。
② 舍养改为放牧时要驱虫,放牧一月驱两次虫,一月后驱三次虫③驱虫后的粪便要集中堆积发酵或沤肥,至少2-3个月才能杀灭虫卵。
④ 采用口服丙硫咪唑、硫双二氯酸。
采用上述粪便处理方法。
3、棘球蚴病(1)病因由棘球蚴虫期引起发病,成虫常呈白色或黄色、长、偏平形寄生于猫、鸡、牛、羊等畜禽内,随粪便排出虫卵污染水草而感染。
(2)症状发病初期和病轻者无明显症状,严重者被毛逆立,常脱毛,消瘦、贫血、呼吸困难;肺部感染时,咳嗽,咳后往往卧地不起;肝感染时,消化不良。
(3)防治① 定期给易感动物(如猫、犬等)灌服丙硫咪唑片或广谱驱虫药,驱除的虫体应集中烧毁或深埋。
② 遇患有虫体包囊器管的羊内脏器管或其他感染动物器管,采取集中烧毁深埋处理。


慎入12种常见的肠道寄生虫在我们的日常生活中,肠道寄生虫可能是一个容易被忽视的健康隐患。
这些小小的生物寄生在我们的肠道内,悄悄地影响着我们的身体。
今天,就让我们一起来了解一下 12 种常见的肠道寄生虫,提高对它们的警惕。
首先,来说说蛔虫。
蛔虫是人体肠道内最大的寄生线虫,成虫呈圆柱形,像一根白色的蚯蚓。
它们主要通过污染的食物、水或者手进入人体。
儿童更容易感染蛔虫,因为他们往往不太注意卫生。
感染蛔虫后,可能会出现食欲不振、腹痛、营养不良等症状,严重的还可能导致肠梗阻等并发症。
接下来是绦虫。
绦虫的身体由许多节片组成,看起来就像一条白色的带子。
人通常是因为吃了未煮熟的含有绦虫幼虫的猪肉或牛肉而感染。
绦虫在肠道内会夺取大量的营养,导致人体消瘦、乏力,还可能引起肠道炎症。
钩虫也是常见的肠道寄生虫之一。
钩虫的体型较小,呈钩状。
它们会通过人体的皮肤侵入,比如赤脚在有钩虫卵的土地上行走。
感染钩虫后,会出现贫血、乏力、气短等症状,因为钩虫会吸食人体的血液。
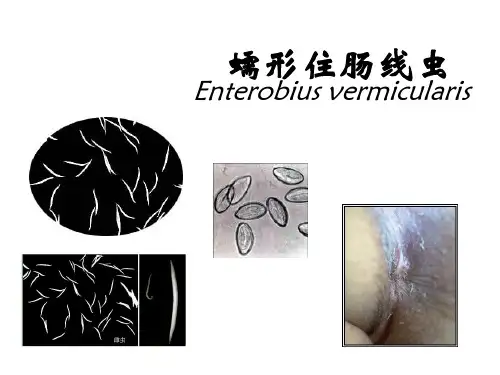
蛲虫则主要在儿童中较为常见。
蛲虫的成虫细小如线头,常在夜间爬到肛门周围产卵,引起肛门瘙痒。
孩子们会因为搔抓肛门而将虫卵带到手上,再通过手口传播造成重复感染。
鞭虫的外形像马鞭,感染鞭虫后,会出现慢性腹泻、腹痛、便血等症状,长期感染还可能影响儿童的生长发育。
姜片虫主要寄生在小肠内,它的形状像姜片。
人如果吃了生的或未煮熟的含有姜片虫囊蚴的菱角、荸荠等水生植物,就容易感染。
感染后会出现消化不良、腹胀、腹痛等症状。
阿米巴原虫也是肠道寄生虫的一种,它会引起阿米巴痢疾,表现为腹痛、腹泻、脓血便等症状。
还有血吸虫,虽然它主要寄生在肝脏和肠道的血管内,但也会对肠道健康造成影响。
血吸虫病在一些地区仍然是一个严重的公共卫生问题。
除了以上这些,还有兰氏贾第鞭毛虫、肠滴虫、旋毛虫等肠道寄生虫。
那么,我们该如何预防这些肠道寄生虫的感染呢?首先,要养成良好的卫生习惯,比如饭前便后洗手,勤剪指甲,不随地大小便。

生物源性蠕虫名词解释生物源性蠕虫是一类寄生在人类和动物身上的寄生虫,分布广泛,种类繁多。
下面是一些常见的生物源性蠕虫以及对它们的解释。
1. 蛔虫:蛔虫是人体寄生的一种常见寄生虫。
它的身体细长,像一条白色细线,成体可以长到20-40厘米。
蛔虫主要寄生在人的小肠中,通过食入感染,常见在饮食卫生条件较差的地区和儿童中。
蛔虫感染可导致腹痛、呕吐、消化不良等症状。
2. 钩虫:钩虫又称鈎蟲,主要寄生在人和动物的小肠中。
通过脚步钩吸附在肠壁上吸取血液进行寄生。
钩虫感染主要通过经过受污染的土壤或食物进入人体。
感染钩虫可以引起贫血、腹痛、腹泻等症状。
3. 十二指肠虫:十二指肠虫是一种居住在人体肠道的蠕虫,主要寄生在人的十二指肠内。
它的身体扁平,呈大约10厘米长的条状,由许多环节组成。
十二指肠虫主要通过食入含虫卵的食物或水而感染。
感染十二指肠虫可导致腹痛、恶心、消化不良等症状。
4. 肠道线虫:肠道线虫是一类寄生在人和动物肠道中的蠕虫,包括钩线虫和蛔线虫等。
肠道线虫寄生在人体肠道中,通过摄取宿主的血液和组织液来生活。
肠道线虫感染主要通过水源、土壤等途径入侵人体。
感染肠道线虫可引起腹泻、贫血、消化不良等症状。
5. 结肠滴虫:结肠滴虫是一种寄生在人体结肠中的原生动物,通过向肠道壁附着,并导致炎症和损伤,引起肠道疾病。
结肠滴虫主要传播通过食物或水源受到感染,感染结肠滴虫可导致腹泻、腹痛、消化不良等症状。
以上仅是生物源性蠕虫的一些常见例子,这些虫子会寄生在人体或动物体内,给宿主带来不同的健康危害。
预防生物源性蠕虫感染的关键是保持良好的个人卫生习惯,合理消毒食物和饮用水,并定期进行体检和驱虫。

猪肠道线虫病诊断方案寄生于猪肠道的线虫主要有类圆线虫、猪蛔虫、猪钩虫、猪结节虫和猪鞭虫,前三种寄生虫在小肠内,后二种寄生在结肠内。
这些寄生虫通常呈线状或毛发状,有的呈圆柱状或纺锤形。
雌雄异体,雌虫常大于雄虫。
大小差别很大,多为乳白色,吸血的常显红色。
它们的发育过程大致相似,这里就不在详述。
诊断要点(1)流行特点及其症状特征在饲养管理不良条件下,特别是猪舍潮湿、卫生条件差的情况下流行普遍。
它们的感染途径是经口或经皮肤感染(如类圆线虫的幼虫可通过仔猪的皮肤感染)。
类圆线虫主要危害3-4周龄的仔猪,寄生在十二指肠;猪蛔虫主要危害3-6月龄的仔猪,常造成"僵猪" ,成年猪多半为带虫者不显症状,病仔猪却可表现贫血、腹泻、呕吐、渐渐消瘦。
这些肠道线虫的成虫皆有致病性,可造成猪体营养损失,严重的使肠壁机械损伤,虫体的代谢产物被猪体吸收可出现全身性中毒;另外,它们的幼虫在猪体内生活过程中也造成损害。
(2)剖检病变当类圆虫的幼虫经皮肤感染仔猪时,可引起仔猪皮肤湿疹,同时也可带入副伤寒杆菌,而造成死亡;此虫体移行到肺时,可引起支气管、肺炎和胸膜炎。
蛔虫的幼虫在猪体内移行时,损害路径脏器和组织,破坏血管,引起血管出血和组织坏死。
常见肝组织致密,表面有大量出血点或暗红色斑点、肝脂肪变性、坏死;蛔虫性肺炎。
结肠壁上有结节。
盲肠和结肠上发现炎性病变和大量虫体,虫体前部细长,深深钻入粘膜内,后部短粗,形似鞭子,故称鞭虫。
(3)实验室检查可用直接涂片法或饱和盐水浮集法检出粪便中的虫卵来确诊。
防治方案(1)场全部驱虫一次。
(2)母猪产仔前1-2周驱虫一次。
(3)种公猪一年驱虫一次。
(4)仔猪断奶转群驱虫一次。
(5)彻底清洁环境,加强粪便管理,防止再次感染。


21绵羊胃肠道线虫病防控措施分析董华友(四川省盐源县右所乡畜牧兽医站615703)摘要:绵羊胃肠道线虫病主要是寄生虫寄生在绵羊肠道内,一旦发病将会对绵羊生长发育产生影响,严重情况下会造成绵羊死亡。
绵羊胃肠道线虫病是一种较为恶劣的寄生虫病,绵羊患病将会对绵羊养殖业造成冲击,带来巨大损失。
关键词:绵羊;胃肠道线虫病;寄生虫随着国家的快速发展,社会经济的不断进步,促使我国绵羊养殖业的快速进步。
但是,在绵羊养殖过程中,会产生胃肠道线虫病,是一种影响较为恶劣的寄生虫病。
绵羊一旦患有此病,不仅会对绵羊生长发育产生不良影响,还会造成绵羊死亡,对绵羊养殖业以及社会经济发展产生制约。
随着科学技术的不断进步,已经研制出绵羊胃肠道线虫病的防控措施。
所以,本文将针对绵羊胃肠道线虫病发病原因以及防控措施进行相应阐述。
1绵羊胃肠道线虫病产生原因绵羊主要胃肠道线虫病分为幼羊细颈线虫病、羊羔以及偶尔发生在年长绵羊身上的寄生虫性肠胃炎两种。
虽然不同类型线虫都能够寄生在绵羊肠道处,但是引发寄生虫性胃肠炎病症主要原因是奥斯特线虫属以及毛圆线虫属,奥斯特线虫属在如今新分类下属于背带线虫属。
巴氏细颈线虫能够存在于大量幼虫之中,并且引发幼羊出现腹泻情况。
因为血矛线虫无法抵御严寒,所以,血矛线幼虫存在于牧区当中多种多样,并且传播形式也会发生改变。
其他类型幼虫只会偶尔附着在绵羊肠道内,引发绵羊患病。
但是其他类型幼虫致病性较弱,可以利用普通药物进行治疗,能够在一定程度上避免长期潜伏寄生虫的流行。
2绵羊胃肠道线虫病有效防控措施2.1药物预防巴氏细颈线虫感染性较强的幼虫会在5月份初期与6月份初期达到巅峰,所以,在5~6月之间管理员应该给绵羊连续用药3周[1]。
情况较轻的绵羊可以利用丙硫咪唑、伊维菌素以及左旋咪唑等药物驱除绵羊肠道内部幼虫,情况严重绵羊需要对症下药,研究其具体发病原因,从而给出有效治疗措施。
羊羔感染胃肠道线虫病是由于围产期母羊粪便造成的,围产期母羊粪便中,含有大量虫卵。
猪的肠道线虫病防治措施与治疗方法猪的肠道线虫主要有猪蛔虫、猪鞭虫、猪结节虫、猪钩虫和猪杆虫。
其中以猪蛔虫和猪鞭虫分布较广,危害严重。
主要症状。
病猪精神较差,吃食少,逐渐消瘦、贫血、下痢,粪便带粘液。
侵害肺部时,出现咳嗽,呼吸急促;侵害肠道时,出现呕吐,严重时卧地、腹痛,肠阻塞或肠破裂。
预防措施。
①加强产仔母猪的管理,对产前母猪要全身擦洗,除去虫卵后,方可赶入消毒后的产房。
产后尽量减少仔猪与母猪粪便的接触,及时清除粪便和垫草,粪便与垫草应堆积发酵,猪舍用3%敌百虫喷洒消毒灭卵。
②喂给驱虫性抗生素,如潮霉素B和越霉素A,每1000千克饲料中添加5~10克。
市售的得利肥素含越霉素A2%,每1000千克饲料中添加250~500克,有良好的驱虫和促进生长作用。
③定期驱虫。
对2~6个月龄的猪,在断奶后要驱虫一次,以后每隔2~3个月驱虫一次。
治疗方法。
①盐酸左旋咪唑。
每千克体重10毫克,可混入饲料或饮水中给予。
②驱虫灵(构椽酸哌哔嗪)。
每千克体重0.2克混入饲料内喂服。
③丙硫苯咪唑(抗蠕敏)。
每千克体重30毫克内服。
④噻嘧啶酒石酸盐。
每千克体重20~30毫克,一次内服。
⑤噻苯唑。
每千克体重50~150毫克内服或按0.1%~0.4%的比例混料喂服。
⑥民间“百虫绝”中药方,生二丑30克,炒杏仁2克,槟榔24克,君子肉21克,雄黄15克,雷丸12克,共为细末,加水分4次内服,日服一次,孕猪禁服。
⑦驱虫净(四咪唑)。
每千克体重30毫克内服,间隔1周再给药一次。
⑧驱虫精。
按每10千克体重用1毫升,用毛笔或棉花球将药液涂于耳朵背面即可。
⑨精制敌百虫。
每千克体重0.1~0.13克,混入饲料内喂服(最大量不超过7克)。
服药前绝食12小时,效果最佳。
传染病防治:线虫与抗线虫药物1.常见的线虫病线虫有寄生于肠道及寄生于组织两类。
前者包括蛔虫、钩虫、蜕虫、鞭虫及类圆线虫等,后者主要有丝虫、旋毛虫(成虫寄生于小肠、幼虫则寄生于肌肉)。
(1)蛔虫病是感染一种肠蠕虫,蛔虫所致。
此感染遍于全球,而更常见于温暖卫生设施不良的地区,因儿童随地排粪便致该地区持久的大量感染。
坳虫在肺中移行可发热,咳嗽,和哮喘。
肠道感染重者可致腹痛,偶可致肠梗阻。
大量的蛔虫可致营养吸收不良,成人偶可阻塞阑尾、胆道或胰管。
检查出粪便标本中蛔虫卵,就可诊断蛔虫感染。
偶尔,在粪便或呕吐物中查到蛔虫,或痰中查到坳虫。
血中嗜酸性细胞增多。
胸X线片可查见移行的影像。
预防需使用完善的卫生设备和不吃不洁的蔬菜。
治疗口服双羟蔡酸咯唳或甲苯咪嗖,但甲苯咪嘎有损胎儿,故不能用于孕妇。
(2)钩虫病是感染十二指肠钩虫或美洲钩虫所致。
世界上有1/4的人口感染钩虫。
此感染最常见于温暖,潮湿,卫生不良的地区。
十二指肠钩虫已见于地中海地区、印度、中国和日本;美洲钩虫已见于非洲热带地区、亚洲和美洲。
钩坳穿入皮肤处出现扁平、突起的痒疹(着地痒),坳虫移行经肺可致发热、咳嗽哮喘。
成虫常致上腹痛。
由于肠出血致缺铁性贫血和低蛋白血症。
在儿童,由于长期的严重失血可致发育迟缓,心力衰竭和全身水肿。
治疗应先纠正贫血,通常口服铁剂以补充铁可改善症状,也可注射铁剂。
在严重病例需输血。
当病人的情况稳定,口服双羟蔡酸喀唳,甲苯咪嗖1~3日,可杀灭钩虫。
这些药不能用于孕妇。
(3)旋毛虫病是感染旋毛虫所致。
旋毛虫病发生于世界许多地区。
人食生的或未熟的加工猪肉或猪肉制品受染。
当食入的包囊在胃或十二指肠内消化,释放出坳虫,穿入小肠壁,2日内,坳虫成熟并交配。
很少的坳虫经淋巴管和血流带至全身,仅到达骨骼肌者才能生存。
坳虫穿入肌肉致发炎,经3个月才成包囊。
上眼睑肿是最早的和最典型的症状之一,突发生于感染后大约第11天。
巩膜和眼底出血,眼痛,继而畏光。
肠道线虫流行病学和防治对策研究进展杨志强 2013181622049(四川大学华西临床医学院2013级临床医学八年制)摘要:肠道线虫主要包括蛔虫,钩虫和鞭虫,寄生于人体肠道内,引起一系列慢性疾病,构成寄生虫感染的一大类医学问题。
肠道线虫几乎在世界范围内分布,但主要分布于热带及亚热带地区。
全球感染人群数目多,中国感染患者近年来有所减少。
防治肠道寄生虫感染主要通过药物治疗,注意个人卫生,提高环境卫生,加强公众教育等方式,达到长期、有效的控制目的。
关键词:肠道线虫;流行病学;防治对策;卫生Epidemiology and control countermeasures of intestinal nematodes: current progressYANG Zhiqiang(West China Clinical Medical School of Sichuan University, Clinical Medicine Eight-year Program, Grade2013)Abstract: Intestinal nematodes mainly include Ascaris lumbricoides, Trichuris trichiura, Ancylostoma duodenale, Necator americanus, inhabiting in human intestinal tracts and inflicting a series of chronic diseases, which are a major medical problem in parasitic infections. Intestinal nematodes distribute across the world, but mainly tropical or subtropical areas. The infected population is large, while China has seen a drop of patients. To prevent and cure intestinal nematode infections and maintain long-lasting effects, chemotherapeutics, personal and environmental hygiene, public awareness are recommended.Key words: intestinal nematode; epidemiology; control countermeasures; hygiene寄生虫感染是一类全球性的医学难题,在发展中国家里尤为严重,其感染率和致死率超过其他感染性疾病,已成为致死性疾病的主因之一。
寄生虫感染中主要有两大类感染,一是医学原虫感染,二是医学蠕虫感染。
其中医学原虫感染是主要的致死性感染,而医学蠕虫感染虽然致死率没有原虫高,但可以引起许多慢性疾病,使人体变得虚弱[1]。
这两类感染都是值得重视的公共卫生性问题。
肠道线虫作为医学蠕虫的一大类,相关研究对于控制寄生虫感染具有重要意义。
本文就肠道线虫的流行病学特点和防治措施的研究现状展开综述。
1流行病学特征1.1肠道线虫种类目前研究表明有超过342种蠕虫与人类紧密相关,其中有197种被认为主要寄生于胃肠道[2]。
肠道线虫属于土源性线虫,在人体胃肠道中广泛分布,然而只有一小部分与疾病发生有关,其中包括似蚓蛔线虫(蛔虫,Ascaris lumbricoides),毛首鞭形线虫(鞭虫,Trichuris trichiura),十二指肠钩口线虫(钩虫,Ancylostoma duodenale),美洲板口线虫(钩虫,Necator americanus)。
这几种肠道线虫在地球上分布广泛而丰富,全球感染人数据估计已达总人口的二分之一[3]。
1.2感染症状感染肠道线虫的症状各不相同,但都可能对人体造成严重的影响。
不论对新生儿,学龄儿童还是成人,都可在营养,生长,身体机能,认知功能和贫血方面产生显著影响[4-7]。
钩虫感染可引起慢性出血,受感染的个人日出血量可达0.57 mL,导致不同程度的贫血。
此外,钩虫感染可延缓儿童身体和心智发育,以及妇女的月经不调,流产,死胎等。
蛔虫感染会扰乱人体正常的消化和吸收功能,导致营养不良[8]。
鞭虫感染与感染密度有显著的联系,会导致慢性结肠炎,贫血,影响不良等临床症状[9]。
1.3全球流行病学特征肠道线虫感染已成为全球范围内最普遍发生的疾病之一。
五十多年以来,随着人类数目的增加,感染人口也在增加,据估计已有超过50%的人口被六大肠道线虫所感染(包括似蚓蛔线虫,毛首鞭形线虫,十二指肠钩口线虫,美洲板口线虫,蠕形住肠线虫,粪类圆线虫)[10],这个数字多达35亿,其中有4.5亿人病情严重,大多数为儿童以及感染钩虫的孕妇。
每年大约有12.5万人患者死亡,主要死因还是在于感染蛔虫,钩虫和鞭虫。
这三种作为肠道线虫感染的主力,分布范围广,在热带地区尤其流行,影响人数分别为13,13和10.5亿。
值得注意的是,虽然大部分患者处于发展中国家以及热带或亚热带地区,但仍有一部分感染侵入高纬度发达国家,即使这些国家拥有高水平的卫生环境和卫生设备[1, 11]。
1.4中国流行病学特征在2003发表的中国范围内的调查研究中[12],钩虫、蛔虫和鞭虫的流行率都较1990年发表的同水平调查有了显著的降低[13],降低率分别为60.7%、71.3%和73.6%。
与此同时,感染土源性线虫(包括肠道线虫)的人数也从1990年的5.36亿人降至2003年的1.29亿人,其中感染蛔虫、钩虫、鞭虫的人数分别约为0.86亿、0.39亿和0.29亿[14]。
但相对于日本和韩国[15, 16],中国的感染率仍处在一个高水平。
中国幅员辽阔,地形与气候条件复杂,而肠道线虫的分布也随着经纬度间温度和湿度的变化而有所不同。
蛔虫、钩虫和鞭虫主要分布于热带及亚热带地区,这与全球性的分布结果一致[17]。
此外,2003年发表的调查显示,大多数寄生虫出现在妇女和儿童体内的几率较高,其中5-9岁和10-14岁年龄组人群中肠道线虫感染率最高[12]。
2防治措施2.1服用驱虫药目前治疗肠道线虫的主要措施为服用或注射世界卫生组织(World Health Organization, WHO)推荐的四种药物——阿苯达唑,甲苯达唑,左旋咪唑和噻吩嘧啶。
而治疗肠道线虫一共有四大类药物,包括苯并咪唑类,咪唑骈噻唑/四氢嘧啶类,巨内脂环类和杂环乙烯胺类药物。
苯并咪唑类抗寄生虫谱广,作用原理为结合游离的微管蛋白,阻止其发生聚合反应,因此能干扰寄生虫依赖微管的葡萄糖摄取。
咪唑骈噻唑/四氢嘧啶类药物可以持续刺激烟酰胺乙酰胆碱受体,导致其过度激活,使神经肌接头受阻,进而导致虫体的强直性瘫痪。
巨内脂环类药物可开放谷氨酸门控的氯离子通道,增加氯离子传导,从而引起神经传导障碍和松弛性麻痹。
杂环乙烯胺类药物通过刺激蛔虫肌肉细胞上的γ氨基丁酸受体,可逆性地阻碍神经肌信号传导,从而导致虫体的松弛性麻痹,进而可由正常的肠蠕动排出体外,仅适用于蛔虫和蛲虫。
值得一提的是,没有一种药对所有线虫都有100%的疗效,因此,多种药物组合服用效果更好,值得推荐。
此外,这些药物都具有一定的副作用,孕妇慎用[1]。
并且近年来,广泛使用抗寄生虫药物造成了人体耐药现象的发生[18].2.2保持卫生和加强教育所有肠道线虫的唯一终宿主都是人,而且除蛲虫外其他肠道线虫都是通过人类粪便传播。
因此人类粪便的合理处理,保持个人的卫生和环境的干净对防治疾病有着重要意义。
此外,由于蛲虫卵可污染被子和衣物等,同时治疗所有家庭成员也是一个重要的策略[19, 20]。
狗作为一些人畜共患寄生虫的保虫宿主,在一定条件下也可以作为蛔虫和鞭虫的传播者。
针对这点,增加大众对人畜共患寄生虫尤其是人狗共患寄生虫的了解,以及给大众宣传维护好公共厕所的重要性等措施,将会极大地减少肠道线虫的传播[21, 22]。
除此之外,与患狗直接接触也可能导致寄生虫传播[23],所以提高公共卫生对减少这些寄生虫的传播具有重要作用。
对于持续性地控制肠道线虫的发展,需要一系列整合性的措施,包括加强卫生教育,提高大众卫生意识,更好地住房、污水处理和生活用水供给,以及完善的疾病关怀。
在这些条件下,再辅以针对性的药物施用,可防止肠道线虫病的复发[24]。
3结语与展望肠道线虫感染是全球性的医学问题,中国虽然经过多年的努力感染人数有所下降,但与其他发达国家相比仍处于较高的水平。
因此,还需进一步加强对肠道线虫的防控工作。
宏观上应适当加大对此经济、人力、科技等方面的投入。
加强宣传教育,提高公共和个人卫生是取得长足防治的根本。
此外,抗虫药的副作用和患者耐药性对全面治疗肠道线虫感染有一定的阻碍。
应保障科技进步,研发出更好的抗虫方法。
参考文献1. Stepek, G., et al., Human gastrointestinal nematode infections: are newcontrol methods required?International Journal of Experimental Pathology, 2006. 87(5): p. 325-341.2. Crompton, D., How much human helminthiasis is there in the world?TheJournal of parasitology, 1999: p. 397-403.3. Hotez, P.J., et al., Rescuing the bottom billion through control of neglectedtropical diseases. The Lancet, 2009. 373(9674): p. 1570-1575.4. Gilgen, D., C. Mascie‐Taylor, and L. Rosetta, Intestinal helminth infections,anaemia and labour productivity of female tea pluckers in Bangladesh.Tropical medicine & international health, 2001. 6(6): p. 449-457.5. Hadju, V., et al., Improvements in appetite and growth in helminth-infectedschoolboys three and seven weeks after a single dose of pyrantel pamoate.Parasitology, 1996. 113(05): p. 497-504.6. Stephenson, L.S., et al., Physical fitness, growth and appetite of Kenyanschool boys with hookworm, Trichuris trichiura and Ascaris lumbricoides infections are improved four months after a single dose of albendazole. 1993.7. WONG, M.S., Treatment of Trichuris trichiura Infections Improves Growth,Spelling Scores and School Attendance in Some Children1Â «2. J. Nutr, 1995.125: p. 1875-1883.8. Chen, Y.-D., L.-H. Tang, and L.-Q. Xu, Current Status of Soil-transmittedNematode Infection in China. Biomedical and Environmental Sciences, 2008.21(2): p. 173-179.9. Stephenson, L., C. Holland, and E. Cooper, The public health significance ofTrichuris trichiura. Parasitology, 2000. 121(S1): p. S73-S95.10. Chan, M.-S., The global burden of intestinal nematode infections—fifty yearson. Parasitology today, 1997. 13(11): p. 438-443.11. Kappus, K.D., et al., Intestinal parasitism in the United States: update on acontinuing problem. The American journal of tropical medicine and hygiene, 1994. 50(6): p. 705-713.12. Xu, L.Q., A national survey on current status of the important parasiticdiseases in human population.Zhongguo ji sheng chong xue yu ji sheng chong bing za zhi= Chinese journal of parasitology & parasitic diseases, 2005.23(5 Suppl): p. 332.13. Xu, L.Q., et al., Soil-transmitted helminthiases: nationwide survey in China.Bulletin of the World Health Organization, 1995. 73(4): p. 507-513.14. Li, T., et al., Major trends in human parasitic diseases in China.Trends inParasitology. 26(5): p. 264-270.15. Takeuchi, T., S. Nozaki, and A. Crump, Past Japanese successes show the wayto accomplish future goals. Trends in parasitology, 2007. 23(6): p. 260-267. 16. Shin, E.-H., et al., Trends in parasitic diseases in the Republic of Korea.Trends in Parasitology. 24(3): p. 143-150.17. Xu, L., et al., Nationwide survey of the distribution of parasites in China--thecharacteristics and rules of geographic distribution of human helminth infection.Zhongguo Ji Sheng Chong Xue Yu Ji Sheng Chong Bing Za Zhi, 1995. 13(2): p. 99-103.18. Sacko, M., et al., Comparison of the efficacy of mebendazole, albendazole andpyrantel in treatment of human hookworm infections in the southern region of Mali, West Africa. Transactions of the Royal Society of Tropical Medicine andHygiene, 1999. 93(2): p. 195-203.19. Cook, G.C., Enterobius vermicularis infection. Gut, 1994. 35(9): p. 1159.20. Kucik, C.J., G.L. Martin, and B.V. Sortor, Common intestinal parasites.American family physician, 2004. 69(5): p. 1161-1168.21. Traub, R.J., et al., The role of dogs in transmission of gastrointestinalparasites in a remote tea-growing community in northeastern India.The American journal of tropical medicine and hygiene, 2002. 67(5): p. 539-545.22. Traub, R.J., et al., Canine gastrointestinal parasitic zoonoses in India. Trendsin parasitology, 2005. 21(1): p. 42-48.23. Wolfe, A. and I. Wright, Human toxocariasis and direct contact with dogs. TheVeterinary Record, 2003. 152(14): p. 419-422.24. Roos, M., The role of drugs in the control of parasitic nematode infections:must we do without? Parasitology, 1997. 114(07): p. 137-144.。