电解质溶液的图像题集
- 格式:docx
- 大小:718.72 KB
- 文档页数:17

专题21 电解质溶液图像分析目录一、热点题型归纳.....................................................................................................................1 【题型一】溶液稀释图像............................................................................................................1 【题型二】水电离度图像............................................................................................................3 【题型三】物质滴定曲线............................................................................................................5 【题型四】浓度比型图像............................................................................................................7 【题型五】分布系数图像............................................................................................................9 二、最新模考题组练 (11)【题型一】溶液稀释图像【典例分析】【典例1】(河南省名校联盟2021~2022学年高三3月联考)常温时,浓度均为1mol ·L -1的CH 3NH 2和NH 2OH 两种碱溶液,起始时的体积都为10mL 。
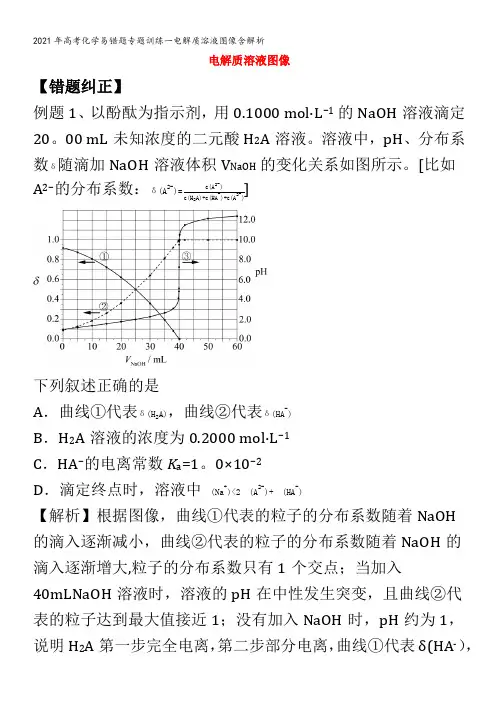
电解质溶液图像【错题纠正】例题1、以酚酞为指示剂,用0.1000 mol·L−1的NaOH溶液滴定20。
00 mL未知浓度的二元酸H2A溶液。
溶液中,pH、分布系数δ随滴加NaOH溶液体积V NaOH的变化关系如图所示。
[比如A2−的分布系数:δ(A2-)=c(A2-)]c(H2A)+c(HA-)+c(A2-)下列叙述正确的是A.曲线①代表δ(H2A),曲线②代表δ(HA-)B.H2A溶液的浓度为0.2000 mol·L−1C.HA−的电离常数K a=1。
0×10−2D.滴定终点时,溶液中c(Na+)<2c(A2-)+c(HA-)【解析】根据图像,曲线①代表的粒子的分布系数随着NaOH的滴入逐渐减小,曲线②代表的粒子的分布系数随着NaOH的滴入逐渐增大,粒子的分布系数只有1个交点;当加入40mLNaOH溶液时,溶液的pH在中性发生突变,且曲线②代表的粒子达到最大值接近1;没有加入NaOH时,pH约为1,说明H2A第一步完全电离,第二步部分电离,曲线①代表δ(HA-),曲线②代表δ(A 2—),根据反应2NaOH+H 2A=Na 2A+2H 2O ,c (H 2A)=0.1000mol/L ×40mL 2×20.00mL =0。
1000mol/L,据此分析作答。
A .根据分析,曲线①代表δ(HA —),曲线②代表δ(A 2-),A 错误;B .当加入40。
00mLNaOH 溶液时,溶液的pH 发生突变,说明恰好完全反应,结合分析,根据反应2NaOH+H 2A=Na 2A+2H 2O,c (H 2A)=0.1000mol/L ×40mL 2×20.00mL =0.1000mol/L ,B 错误;C .根据曲线当δ(HA -)=δ(A 2—)时溶液的pH=2,则HA —的电离平衡常数K a =c(A 2-)⋅c (H +)c (HA -)=c (H +)=1×10—2,C 正确;D .用酚酞作指示剂,酚酞变色的pH 范围为8.2~10,终点时溶液呈碱性,c (OH —)>c (H +),溶液中的电荷守恒为c (Na +)+c (H +)=2c (A 2-)+c (HA —)+c (OH -),则c (Na +)>2c (A 2—)+c (HA -),D 错误;答案选C 。

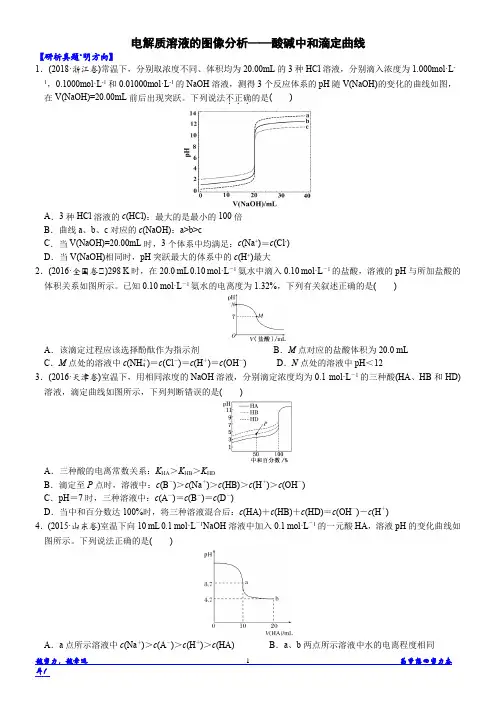
电解质溶液的图像分析——酸碱中和滴定曲线【研析真题•明方向】1.(2018·浙江卷)常温下,分别取浓度不同、体积均为20.00mL的3种HCl溶液,分别滴入浓度为1.000mol·L-1,0.1000mol·L-1和0.01000mol·L-1的NaOH溶液,测得3个反应体系的pH随V(NaOH)的变化的曲线如图,在V(NaOH)=20.00mL前后出现突跃。
下列说法不正确...的是()A.3种HCl溶液的c(HCl):最大的是最小的100倍B.曲线a、b、c对应的c(NaOH):a>b>cC.当V(NaOH)=20.00mL时,3个体系中均满足:c(Na+)=c(Cl-)D.当V(NaOH)相同时,pH突跃最大的体系中的c(H+)最大2.(2016·全国卷Ⅰ)298 K时,在20.0 mL 0.10 mol·L-1氨水中滴入0.10 mol·L-1的盐酸,溶液的pH与所加盐酸的体积关系如图所示。
已知0.10 mol·L-1氨水的电离度为1.32%,下列有关叙述正确的是()A.该滴定过程应该选择酚酞作为指示剂B.M点对应的盐酸体积为20.0 mLC.M点处的溶液中c(NH+4)=c(Cl-)=c(H+)=c(OH-) D.N点处的溶液中pH<123.(2016·天津卷)室温下,用相同浓度的NaOH溶液,分别滴定浓度均为0.1 mol·L-1的三种酸(HA、HB和HD)溶液,滴定曲线如图所示,下列判断错误的是()A.三种酸的电离常数关系:K HA>K HB>K HDB.滴定至P点时,溶液中:c(B-)>c(Na+)>c(HB)>c(H+)>c(OH-)C.pH=7时,三种溶液中:c(A-)=c(B-)=c(D-)D.当中和百分数达100%时,将三种溶液混合后:c(HA)+c(HB)+c(HD)=c(OH-)-c(H+)4.(2015·山东卷)室温下向10 mL 0.1 mol·L-1NaOH溶液中加入0.1 mol·L-1的一元酸HA,溶液pH的变化曲线如图所示。
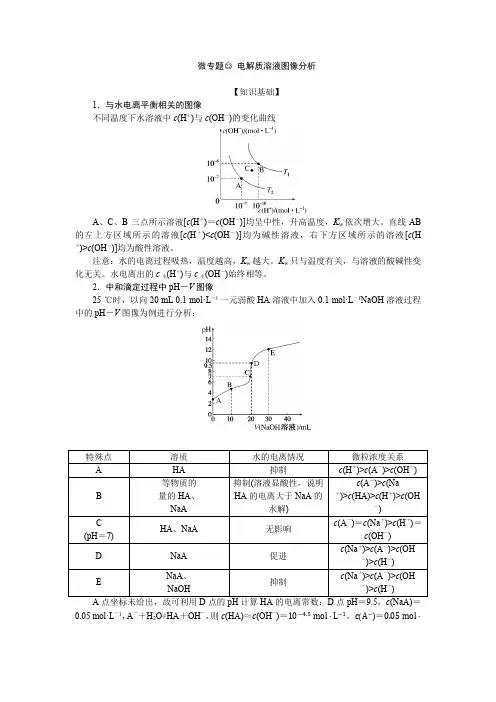
微专题○22电解质溶液图像分析【知识基础】1.与水电离平衡相关的图像不同温度下水溶液中c(H+)与c(OH-)的变化曲线A、C、B三点所示溶液[c(H+)=c(OH-)]均呈中性,升高温度,K w依次增大。
直线AB 的左上方区域所示的溶液[c(H+)<c(OH-)]均为碱性溶液,右下方区域所示的溶液[c(H +)>c(OH-)]均为酸性溶液。
注意:水的电离过程吸热,温度越高,K w越大。
K w只与温度有关,与溶液的酸碱性变化无关。
水电离出的c水(H+)与c水(OH-)始终相等。
2.中和滴定过程中pH-V图像25 ℃时,以向20 mL 0.1 mol·L-1一元弱酸HA溶液中加入0.1 mol·L-1NaOH溶液过程中的pH-V图像为例进行分析:0.05 mol·L-1,A-+H2O⇌HA+OH-,则c(HA)≈c(OH-)=10−4.5 mol·L−1,c(A−)=0.05 mol·L −1 −10−4.5mol ·L−1≈0.05 mol ·L −1,K h (A-)=c (HA )·c (OH −)c (A −)=10−4.5×10−4.50.05=2×10-8,则K a (HA)=K w K h (A −)=10−142×10−8=5×10−7。
3.分布分数图像分布分数图像一般是以pH 为横轴、分布分数(组分的平衡浓度占总浓度的分数)为纵轴的关系曲线,以草酸H 2C 2O 4为例,含碳元素的各组分分布分数(δ)与pH 的关系如图所示。
曲线含义分析:随着pH 的逐渐增大,溶质分子的浓度逐渐减小,酸式酸根离子浓度先逐渐增大后逐渐减小,酸根离子浓度逐渐增大,所以δ0表示H 2C 2O 4、δ1表示HC 2O 4−、δ2表示C 2O 42−。
特殊点的应用:对于物种分布分数图像,一般选择“交点”处不同微粒的等浓度关系,代入电离常数公式计算各级电离常数。



专题7-电解质溶液图像题真题演练1. 【2021广东选择考适应性测试9】. 叠氮酸(HN 3)与NaOH 溶液反应生成NaN 3。
已知NaN 3溶液呈碱性,下列叙述正确的是A. 0.01 mol·L -1HN 3溶液的pH=2 B. HN 3溶液的pH 随温度升高而减小 C. NaN 3 的电离方程式: NaN 3= Na ++3N 3-D. 0.01 mol·L -1 NaN 3溶液中: c (H +)+ c (Na + )= c (N 3-)+ c (HN 3) 【答案】B【解析】A .由题意,NaN 3溶液呈碱性,叠氮酸根(N 3-)会发生水解,说明HN 3为弱酸,在水溶液中不能完全电离,故0.01 mol·L -1 HN 3溶液的pH>2,A 错误;B .HN 3为弱酸,电离方程式为HN 3=H + +N 3-,电离是吸热过程,升高温度促进HN 3的电离,c (H +)增大, pH 减小,B 正确;C .NaN 3是强电解质,完全电离出Na +和N 3-,电离方程式为 NaN 3= Na ++ N 3-,C 选项错误;D .0.01 mol·L -1 NaN 3溶液中:由物料守恒 c (Na +)= c (N 3-)+ c (HN 3),故D 错误。
2.2.【2021重庆市学业水平选择性考试13】 草酸H 2C 2O 4是二元弱酸。
向100 mL 0.40 mol/L H 2C 2O 4溶液中加入1.0 mol/L NaOH 溶液调节pH ,加水控制溶液体积为200 mL 。
测得溶液中微粒的δ(x)随 pH 变化曲线如图所示,δ(x)=-2-2242424c(x)c(H C O )+c(HC O )+c(C O ),x 代表微粒H 2C 2O 4、HC 2O -4或C 2O 2-4。
下列叙述正确的是A. 曲线Ⅰ是HC 2O -4的变化曲线 B. 草酸H 2C 2O 4的电离常数K= 1.0×10-1.22C. 在 b 点,c(C 2O 2-4)+2c(OH -)= c(HC 2O -4)+c(H +) D. 在c 点,c(HC 2O -4)=0.06 mol/L 【答案】B【解析】A .当酸性越强时,曲线Ⅰ表示的微粒的含量越高,可推知曲线Ⅰ是H 2C 2O 4的变化曲线,曲线Ⅱ是HC 2O -4的变化曲线,曲线Ⅲ是C 2O 2-4的变化曲线,A 错误;B .在a 点H 2C 2O 4的浓度和HC 2O -4的浓度相等,pH=1.22,则草酸H 2C 2O 4的电离常K =()()()-24224c HC O ?c H c H C O+=()c H +=10-1.22,则B 正确;C .在 b 点,c(C 2O 2-4)= c(HC 2O -4),且溶液呈酸性,若c(C 2O 2-4)+2c(OH -)= c(HC 2O -4)+c(H +),则2c(OH -)= c(H +),显然不成立,C 错误;D .在c 点,HC 2O -4的含量为0.15,而H 2C 2O 4的物质的量为0.1L× 0.40 mol/L=0.04 mol,则HC 2O -4的物质的量为0.15×0.04 mol=0.006 mol,溶液体积为0.2L ,c(HC 2O -4)=0.006 mol÷0.2L=0.03 mol/L,D 错误。



电解质溶液图像专题电解质溶液的图像题,从知识载体的角度看:一可用于考查溶液中离子浓度的大小比较;二可考查溶液中离子浓度的守恒问题;三可考查有关电解质溶液的各种计算;四可结合生产和生活实际考查分离和提纯等具体的化学应用问题。
常见的图像题类型:1.pH(或pOH)—体积的变化曲线2.微粒分布分数(或系数)—pH(或pOH)的变化曲线3.浓度—浓度的变化曲线4.对数的变化曲线5.导电能力(或电导率) —体积(或浓度)变化曲线【练1】分布分数图:可以表示溶液中各种组分随pH的变化而变化的曲线。
1.25℃,c(CH3COOH)+c(CH3COO-)=0.1mol·L-1的一组醋酸和醋酸钠混合溶液,溶液中c(CH3COOH)、c(CH3COO-)与pH的关系如图所示。
下列有关离子浓度关系叙述正确的是()A.pH=5.5溶液中:c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-)B.W点表示溶液中:c(Na+)+c(H+)=c(CH3COOH)+c(OH-)C.pH=3.5溶液中:c(Na+)+c(H+)-c(OH-)+c(CH3COOH)=0.1mol·L-1D.向W点所表示的1.0L溶液中通入0.05molHCl气体(溶液体积变化可忽略):c(Na+)+c(H+)=c(CH3COOH)+c(OH-) +c(Cl-)2.草酸(H2C2O4)是一种易溶于水的二元中强酸,在水中它的存在形态有H2C2O4、HC2O4-、C2O42-,各形态的分布系数(浓度分数)α随溶液pH变化的关系如图所示:(1)图中曲线1表示的分布系数变化;曲线3表示的分布系数变化.现有物质的量浓度均为0.1mol/L的下列溶液:①Na2C2O4 ②NaHC2O4 ③H2C2O4 ④(NH4)2C2O4 ⑤NH4HC2O4 已知NaHC2O4溶液显酸性.(2)Na2C2O4溶液中,c(Na+)/c(C2O42-) 2 (填“>”、“=”、“<”),原因是(用离子方程式表示).(3)常温下,向10mL 0.1mol/L H 2C 2O 4溶液中滴加0.1mol/L NaOH 溶液,随着NaOH 溶液体积的增加,当溶液中c (Na +)=2c (C 2O 42-)+c (HC 2O 4-)时,溶液显 性(填“酸”、“碱”或“中”),且V (NaOH ) 10mL (填“>”、“=”或“<”).(4)下列关于五种溶液的说法中,正确的是A .溶液②中,c (C 2O 42-)<c (H 2C 2O 4)B .溶液②中,c (H 2C 2O 4)+c (OH -)=c (C 2O 42-)+c (H +)C .溶液④⑤中都符合c (NH 4+)+c (H +)=c (HC 2O 4-)+2c (C 2O 42-)+c (OH -)D .五种溶液都符合c (H 2C 2O 4)+c (HC 2O 4-)+c (C 2O 42-)=0.1mol ·L -1.(5)五种溶液中c (H 2C 2O 4)由大到小排列的顺序是具体解法:“四看三联系一注意”:四看:(1)先看图像的面与线,面要看横坐标和纵坐标的含义,线要看各组分浓度随pH 的变化趋势(2)再看图像的点,点要看起点,终点和交点对应的pH(3)点还要看最高点和最低点对应的pH 和各组分存在的pH 范围(4)最后看各条曲线相互重叠程度的大小三联系: 找出某个pH 对应的成分后再联系电离平衡和水解平衡的规律进行判断;一注意: 答题时还要特别注意在图表中没有提供的信息或潜在信息。
专题练习8 电解质溶液的图表类综合题(一)弱电解质的电离平衡部分1.某醋酸溶液的pH=a,将此溶液稀释1倍后,溶液的pH=b,则a>b (×)2.在滴有酚酞溶液的氨水里,加入NH4Cl至溶液恰好无色,则此时溶液的pH<7 (×)3.1.0×10-3mol·L-1盐酸的pH=3.0,1.0×10-8mol·L-1盐酸的pH=8.0 (×)4.25 ℃时若1 mL pH=1的盐酸与100 mL NaOH溶液混合后,溶液的pH=7,则NaOH溶液的pH=11(√)5.分别和等物质的量的盐酸和硫酸反应时,消耗NaOH的物质的量相同(×)6.pH=4的醋酸加水稀释过程中,所有离子浓度都降低(×)7.0.1 mol·L-1 CH3COOH溶液中加入冰醋酸,醋酸的电离程度变小(√)8.在室温下,CH3COOH分子可以完全以分子的形式存在于pH=8的溶液中(×)9.强电解质溶液中没有分子,只有离子(×)(二)水的电离和溶液的pH部分1.pH=6的溶液呈酸性(×)2.只要是纯水,肯定呈中性(√)3.纯水的pH=7 (×)4.无论在酸溶液中还是碱溶液中,由水电离出的c(H+)=c(OH-) (√)5.pH=0,溶液中c(H+)=0 mol·L-1 (×)6.某溶液中滴入酚酚呈无色,溶液呈酸性(×)7.用pH试纸测定溶液的pH值,不能用水浸湿,否则一定会产生误差(×)8.pH=5.6的CH3COOH与CH3COONa混合溶液中,c(Na+) >c(CH3COO-) (×)9.两种醋酸的物质的量浓度分别为c1和c2,pH分别为a和a+1,则c1=10c2 (×)10.将Ca(OH)2的饱和溶液加热,pH和K w均增大(×)(三)盐类水解部分1.NaHS水溶液中只存在HS-的电离和水解两种平衡(×)2.在饱和氨水中加入同浓度的氨水,平衡正向移动(×)3.HA比HB更难电离,则NaA比NaB的水解能力更强(√)4.HA-比HB-更难电离,则NaHA溶液的pH值一定比NaHB溶液的大(×)5. 常温下,pH=1的CH3COOH溶液与pH=2的CH3COOH溶液相比,两溶液中由H2O电离出的c(H+)是10∶1 (×)6.常温下,pH=2与pH=3的CH3COOH溶液,前者的c(CH3COOH)是后者的10倍(×)7.强电解质溶液中一定不存在电离平衡(×)8.改变条件使电离平衡正向移动,溶液的导电能力一定增强(×)9.只有pH=7的溶液中才存在c(H+)=c(OH-) (×)10.将NH4Cl溶于D2O中,生成物是NH3·D2O和H+(×)11.常温下,pH=7的氯化铵和氨水的混合溶液中,离子浓度顺序为:c(NH+4)=c(Cl-)>c(OH-)=c(H+) (√)12.中和pH和体积均相同的盐酸和醋酸,消耗NaOH的体积相同(×)13.常温下,同浓度的Na2S和NaHS,前者的pH大(√)14.0.1 mol·L-1的CH3COOH溶液加水稀释,CH3COOH的电离平衡向正反应方向移动,n(H+)增大(√)15.25 ℃时,将pH=3的HA和pH=11的BOH等体积混合,所得溶液的pH<7,则NaA溶液的pH>7(√)16.将AlCl3溶液和Na2SO3溶液分别蒸干并灼烧,得到Al2O3和Na2SO3 (×)17.在NaHSO4溶液中,c(H+)=c(OH-)+c(SO2-4) (√)18.常温下,向10 mL pH=12的氢氧化钠溶液中加入pH=2的HA至pH=7,所得溶液的总体积≤20 mL(√)19.常温下,等体积的盐酸和CH3COOH的pH相同,由水电离出的c(H+)相同(√)20. CH3COONa和CH3COOH以任意比例混合,都有c(Na+)+c(H+)=c(CH3COO-)+c(OH-)(√) 21.同c(NH+4)的溶液:①NH4Al( SO4)2②NH4Cl ③NH3·H2O④CH3COONH4溶液,物质的量浓度最大的是③(√)22.溶液均为0.1 mol·L-1的①CH3COOH②NH4Cl ③H2SO4三种溶液中,由水电离出的c(H+):②>①>③(√)23.常温下,体积和浓度都相同的盐酸和CH3COOH,中和NaOH的能力盐酸强(×)24.将纯水加热,K w变大,pH变小,酸性变强(×)25.0.1 mol·L-1氨水中加入CH3COONH4固体,c(OH-)/c(NH3·H2O)比值变大(×)26.用标准NaOH溶液滴定未知浓度的CH3COOH到终点时,c(Na+)=c(CH3COO-) (×)27.室温时,将x mL pH=a的稀NaOH溶液与y mL pH=b的稀盐酸混合充分反应,若x=10y,且a+b =14,则pH>7 (√)28.酸性溶液中不可能存在NH3·H2O分子(×)29.NH4HSO4溶液中各离子浓度的大小关系是c(H+)>c(SO2-4)>c(NH+4)>c(OH—) (√)30.某温度下,Ba(OH)2溶液中,K w=10-12,向pH=8的该溶液中加入等体积pH=4的盐酸,混合溶液的pH=7 (×)31.任意稀盐酸溶液中c(H+)的精确计算式可以表示为c(H+)=c(Cl-)+K w/c(H+) (√)32.将pH=3的盐酸和pH=3的醋酸等体积混合,其pH=3 (√)33.室温时,向等体积pH=a的盐酸和pH=b的CH3COOH中分别加入等量的氢氧化钠后,两溶液均呈中性,则a>b (×)34.物质的量浓度相等的CH3COOH和CH3COONa溶液等体积混合:2c(Na+)=c(CH3COOH)+c(CH3COO -) (√)35.常温下,NaB溶液的pH=8,c(Na+)-c(B-)=9.9×10-7 mol·L-1 (√)36.在一定条件下,某溶液的pH=7,则c(H+)一定为1×10-7mol·L-1,其溶质不可能为NaOH(×)37.常温下,浓度均为0.2 mol·L-1的NaHCO3和Na2CO3溶液中,都存在电离平衡和水解平衡,分别加入NaOH固体恢复到原来的温度,c(CO2-3)均增大(√)38.已知乙酸(HA)的酸性比甲酸(HB)弱,在物质的量浓度均为0.1 mol·L-1的NaA和NaB混合溶液中,有c(Na+)>c(B-)>c(A-)>c(OH-)>c(HA)>c(HB)>c(H+) (√)39.pH相同的CH3COONa溶液、C6H5ONa溶液、Na2CO3溶液、NaOH溶液,其浓度:c(CH3COONa)>c(C6H5ONa)>c(Na2CO3)>c(NaOH) (√)40.一定温度下,pH相同的溶液,由水电离产生的c(H+)相同(×)1.下表是几种弱电解质的电离平衡常数、难溶电解质的溶度积K sp(25 ℃)。
电解质溶液的图像题集————————————————————————————————作者:————————————————————————————————日期:电解质溶液图像表格题集一、选择题1.一定温度下,水溶液中H+和OH-的浓度变化曲线如图。
下列说法正确的是() A.升高温度,可能引起由c向b的变化B.该温度下,水的离子积常数为1.0×10-13C.该温度下,加入FeCl3可能引起由b向a的变化D.该温度下,稀释溶液可能引起由c向d的变化2.如图曲线a和b是盐酸与氢氧化钠的相互滴定的滴定曲线,下列叙述正确的是() A.盐酸的物质的量浓度为1 mol·L-1B.P点时反应恰好完全,溶液呈中性C.曲线a是盐酸滴定氢氧化钠的滴定曲线D.酚酞不能用作本实验的指示剂3.常温下,向20 mL某盐酸溶液中逐滴加入0.1 mol·L-1的氨水,溶液pH的变化与加入氨水的体积关系如图所示,下列叙述正确的是()A.盐酸的物质的量浓度为1 mol·L-1B.在①、②之间的任意一点:c(Cl-)>c(NH+4),c(H+)>c(OH-)C.在点②所示溶液中:c(NH+4)=c(Cl-)>c(OH-)=c(H+),且V<20D.在点③所示溶液中:由水电离出的c(OH-)>10-7 mol·L-14.室温下向10 mL 0.1 mol·L-1 NaOH溶液中加入0.1 mol·L-1的一元酸HA,溶液pH的变化曲线如图所示。
下列说法正确的是()A.a点所示溶液中c(Na+)>c(A-)>c(H+)>c(HA)B.a、b两点所示溶液中水的电离程度相同C.pH=7时,c(Na+)=c(A-)+c(HA)D.b点所示溶液中c(A-)>c(HA)5.水的电离平衡曲线如图所示,下列说法正确的是()A.图中五点的K w的关系:b>c>a>d>eB.若从a点到d点,可采用:温度不变在水中加入少量的酸C.若从a点到c点,可采用:温度不变在水中加入适量的CH3COONa固体D.处在b点时,将0.5 mol·L-1的H2SO4溶液与1 mol·L-1的KOH溶液等体积混合后,溶液显酸性6.室温下,用相同浓度的NaOH溶液,分别滴定浓度均为0.1 mol·L-1的三种酸(HA、HB 和HD)溶液,滴定曲线如图所示,下列判断错误的是()A.三种酸的电离常数关系:K HA>K HB>K HDB.滴定至P点时,溶液中:c(B-)>c(Na+)>c(HB)>c(H+)>c(OH-)C.pH=7时,三种溶液中:c(A-)=c(B-)=c(D-)D.当中和百分数达100%时,将三种溶液混合后:c(HA)+c(HB)+c(HD)=c(OH-)-c(H+)7.298 K时,在20.0 mL 0.10 mol·L-1氨水中滴入0.10 mol·L-1的盐酸,溶液的pH与所加盐酸的体积关系如图所示。
已知0.10 mol·L-1氨水的电离度为1.32%,下列有关叙述正确的是A.该滴定过程应该选择酚酞作为指示剂B.M点对应的盐酸体积为20.0 mLC.M点处的溶液中c(NH+4)=c(Cl-)=c(H+)=c(OH-)D.N点处的溶液中pH<128.如图曲线a和b是盐酸与氢氧化钠溶液相互滴定的滴定曲线,下列叙述不正确的是() A.盐酸的物质的量浓度为0.1 mol·L-1B.P点时恰好完全中和,溶液呈中性C.曲线a是盐酸滴定氢氧化钠溶液的滴定曲线D.酚酞或甲基橙均可以用作本实验的指示剂9.下图表示水中c(H+)和c(OH-)的关系,下列判断错误的是()A.两条曲线间任意点均有c(H+)×c(OH-)=K wB.M区域内任意点均有c(H+)<c(OH-)C.图中T1<T2D.XZ线上任意点均有pH=710.室温下,0.1 mol·L-1的某二元酸H2A溶液中,可能存在的含A粒子(H2A、HA-、A2-)的物质的量分数随pH变化的关系如图所示,下列说法正确的是()A.H2A的电离方程式:H2A H++HA-B.pH=5时,在NaHA和Na2A的混合溶液中:c(HA-)∶c(A2-)=1∶100C.等物质的量浓度的NaHA和Na2A溶液等体积混合,离子浓度大小关系为:c (Na +)>c (HA -)>c (A 2-)D .Na 2A 溶液必存在c (OH -)=c (H +)+c (HA -)+2c (H 2A),各粒子浓度均大于0 11.浓度均为0.10 mol·L -1、体积均为V 0的MOH 和ROH 溶液,分别加水稀释至体积V ,pH 随lg VV 0的变化如图所示。
下列叙述错误的是( )A .MOH 的碱性强于ROH 的碱性B .ROH 的电离程度:b 点大于a 点C .若两溶液无限稀释,则它们的c (OH -)相等 D .当lg VV 0=2时,若两溶液同时升高温度,则c M +c R +增大12.常温下,0.2 mol·L-1的一元酸HA 与等浓度的NaOH 溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示。
下列说法正确的是( )A .HA 为强酸B .该混合溶液pH =7.0C .该混合溶液中:c (A -)+c (Y)=c (Na +) D .图中X 表示HA ,Y 表示OH -,Z 表示H +13.常温下,用0.100 0 mol·L -1NaOH 溶液分别滴定20.00 mL 0.100 0 mol·L -1盐酸和20.00 mL 0.100 0 mol·L -1醋酸溶液,得到2条滴定曲线,如图所示。
若以HA 表示酸,下列说法正确的是( )A .滴定盐酸的曲线是图乙B .达到B 、D 点所处状态时,两溶液 中离子浓度均为c (Na +)=c (A -)C .达到B 、E 状态时,反应消耗的n (CH 3COOH)>n (HCl)D .当0 mL<V (NaOH)<20.00 mL 时,对应混合溶液中各离子浓度由大到小的顺序均为: c (A -)>c (Na +)>c (H +)>c (OH -)14.室温下,将一元酸HA 的溶液和KOH 溶液等体积混合(忽略体积变化),实验数据如下表:下列判断不正确的是( )A .实验①反应后的溶液中:c (K +)>c (A -)>c (OH -)>c (H +)B .实验①反应后的溶液中:c (OH -)=c (K +)-c (A -)=K W 1×10-9 mol·L -1 C .实验②反应后的溶液中:c (A -)+c (HA)>0.1 mol·L -1实验编号 起始浓度/(mol·L -1) 反应后溶液的pHc (HA) c (KOH) ① 0.1 0.1 9 ②x0.27D.实验②反应后的溶液中:c(K+)=c(A-)>c(OH-) =c(H+)15.40 ℃,在氨-水体系中不断通入CO2,各种离子的变化趋势如下图所示。
下列说法不正确的是()A.在pH=9.0时,c(NH+4)>c(HCO-3)>c(NH2COO-)>c(CO2-3)B.随着CO2的通入,c OH-c NH3·H2O不断增大C.不同pH的溶液中存在关系:c(NH+4)+c(H+)=2c(CO2-3)+c(HCO-3)+c(NH2COO-)+c(OH-)D.在溶液pH不断降低的过程中,有含NH2COO-的中间产物生成16.室温下,将一元酸HA溶液和NaOH溶液等体积混合,实验数据如表:实验编号起始浓度c(HA) 起始浓度c(NaOH) 反应后溶液的pH①0.1 mol·L-10.1 mol·L-19②x0.2 mol·L-17下列说法正确的是()A.实验①反应前HA溶液中:c(H+)=c(OH-)+c(A-)B.实验①反应后溶液中:c(A-)>c(Na+)C.实验②反应前HA溶液浓度:x=0.2 mol·L-1D.实验②反应后溶液中:c(A-)+c(HA)=c(Na+)17.已知Ag2SO4的K sp为2.0×10-5,将适量Ag2SO4固体溶于100 mL水中至刚好饱和,该过程中Ag+和SO2-4浓度随时间变化关系如下图[饱和Ag2SO4溶液中c(Ag+)=0.034 mol·L-1]。
若t1时刻在上述体系中加入100 mL 0.020 mol·L-1 Na2SO4溶液,下列示意图中,能正确表示t1时刻后Ag+和SO2-4浓度随时间变化关系的是(B)18.常温下,有关物质的溶度积如表所示。
物质CaCO3MgCO3Ca(OH)2Mg(OH)2Fe(OH)3K sp 4.96×10-9 6.82×10-6 4.68×10-6 5.61×10-12 2.64×10-39下列有关说法不正确的是()A.常温下,除去NaCl溶液中的MgCl2杂质,选用NaOH溶液比Na2CO3溶液效果好B.常温下,除去NaCl溶液中的CaCl2杂质,选用Na2CO3溶液比NaOH溶液效果好C.向含有Mg2+、Fe3+的溶液中滴加NaOH溶液,当两种沉淀共存且溶液的pH=8时,c(Mg2+)∶c(Fe3+)=2.125×1021D.无法利用Ca(OH)2制备NaOH19.一定温度下的难溶电解质A m B n在水溶液中达到沉淀溶解平衡时,其平衡常数:K sp=c m(A n+)·c n(B m-),称为难溶电解质的溶度积。
已知25 ℃时,以下五种物质的K sp:物质AgCl Ag2CrO4AgBr AgI Ag2SK sp2×10-102×10-12 5.4×10-138.3×10-17 6.3×10-50颜色白色砖红色淡黄色黄色黑色现以0.1 mol·L-1的AgNO3溶液测定某溶液中c(Cl-),适宜作滴定指示剂的物质是() A.K2CrO4B.KBr C.KI D.K2S20.已知难溶性物质K2SO4·MgSO4·2CaSO4在水中存在如下平衡:K2SO4·MgSO4·2CaSO4(s)2Ca2++2K++Mg2++4SO2-4,不同温度下,K+的浸出浓度与溶浸时间的关系如图所示,则下列说法错误的是()A.向该体系中加入饱和NaOH溶液,溶解平衡向右移动B.向该体系中加入饱和碳酸钠溶液,溶解平衡向右移动C.升高温度,反应速率增大,平衡向正反应方向移动D.该平衡的K sp=c(Ca2+)·c(K+)·c(Mg2+)·c(SO2-4)21.如图是碳酸钙(CaCO3)在25 ℃和100 ℃两种情况下,在水中的沉淀溶解平衡曲线。