第二单元 探秘水世界汇总
- 格式:ppt
- 大小:5.68 MB
- 文档页数:161


第二单元水和溶液一、水分子的运动1、水是由水分子构成的,水分子的运动导致了水的状态变化。
水分子获得能量,运动加快,间隙增大,由液态变为气态;失去能量,运动减慢,间隙减少,由气态变为液态。
2、固态的水:分子有序排列,分子在固定的位置上振动;液态的水:水分子无序排列,在一定的体积内较自由的运动;气态的水,水分子自由运动,充满整个容器。
3、分子是构成物质的和一种粒子,基本属性是:a)分子体积很小,质量轻,(如:1滴水中有1021个水分子)b)分子间有间隙,存在相互作用。
(如:气体受压,体积缩小)③分子总在不停地运动。
受热运动加剧,遇冷运动减慢。
(如:酒香不怕巷子深)4、水的三太变化是物理变化,仅是水分子之间的距离和分子的排列方式变化,水分子的大小和数目不会变化。
5、水分子存在的佐证-布朗的花粉运动6、水循环的动力是太阳能;水天然循环的作用①实现了水的自身净化②完成水资源的重新分配二、水资源、、水的净化(1)水资源A.地球表面71%被水覆盖,大约97.5%的水集中在海洋和咸水湖中但供人类利用的淡水占水总量的 0.3%B.海洋是地球上最大的储水库。
海水中含有80多种元素。
海水中含量最多的物质是H2O ,最多的金属元素是 Na ,最多的元素是 O 。
C.我国水资源的状况分布不均,人均量少。
(2)水的净化①天然水的净化成纯水的步骤:沉降;过滤;吸附;蒸馏效果由低到高的是静置沉降、过滤、吸附、蒸馏(均为物理方法),其中净化效果最好的操作是蒸馏。
②各步骤的作用:静置沉降-是除去较大颗粒的不溶性杂质,过滤-是除去不溶性杂质(较小颗粒的悬浮杂质用明矾吸附沉降再过滤)吸附-是利用活性炭除去水中有色或有气味的杂质;(吸附是物理变化)蒸馏-是除去可溶性杂质。
(3)自来水的净化步骤:①沉降②过滤③灭菌(为化学变化)消毒剂有:氯气、漂白粉、二氧化氯、紫外线。
(4)硬水与软水 A.定义硬水是含有较多可溶性钙、镁矿物质的水;(如:矿泉水)B软水C点燃 D .长期使用硬水的坏处:浪费肥皂,洗不干净衣服;锅炉容易结成水垢,不仅浪费燃料,还易使管道变形甚至引起锅炉爆炸。

第二单元探秘水世界复习复习目标: 1.知道分子、原子、离子是构成物质的微观粒子,理解三种粒子之间的关系,原子的内部结构,能用微粒的观点解释某些日常现象。
2.通过水的分解与合成,分析化学变化的实质,了解化合反应和分解反应的概念。
3.知道物质多样性,能进行简单的分类和区分。
4.记住常见元素的名称和符号及意义,知道元素的简单分类,初步认识元素周期表。
5.了解物质的称量方法(即天平和量筒的使用)、仪器的连接与洗涤。
复习重难点:1. 分子、原子、离子的特征,物质、分子、原子、离子、元素之间的相互关系。
2. 从组成上对物质进行简单的分类,学会分类的方法。
学前准备:多媒体教学素材过程设计:本单元的复习通过四个主题的活动完成(上面为流程图,下面为设计意图)。
复习过程:【活动一自主复习——相信你还记得】环节一:自主梳理感知1、整理知识的时候,为学生提供知识树结构图,让学生把本单元的重点知识填写在相应的位置(具体地址在课本上)。
2、依据学案,要求学生填写学案上的知识要点,进一步熟悉本单元的主要知识点。
(具体的题目的设置见附件)环节二:师生交流反馈组织学生以小组为单位进行反馈,根据相关知识点把学生自主整理和小组交流时收集到的资源及时矫正、渗透和点拨,同时对某些知识点进行一定的拓展和深究,让学生对知识的掌握从识记的层面上升到理解内化的层面。
【活动二合作探究】环节一:相信你会归纳教师组织学生就导学案上的相关内容进行合作探究,要求先填写知识资料,然后根据以上的相关资料归纳出物质、元素、分子、原子、离子之间的关系。
知识资料:请先填一填水是由元素组成的,是由构成的,水分子是由构成的。
铁是由元素组成的,是由直接构成的。
氯化钠是由元素组成的,是由构成的。
钠原子的最外层电子数是1,参加化学反应时易(填“得”或“失”)电子,变成。
氯原子的最外层电子数是7,参加化学反应时易(填“得”或“失”)电子,变成。
归纳要求:你能根据以上的相关资料归纳出物质、元素、分子、原子、离子之间的关系吗?试一试归纳填写。



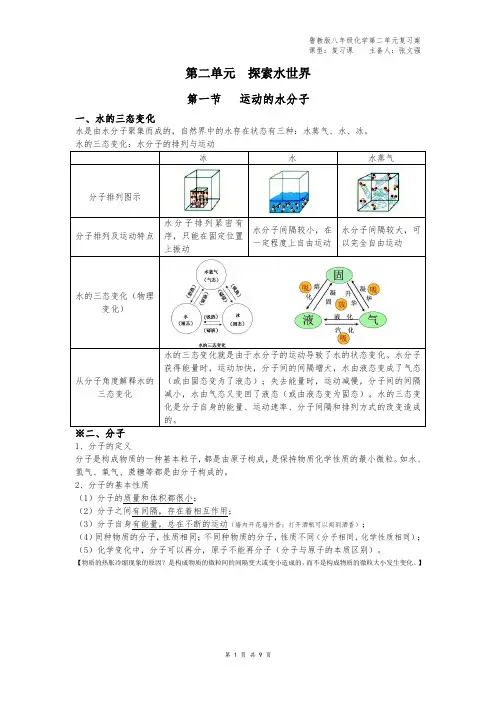
第二单元探索水世界第一节运动的水分子一、水的三态变化水是由水分子聚集而成的,自然界中的水存在状态有三种:水蒸气、水、冰。
冰水水蒸气分子排列图示分子排列及运动特点水分子排列紧密有序,只能在固定位置上振动水分子间隔较小,在一定程度上自由运动水分子间隔较大,可以完全自由运动水的三态变化(物理变化)从分子角度解释水的三态变化水的三态变化就是由于水分子的运动导致了水的状态变化。
水分子获得能量时,运动加快,分子间的间隔增大,水由液态变成了气态(或由固态变为了液态);失去能量时,运动减慢,分子间的间隔减小,水由气态又变回了液态(或由液态变为固态)。
水的三态变化是分子自身的能量、运动速率、分子间隔和排列方式的改变造成的。
1、分子的定义分子是构成物质的一种基本粒子,都是由原子构成,是保持物质化学性质的最小微粒。
如水、氢气、氧气、蔗糖等都是由分子构成的。
2、分子的基本性质(1)分子的质量和体积都很小;(2)分子之间有间隔,存在着相互作用;(3)分子自身有能量,总在不断的运动(墙内开花墙外香;打开酒瓶可以闻到酒香);(4)同种物质的分子,性质相同;不同种物质的分子,性质不同(分子相同,化学性质相同);(5)化学变化中,分子可以再分,原子不能再分子(分子与原子的本质区别)。
【物质的热胀冷缩现象的原因?是构成物质的微粒间的间隔变大或变小造成的,而不是构成物质的微粒大小发生变化。
】⎪⎪⎪⎩⎪⎪⎪⎨⎧⎪⎪⎩⎪⎪⎨⎧68%18.3%11.8%1.2%%5.2%5.97冰深层地下水浅层地下水河流湖泊等淡水海洋和咸水湖中的水天然水第二节 自然界中的水一、水的天然循环水的天然循环是通过水的三态变化实现的,是自动完成的循环过程。
太阳光为水分子提供能量,使其运动加快,达到一定程度后,些水分子便克服了分子之间的相互作用,变成水蒸气,扩散到空气中,在高空中遇冷凝结成云,再遇冷转变成雨或雪降落到地面。
大自然通过水分子的运动既实现了水的自身净化,又完成了水资源的重新分配。

第二单元探秘水世界复习课标要求:培养学生的微粒观、元素观内容。
学情分析:本单元培养学生从化学的视角认识物质世界的能力,本单元还穿插了一些科学方法、化学实验方法以及化学科学思想的教育内容。
例如,物质的分类(纯净物与混合物、单质与化合物)、混合物的分离与提纯(天然水的净化)。
教学目标:(1)本单元需要帮助学生对微粒观和元素观形成相关的认识。
(2)循序渐进引领学生从微粒的视角看物质及物质的变化。
(3)学会物质的分类。
学习目标:1.通过分析水分子的运动,认识分子的特性,理解状态变化这类物理变化的本质。
2.通过对“水的电解”和“氢气燃烧”实验的微观分析,初步揭示化学变化的本质。
重点:化学变化的实质。
复习准备:多媒体;导学案学习过程:【知识梳理】(一)、运动的水分子一、水的三态变化 1、水分子的运动导致了水的三态变化。
水分子获得______时,运动加快,分子间的______,水由_____变为_____;失去_____时,运动减慢,分子间的________,水由_____变回_______。
2、分子的性质:①____________,②____________,③_______________。
二、水的天然循环三、水的人工净化1、生活用水的净化方法一般有、、、等方法,其中净化效果最好的操作是。
自来水厂净化过程一般为:原水→→絮凝沉淀→反应沉淀→→→消毒→生活用水,其中过程为化学变化。
2、纯净物和混合物:黄泥水是由水、泥沙、矿物质等多种物质组成的,像这样由多种物质组成的物质成为_______,如等,在混合物中,各种物质都保持各自原有的性质。
由单一物质组成的物质称为_________。
如等。
3、混合物的分离:分离和提纯物质的方法很多,常用的有________、_________、__________等。
把__________与________分离可用过滤法,如分离黄泥水中的泥沙;把溶解在液体中的固体分离出来可以用_______的方法,如把食盐水放在蒸发皿中加热,食盐水中的水气化逸出,留下的就是食盐晶体;液体和液体的分离可以用___________,我国传统的烧酒工艺就要用到________,以便提高酒精的质量。


鲁教版(五四制)八年级全第二单元探秘水世界复习提纲
第二单元探秘水世界知识清单
概念:分子是保持物质化学性质的一种微粒(由分子构成的物质,分子保持物质
的化学性质)
基本特征(质量和体积都很小;有间隔
存,在相互作用;有能量,不断运
动;同种分子性质相同)
固态的水:水分子能量最低,间隔较小(特殊),相互作用强烈,分子排列
有序,在固定的位置震动液态的水:水分子能量较低,间隔较小,相互作
用强烈,水分子排列不固定,
在一定的空间内自由运动
气态的水:水分子能量较高,间隔较大,
相互作用很弱,在一定的空间内自
由运动。
水的三态变化:属于物理变化。
水分子
的能量变化,引起运动速率的改变,
从而使分子间隔发生改变,实现了
水的三态变化。
2、自然界中的水
是水分子运动的结果。
既实现了构
成
物
质
的
粒
分子
水分子
杀菌消毒:除去细菌和
病毒(化学变化Cl
2 ClO
2
O
3
)
蒸馏:利用各种成分沸
点不同加以分离。
工业:加入化学药品
家庭:煮沸鉴别方法:取等量的
水分别加入等量的肥皂水震荡,
泡沫高的为软水。
硬水
水的分解和合成
条件:水通直流电或加热到1800摄氏度以
上
条件:在空气中点燃纯净的氢气(验纯?)。
现象:在空气中燃烧,火焰淡蓝色,烧杯内
壁有水雾,烧杯壁发烫。
结果:氢气在空气
物理性质:物质不需要发生化学变化就表现出水
的
水
的
物
质。
第二单元探秘水世界复习知识点复习目标:1、知道水的三态变化的原因2、熟练掌握水的分解与合成的现象3、知道原子的复杂结构及相对原子质量4、知道物质由元素组成,,记住常见元素符号,知道元素周期表中各部分含义5、学会实验基本操作复习过程:【知识清单】一、运动的水分子1、分子(1)水的三态变化只是水分子的间隔和排列方式发生改变,水分子本身没变所以水的三态变化是物理变化(2)、分子的特征:①分子很小,质量和体积都很小。
②分子总是在不停地运动,并且温度越高,分子的能量越大,运动速度也就越快。
③分子间有间隔。
气体分子间的间隔大,液体和固体分子间的间隔小(3)、用分子知识解释物理变化和化学变化物理变化:分子本身没有改变,只是分子的间隔和排列方式改变.如水的蒸发化学变化:分子本身变了,变成了其他物质的分子.如水的电解2、水的净化(1)水的净化方法:①、沉降:加入絮凝剂明矾吸附杂质(吸附沉淀)②、过滤:分离不溶性固体与液体物质组成的混合物(注意:“一贴”“二低” “三靠”)需要的仪器有铁架台、烧杯、漏斗、玻璃棒(引流)③、吸附:活性炭可以吸附色素而使液体变无色,也可以除臭味。
(物理变化)④、消毒(加氯气),属于化学变化。
⑤、蒸馏:除去可溶性杂质,净化程度最高(2)分离和提纯物质的方法:①过滤:分离不溶性固体与液体②蒸馏:分离液体与液体③蒸发:分离可溶性固体与液体(3)硬水和软水①鉴别:分别加入肥皂水,易起泡沫的为软水,不易起泡沫的为硬水②硬水的软化方法:煮沸或蒸馏二、水的分解与合成1、水的分解(1)电解水反应的文字表达式为属于分解反应(2)、氢负氧正,氢2氧1电解水实验,正负两极气体体积比为1:2。
负极气体为氢气可燃烧,产生淡蓝色的火焰,正极气体为氧气能使带火星的木条复燃。
此实验证明:水是由氢氧元素组成的,还可以证明在化学变化中分子可以再分,原子不可再分,原子是化学变化中的最小粒子。
(3)水的组成:水是纯净物,是一种化合物。
第二单元探秘水世界(复习提纲)一、运动的水分子1、水的三态变化:冰→水→水蒸气(吸收热量)水蒸气→水→冰(放出热量)2、水的天然循环:能量来源:太阳能作用:净化水、调节水资源平衡3、水的人工净化:A、沉降:除去大颗粒固体B、过滤:分离不溶性固体和液体(一贴二低三靠)C、吸附:除去色素和异味D、蒸馏:据各成分沸点不同分离E、蒸发:从溶液中分离出可溶性固体F、除菌:利用化学变化除去细菌等4、如何区别硬水和软水:用肥皂水(硬水会出现大量白色沉淀物)二、物质的分类1、混合物:由多种物质组成,没有固定的组成,没有固定的熔沸点。
纯净物:由一种物质组成,有固定的化学式,有固定的熔沸点。
单质:由一种元素组成的纯净物。
化合物:由多种元素组成的纯净物。
2、分类关系混合物物质单质(金属、非金属、稀有气体)纯净物化合物(氧化物:二元必有氧)三、水的组成1、水的分解(电解水)A、反应原理:2H2O=2H2↑+O2↑(分解反应:一变多)B、两极产生的气体:负氢正氧、氢二氧一(体积比)C、两种气体的检验:氧气:能使带火星的木条复燃氢气:能被点燃并产生淡蓝色火焰2、水的合成+O2=2H2O(化合反应:多变一)A、反应原理:2H2B、现象:产生淡蓝色火焰并放热3、上述两个实验得出的结论:水是由氢、氧两种元素组成的。
四、水的构成1、水由水分子构成、水分子由氢原子和氧原子构成。
2、原子内部结构:质子(带正电)原子核原子中子(不带电)核外电子(带负电)3、原子内部的几个等量关系:核电荷数=质子数=核外电子数=原子序数相对原子质量=质子数+中子数4、原子结构示意图:金属:最外层电子数一般少于4个、易失电子、带正电、化合价显正价非金属:最外层电子数一般大于4个、易得电子、带负电、化合价显负价稀有气体:最外层电子数为8个(稳定结构)、不易得失电子、性质稳定结论:最外层电子数决定元素原子的化学性质。
5、分子、原子、离子的特点:A、体积小、质量小B、在不断的运动C、相互之间有间隙五、元素1、元素的概念:含有相同质子数的一类原子的总称。
第二单元探秘水世界第一节运动的水分子1、水的三态变化,水蒸气、水、冰这三种状态在一定条件下可以相互转化。
2、水分子的运动导致了水的三态变化。
水分子获得能量时,运动加快,分子间的间隔增大,相互作用减弱,水由液态变为气态,失去能量时,运动减慢,分子间的间隔减小,相互作用增强,水又由气态变回液态。
这个过程中没有新物质生成,是物理变化。
3、分子是构成物质的一种基本粒子,由原子构成。
水、二氧化碳、氢气、氧气、蔗糖都是由分子构成。
有的物质由原子直接构成,如铁、硅、碳、氦气等。
4、分子的特征(1)分子的质量和体积都很小。
(2)分子间有间隔。
(3)分子间存在着相互作用。
(4)分子总是在不断运动。
运动速度与温度有关。
温度越高运动越快。
(5)同种分子性质相同,不同种分子性质不同。
5、用分子的性质解释生活中的现象。
(1)分子的质量和体积都很小,一滴水中含1021个水分子,水能透过滤纸。
(2)分子间有间隔。
热胀冷缩、不同液体混合总体积减小。
气体容易补压缩,阳光下轮胎爆炸。
(3)分子总是在不断运动:很远闻到花香,挥发,扩散,溶解第二节自然界中的水一、水的天然循环水的天然循环是通过三态变化实现的。
太阳为水分子提供能量,大自然通过水分子的运动,既实现了水的自身净化,又完成了水资源的重新分配。
二、水的净化方法1、水的净化过程:①沉降(除去水中颗粒较大的不溶性杂质),(明矾:絮凝剂,促进悬浮物质的沉降)②过滤(除去水中不溶性固体杂质)③吸附(除去水中的色素或异味的物质)、(活性炭:表面疏松多孔)④消毒杀菌。
(液氯、漂白粉。
化学变化)⑤蒸馏(除去水中可溶性杂质,净化程度最高---得到的是蒸馏水)、2、分离物质的方法:(1)过滤:分离颗粒大小不同的混合物的方法。
如不溶性固体和液体。
仪器:铁架台、烧杯、漏斗、滤纸、玻璃棒操作要点:“一贴”、“二低”、“三靠”“一贴”滤纸紧贴漏斗内壁;“二低”①滤纸边缘低于漏斗边缘②液面稍低于滤纸边缘;“三靠”①倾倒液体时,烧杯嘴紧靠玻璃棒;②玻璃棒轻靠三层滤纸一边;(防止玻璃棒将滤纸划破,玻璃棒起的作用引流)③漏斗下端管口紧靠烧杯内壁。
第二单元-探秘水世界-知识-CAL-FENGHAI-(2020YEAR-YICAI) JINGBIAN第二单元探秘水世界一、运动的水分子1、水的三态变化:①水分子的排列与运动②水分子的运动导致了水的三态变化。
③用分子观点解释水的三态变化:水分子获得能量,运动速率加快,分子间隔增大,水由固态变为液态(或由液态变为气态)。
水分子失去能量,运动速率减慢,分子间隔减小,水由气态变为液态(或由液态变为固态)。
2、分子的性质:①分子的体积、质量小。
②分子之间有间隔,存在相互作用。
③分子自身有能量,总在不断运动。
④同种物质的分子,性质相同;不同种物质的分子,性质不同。
⑤化学变化中,分子可以再分,原子不能再分子。
(分子与原子的本质区别)3、分子性质的应用:解释宏观现象误区:物质的热胀冷缩现象的原因是构成物质的微粒间的间隔变大或变小造成的,而不是构成物质的微粒大小发生变化。
二、自然界中的水1、水的天然循环:过程:太阳为水提供能量,水通过三态变化,实现自身的天然循环。
地球上的水通过海水蒸发、土壤蒸发、植物蒸腾作用、冰雪升华等形成水蒸气扩散到空气中,并在空气中凝结成云,遇冷后以雨雪的形式再降到地面以及江河湖海。
意义:既实现了水的自身净化,乂完成了水资源的重新分配。
2、水的人工净化:(1)沉降(颗粒较大的不溶性杂质)明矶:一种净水剂,溶于水后可促进水中悬浮杂质的沉降,从而起到一定的净水作用。
[溶于水形成胶状物吸附杂质,加速沉降](2)过滤(颗粒较小的不溶性杂质)一贴:滤纸紧贴漏斗内壁(加快过滤的速率)二低:①滤纸边缘低于漏斗边缘(防止滤纸被润湿后破损)②漏斗内液面低于滤纸边缘(防止液体从滤纸与漏斗间隙流下,过滤失败)三靠:①烧杯紧靠引流的玻璃棒(防止液体溅到漏斗外面)②玻璃棒下端紧幕三层滤纸处(防止玻璃棒戳破滤纸)③漏斗末端管口长角紧靠烧杯内壁(防止液体溅出)(3)吸附(颜色、异味)活性炭:疏松多孔表面积很大,具有较强的吸附作用。
第二单元探秘水世界期末考点大串讲一、运动的水分子1.水的三态变化实质:水分子本身没有发生变化,改变的只是水分子之间的间隔,没有新物质生成,属于物理变化。
在运动过程中伴随着能量的变化。
2.水的天然循环水的天然循环是通过其三态变化实现的。
3.爱护水资源地球上水资源总量很丰富,但真正可供人类利用的河水、淡水湖泊水以及浅层地下水等只占0.7%左右,而且分布不均衡;我国淡水资源相对丰富,但人均淡水量少,并且分布不均衡,部分地区严重缺水,面对如此严峻的水资源形势,我们应该爱护水资源。
爱护水资源一方面要节约用水,另一方面要防止水体污染。
(1)节约用水的方法工业上:用水循环使用农业上:采用喷灌和滴灌代替漫灌来灌溉作物生活上:注意水的二次利用(2)水的污染及防治水污染的原因防治办法工业上生产中废水、废渣、废气的任意排放工业“三废”要经过处理后再排放农业上农药、化肥的不合理使用农业上合理使用农药、化肥生活中生活污水的随意排放生活污水要经过集中处理后再排放4.天然水的人工净化净化方法原理作用沉降静置沉降,使难溶性大颗粒物质沉淀下来,与水分离除去大颗粒不溶性物质吸附沉降,加入净水剂明矾,使难溶性的小颗粒不溶物质沉降下来除去小颗粒不溶性物质过滤把不溶于液体的固体物质与液体进行分离除去难溶性物质吸附利用活性炭的吸附作用除去自然界水中的一些色素和异味物质除去色素和异味蒸馏利用混合物中各成分的沸点不同将其分离除去各种杂质(净化程度最高)注意:上述过程均是物理变化,其中净化程度最高的是蒸馏。
5.过滤、蒸发和蒸馏(1)过滤操作要点:一贴、二低、三靠一贴:滤纸紧贴漏斗内壁;——加快过滤速度二低:滤纸边缘低于漏斗边缘,液面低于滤纸边缘;三靠:倾倒滤液的烧杯尖嘴紧靠玻璃棒(目的:防止液体溅出),玻璃棒紧靠三层滤纸处(目的:防止戳破滤纸),漏斗下端管口紧靠烧杯内壁(目的:防止滤液溅出)。
注意:过滤只能除去不溶性杂质,无法除去可溶性杂质。
(2)蒸馏用于分离液体混合物的方法原理:利用液体混合物中各组分沸点不同,使低沸点组分先蒸发,再冷凝,以分离整个组分。