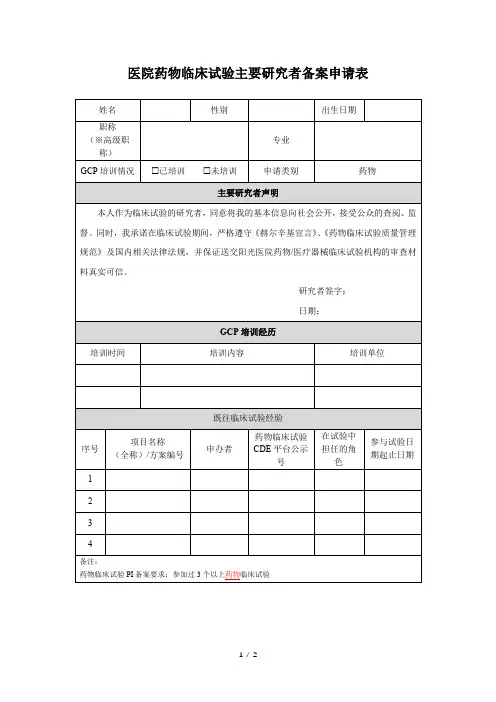
医院药物临床试验主要研究者备案申请表
- 格式:docx
- 大小:14.43 KB
- 文档页数:2


研究人员变更申请
吉林大学第一医院药物临床试验机构:
由***科负责承担的名称为“****”项目(申办者:***),已通过吉林大学第一医院伦理委员会审核,同意在吉林大学第一医院***科开展,主要研究者***主任,现因***主任工作***,无法继续承担该试验项目的主要研究者工作,故向吉林大学第一医院药物临床试验机构申请将该项目主要研究者变更为***主任。
现任主要研究者:
日期:
拟任主要研究者:
日期:
--------------------申请回执---------------------- 吉林大学第一医院药物临床试验机构意见:
签名:日期:。


滨州医学院附属医院国家药物临床试验机构文件编码:JG-SOP-005-3.0
药物临床试验审批表
项目名称
申办者CRO
药物名称剂型规格
研究分期注册分类
专业科室主要研究者
形式审查资料目录:
□临床试验申请表□SFDA批件、组长单位批件
□委托公函□申办者及CRO资质
□研究者手册□药检报告
□临床试验方案□研究者简历
□知情同意书□病例报告表
□研究病历□药品说明书
□受试者日记卡□招募广告
□监查员名片、GCP培训证书、身份证及学位证复印件
□如果样本在外地检测的要提供检测实验室的名称和资质证明;
□其它
机构办公室秘书形式审查意见:
签字:日期:年月日机构办公室主任对立项审核要点:
1.本项目主要研究者是否已对项目充分了解,提交了申请并做出试验相关保证?□是□否
2.本专业组在研项目数量是否符合要求?□是□否
3.本项目监查员是否被机构认可?□是□否
4.本项目是否在机构进行过充分讨论?□是□否
5.关于项目费用分配问题,机构是否已了解并初步同意?□是□否
6.提交的备案资料是否还存在不全或者不符合要求等问题?□是□否
7.本项目是否存在需要说明或者有争议的问题?□是□否如存在,请简单说明:。
机构办公室主任意见:
□同意□不同意□补充完善资料后同意□修改部分内容后同意
□其他:
签字:日期:年月日机构主任意见:
□同意□不同意□其他:
签字:日期:年月日。
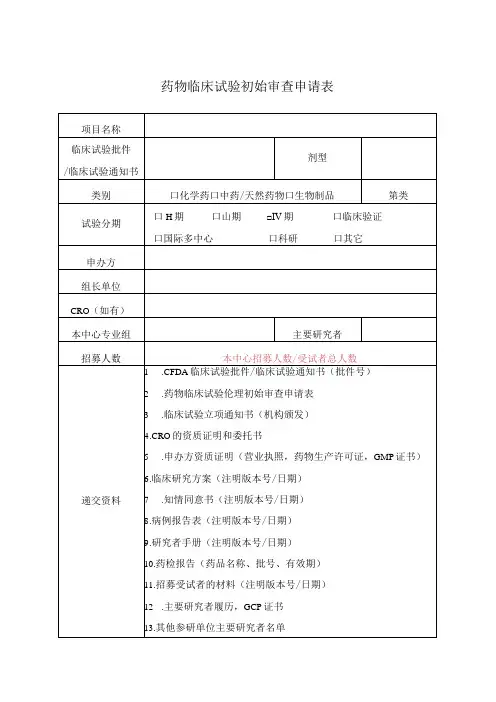
药物临床试验初始审查申请表
备注:(递交资料时删除备注内容)
1.提供全套资料贰份,并盖章(首页盖章+骑缝章),同时提供电子版一套(PDF版)。
使用两孔文件夹装订,附隔页纸。
2.另附方案、知情同意书、保险和招募受试者的材料(如有)一式12份。
使用拉杆夹装订,附隔页纸。
3.所需标注处,使用区进行标记。
4.有版本号/版本日期的资料,必须填写版本号/版本日期。
医疗器械临床试验伦理审查申请表
备注:(递交资料时删除备注内容)
1.提供全套资料贰份,并盖章(首页盖章+骑缝章),同时提供电子版一套(PDF版)。
使用两孔文件夹装订,附隔页纸。
2.另附方案、知情同意书、保险和招募受试者的材料(如有)一式12份。
使用拉杆夹装订,附隔页纸。
5.所需标注处,使用区进行标记。
6.有版本号/版本日期的资料,必须填写版本号/版本日期。