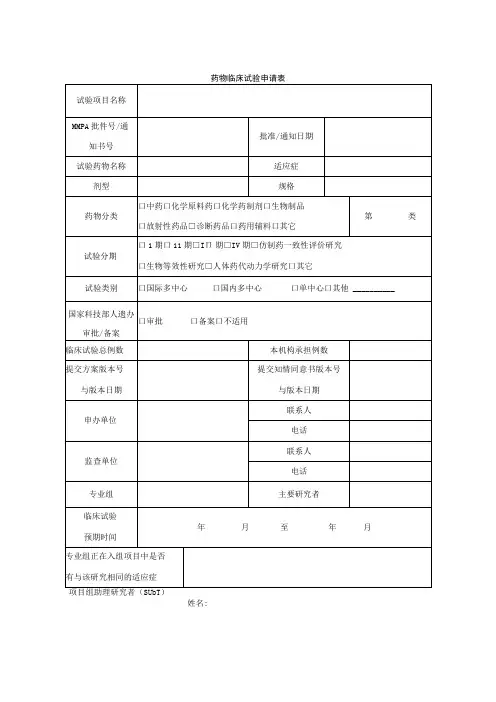
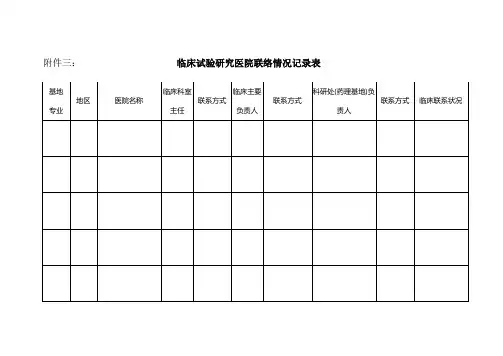
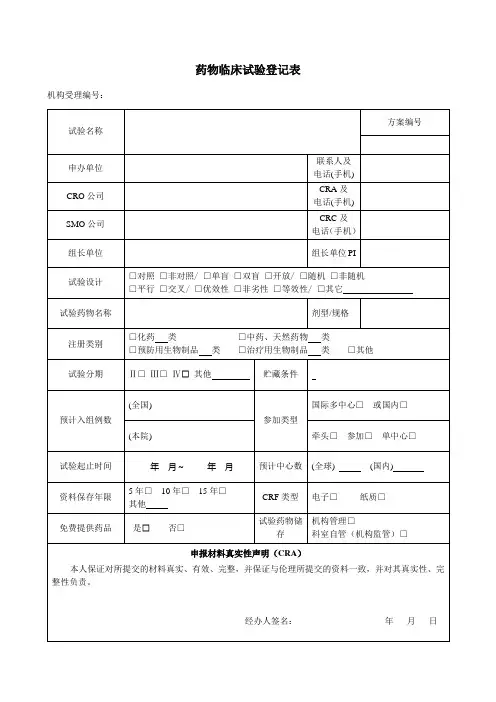
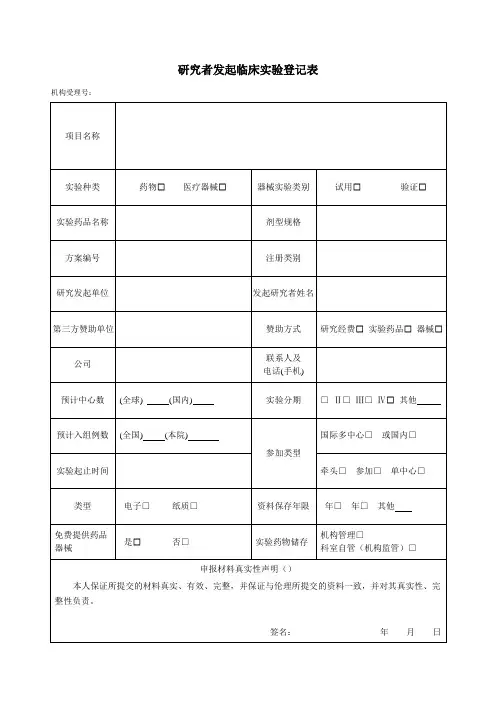
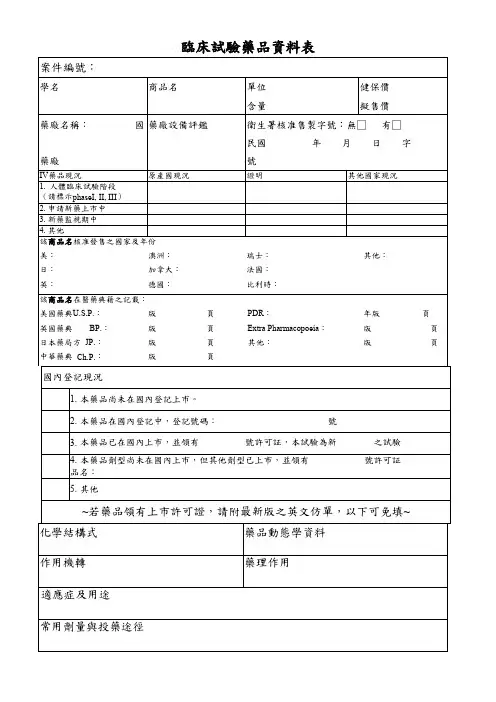
药物临床试验登记表
- 格式:doc
- 大小:60.00 KB
- 文档页数:2

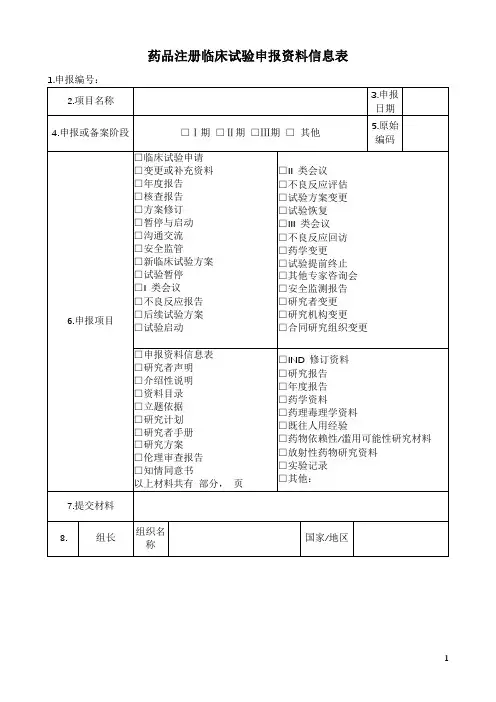
药物临床试验登记填写指南(V2.0版)国家药品监督管理局药品审评中心2020年7月目录1一、简要说明 (4)2二、登记表填写指南 (6)3(一)题目和背景信息 (7)41.登记号(不可更新项、公示项) (7)52.相关登记号(可更新项、公示项) (7)63.药物名称*(不可更新项、选择公示项) (7)74.曾用名(可更新项、选择公示项) (7)85.药物类型*(不可更新项、公示项) (8)96.受理号/备案号*(不可更新项、选择公示项) (8)107.批件号(备案号)/批准日期(默示许可日期/备案日期)*(不可更11新项、不公示项) (8)128.适应症*(不可更新项、公示项) (8)139.试验专业题目*(不可更新项、公示项) (9)1410.试验通俗题目*(可更新项、公示项) (9)1511.试验方案编号*(不可更新项、公示项) (9)1612.试验方案编号重复原因(可更新项、不公示项) (9)1713.方案最新版本号*(可更新项、公示项) (9)1814.版本日期*(可更新项、公示项) (10)1915.是否联合用药*(不可更新项、公示项) (10)2016.联合用药受理号和联合用药批准证明*(不可更新项、不公示项)21 (10)22(二)申请人信息 (10)231.申请人名称(不可更新项、公示项) (10)242.联系人姓名*(可更新项、公示项) (10)253.联系人座机*(可更新项、公示项) (11)264.联系人手机号(可更新项、公示项) (11)275.联系人Email*(可更新项、公示项) (11)286.联系人邮政地址*(可更新项、公示项) (11)297.联系人邮编*(可更新项、公示项) (11)308.经费来源*(可更新项、不公示项) (11)31(三)临床试验信息 (12)321.试验目的*(不可更新项、公示项) (12)332.试验设计* (12)343.受试者信息 (15)354.试验分组 (15)365.终点指标 (17)376.数据安全监查委员会(DMC)*(可更新项、公示项) (18)387.为受试者购买试验伤害保险*(可更新项、公示项) (18)39(四)研究者信息 (19)401.主要研究者信息(可更新项、公示项) (19)412.各参加机构信息(可更新项、公示项) (20)42(五)伦理委员会信息*(不可更新项、公示项) (20)43(六)试验状态信息 (21)441.试验状态*(可更新项、公示项) (21)452.试验人数 (23)463.受试者招募及试验完成日期(不可更新项、公示项) (24)47(七)临床试验方案*(不可更新项、不公示项) (24)48(八)临床试验结果摘要(不可更新项、公示项) (25)49(九)其他附件(不可更新项、不公示项) (25)50(十)登记人及其联系方式 (25)515253一、简要说明54本指南是根据国家药品监督管理局《药品注册管理办法》(国家市场监督55管理总局令第27号)关于药物临床试验登记与信息公示的要求和药品审评中心56(以下简称“药审中心”)《药物临床试验登记与信息公示管理规范(试行)》57(以下简称“登记规范”)的要求以及对“药物临床试验登记与信息公示平台”(以58下简称“登记平台”)的总体目标要求,结合网络实现的具体设计而起草。

附件 3:药物临床试验资料归档表项目名称:项目起止时间:年月日至年月日科室:主要研究者:编号内容1CFDA 临床试验批件2药检报告3研究者手册4多方协议(已签名)(研究者、申办者、合同研究组织)5受试者补贴或检查费等发放记录6试验方案及其修正案、知情同意书、病例报告表样表7伦理委员会审批件8学术委员会审批件9临床试验有关实验室检查正常值范围10医学或实验室操作的质控证明11研究者履历及相关文件12研究者职责分工及签名样张13培训记录14监查员访视记录15受试者鉴认代码表、受试者筛选表与入选表记录16完成试验受试者编码目录17试验用药品与试验相关物资的运货单18试验用药品登记表(保管、发放及清点记录)19临床试验用药最终清点记录、申办者收回药量、记录及销毁证明20已签名的知情同意书21原始医疗文件22病例报告表(已填写,签名,注明日期)23研究者致申办者的严重不良事件报告24申办者致药品监督管理局、伦理委员会的严重不良事件申办者:有否说明□有□无□有□无□有□无□有□无□有□无□有□无□有□无□有□无□有□无□有□无□有□无□有□无□有□无□有□无□有□无□有□无□有□无□有□无□有□无□有□无ICF 份□□有无□□CRF 份有无□有□无□□有无报告25 中期或年度报告□ □有 无26 临床试验总结报告□有 □无27 其他□ □有 无主要研究者签名:机构审核接收者签名:归档者签名:日期:日期:年 月 日年 月 日。
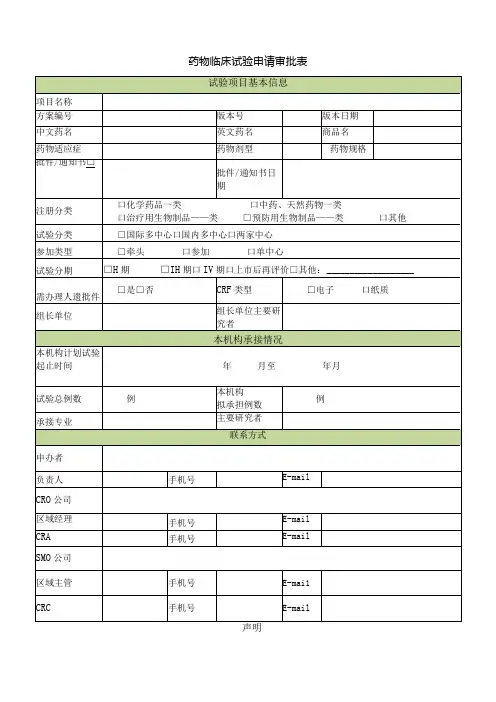
药物临床试验申请审批表申办者声明我保证以上信息真实准确,并负责该临床试验全过程的质量保证,承诺该临床试验数据真实可靠,操作规范,符合NMPA 《药物临床试验质量管理规范》(GCP )要求。
如有失实,愿意承担相关责任。
申办者代表签名(盖章):年月日CRO 公司声明我保证以上信息真实准确,并负责该临床试验全过程的质量保证,承诺该临床试验数据真实可靠,操作规范,符合NMPA 《药物临床试验质量管理规范》(GCP )要求。
如有失实,愿意承担相关责任。
CRo 代表签名(盖章):年月日主要研究者声明我保证以上信息真实准确,并负责该临床试验全过程中的质量保证,承诺该临床试验数据真实可靠,操作规范,符合NMPA 《药物临床试验质量管理规范》(GCP )要求。
本人承诺本研究团队人员与该项目无利益冲突。
如有失实,愿意承担相关责任。
主要研究者签字:_________________________________ 年月日审批意见(手签)主要研究者对本试验的评估及意见:L 试验的入排标准是否合理:2 .病源病种是否能够满足方案要求:3 .研究人员是否有足够的试验时间:4 .科室的场地和设施是否能保障:5 .是否能对试验质量进行保证:6 .是否保证能在约定时间内完成试验:7 .科室在研项目情况:是否有竞争入组临床试验在研:在研药物临床试验数量:项,其中处于筛选期和治疗期的项 8 .主要研究者决定:同意承接口主要研究者(签字):年月日科室意见:同意承接口不同意承接口专业负责人(签字):机构办公室意见:同意承接口项目编号: 不同意承接口机构办主任(签字):机构意见]同意承接口不同意承接口机构主任(签字):注:(1)表格内的选择框内勾选均采用“国)”:(2)请使用A4纸双面打印。
□ □□□□□ □ 否否否否否否 否 □□□□□□ □ 是是是是是是 是。