Ⅰ期临床试验文件归档明细表(监查员版)
- 格式:docx
- 大小:20.41 KB
- 文档页数:3

临床试验不同阶段提供/保存资料一、提供文件清单临床试验准备阶段:申办者:1)国家食品药品监督管理局临床试验批文2)国家食品药品监督管理局批准的试验方案/CRF(版本号)3)临床试验方案(初稿)(版本号)4)CRF(初稿)(版本号)5)研究者手册(初稿)(版本号)6)知情同意书(初稿)(版本号)7)试验经费预算和相关财务规定8)实验室检查正常值范围表(空白)9)第一次临床试验筹备会会议参加人员签到表(空白)10)临床试验多中心协调委员会联络小组成员表(空白)11)药品(含对照药和安慰剂)的标签12)药品(含对照药和安慰剂)质检报告13)药品临床试验编盲记录14)随机化设计方案15)盲码表和盲底16)应急信件17)项目操作的标准操作规程(SOPs)18)研究者履历表(空白)19)研究者声明(空白)20)严重不良事件(SAE)报告表(空白)21)药品临床试验用品运送分发确认表(空白)22)临床试验方案(会议修订稿)(版本号)23)C RF(会议修订稿)(版本号)24)研究者手册(会议修订稿)(版本号)25)知情同意书(会议修订稿)(版本号)26)伦理委员会批准临床试验方案(版本号)27)伦理委员会批准CRF(版本号)28)伦理委员会批准研究者手册(版本号)29)伦理委员会批准知情同意书(版本号)30)第一次临床试验筹备会会议参加人员签到表31)临床试验多中心协调委员会联络小组成员表32)患者日记(含服药记录卡)(空白)33)受试者试验用药使用、分发和回收记录表(空白)34)临床试验申请书(申办者)研究者1)伦理委员会成员表2)伦理委员会临床试验批准文件3)国家药品临床研究基地的资质、资格文件4)研究者履历表5)研究者声明6)药品临床试验用品运送分发确认表7)实验室检查正常值范围表8)申办者、研究者之间的临床试验协议书9)临床试验申请书(研究者面向SFDA)10)临床试验筹备会会议纪要11)C RO组织12)监查员个人(CV)资格表13)C RO组织与申办者之间的协议书14)监查报告格式15)项目监查工作计划16)药品临床试验监查工作现场访视记录表17)药品临床试验监查工作电询访视记录表18)药品临床试验受试者观察记录一览表19)受试者临床试验观察编码表(空白)20)药品临床试验筹备会会议监查报告21)监查员监查工作日志22)药品临床试验CRF填写指南临床试验过程:申办者:1)伦理委员会批准的临床试验方案(版本号)2)CRF3)伦理委员会批准的研究者手册(版本号)4)伦理委员会批准的知情同意书(版本号)5)患者日记(含服药记录卡)6)受试者试验用药使用、分发和回收记录表7)研究者履历表8)研究者声明签字页9)临床试验方案确认页10)修订后的项目操作的标准操作规程(SOPs)11)临床试验经费预算和财务决议12)试验用药品与试验相关物资的运货清单13)向SFDA致备案资料14)临床试验稽查报告15)中期分析计划与报告16)向SFDA致年度报告17)申办者致SFDA/IEC/IRB的严重不良事件报告18)申办者致SFDA/IEC/IRB及各研究中心的中止临床试验的报告19)临床试验中期协调会议参加人员签名册20)临床试验统计分析计划书21)药品临床试验数据库研究者:1)研究者填写的CRF2)受试者签订的知情同意书3)受试者身份签认代码表4)受试者筛选表和入选表5)已签字的受试者日记6)试验用药品药品登记表(使用、分发、回收和记录)7)更新的(试验方案、CRF、知情同意书、书面通知的情况)试验文件8)更新的研究者手册9)更新的研究者履历表10)更新的实验室或实验室检测正常值范围表11)原始医疗文件(源数据/源文件)12)研究者致SFDA和申办者/IEC/IRB的严重不良事件报告表13)研究者致申办者、SFDA、IEC/IRB及各研究中心的中止临床试验的报告14)拆阅或未拆阅的应急信件15)临床试验中期协调会议纪要CRO组织:1)监查员监查工作日志2)监查员电讯监查登记表3)药品临床试验现场访视登记表4)药品临床试验受试者观察跟踪一览表5)监查员访视报告6)数据疑问表(DQF)7)原始文件的核对与监查8)药品临床试验CRF传递表9)临床试验用药品回收、清点记录10)监查员致申办者的严重不良事件报告表11)更新的监查员监查工作计划临床试验结束:申办者:1)临床试验CRF传递表2)完成试验受试者编码目录3)临床试验稽查报告4)试验药物销毁证明5)致IEC/IRB、SFDA试验完成(关闭试验中心)报告6)数据库建立与数据库文件7)数据库检查与比较记录8)数据疑问表(DQF)9)盲态审核数据提纲10)盲态审核报告11)数据传输与移交记录12)统计分析计划书(版本号)13)统计分析报告14)临床试验试验总结会会议纪要15)第二次揭盲记录16)盲底与应急信件研究者:1)填写完整的CRF2)患者日记(含患者服药记录卡)3)受试者试验药品登记(使用、分发、回收和清点)表4)原始医学文件5)试验文件归档目录(地点、卷宗号、目录、页码数和保管者与期限)6)研究者确认签字页7)临床试验总结报告CRO组织1)最终监查报告2)试验中心关闭报告3)设盲试验的揭盲监查记录4)监查文件的归档与保存目录(地点、卷宗号、目录、页码数和保管者与期限)5)临床试验监查评估(科学、伦理原则)报告二、保存文件清单临床试验准备阶段临床试验进行阶段临床试验完成后。
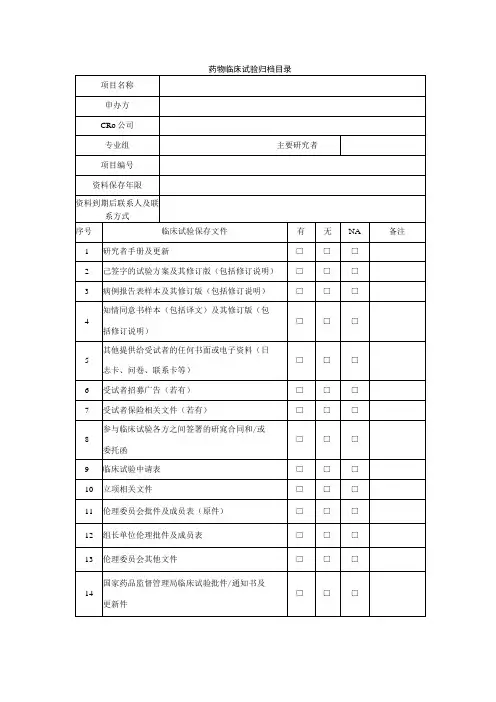
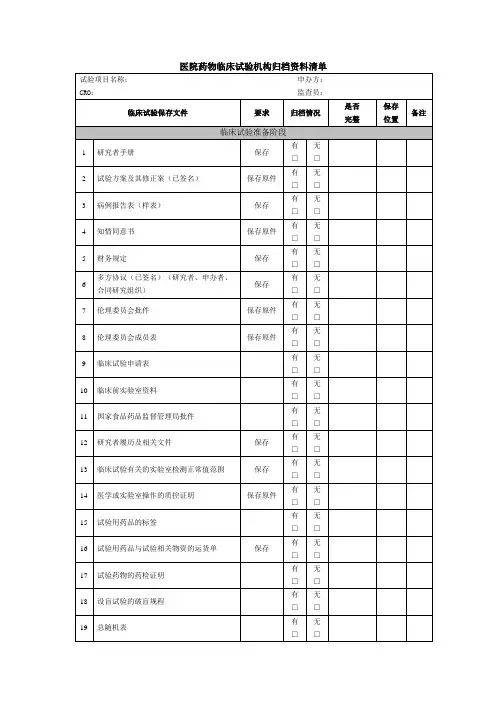
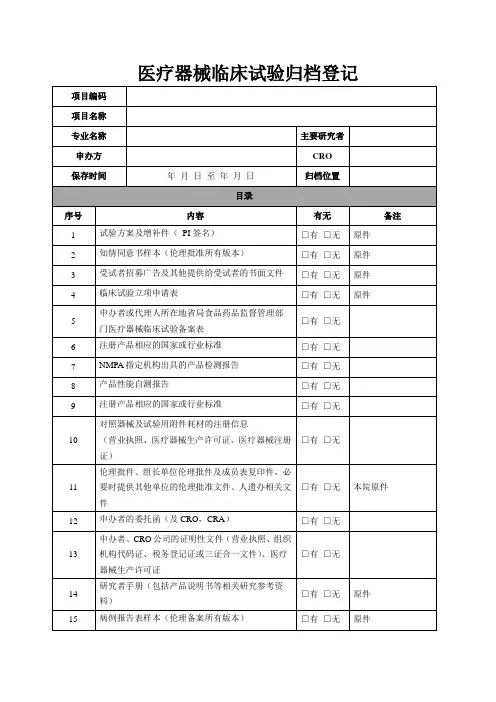
医院药物临床试验机构归档资料清单
科室质控员签名:日期:
主要研究者签名:日期:
资料递交人签名:日期:
机构办公室人员签名:日期:
资料保存到期联系人及联系方式:
归档要求
1. 所有文件请用黑色A4打孔两孔文件夹,厚薄根据递交内容选择
2. 每个文件夹侧面标签格式为:机构编码:留空方便机构填写;项目名称;类别;申办方;CRO;PI;研究时间;归档时间。
3. 不同项用隔页纸隔开归档
4. 项目归档每个文件夹需有中文目录
5. 以上“保存位置”需说明保存在第几个归档文件夹第几个目录下
6. 需在多项保存的文档,仅在一项保存,其他项告知在哪项保存即可
7. 研究者手册、试验方案、知情同意书、病例报告表有多个版本的必须罗列清单,内容包括版本,版本日期,被批准使用日期。
8. 本院发生的SAE请归档时,罗列清单(见SAE附表)
9. 对于缺项的内容,请予以说明缺失原因
10. 请确保内容齐全,再递交至机构(根据本院机构的归档资料清单表,先自检有无每项相关资料,并在备注项注明在哪个文件夹中)
11. 请确保所有CRF中,研究者均签署姓名及日期
12.根据合同要求,所有款项已付清,请研究者审核实际发生费用,并签字确认无误
13.所有问题都在关闭中心访视期间解决
14.项目归档前,请各级质控员完成质量控制工作,最后需科室质控员签字确保所归档资料完整,已完成科室质量控制工作;由主要研究者签名确保试验归档资料完整、数据真实可靠。



临床试验不同阶段提供/保存资料一、提供文件清单临床试验准备阶段:申办者:1)国家食品药品监督管理局临床试验批文2)国家食品药品监督管理局批准的试验方案/CRF(版本号)3)临床试验方案(初稿)(版本号)4)CRF(初稿)(版本号)5)研究者手册(初稿)(版本号)6)知情同意书(初稿)(版本号)7)试验经费预算和相关财务规定8)实验室检查正常值范围表(空白)9)第一次临床试验筹备会会议参加人员签到表(空白)10)临床试验多中心协调委员会联络小组成员表(空白)11)药品(含对照药和安慰剂)的标签12)药品(含对照药和安慰剂)质检报告13)药品临床试验编盲记录14)随机化设计方案15)盲码表和盲底16)应急信件17)项目操作的标准操作规程(SOPs)18)研究者履历表(空白)19)研究者声明(空白)20)严重不良事件(SAE)报告表(空白)21)药品临床试验用品运送分发确认表(空白)22)临床试验方案(会议修订稿)(版本号)23)C RF(会议修订稿)(版本号)24)研究者手册(会议修订稿)(版本号)25)知情同意书(会议修订稿)(版本号)26)伦理委员会批准临床试验方案(版本号)27)伦理委员会批准CRF(版本号)28)伦理委员会批准研究者手册(版本号)29)伦理委员会批准知情同意书(版本号)30)第一次临床试验筹备会会议参加人员签到表31)临床试验多中心协调委员会联络小组成员表32)患者日记(含服药记录卡)(空白)33)受试者试验用药使用、分发和回收记录表(空白)34)临床试验申请书(申办者)研究者1)伦理委员会成员表2)伦理委员会临床试验批准文件3)国家药品临床研究基地的资质、资格文件4)研究者履历表5)研究者声明6)药品临床试验用品运送分发确认表7)实验室检查正常值范围表8)申办者、研究者之间的临床试验协议书9)临床试验申请书(研究者面向SFDA)10)临床试验筹备会会议纪要11)C RO组织12)监查员个人(CV)资格表13)C RO组织与申办者之间的协议书14)监查报告格式15)项目监查工作计划16)药品临床试验监查工作现场访视记录表17)药品临床试验监查工作电询访视记录表18)药品临床试验受试者观察记录一览表19)受试者临床试验观察编码表(空白)20)药品临床试验筹备会会议监查报告21)监查员监查工作日志22)药品临床试验CRF填写指南临床试验过程:申办者:1)伦理委员会批准的临床试验方案(版本号)2)CRF3)伦理委员会批准的研究者手册(版本号)4)伦理委员会批准的知情同意书(版本号)5)患者日记(含服药记录卡)6)受试者试验用药使用、分发和回收记录表7)研究者履历表8)研究者声明签字页9)临床试验方案确认页10)修订后的项目操作的标准操作规程(SOPs)11)临床试验经费预算和财务决议12)试验用药品与试验相关物资的运货清单13)向SFDA致备案资料14)临床试验稽查报告15)中期分析计划与报告16)向SFDA致年度报告17)申办者致SFDA/IEC/IRB的严重不良事件报告18)申办者致SFDA/IEC/IRB及各研究中心的中止临床试验的报告19)临床试验中期协调会议参加人员签名册20)临床试验统计分析计划书21)药品临床试验数据库研究者:1)研究者填写的CRF2)受试者签订的知情同意书3)受试者身份签认代码表4)受试者筛选表和入选表5)已签字的受试者日记6)试验用药品药品登记表(使用、分发、回收和记录)7)更新的(试验方案、CRF、知情同意书、书面通知的情况)试验文件8)更新的研究者手册9)更新的研究者履历表10)更新的实验室或实验室检测正常值范围表11)原始医疗文件(源数据/源文件)12)研究者致SFDA和申办者/IEC/IRB的严重不良事件报告表13)研究者致申办者、SFDA、IEC/IRB及各研究中心的中止临床试验的报告14)拆阅或未拆阅的应急信件15)临床试验中期协调会议纪要CRO组织:1)监查员监查工作日志2)监查员电讯监查登记表3)药品临床试验现场访视登记表4)药品临床试验受试者观察跟踪一览表5)监查员访视报告6)数据疑问表(DQF)7)原始文件的核对与监查8)药品临床试验CRF传递表9)临床试验用药品回收、清点记录10)监查员致申办者的严重不良事件报告表11)更新的监查员监查工作计划临床试验结束:申办者:1)临床试验CRF传递表2)完成试验受试者编码目录3)临床试验稽查报告4)试验药物销毁证明5)致IEC/IRB、SFDA试验完成(关闭试验中心)报告6)数据库建立与数据库文件7)数据库检查与比较记录8)数据疑问表(DQF)9)盲态审核数据提纲10)盲态审核报告11)数据传输与移交记录12)统计分析计划书(版本号)13)统计分析报告14)临床试验试验总结会会议纪要15)第二次揭盲记录16)盲底与应急信件研究者:1)填写完整的CRF2)患者日记(含患者服药记录卡)3)受试者试验药品登记(使用、分发、回收和清点)表4)原始医学文件5)试验文件归档目录(地点、卷宗号、目录、页码数和保管者与期限)6)研究者确认签字页7)临床试验总结报告CRO组织1)最终监查报告2)试验中心关闭报告3)设盲试验的揭盲监查记录4)监查文件的归档与保存目录(地点、卷宗号、目录、页码数和保管者与期限)5)临床试验监查评估(科学、伦理原则)报告二、保存文件清单临床试验准备阶段临床试验进行阶段临床试验完成后。


I期临床试验研究室文件归档与保存制度【目的】根据GCP的相关规定和I期临床试验研究室的实际情况,建立资料归档和保存的标准操作规程,以保证临床试验资料归档、保存的科学性、有效性及安全性。
【适用范围】适用于所有临床试验资料的归档与保存。
【规程】1.研究者应当建立的各项研究档案(1)临床试验涉及所有的标准操作规程;(2)临床试验的记录文件:如简易病历表、病例报告表、人组随机数字表、实验室记录、样品记录、试验用药记录、不良事件及其报告的记录、试验结果记录、原始资料、总结报告等;(3)临床试验的其他文件:如研究者手册、试验方案、受试者招募材料、知情同意书、伦理委员会批文、研究人员履历、研究人员名单、试验监查记录、药品监管部门批文、与申办者签定的合同等。
2.临床试验文件资料归档为便于管理和查阅,可将每个临床试验的文件、资料分类管理。
(1)试验方案及补正、批文;(2)研究者手册及更新;(3)与伦理委员会的沟通文件;(4)与药品监督管理部门的沟通文件;(5)知情同意书和知情同意资料;(6)受试者的招募、筛选和入选记录;(7)临床试验涉及所有的标准操作规程及更新版本;(8)试验用药记录;(9)紧急情况下使用的揭盲密码信封及揭盲程序;(10)与申办者、监查员的联系文件(包括合作协议书、一般联系方式等);(11)研究人员名单及履历表;(12)试验原始资料;(13)简易病历表、病例报告表;(14)药品接收、分发、清点、回收及销毁记录等。
3.临床试验文件的保存研究者必须按照GCP的最低要求保存各种试验资料、记录及文件,具体需要保存的文件可参见现行GCP附录2中提到的必须保存的文件清单。
4.文件归档保存中的一些问题(1)凡上级主管部门下发的文件,应及时登记,交至有关领导传阅,同时留1份存档;(2)应标明并保存参加试验的受试者病历,当文件被转至其他地方保管时需注明应与谁联系;(3)当对如何保管及存放时间有疑问时,应随时咨询监查员;(4)研究者时间有限时,可任命助理研究者或秘书来负责各种文件和档案的管理工作。