人教版初三化学下册溶解中的吸热和放热现象
- 格式:doc
- 大小:44.00 KB
- 文档页数:4



溶解吸热、放热实验的改进湖北省鄂州市华容镇熊江勇人教版《化学》九年级下册《溶液的形成》第二部分——溶质溶解时的吸热、放热现象。
教材将此实验设计为“活动与探究”进行学生分组实验教学,有利于学生形成溶质溶解在溶剂中能量(内能)发生变化的理念,有利于培养学生科学探究能力。
在教学中,为了让学生形成科学探究的方法,同时能在视觉感官上形成效果,我从以下两个方面进行了改进:1.设计对照实验。
2.将皮肤触摸感觉改为直观视觉感受。
一、实验设计方案:1.选用溶解热(绝对值)较小的物质,如氯化钠、硝酸钾等固体溶质与氢氧化钠、硝酸铵进行对照实验。
2.将原实验用手触摸感觉放热或吸热的验证方法改为直观沸腾或凝固现象表现。
二、实验过程:1.氢氧化钠固体溶于水放热:①.分别人两支试管中倒入10mL水,在酒精灯上加热至沸腾,停止加热后停止沸腾。
②.分别向已停止沸腾的水中加入氢氧化钠固体和氯化钠固体,观察加入氢氧化钠固体的试管内的水重新沸腾,对照组(加入氯化钠固体)的试管没有重新沸腾。
2.硝酸铵固体溶于水吸热:①.分别向两个100mL烧杯中各加入0℃的水约30mL(事先置于冰箱冷冻室约30分钟),另在两支小试管中各倒入约1mL清水。
②.将两支小试管分别放入小烧杯中约2分钟,发现小试管中的水并没有结冰。
分别取出试管。
③.分别向两个烧杯中加入约25g硝酸铵固体和25g硝酸钾固体,搅拌,让两种固体充分溶解,再将盛有清水的两支小试管分别放入烧杯中,静置,2分钟后观察。
溶解硝酸铵烧杯内的小试管中的水结冰,对照组(溶解硝酸钾烧杯内)的小试管中的水没有结冰。
实验反思:1.改进后的实验,利用学生日常生活熟悉的沸腾和凝固现象,更直观认知溶质溶解过程中的能量变化,能收到较好的实验效果。
2.实验过程能更好培养学生的动脑动手能力和团结协作精神。
3.设计了对照实验,一方面能突现出实验现象,另一方面让学生认识到不同的固体溶质在水中溶解时,内能变化(增加或减少)和多少是各不相同的。

物质溶解放热、吸热的原因物质溶解时,为什么会有吸热或放热的现象呢?这是因为:物质溶解,一方面是溶质的微粒──分子或离子要克服它们本身的相互之间的吸引力离开溶质,另一方面是溶解了的溶质要扩散到整个溶剂中去,这些过程都需要消耗能量,所以物质溶解时,要吸收热量。
溶解过程中,温度下降原因就在于此。
如果溶解过程只是单纯的扩散,就应该全是吸热的,为什么还有的放热呢?原来,在溶解过程中,溶质的微粒──分子或离子不仅要互相分离而分散到溶剂中去,同时,溶解于溶剂中的溶质微粒也可以和溶剂分子生成溶剂化物(如果溶剂是水,就生成水合物)。
在这一过程里要放出热量。
因此,物质溶解时,同时发生两个过程:一个是溶质的微粒──分子或离子离开固体(液体)表面扩散到溶剂中去,这一过程吸收热量,是物理过程;另一个过程是溶质的微粒──分子或离子和溶剂分子生成溶剂化物,多余的动能就要以热量的方式释放出来,这是化学过程。
这两个过程对不同的溶质来说,吸收的热量和放出的热量并不相等,当吸热多于放热,例如硝酸钾溶解在水里的时候,因为它和水分子结合的不稳定,吸收的热量比放出的热量多,就表现为吸热,在溶解时,溶液的温度就降低。
反之,当放热多于吸热,例如浓硫酸溶解在水里的时候,因为它和水分子生成了相互稳定的化合物,放出的热量多于吸收的热量,就表现为放热,所以溶液的温度显著升高。
一种物质溶解在水里,究竟是温度升高还是降低,取决于溶解过程中两种过程所吸收或放出的热量多少用Q放代表溶质微粒扩散所吸收的热量,用Q吸代表溶质微粒水合时放出的热量。
若:Q吸>Q放溶液温度下降Q吸<Q放溶液温度升高Q吸≈Q放溶液温度无明显变化溶质溶解过程的热量变化,我们可以用仪器测得。
常见的物质:浓硫酸、氢氧化钠、氧化钙等物质溶于水时放热,弱酸根,弱碱阳离子、水解吸热,硝酸类如硝酸铵、氯化铵等物质溶于水、硝酸根水合吸热。
溶于水大量放热:浓硫酸,NaOH,与水反应大量放热:CaO溶于水吸热:NH4NO3例如:硝酸铵。

《探究物质溶解过程的吸热放热现象》教学教案
葵城中学梁家华
一、教学目标:
1、知道物质在溶解过程中温度会发生变化;
2、探究不同物质在溶解过程中的温度变化情况。
二、教学重点:
不同物质在溶解过程中的温度变化情况。
三、教学难点:
学生自己动手做探究实验。
四、教学方法:
探究法。
五、教学过程:
1、新课导入:
①通过讲述食品干燥剂发生爆炸的新闻事件,引入主题,提起学生兴趣;
②回忆书本中的NaOH和NH4NO3溶解实验现象,开始实验。
2、讲授新课:
①分组实验Ⅰ:
用温度传感器测量NaOH溶解时的温度变化情况,并记录相关实验数据。
(水:30ml ;固体NaOH:1药匙)
②分组实验Ⅱ:
用温度传感器测量Ca(OH)2溶解时的温度变化情况,并记录相关实验数据。
(水:30ml ;固体Ca(OH)2 :1药匙)
③用洗衣粉洗衣服时,手的感觉是?
我们会感觉到水会变暖。
因为洗衣粉中,也有类似于NaOH的碱性物质,所以洗衣粉在溶解时也会放出热量,造成水温升高。
④堂上练习。





2020年中考化学考点之溶解时的吸热或放热现象
溶解时的吸热或放热现象
溶解过程中发生了两种变化。
一种是溶质的分子(或离子)向水中扩散,这一过程吸收热量。
另一种是溶质的分子(或离子)和水分子作用,生成水合分子(或水合离子),这一过程放出热量。
有的溶质溶解时,扩散过程吸收的热量小于水合过程放出的热量,表现为溶液的温度升高如:NaOH、浓H2SO4;
有的溶质溶解时,扩散过程吸收的热量大于水合过程放出的热量,表现为溶液的温度降低如:
NH4NO3。
第九单元溶解时的吸热或放热现象实验仪器:烧杯、玻璃杯、温度计实验药品:固态氯化钠、硝酸铵、氢氧化钠实验步骤:1、向烧杯中加入100ml的蒸馏水,用温度计测其稳度,记录下来。
2、向烧杯中加入10g固态氯化钠,并用玻璃杯搅拌至氯化钠全部溶解,测出氯化钠溶解后溶液的温度,记录下来。
3、用同样的方法测出硝酸铵、氢氧化钠溶解前后水和溶液的温度,记录下来。
实验结论:氯化钠溶解后溶液温度不变,硝酸铵溶解后溶液温度下降,氢氧化钠溶解后溶液温度上升。
9-5氯化钠在水中的溶解实验仪器:烧杯、玻璃杯实验药品:固态氯化钠实验步骤:1、在室温下,向盛有20ml蒸馏水的烧杯中加入5g氯化钠,搅拌。
2、再向1中加入5g氯化钠,搅拌。
3、再向2中加入15ml的蒸馏水,搅拌。
实验现象:1、杯中形成无色溶液2、烧杯中溶液底部有未溶解的固体3、杯中形成无色溶液实验结论:1、20ml蒸馏水能完全溶解5g氯化钠。
2、20ml蒸馏水不能完全溶解10g氯化钠。
3、增大溶剂的量可将未溶物质溶解。
9-6硝酸钾在水中的溶解实验仪器:烧杯、玻璃杯实验药品:固态硝酸钾实验步骤:1、在室温下,向盛有20ml蒸馏水的烧杯中加入5g硝酸钾,搅拌。
2、再向1中加入5g硝酸钾,搅拌。
3、当烧杯中硝酸钾固体有剩余而不再溶解时,加热烧杯一段时间,观察剩余固体有什么变化。
4、再向3中加入5g硝酸钾,搅拌。
5、溶液冷却后,观察现象。
实验现象:1、杯中形成无色溶液2、烧杯中溶液底部有未溶解的固体3、烧杯中未溶解的固体溶解了,杯中形成无色溶液。
4、杯中形成无色溶液5、固体从溶液中结晶出来。
实验结论:1、20ml蒸馏水能完全溶解5g硝酸钾。
2、20ml蒸馏水不能完全溶解10g硝酸钾。
3温度升高硝酸钾溶解能力增强。
4、同35、温度降低硝酸钾溶解能力降低。
溶液的形成(第二课时)
——溶解中的吸热和放热现象
天津市实验中学化学组李侠
教学目标
1.知识与技能:通过探究物质在水中溶解时溶液的温度变化,理解溶解时的吸热和放热现象。
2.过程与方法:经历和体验科学探究的基本过程,激发学生学习化学的兴趣。
3.情感态度和价值观:发展学生善于合作、勤于思考、勇于创新的科学品质。
重点和难点
重点:实验方案的设计和比较。
难点:实验方案的评价以及从微观角度理解物质在水中溶解时溶液温度变化的实质。
教学准备
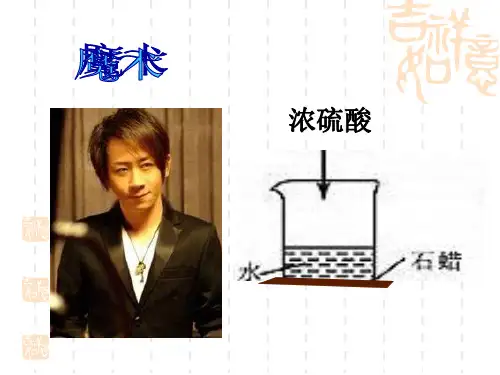
演示实验用品:底部用石蜡粘着一橡胶塞的烧杯、NaOH固体、水、玻璃棒、药匙。
分组实验用品:三份质量相同的固体NaCl、NH4NO3、NaOH,三只250 mL的烧杯、药匙、温度计等。
其他准备:投影仪及PPT演示文稿。
教学设计(见下页)
教学过程
附:学生探究报考
溶解中吸热和放热现象的探究
阅读教材第30页内容,完成下列探究活动
明确实验目的
确定实验用品
设计实验方案
实验装置简图
实验记录与结论
结论:
如果没有温度计,如何通过实验来探究溶解时的吸热和放热?请大家用实验装置简图表示出来。