《溶解时的吸热和放热现象》 ppt课件
- 格式:ppt
- 大小:600.50 KB
- 文档页数:11

溶解时的吸热或放热现象
溶解是指溶质(立方体)从化合物(其中使用平衡水)中分离出来,在恒定温度和压力下,这种物质构成新化合物的过程。
溶解是一个物理化学过程,在这个过程中可能会发生吸热或放热现象。
物质溶解时会发生吸热或放热现象的原因主要有两个:第一是化学反应产生的热量,第二就是溶质分离开来或融合到另一种物质中时产生的热量。
正如物理学家所说的,溶解的过程中化学反应的每一步都会产生热量,而将溶质分离开来或结合到另一种物质中时也将会产生热量。
当沸点低于溶质的温度时,溶质就会慢慢溶解,溶质分子会慢慢从物质中分离出来,这时溶解所需要的热量就会向外散发,就可以说溶解发生时有放热现象。
例如,在水温平衡时,在容器里放入一些食盐,由于食盐的温度低于水的,随着食盐的溶解,向容器外发出的热量将更大,就会产生放热现象。
此外,溶解过程中会发生化学反应,而化学反应在发生时也会产生一定的热量,这些热量可能会产生吸热或放热效应,具体取决于化学反应中所发生的化学变化。
总而言之,溶解发生时就会有吸热或放热现象,这是因为在溶解过程中可能会发生化学反应、溶质分离或融合到另一种物质中时,都会产生一定的热量,这些热量可能会由于沸点差异而产生一定的吸热或放热现象,从而影响溶解过程。

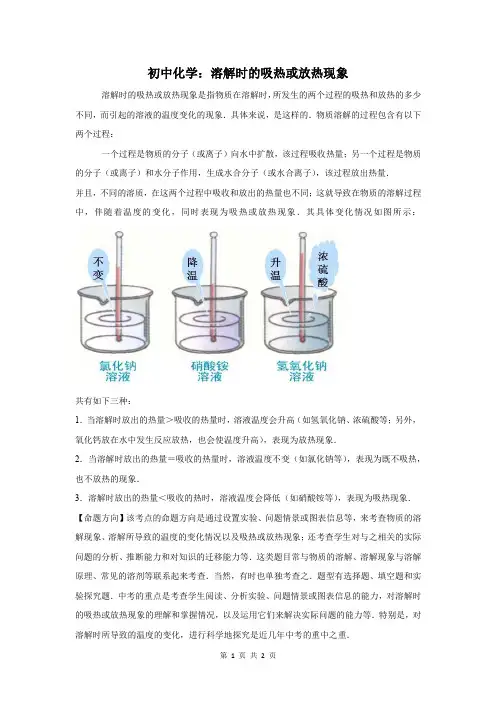
初中化学:溶解时的吸热或放热现象溶解时的吸热或放热现象是指物质在溶解时,所发生的两个过程的吸热和放热的多少不同,而引起的溶液的温度变化的现象.具体来说,是这样的.物质溶解的过程包含有以下两个过程:一个过程是物质的分子(或离子)向水中扩散,该过程吸收热量;另一个过程是物质的分子(或离子)和水分子作用,生成水合分子(或水合离子),该过程放出热量.并且,不同的溶质,在这两个过程中吸收和放出的热量也不同;这就导致在物质的溶解过程中,伴随着温度的变化,同时表现为吸热或放热现象.其具体变化情况如图所示:共有如下三种:1.当溶解时放出的热量>吸收的热量时,溶液温度会升高(如氢氧化钠、浓硫酸等;另外,氧化钙放在水中发生反应放热,也会使温度升高),表现为放热现象.2.当溶解时放出的热量=吸收的热量时,溶液温度不变(如氯化钠等),表现为既不吸热,也不放热的现象.3.溶解时放出的热量<吸收的热时,溶液温度会降低(如硝酸铵等),表现为吸热现象.【命题方向】该考点的命题方向是通过设置实验、问题情景或图表信息等,来考查物质的溶解现象、溶解所导致的温度的变化情况以及吸热或放热现象;还考查学生对与之相关的实际问题的分析、推断能力和对知识的迁移能力等.这类题目常与物质的溶解、溶解现象与溶解原理、常见的溶剂等联系起来考查.当然,有时也单独考查之.题型有选择题、填空题和实验探究题.中考的重点是考查学生阅读、分析实验、问题情景或图表信息的能力,对溶解时的吸热或放热现象的理解和掌握情况,以及运用它们来解决实际问题的能力等.特别是,对溶解时所导致的温度的变化,进行科学地探究是近几年中考的重中之重.【解题方法点拨】解答这类题目时,首先,要明确什么是溶解,溶解过程又包含哪两个过程;并且,还要弄清哪一个过程吸收热量,哪一个过程放出热量;吸收的热量多,还是放出的热量多.特别是记住哪些典型的物质,例如:氢氧化钠、浓硫酸溶解放热多,温度升高(另外,氧化钙放在水中发生反应放热,也会使温度升高),溶解时表现为放热现象;硝酸铵溶解吸热多,温度降低,溶解时表现为吸热现象;其它的物质则可以认为吸热和放热相等,温度不变,表现为既不吸热,也不放热的现象.然后,根据实验、问题情景或图表信息等,细致地阅读、分析题意等,联系着生活实际,细心地进行探究解答即可.。
