第八节 最终灭菌大容量注射剂型 生产质量管理
- 格式:ppt
- 大小:129.50 KB
- 文档页数:5

如何保证注射剂产品质量戴天201218590104澄明度1.工艺用水应该认真按照GMP要求,严格遵守标准操作规程来制备,确证工艺用水质量;定期对工艺用水设备设施清洗灭菌;实时监控工艺用水的杂质、PH值、电导率等参数;利用折叠式精密滤芯过滤清洗用注射用水、纯化水及与注射用水储罐、纯化水储罐接触的空气,更好地改善工艺用水的澄明度及接触工艺用水储罐的空气质量;在用水终端,如器具清洗、胶塞清洗等关键岗位使用折叠式精密滤芯过滤器,严格控制与药液直接接触的内包材、容器具的清洗工艺用水质量;利用微孔滤膜有效过滤药液,保证药液质量。
对于工艺用水温度高带来的隐患,可以采用一定的装置降低工艺用水的水温;使工艺用水温度对设备设施及胶塞清洗的影响降低,实现用冷配法配制药液,有效地控制溶液中的白点、白块数。
2.过滤应该选择效率高、技术先进、安全可靠的过滤器和质量好的滤膜;微孔滤膜过滤器在使用前后进行气泡点试验是非常必要的,可以及时发现滤膜是否有泄漏;还需要定期对微孔过滤器进行外观完好性、完整性试验、保压试验、气体扩散试验等进行验证,确保过滤效果能满足澄明度要求及工艺要求。
无菌、无热原1.最终灭菌小容量注射剂关键工序的控制要点:安瓿:清洁度和干燥程度。
配药:批号划分与编制、主药含量、pH值、澄明度、色泽、过滤器材的检查等。
灌封:长度、外观、装量、澄明度。
灭菌:灭菌柜——标记、装量、温度、时间、真空度、记录。
灭菌前后半成品——外观清洁度、标记、存放区。
灯检:抽查澄明度、每盘标记、灯检者代号、存放区。
2.最终灭菌大容量注射剂关键工序的控制要点:纯水:增加pH值、氯化物。
注射水:硫酸盐、钙盐、内毒素、微生物等项目检测。
洗瓶:滤后的纯水与注射水需检查澄明度、水温、水压、毛刷、清洗剂浓度、残留水滴、淋洗水pH值、瓶清洁度。
配药:复核配制原辅料,药液检测主药含量、pH值、澄明度,微孔滤膜需进行完整性试验。
灌封:涤纶薄膜—洗涤水澄明度、氯化物;灌装后半成品—药液装量、澄明度、铝盖紧密度;灌装后半成品—微生物污染水平。

制药有限公司大容量注射液生产工艺规程颁发单位:GMP办公室工艺规程批准程序目录1. 剂型、规格 (3)2. 生产工艺流程 (3)3. 操作过程及工艺条件 (4)4.质量控制要点 (6)5.设备一览表、主要设备生产能力 (7)6.工艺过程中的SOP (7)7.中间产品的控制 (8)8.验证工作要点 (8)9.工艺卫生和环境卫生 (10)10.劳动组织及岗位定员 (10)一、制剂类型:最终灭菌大容量注射液,100ml规格,西林瓶包装。
二、流程图:大容量注射剂工艺流程图三、操作过程及工艺条件1 生产前的检查与确认1.1 是否还留有前批生产的产品或物料,是否已清洁并取得“清场合格证”。
1.2 检查确认生产现场的机器设备和器具是否已清洁并准备完毕挂上“合格”标示。
1.3 所使用原辅料是否准备齐全。
是否有质量检验报告单,合格品才能使用。
1.4 检查工艺用水是否新鲜制备,贮存不得超过24小时。
1.5 检查确认与生产品种相适应的批生产指令、配套文件及有关记录是否已准备齐全。
1.6 检查确认生产场所的温度是否在规定范围内(18-26℃,相对湿度在30%-65%)。
2 洗瓶、塞、铝盖2.1理瓶:根据“批生产指令”准备所需的清洁盘、领取必须的西林瓶。
在理瓶室将西林瓶的合格品摆满瓶盘。
2.2清洗:把西林瓶放在不锈钢传送链条上,开动洗瓶机,定时检查安瓿的清洁度:目检1000ml注射用水无可见异物,抽50支,毛、块≤2%。
洗瓶岗位按清场SOP进行清场,并填写生产记录。
2.3 理塞、铝盖:根据《生产指令》准备所需的丁基胶塞和铝盖,分别、依次放入多功能胶塞漂洗机。
2.4清洗:将丁基胶塞放入多功能漂洗机后,加入纯化水,开动机器进行清洗,清洗后捞出、沥干。
排除纯化水后再加入注射用水清洗,捞出、沥干。
将铝盖放入多功能漂洗机后,加入纯化水,开动机器清洗,清洗后捞出、沥干。
排除纯化水后再加入注射用水清洗,捞出、沥干。
清洗过后,按岗位清场操作规程进行清场,填写清场合格证,并填写生产记录。


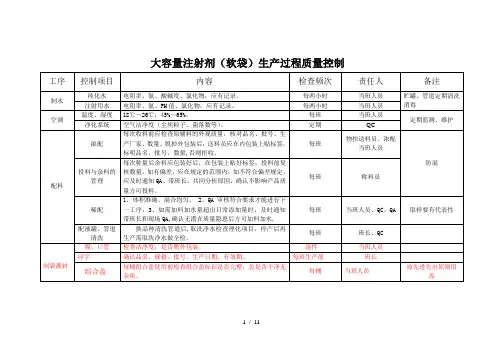
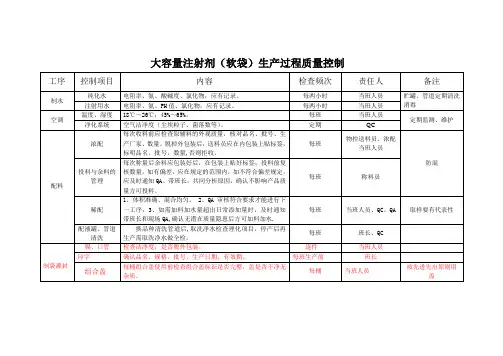

注射剂生产过程的质量控制(一)生产过程的质量控制生产数量保证了,质量必须合格,否则不能出厂,尤其是安全指标一点都不能含糊,如:热原、无菌、过敏、异常毒性、降压物质、鉴别项等,,有一样不合格都会要人命的,叫不准重做。
齐二药是假辅料、华源是无菌热原的问题。
现在对药品的质量要求的越来越严了,有一项不合格就算劣药,要没收非法所得,并处以货值1-3倍的罚款,要求生产的药品必须合格,生产合格率要达到100%是非常难的,尤其是生化药针剂更难,但这是每个企业永恒追求的目标。
产品的合格率指两方面:一个是批成品率、一是批次合格率。
(二)提高批成品率:设备必须好使:如有打瓶可能有玻璃屑、灌针有问题水针有碳化点、止灌不好使浪费药液、装量控制不好灌高了产量低、灌低了不合格等,最好刚灌装前十支应传出去灯检,有问题及时调整,没问题再正式灌装。
还有就是控制好含量,既保证含量合格又不浪费,这也要求药液混合均匀、溶解充分、取样有代表性、检验准确。
(三)如何提高批合格率:1 提高主要原辅料的内控质量标准:主要是化学原料药和使用量较大的辅料。
针剂用原辅料国家标准有的制定的不严格不科学,要用内控标准来补充,如有的品种原料不检热原,若原料带热原就有可能导致成品不合格,有的品种在原料生产时可能有毒性,这样的原料就应做异常毒性,因为制剂的工艺过程是无法除毒性物质的,降压物质也是一样,总之,成品要检的项目如果原料有可能带来就应检原料,内控标准就应制定相应的项目,采购时应先与厂家讲清楚,合同中应附带内控标准。
从源头控制产品质量。
2生化药提取原液应检测成品的相关项目,如高分子、过敏试验、降压物质、活性等。
当提取车间更换超滤柱子膜包时和改变工艺及时通知化验室,做溶液的过敏和高分子等,避免生产出的成品不合格,无法挽救,造成损失。
3 半成品的质量标准尤其是新品种的内控质量标准的制定,最近陆续有批准生产的新品种,必须制定科学合理的内控标准,制定时生产和质量共同商量,采购也要参与,原辅料采购时要执行。


注射剂质量风险管理知识首先,注射剂生产过程中应严格执行GMP(Good Manufacturing Practice)要求,确保每个环节的操作符合标准。
包括原料采购、生产设备的维护和清洁、生产操作的规范等。
同时,应建立质量控制系统,对每个生产步骤进行记录和检验,并留存样品供后期检测和追溯。
其次,注射剂的运输过程中需要注意温度、湿度、光照等因素的控制。
药物的质量易受环境条件的影响,特别是在运输过程中,如果无法保持合适的环境条件,可能会导致药物的质量受损。
因此,运输过程中应选择合适的包装材料和保护措施,确保药物质量的稳定性和安全性。
注射剂在存储过程中也需要进行有效的管理和控制。
药物的存储环境应符合标准,避免受到高温、潮湿、阳光直射等不利因素的影响。
同时,应制定合理的库存管理制度,保证存储的注射剂按期使用,避免质量问题的发生。
在注射剂的使用过程中,医务人员应严格按照操作规程进行操作,避免任意更换药物、过量使用、不当保存等情况发生。
此外,还需要定期对注射剂的使用情况进行回顾和评估,及时发现并排除潜在的质量问题。
最后,对于已经上市的注射剂,应建立完善的药物不良反应监测体系,及时收集和分析相关数据,发现质量问题后能够及时采取措施,保障患者的用药安全。
总之,注射剂质量风险管理是一个非常重要的环节,它涉及生产、运输、存储和使用等多个环节,需要各个环节的相关人员密切合作,共同确保注射剂的质量安全。
通过严格遵守标准和规程,采取有效的管理措施,可以降低质量风险,保障患者的用药安全。
(续)注射剂质量风险管理是一个综合性的工作,旨在确保注射剂的质量安全,防范可能的质量风险,并及时采取措施进行管理和控制。
在注射剂质量风险管理中,以下几个方面尤为重要。
首先,注射剂的原材料采购是关键的环节之一。
优质的原材料是保证注射剂质量的基础,因此在采购过程中,应严格遵守相关标准和规范,确保原材料的质量符合要求。
同时,应建立供应商评估和管理体系,对供应商进行定期的质量评估和审核,确保供应商提供的原材料能够稳定地满足生产需要。

