化学能与热能的相互转化
- 格式:ppt
- 大小:562.00 KB
- 文档页数:1

化学能与热能的相互转化教案一、教学目标1. 让学生了解化学能和热能的概念及其相互转化关系。
2. 掌握化学反应中的能量变化,认识放热反应和吸热反应。
3. 能运用能量守恒定律解释化学反应中的能量变化。
4. 培养学生的实验操作能力和观察能力,提高学生分析问题、解决问题的能力。
二、教学内容1. 化学能和热能的概念2. 化学反应中的能量变化3. 放热反应和吸热反应4. 能量守恒定律在化学反应中的应用5. 实验:测定反应热三、教学重点与难点1. 教学重点:化学能与热能的相互转化关系,化学反应中的能量变化,放热反应和吸热反应的判断。
2. 教学难点:能量守恒定律在化学反应中的应用,实验操作和数据处理。
四、教学方法1. 采用讲授法、实验法、讨论法、提问法等多种教学方法,引导学生主动探究、积极思考。
2. 通过实验操作和数据分析,培养学生的实践能力和科学素养。
3. 利用多媒体课件辅助教学,提高学生的学习兴趣和效果。
五、教学过程1. 导入新课:以一个实际例子引入化学能与热能的相互转化,激发学生的学习兴趣。
2. 讲解化学能和热能的概念,阐述它们之间的相互转化关系。
3. 讲解化学反应中的能量变化,介绍放热反应和吸热反应的特点。
4. 引导学生运用能量守恒定律解释化学反应中的能量变化。
5. 布置实验:测定反应热,让学生亲自动手操作,观察实验现象。
6. 数据处理与分析:引导学生运用实验数据验证能量守恒定律。
7. 总结本节课的主要内容和知识点,强调重点和难点。
8. 布置作业:巩固本节课所学知识,提高学生的应用能力。
9. 课后反思:对本节课的教学效果进行总结和评价,为下一步教学提供参考。
六、教学评价1. 评价学生对化学能和热能概念的理解程度。
2. 评价学生对化学反应中能量变化的掌握情况。
3. 评价学生对放热反应和吸热反应的判断能力。
4. 评价学生对能量守恒定律在化学反应中应用的理解。
5. 评价学生在实验操作中的技能和实验数据的处理能力。

各种能量转换的原理能量转换是自然界中常见的过程,它涉及到不同形式的能量之间的相互转换。
从化学能转化为热能,再到动能或电能转化为光能,各种能量之间的转换相互交织,构成了宇宙运行的基础。
本文将探讨几种常见的能量转换原理。
一、化学能转换为热能的原理化学能是物质的一种内部能量,当物质发生化学反应时,化学能会被释放出来,形成热能。
这种能量转换的原理可以通过燃烧反应来解释。
例如,当燃料与氧气发生燃烧时,化学键断裂,原子重新排列,释放出大量的热能。
热能可以使物体温度升高,或者用于蒸汽发电,将热能转化为电能。
二、动能转换为电能的原理动能是物体运动时所具有的能量,而电能则是电荷运动所具有的能量。
动能可以通过发电机来转化为电能。
发电机内部的导线在磁场中旋转时,因运动电荷的相互作用,会产生电流,从而将动能转换为电能。
这种能量转换的原理被应用于各种发电设备,如水力发电、风力发电和核能发电。
三、电能转换为光能的原理电能可以转化为光能的现象被称为电-光转换,其中最常见的就是光源的工作原理。
例如,当电流通过电灯泡的丝状灯丝时,灯丝会发热,温度升高,然后发射出可见光。
这是由于电子在碰撞中释放能量,激发光子的原子以光的形式释放出来。
这种能量转换在日常生活中广泛应用,比如电视、激光器和LED显示屏等。
四、热能转换为机械能的原理热能可以通过热机转换为机械能。
热机包括蒸汽机和内燃机等,其工作原理都是利用燃料的热能产生高温高压的蒸汽或燃烧气体,从而推动活塞或涡轮旋转,将热能转化为机械能。
这种能量转换在工业和交通运输领域有着广泛的应用,推动了社会的发展。
五、机械能转换为声能的原理机械能可以通过振动物体来转化为声能。
当一个物体振动时,会产生压缩和稀疏的空气波动,形成声波。
声波通过空气传播,最终被我们的耳朵接收和感知。
这种能量转换的原理被应用于音乐、通讯和声波传感器等领域。
总结起来,各种能量之间的转换是宇宙运行的基础。
化学能转化为热能,动能转化为电能,电能转化为光能,热能转化为机械能,机械能转化为声能,不同形式的能量相互转换,推动着世界的运转。

第二章第一节化学能与热能第二课时化学能与热能的相互转化【学习目标】1.了解化学能与热能的相互转化,理解中和热的概念。
2.理解热化学方程式的含义,掌握热化学方程式的书写和正误的判断。
3.了解中和热的测定和化学反应热的实验方法。
【新知探究】一、化学能与热能的相互转化1.两个基本自然规律——“质量守恒”和“能量守恒”(1)质量守恒定律:自然界中的物质发生转化时________保持不变。
(2)能量守恒定律:不同形式的能量发生转换时________保持不变。
2.吸热反应和放热反应(1)定义吸热反应:________热量的化学反应;放热反应:________热量的化学反应。
(2)实验探究223.中和热(1)定义:酸和碱发生中和反应生成 ________水时所释放的热量。
(2)中和反应反应热的测定。
【选修四P4】【归纳】常见的放热反应和吸热反应二、热化学方程式的书写阅读选修四P3-4,归纳热化学方程式的书写时须注意事项 【例1】注意:① ;② 。
【例2】因此:书写热化学方程式一定要注明参加反应的物质的状态。
【思考】热化学方程式中化学计量数表示什么含义和热化学方程式的含义?含义:1molH 2和1/2molO 2反应生成1mol 气态水,放出241.8kJ 的热量。
2H 2(g )+O 2(g )2H 2O (g )ΔH=-483.6kJ/mol含义:1、热化学方程式:(1)定义:表示参加反应 和 关系的化学方程式。
(2)意义:它既表明了化学反应中的 变化,也表明了其中的 变化。
2、热化学方程式的书写:(与化学方程式相比)【例3】1molN 2(g)与适量的H 2(g)反应生成NH 3(g),放出92.2KJ 热量热化学方程式:【变式】1molC(s)与适量的H 2O (g)反应生成CO(g)和H 2(g),吸收131.5KJ 热量热化学方程式:注意事项:(1)指明反应的 和 ,若不指明,则说明反应热在25 ℃、101 kPa 下测定的。

化学能与热能的转化人类的生产和生活离不开能源,而化学能和热能则是常用的能源之一。
化学能指的是物质在化学反应中所拥有的能量,而热能则是物体的温度所带有的能量。
这两种能量之间的相互转化在我们的日常生活中十分普遍,本文将为您详细介绍化学能和热能的转化方式及其应用。
一、化学能转化为热能化学能转化为热能是指在化学反应中放出的热量。
例如将羟基乙酸钠和硫酸反应,就能放出大量热量。
这是因为反应中羟基乙酸钠和硫酸之间所形成的化学键能量降低,化学反应后所形成的化学键能量提升,通过反应所放出的能量就是热能。
化学能转化为热能是一种常见的现象。
在燃烧过程中,有机物和氧气发生反应,也是将化学能转化为热能的过程。
例如火柴点燃的时候,木头中的碳、氢等元素与空气中的氧气发生燃烧反应,放出大量热量,照明上则是使用切合成形、可持续风能转化电能的 LED。
这些发光二极管能够在低功率的驅動下發出強光,並在長時間使用後不會發熱。
二、热能转化为化学能热能转化为化学能的实例比较少,但也不是没有。
例如在日常生活中,煮饭的时候需要用到热能,而食物中的化学能则是在加饭的过程中得到转化并存储在食物中的。
另外,人类使用太阳能的方式中,也存在热能转化为化学能的过程。
我们可以通过光合作用将太阳能转化为植物体内的化学能,植物在这个过程中将光能转化成化学能,并储存在植物体内。
当我们食用植物时,就能将这些化学能转化为人体能量。
三、化学能和热能的应用化学能和热能作为常用的能源,在我们日常生活中有很多应用。
例如在煮茶或煮酒的时候,萎缩干燥的茶叶或果皮会被水蒸气中的热能软化、膨胀,释放出茶香或酒香。
同样,在生产过程中,也需要化学能和热能的应用。
例如在工业生产中,压缩空气的作用过程中就需要使用热能,这样可以降低压缩空气时所需要消耗的能量。
总的来说,化学能和热能的转化是人类生产和生活中不可或缺的一部分。
通过对化学能和热能的充分利用,我们可以更加高效地生产和生活,推动社会进步和发展。


第六章化学反应与能量第一节化学反应与能量变化【学习目标】1.知道化学反应可以实现化学能与热能的转化,认识吸热和放热反应。
2.能用化学键解释某些吸热反应和放热反应。
3.设计实验认识构成原电池的条件。
4.理解原电池的概念及工作原理,能正确判断原电池的正负极。
5.知道干电池、充电电池、燃料电池等化学电源的特点。
6.掌握构成电池的要素,了解不同电极材料对电池性能的影响。
7.能正确书写简单化学电源的电极反应式。
【基础知识】一、化学反应与热能1、实验探究(1)向Mg与稀盐酸反应的溶液中插入温度计,温度计显示的温度升高,说明该反应为放热反应。
(2)将20 g Ba(OH)2·8 H2O晶体粉末与10 g NH4Cl晶体混合放入烧杯中,将烧杯放在滴有几滴水的木片上。
用玻璃棒快速搅拌,闻到有刺激性气味时用玻璃片盖上烧杯,用手触摸杯壁下部感觉冰凉,烧杯与木片间有结冰现象,说明该反应为吸热反应。
2、放热反应与吸热反应(1)放热反应:释放热量的化学反应,如活泼金属与酸的反应,燃烧反应,中和反应等。
(2)吸热反应:吸收热量的化学反应,如氢氧化钡与氯化铵的反应,盐酸与碳酸氢钠的反应,灼热的炭与二氧化碳的反应。
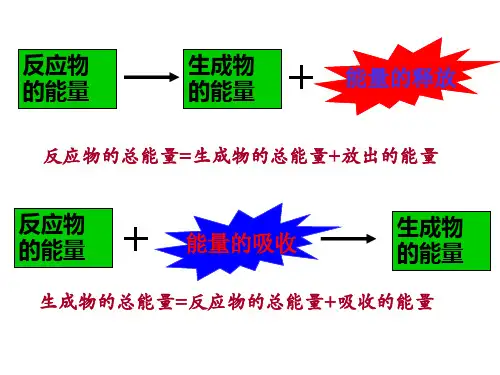
3、化学反应存在能量变化的原因(1)从化学键的变化理解——主要原因(2)从物质储存化学能的角度理解宏观解释放热反应示意图吸热反应示意图化学反应 放出热量化学反应 吸收热量①放热反应可以看成是反应物所具有的 化学 能转化为 热 能释放出来。
②吸热反应可以看成是 热 能转化为 化学 能被生成物所“储存”。
4、人类对能源的利用 (1)利用的三个阶段柴草时期——树枝杂草 ↓化石能源时期—— 煤 、 石油 、 天然气 ↓多能源结构时期——太阳能、氢能、核能、海洋能、风能、地热能等(2)化石燃料利用过程中亟待解决的两方面问题 ①一是其短期内 不可再生 ,储量有限;②二是煤和石油产品燃烧排放的粉尘、 SO 2、NO x 、CO 等是大气污染物的主要来源。



化学能与热能的相互转化教案一、教学目标1. 让学生了解化学能与热能的概念及其相互转化原理。
2. 培养学生运用实验方法观察和分析化学反应中能量变化的能力。
3. 引导学生运用能量守恒定律解释化学反应中的热现象。
4. 提高学生对能量转化和利用的兴趣,培养其创新意识和实践能力。
二、教学内容1. 化学能与热能的概念及特点2. 化学反应中的能量变化3. 热能的测量与表达4. 放热反应与吸热反应5. 能量守恒定律在化学反应中的应用三、教学方法1. 采用问题驱动的教学模式,引导学生主动探究化学能与热能的相互转化。
2. 利用实验现象,培养学生的观察能力和分析能力。
3. 运用案例教学,使学生能够将理论知识应用于实际问题。
4. 采用小组讨论、合作交流的方式,提高学生的团队协作能力。
四、教学准备1. 实验室用具:烧杯、试管、酒精灯、温度计等。
2. 实验试剂:氢氧化钠、硫酸铜、氨水等。
3. 教学课件与视频资料。
五、教学过程1. 引入新课:通过一个简单的化学反应(如酸碱中和反应)引导学生思考化学能与热能的关系。
2. 讲解化学能与热能的概念:解释化学能是指物质在化学反应中释放或吸收的能量,热能是指物体内部分子运动的能量。
3. 实验观察:安排学生进行实验,观察化学反应中的热现象,如氢氧化钠与硫酸铜反应时的放热现象。
4. 分析与讨论:引导学生分析实验现象,解释化学反应中的能量变化原因,认识放热反应与吸热反应。
5. 能量守恒定律的应用:讲解能量守恒定律在化学反应中的应用,让学生理解化学反应中的能量转化过程。
6. 案例分析:通过实际案例,使学生能够将所学知识应用于解决实际问题。
7. 课堂小结:总结本节课所学的化学能与热能的相互转化原理及其应用。
8. 作业布置:布置一些有关化学能与热能转化的练习题,巩固所学知识。
9. 课后反思:鼓励学生反思自己的学习过程,总结收获与不足。
六、教学评价1. 评价学生对化学能与热能的概念的理解程度。
2. 评价学生对化学反应中能量变化的观察和分析能力。

化学能与热能的转化在自然界中,能量是一种基本的物理量,它能够使事物发生变化和实现工作。
能量可以以不同的形式存在,其中化学能和热能是最为常见和重要的两种形式。
本文将探讨化学能与热能之间的转化关系,以及在实际应用中的一些例子。
一、化学能是什么?化学能是指物质所具有的化学反应中能够释放出来的能量。
它主要来源于化学键的形成和断裂过程。
当化学反应发生时,原子之间的键能会发生变化,从而释放出或吸收能量。
二、热能是什么?热能是指物体因温度差异而具有的能量。
根据热力学第一定律,热能可以与其他形式的能量相互转换,且能量守恒。
三、化学能与热能的转化过程在化学反应中,化学能可以转化为热能,反之亦然。
这种转化过程可以通过热化学方程式来描述。
例如,燃烧反应是一种常见的化学反应,将化学能转化为热能。
以燃烧甲烷为例:CH4(g) + 2O2(g) -> CO2(g) + 2H2O(g) + 热能在这个反应中,甲烷和氧气发生氧化还原反应,生成了二氧化碳和水,同时释放出热能。
这个热能来源于甲烷分子中碳氢键的断裂和新键的形成过程。
四、化学能与热能的应用化学能和热能的转化在日常生活和工业生产中有着广泛的应用。
以下是一些例子:1. 燃料的燃烧:化石燃料(如煤、石油和天然气)中的化学能可以通过燃烧转化为热能,用于加热和发电。
2. 燃料电池:燃料电池利用化学能来产生电能。
它将氢气和氧气反应生成水,同时释放出电能。
3. 食物的消化:我们的身体将食物中的化学能转化为热能,提供机体所需的能量。
4. 火柴点燃:火柴中的摩擦会导致硫磺和磷等物质的反应,产生能够点燃木柴的化学能。
五、能量守恒定律化学能与热能的转化过程符合能量守恒定律。
能量守恒定律指出,能量在转化过程中不会凭空消失或产生,总能量保持不变。
因此,在化学反应中,化学能转化为热能时,总能量不会增加或减少。
六、总结化学能和热能是能量的两种常见形式。
化学能可以与热能相互转化,例如在燃烧反应中化学能转化为热能。
化学能与热能的相互转化教案(精选6篇)知识与技能1、能从化学键的角度理解化学反应中能量变化的主要原因2、通过化学能与热能的相互转变,理解“能量守恒定律”过程与方法能从微观的角度来解释宏观化学现象,进一步发展想象能力。
情感态度与价值观1、初步建立起科学的能量观,加深对化学在解决能源问题中重要作用的认识。
2、通过师生互动,增加师生感情教学重点1.化学能与热能的内在联系及相互转变。
2.从本质上理解化学反应中能量的变化,从而建立起科学的能量变化观。
教学难点1.化学能与热能的内在联系及相互转变。
2.从本质上理解化学反应中能量的变化,从而建立起科学的能量变化观。
教学方法启发引导、探究式教学媒体多媒体、实验教学内容师生活动[[创设问题情景]氢气和氯气的混合气体遇到强光会发生什么现象?为什么?[学生思考、讨论]氢气和氯气的混合气体遇到强光会发生爆炸。
这是因为反应在有限的空间里进行,放出大量的热,使周围气体急剧膨胀。
[进一步思考]反应中的热量由何而来?氢气和氯气反应的本质是什么?[学生思考、讨论]从化学键角度分析氢气和氯气反应的本质。
板书:一、化学键与化学反应中能量的变化关系[教师补充讲解]化学反应的本质是反应物中化学键的断裂和生成物中化学键的形成。
化学键是物质内部微粒之间强烈的相互作用,断开反应物中的化学键需要吸收能量,形成生成物中的化学键要放出能量。
氢气和氯气反应的本质是在一定的条件下,氢气分子和氯气分子中的h-h键和cl-cl键断开,氢原子和氯原子通过形成h-cl键而结合成hcl分子。
1molh2中含有1molh-h键,1mol cl2中含有1mol cl-cl 键,在25℃和101kpa的条件下,断开1molh-h键要吸收436kj的能量,断开1mol cl-cl键要吸收242 kj的能量,而形成1molhcl分子中的h-cl键会放出431 kj 的能量。
这样,由于破坏旧键吸收的能量少于形成新键放出的能量,根据“能量守恒定律”,多余的能量就会以热量的形式释放出来。
化学的热力学热能与化学能的转换热力学是研究热能与其他形式能量之间相互转换和传递关系的科学。
在化学反应中,热能与化学能之间的转换是热力学的重要研究内容之一。
本文将探讨化学反应中热能与化学能的转换原理及其在实际应用中的意义。
一、热力学基本概念热力学是物质热现象与能量转移规律的研究。
在热力学中,能量的转移和转换是一个核心问题。
根据能量形式的不同,可以将能量分为热能、化学能、机械能等。
在化学反应中,主要涉及到热能与化学能之间的转换。
二、热力学方程与焓变热力学中的方程主要有能量守恒定律、熵增原理等。
在化学反应中,焓变是一个重要的物理量。
焓是过程中系统的能量与外界的压力、体积等因素的综合体现。
化学方程式可以表示为:C6H12O6 + 6O2 → 6CO2 + 6H2O在这个方程中,葡萄糖与氧气发生反应生成二氧化碳和水,产生热能。
焓变就是在化学反应过程中吸热还是放热的一个指标。
在这个方程中,焓变可以表示为:ΔH = Q其中,ΔH表示焓变,Q表示热能的变化。
三、内能与焓的关系在热力学中,内能是物质的一个重要性质,是系统与外界交换能量的能力。
热力学第一定律表明,内能的变化等于系统对外做的功与系统吸收的热量之和。
在化学反应中,系统的内能与焓有一定的关系。
根据热力学第一定律,内能的变化等于吸热或放热与对外做功之和。
对于恒压条件下的化学反应,焓变可以表示为:ΔH = ΔU + PΔV其中,ΔU表示内能的变化,P表示恒定的压强,ΔV表示体积的变化。
当压强恒定时,ΔH就等于ΔU。
四、化学能的应用化学能是物质之间能量转换的一种形式。
在现实生活中,化学能的转化广泛应用于许多领域。
例如,汽车的燃料是通过化学反应释放能量来推动汽车运行的。
火药爆炸产生的能量也是化学能转化为热能的典型例子。
此外,化学能的应用还涵盖了能源领域。
例如化学电池就是利用化学能转换为电能的装置,广泛应用于移动通讯、电子产品等领域。
五、热力学研究的意义热力学的研究对于认识物质的性质和相互关系具有重要的科学意义。
各种形式的能量之间相互转化的实例能量在物理学中定义为物体所具有的使其产生变化的能力。
能量可以以不同的形式存在,例如机械能、热能、电能、化学能等等。
这些不同形式的能量在现实生活中可以相互转换。
以下是一些能量之间相互转化的实例:1.机械能和热能之间的转化:当一个物体被加热时,其分子运动加快,由此增加了其热能。
同时,分子的运动也会引起物体的位移,从而改变其机械能。
2.机械能和电能之间的转化:水力发电是一个很好的例子。
水流下坡时可以使涡轮旋转,旋转的动能通过发电机转变为电能。
3.电能和热能之间的转化:当电流通过一个导体时,导体会受到电阻而发热。
这种电能转化为热能的过程在电炉、电热器等电器中得到了应用。
4.热能和化学能之间的转化:化学反应可以释放热能。
例如,燃烧是一种化学反应,燃烧过程中存储在化学键中的能量被释放出来,产生热能。
5.电能和光能之间的转化:光源(如灯泡)通过加热电丝来产生光。
电能转化为热能,再转化为光能。
6.机械能和声能之间的转化:当一个物体振动时,其机械能转化为声能。
例如,敲击乐器时,敲击棒撞击乐器表面产生振动,其机械能转化为声音能量。
7.势能和动能之间的转化:在一个摆锤系统中,当摆锤下落时,其势能转化为动能;而当摆锤上升时,动能被转化为势能。
8.化学能和电能之间的转化:电池是将化学能转化为电能的典型例子。
化学反应在电池内发生,产生电子流动,最终转化为电能供给电路。
9.核能和热能之间的转化:核反应可以释放出巨大的能量,这些能量可以通过冷却剂等途径转化为热能,用于产生蒸汽驱动涡轮和发电机。
总之,能量之间的相互转化贯穿于我们的日常生活和科学研究的方方面面。
人类通过理解和利用这些能量转化的原理,为我们的生活带来了便利,并推动了科学技术的发展。
教学过程课堂导入1.“十一”长假期间,小明和爸爸妈妈一起到野外旅游。
临到中午时,他们一家围在一起准备就餐,只见小明爸爸拿出一个包装盒,轻轻一拉露在外面的绳头,几分钟后打开盒盖,热气腾腾的饭菜便呈现在眼前。
周围的人惊叹不已:他们没有生火为什么吃的饭是热的呢?原来,盒底部有夹层,内部设有水袋和氧化钙加热袋,当拉起开关时,水袋中的水和氧化钙接触,反应放出的热量使饭菜变热。
反应过程中反应物结构发生了怎样的变化?该反应为什么能够放热?所有反应都能够放热吗?2.【引入】演示实验:往一片棉花里加入两药匙的过氧化钠,然后滴加几滴水,观察现象。
【提问】问什么棉花可以燃烧,燃烧的条件是什么?【分析】燃烧的条件:可燃物、氧气、可燃物的温度达到着火点2Na2O2+2H2O==4NaOH+2O2↑【讲解】可燃物是棉花、反应产生了氧气,那么可燃物达到着火点的温度是怎么产生的?【回答】该反应放出热量使得棉花温度升高从而达到棉花的着火点【设问】热能是能量的一种表现形式。
那么,除刚才的这个反应,其它的化学反应过程中是不是也会有能量变化呢?其表现形式又是怎样的?根据你已有的知识经验举例说明。
【回答】学生回答并举例【归纳小结】物质在发生化学反应的同时都还伴随着能量的变化,这些能量变化通常又表现为热量的变化。
(除此之外还有的反应表现为还有光能、电能的变化)一、复习预习【学生阅读】前言内容,通过阅读本章前言,我们知道本章我们要解决的核心问题:在现代广泛使用的各种能源中,那些与化学密切相关?面对能源枯竭的危机,提高能源利用率和开辟新能源是解决这一问题的两个主要方向,在这方面化学能做出什么贡献?【提问】]煤、石油和天然气等化石燃料或它们的制品的燃烧所产生的热能从何而来?与化学物质及化学反应有什么关系?石灰石经高温煅烧生成生石灰,高温提供的热能在分解反应中起什么作用?【回答】这里所列举的两类反应说明了化学反应与热能之间的辩证关系以及它们之间的相互转化。
热能与化学能的转换能量是人们生活中必不可少的存在,无论是从地球内部的热能,还是从化学反应中释放出来的化学能,都将被转化为我们所需要的形式。
热能和化学能是两种不同的能量形式,但是,它们之间可以相互转换,这为人们想要更有效地利用能源创造了更多的机会。
一、热能的转化热能是指物体内部分子或原子的热运动所具有的能量。
热能的传递是在高温物体和低温物体之间的热传导、热辐射和热对流中进行的。
人们利用热能形式的能源很多,如太阳能、地热能、水能等。
其中,太阳能是最常见的能量形式,由于我们的地球每天都会受到来自太阳的辐射,因此我们可以通过太阳能的收集和使用来满足一部分的能源需求。
热能可以转换为电能、机械能等,这在生活中也有很多应用,例如蒸汽机就是将热能转化为机械能的典型实例。
在热能向其他能量形式转换的过程中,往往会伴随着一些能量损失,这是由于热能的传递不能完全避免热量流失的原因造成的。
因此,在热能的收集和利用过程中,需要特别注意如何减小能量损失。
二、化学能的转化化学能是指物质中的化学键所具有的能量。
许多物质在化学反应中,由于化学键的形成或断裂,会释放出能量。
这种能量形式的来源也非常广泛,例如食物中所含的营养物质、燃料中所含的化学能等等。
化学能的转换也是十分常见的,例如化学电池(如干电池、锂电池等)就是通过化学反应转化为电能的具体实例。
除此之外,许多生物体也能将化学能转化为其他能量形式,例如植物利用光合作用将太阳能转化为化学能,动物将所摄入的食物中的化学能转化为机械能等。
化学能的利用过程中,需要注意如何避免产生有害的废物,并且在能量转化的过程中要尽可能地减小能量损失。
三、热能与化学能的转化除了各自单独应用的情况外,热能和化学能之间还可以相互转化。
热能可以通过化学反应转化为化学能,例如燃料燃烧时就是将热能转化为化学能的过程。
而化学能也可以被转化为热能,例如人体的代谢过程就是通过化学反应将食物中的化学能转化为热能,从而维持人体的正常温度。