晶体场理论分析解析
- 格式:ppt
- 大小:2.77 MB
- 文档页数:28

第四章配合物的化学键理论目标:解释性质,如配位数、几何结构、磁学性质、光谱、热力学稳定性、动力学反应性等。
三种理论:①价键理论(Valence bonding theory VBT)②晶体场理论(Crystal field theory CFT)③分子轨道理论(Molecular orbital theory MOT)第一节价键理论由L. C. Pauling提出要点:①配体的孤对电子可以进入中心原子的空轨道;②中心原子用于成键的轨道是杂化轨道(用于说明构型)。
一、轨道杂化(Hybrid orbital)及对配合物构型的解释能量相差不大的原子轨道可通过线性组合构成相同数目的杂化轨道。
对构型的解释(依据电子云最大重叠原理:杂化轨道极大值应指向配体)指向实例sp 3、sd 3杂化 四面体顶点 Ni(CO)4COCOOCCOsp 2、sd 2、dp 2、d 3杂化 三角形顶点 [AgCl 3]2-Cl ClClAgdsp 2、d 2p 2 杂化 正方形顶点 [PtCl 4]2-ClClClClPtd 2sp 3杂化 八面体顶点 [Fe(CN)6]4-CNNCFeNCCNsp杂化直线型[AgCl2]-二、AB n型分子的杂化轨道1、原子轨道的变换性质考虑原子轨道波函数,在AB n分子所属点群的各种对称操作下的变换性质。
O.+xf = x(p x) = ?类型轨道多项式sp x xp p y yp z zd xy xyd xz xzd d yz yzd x2-y2x2-y2d z22z2-x2-y2(简记为z2)*s轨道总是按全对称表示变换的。
2、如何判定原子轨道波函数的对称类型例:[HgI 3]− (D 3h 群)平面三角形III HgD 3hE 2C 33σv 11111-12-10z(x, y)x 2+(x 2(x3C 2σh 2S 3A 1'A 2'E'A 1"A 2"11111-12-101111-1-111-1-1-112-1-21E"A1′:d z2、sE′:(p x、p y )、(d x2-y2、d xy)A2″:p zE″:(d xz、d yz)3、轨道杂化方案步骤:A、以一组杂化轨道集合作为分子所属点群表示的基,写出群的表示。


晶体场理论§3-2 晶体场理论㈠晶体场模型晶体场理论的基本观点:络合物的中⼼原⼦(或离⼦)和周围配体之间的相互作⽤是纯粹的静电作⽤。
? 这种化学键类似于离⼦晶体中正、负离⼦间的静电作⽤,不具有共价键的性质。
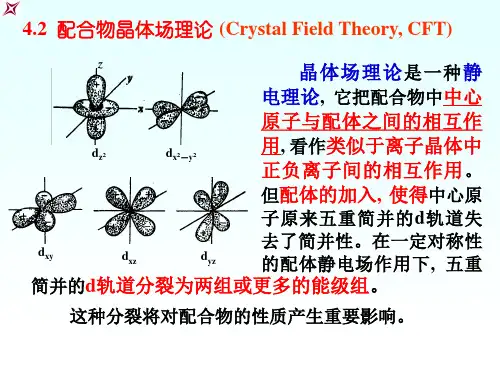
在⾃由的过渡⾦属离⼦中,5个d 轨道是能量简并的,但在空间的取向不同。
下⾯的⾓度分布图画出了各个d 轨道的空间取向,xyd xyxzd xzyzd yzxyd x 2-y2xzd z2在电场的作⽤下,原⼦轨道的能量升⾼。
①在球形对称的电场中,各个d 轨道能量升⾼的幅度⼀致。
能量⾃由原⼦中的d 轨道球对称电场中原⼦中的d 轨道②在⾮球形对称的电场中,由于5个d 轨道在空间有不同取向,根据电场的对称性不同,各轨道能量升⾼的幅度可能不同,即,原来的简并的d 轨道将发⽣能量分裂,分裂成⼏组能量不同的d 轨道。
配体形成的静电场是⾮球对称的。
配位场效应:中⼼原⼦(或离⼦)的简并的d 轨道能级在配体的作⽤下产⽣分裂。
㈡晶体场中的 d 轨道能级分裂⑴正⼋⾯体场(O h )中的d 轨道能级分裂① d 轨道的分裂六个配体沿 x,y,z 轴的正负6个⽅向分布,以形成电场。
配体的孤对电⼦的负电荷与中⼼原⼦d 轨道中的电⼦排斥,导致d 轨道能量升⾼。
如果将配体的静电排斥作⽤进⾏球形平均,该球形场中,d 轨道能量升⾼的程度都相同,为E s 。
实际上各轨道所受电场作⽤不同, d z 2和d x 2-y 2的波瓣与六个配体正对,受电场的作⽤⼤,因此能量的升⾼程度⼤于在球形场中能量升⾼的平均值。
⽽d xy 、d yz 、d xz 不与配体相对,能量升⾼的程度相对较少。
⾃由原⼦xy yz xzd x 2-y 2d z 2(d g 或e g )(d e 或t 2g )⾼能量的d z 2和d x 2-y 2轨道(⼆重简并)统称为d g 或e g 轨道;能量低的d xy 、d yz 、d xz 轨道(三重简并)统称为d e 或t 2g轨道。


晶体场理论概要知识点总结晶体场理论概要知识点总结晶体场理论是固体物理学中重要的研究分支之一,它主要研究晶格中存在的离子间相互作用。
晶体场理论的提出和发展,极大地推动了我们对晶体结构和性质的理解。
本文将对晶体场理论的概要知识点进行总结。
1. 晶体场模型晶体场理论的基础是晶体场模型,它是对晶格中存在的电荷离子和周围电子云相互作用的描述。
晶体场模型基于两个基本假设:一是晶格中的离子被认为是点电荷,可以看作是电子云的源;二是离子间的相互作用可以通过电子云的重叠来描述。
晶体场模型的核心是晶格上的位置和离子性质。
2. 晶体场势能晶体场势能是描述离子受到晶体场作用的函数。
它可以通过考虑电子在离子周围的散射来计算。
晶体场势能可以分解为两个部分:一是离子的库仑势能,即离子间作用的库仑能;二是晶格极化能,即晶格中电子云极化所带来的能量变化。
晶体场势能的确定对于理解晶体的结构和性质至关重要。
3. 晶体场分析晶体场分析是利用晶体场理论解释和计算晶格中离子的电子结构和性质的方法。
晶体场分析的关键是确定晶体场势能。
在晶体场分析中,常常采用的方法是将晶体场势能展开成多项式形式,然后求解电子的波函数和能级。
晶体场分析可以用于解释晶体的各种物理性质,比如磁性、光学性质等。
4. 晶体场参数晶体场参数是描述晶体场的物理量,它们对于理解晶体的性质和行为至关重要。
晶体场参数包括晶体场势能的系数、晶格的结构参数等。
晶体场参数的确定可以通过实验或者计算得到,它们是理解晶体结构和性质的重要依据。
5. 晶体场效应晶体场效应是指晶体场对离子电子结构和性质的影响。
晶体场效应使得离子能级发生分裂,形成能级结构。
晶体场效应是解释和理解晶体中多种物理现象和性质的基础。
例如,晶体场效应可以解释磁性行为、晶格振动性质、光学性质等。
总之,晶体场理论是研究晶体中离子相互作用的重要理论框架。
通过研究晶体场模型、晶体场势能、晶体场分析、晶体场参数和晶体场效应等知识点,我们可以更好地理解晶体的结构和性质。


第四节晶体场理论(CFT)一.知识储备1.晶体场理论的主要内容1.中心离子与配位体之间是纯粹的静电作用。
2.中心离子d轨道发生分裂:中心离子价电子所处的d轨道受到配位体所形成的晶体场的影响,d轨道发生分裂,有的能量升高,有的能量降低。
在配位体形成的八面体的负电场中,5个简并的d轨道在八面体场中分裂成两组:(1)能量较高的e g轨道或dγ轨道:d x2-y2、d z2;(2)能量较低的t2g轨道或dε轨道:d xy、d xz、d yz。
3.晶体场分裂能(△):在晶体场理论中,把d轨道分裂后,最高能级同最低能级间的能量差叫做分裂能△。
八面体场:令△o=10Dq,则E(dγ)-E(dε)=10Dq 解方程组得E(dr)=6Dq2E(dγ)-3E(dε)=0 E(dε)=-4Dq4.分裂能的影响因素:中心离子价层d轨道的分裂能决定于配合物的几何构型、中心离子电荷、半径、配体配位能力的强弱等(1)中心离子电荷越高,分裂能越大中心离子电荷越高,对配体的吸引力越大,中心离子与配体间的距离越近,因此价层d 轨道与配体负电场的排斥作用越强,分裂能越大。
对于第四周期常见过渡金属离子来讲,+2和+3氧化态的6配位的水合离子价层d轨道的分裂能大约为:∆o[M(H2O)62+]=7500~14000 cm-1∆o[M(H2O)63+]=14000~21000 cm-1(2)中心离子周期数越高,分裂能越大例如Cr3+与Mo3+同属VIB族,所带电荷也相同,但由于Cr3+属于第四周期,Mo 3+属于第五周期,MoCl 63-和CrCl 63的分裂能数值分别为:∆o [CrCl 63-]=13600cm -1,∆o [MoCl 63-]=19200cm -1。
(3)配体的种类配体的配位能力越强,配位原子提供的孤对电子形成的负电场也越强,中心离子价层d轨道与配体负电场的相互作用越大,因此分裂能越大。
例如CN -的配位能力远远大于F -的配位能力,因此[Fe(CN)63-]的分裂能远远大于[FeF 63-]的分裂能,其数值分别为:∆o [Fe(CN)63-]=34250cm -1,∆o [FeF 63-]=13700cm -1。

晶体场理论在材料研究中的应用随着科学技术的不断发展,材料科学已成为现代科学发展中重要的一部分,晶体场理论作为材料研究的一种理论方法,在材料结构和性质研究中扮演着重要的角色。
本文将介绍晶体场理论的基本概念以及其在材料研究中的应用。
一、晶体场理论的基本概念晶体场理论是指以中心原子为核心的离子,其周围分布着与离子间直接作用力不同的电场或磁场,这种场被称为晶体场。
晶体场理论认为,晶体场作用下,原子的电子云被偏离了平衡位置,形成了一定的分布,这导致了原子结构和性质的改变。
晶体场理论的应用非常广泛,特别是在材料的物理、化学和工程学等领域。
晶体场理论可以用来解释和预测材料中的各种现象和性质,例如吸收光谱、电子结构和磁性等等。
二、晶体场理论的应用晶体场理论在材料研究中的应用非常广泛,下面将介绍一些具体的应用。
1、材料的电子结构研究晶体场理论可以用来计算材料的电子结构。
例如,对于一个单晶体,离子的晶体场能量可以被描述为电子的波函数关于晶格点的等效位移。
这些等效位移可以被用来构造一个完整的电子能级图,从而研究晶体的电子结构。
2、吸收光谱研究晶体场理论可以被用来解释吸收光谱中的现象。
当光子通过物质时,光子能量被吸收,这导致物质中的电子能量发生变化。
晶体场理论可以计算光子能量和离子的晶体场能量之间的关系,进而预测吸收光谱中的各种现象和特征。
3、材料热力学研究晶体场理论可以被用来描述材料的热力学行为,例如材料的比热容和热膨胀系数等。
这是因为晶体场能量可以被描述为由离子之间的距离差异和位移引起的势能差异。
这些差异可以被用来研究材料的热力学行为。
4、材料的磁性研究晶体场理论可以被用来研究材料的磁性。
磁场可以引起离子周围的晶体场变化,而晶体场理论可以用于预测磁场对离子能量的影响。
这些磁场的影响可以被用来构建材料的磁结构,从而研究材料的磁性质。
三、结语晶体场理论作为一种重要的理论方法,已经被广泛应用于材料研究中。
晶体场理论可以用于研究材料的电子结构、吸收光谱、热力学性质和磁性质等。

晶体场理论解释配合物颜色
晶体场理论是一种结构化的理论,它用来解释有机分子的活性、化学反应以及其他相关物理化学现象。
它对于解释配合物的颜色也很有用。
本文将介绍晶体场理论是如何解释配合物的颜色的。
配合物的颜色是由其分子结构决定的。
当有机分子发生反应时,其分子结构内部会发生变化,从而导致配合物的颜色发生变化。
晶体场理论提供了一种理解有机分子结构变化以及其对配合物颜色产生
影响的解释方法。
晶体场理论基于电子轨道假设,认为有机物分子的电子轨道会存在从电子轨道中抽取或注入电子的能量。
当这些能量发生变化时,有机物分子的结构也会随之发生变化,从而导致其分子上的活性或颜色发生变化。
晶体场理论表明,电子轨道的能量改变会影响有机物分子的结构。
如果一个分子的电子轨道能量有所变化,那么它的结构就会发生变化,而有机物的结构变化又会影响它的光谱特性。
这就是说,分子上电子轨道能量的变化会影响它的颜色。
晶体场理论还可以解释有机物中分子电子轨道能量的变化。
例如,有机物分子可以通过共价键的形成或断裂来改变它的电子轨道能量。
共价键的形成或断裂会导致有机物分子的结构发生变化,从而影响它的光谱特性,而这又会影响它的颜色。
总之,晶体场理论可以用来解释配合物的颜色。
晶体场理论一方面可以解释配合物的颜色是由其结构决定的,另一方面,它还能解释
有机物分子结构变化如何影响它的颜色。
因此,晶体场理论是一种有效的方法来解释配合物的颜色。

晶体场参数-概述说明以及解释1.引言1.1 概述晶体场参数是固体物理学研究中一个重要的概念,它是描述晶体内原子相互作用以及晶格结构的参数。
晶体场参数可以影响物质的性质和行为,因此在材料科学、物理化学以及其他领域中具有重要的应用价值。
本文将对晶体场参数的定义、作用以及计算方法进行介绍,旨在帮助读者深入了解晶体场参数的重要性以及其在科学研究和工程应用中的潜在作用。
通过深入研究晶体场参数,我们可以更好地理解晶体内部的微观结构和性质,为材料设计和性能优化提供重要的参考依据。
在接下来的正文部分,我们将详细探讨晶体场参数的定义、作用以及计算方法,希望读者可以通过本文对晶体场参数有一个全面而深入的了解,从而为未来的科研工作和工程实践提供有益的启示。
1.2 文章结构文章结构部分:本文主要包括三个部分: 引言、正文和结论。
在引言部分中,将首先进行概述晶体场参数的重要性和作用,接着介绍本文的结构和目的。
在正文部分中,将详细讨论晶体场参数的定义、作用以及计算方法,以便读者更好地理解和应用这一概念。
在结论部分中,将总结晶体场参数的重要性,并展望其在未来的应用前景,最后进行结语。
整个文章结构清晰,层次分明,有助于读者理解和吸收文章内容。
1.3 目的晶体场参数是固体物理中非常重要的参数,对于描述晶体结构和性质具有关键作用。
本文的主要目的是探讨晶体场参数的定义、作用和计算方法,深入理解其在物理学领域中的重要性和应用价值。
通过对晶体场参数的研究与分析,可以更好地了解晶体的特性和行为规律,为材料科学、物理化学等领域的研究提供重要参考。
同时,本文也旨在促进晶体场参数的进一步研究和应用,推动晶体学领域的发展与进步。
2.正文2.1 晶体场参数的定义晶体场参数是指描述晶体结构中原子位置和电子分布之间相互作用的参数。
晶体场参数的本质是描述晶体中局部电场的强度和方向,这些参数影响着晶格中电子的能级分布和轨道结构。
晶体场参数的大小和符号对于晶体的电学性质、光学性质和磁学性质都具有重要影响。
物理学中的晶体学与场论晶体学是物理学的重要分支之一,它研究物质内部的结构与性质的关系。
而场论则是描述物质中各种场的性质与相互作用的一种理论。
虽然它们看似毫不相干,但实际上,晶体学与场论是息息相关的。
晶体学中的结构研究可以帮助我们了解物质中原子、分子和离子的排列方式。
而这些排列方式对材料的性质产生着巨大的影响。
例如,金属中原子的结构会影响导电性能和力学性能,化合物中分子的结构则会决定其化学稳定性和反应性。
因此,对于材料科学和化学来说,晶体学的研究至关重要。
而在场论中,场是一种物质或物理现象的描述,可以是电场、磁场、引力场等等。
它们在物质内部产生相互作用,从而影响着物质的性质和行为。
场论的研究可以帮助我们理解物质中相互作用的本质,也是许多基础物理学理论的基础。
从晶体学与场论的角度出发,我们可以将材料和物质看作是由原子和分子组成的晶体结构,在其内部存在各种场的相互作用。
这些场的相互作用会引起材料内部的微观变化,进而影响其宏观性质。
例如,光的色散现象就可以用晶体学和场论相结合的方法来解释。
当光通过晶体时,它会与晶体中的原子和分子相互作用,这些相互作用会影响光的传播速度和方向,从而导致光的折射和色散现象。
此外,在许多领域中,晶体结构和场论应用得越来越广泛。
例如,在物理学和材料科学领域中,研究晶体的同步辐射实验已成为一种非常有效的手段。
通过在晶体中产生高能量的同步辐射光,可以探测材料内部的结构和场的分布,从而得到材料的微观特性信息。
总之,晶体学与场论的研究为我们提供了解物质内部结构和相互作用的一种有效途径。
它们的相互关系不仅帮助我们理解材料的性能和行为,也在许多实际应用中发挥着重要作用。