新版九年级化学演示实验一览表
- 格式:doc
- 大小:12.00 KB
- 文档页数:2

九年级化学演示实验计划九年级.(上)化学演示实验一.1、水加热沸腾;2、研碎胆矾;3、胆矶溶解于水并和…NaOH反应4、石灰石和盐酸反应把产生的气体通入澄清石灰水中;.5、闻气体气味的方法;一…6、固体颗粒的取用…(锌粒);……7、固体粉末的取用…(…Na2CO3粉末);…8、液体的取用;…9、…Na2CO3和盐酸反应;…10、酒精灯的使用;……11、加热…NaQH.和.CuSO4 .的混合溶液;…12、洗涤玻璃仪器;……13、测定空气中氧气的含量;一……14、带火星的木条伸入氧气中;一……15、、…硫在空气和氧气中燃烧;……16、木炭在空气和氧气中燃烧;一……17、…细铁丝在氧气中燃烧;……18、…用过氧化氢溶液制取氧气;一……19、加热.KCIQ.3和,MnQ.2混合物制取氧气;―20、、…电解水实验;……21、品红在水中扩散实验;……22、软硬水的区分…23、蒸馏水的制取…24、用盐酸和碳酸钠反应验证质量守恒定律………25、镁条在空气中燃烧验证质量守恒定律;.……26、活性炭旳吸附性;…27、木炭还原氧化铜;…28、收集.一CO2并验满29、灯火实验;…30、CO2溶于水的验证;…31、CO2和水的反应;32、燃烧的条件的实验;…33、…灭火的原理;……34、粉尘爆炸;…35、点燃甲甲烷;…36、用…Mg 一和盐酸反应验证化学反应中的能量变化;…….九年级下化学演示实验1、比较黄铜片和铜片、…焊锡和锡;……2、蔗糖溶解;3、」2和KMnO.4在水和汽油中的溶解性实验;…4、、水和乙醇能否互溶实验;……5、洗涤剂的乳化功能;…6、…三种不同组成的硫酸铜溶液;…….7、配制一定溶质质量分数的…一NaCL .溶液;.8、向溶液中加入酸碱指示剂;……9、观察盐酸、硫酸的颜色和状态、…气味;………10、浓硫酸的腐蚀性实验;……11、浓…H2SO4稀释;…12、把水慢慢注入浓...H2SO4 ;.13、NaOH的物理性质观察;…14、生石灰和水反应…15、…溶液的导电性;……16、中和反应一17、、Na2CO3一和HCl 反应;18、...Na2CQ3溶液和澄清的石灰水反应;……19、聚乙烯塑料的热塑性;……九年级(上)化学探究实验1、观察和描述——对蜡烛及其燃烧的探究;……2、我们吸入的空气和呼出的气体有什么不同; ...3、实验室制取…02,- O z的性质实验;….4、对分子运动现象的探究;……5、水的净化——过滤液体;……6、对质量守恒定律的探究;一.…(铁与硫酸铜反应)7、实验室制取二氧化碳的探究;…….8、对燃烧条件的探究;…9、自己设计、制作并使用简易灭火器;10、酸雨危害的模拟实验;……九年级(下)化学探究实验1、金属活动性的探究;..(与酸反应、与盐溶液反应).2、铁的生锈条件的探究;….…3、物质溶解时的热现象;….…4、饱和溶液、不饱和溶液的探究;.……5、绘制溶解度曲线;……6、自制指示剂;…7、酸的化学性质;..…8、碱的化学性质;..…9、中和反应;10、用.PH试纸测溶液的…PH;11、溶液酸碱度对头发的影响;一……12、粗盐提纯;…13、探究初步区分氮肥、磷肥和钾肥的方法?………。

九年级化学演示实验计划九年级(上)化学演示实验1、水加热沸腾;2、研碎胆矾;3、胆矾溶解于水并和NaOH反响;4、石灰石和盐酸反响把产生的气体通入澄清石灰水中;5、闻气体气味的方法;6、固体颗粒的取用(锌粒);7、固体粉末的取用(Na2CO3粉末);8、液体的取用;9、Na2CO3和盐酸反响;10、酒精灯的使用;11、加热NaOH和CuSO4的混淆溶液;12、清洗玻璃仪器;13、测定空气中氧气的含量;14、带火星的木条伸入氧气中;15、硫在空气和氧气中焚烧;16、木炭在空气和氧气中焚烧;17、细铁丝在氧气中焚烧;18、用过氧化氢溶液制取氧气;19、加热KClO3和MnO2混淆物制取氧气;20、电解水实验;仅供个人学习参照21、品红在水中扩散实验;22、软硬水的划分23、蒸馏水的制取24、用盐酸和碳酸钠反响考证质量守恒定律;25、镁条在空气中焚烧考证质量守恒定律;26、活性炭的吸附性;27、木炭复原氧化铜;28、采集CO2并验满;29、灯火实验;30、CO2溶于水的考证;31、CO2和水的反响;32、焚烧的条件的实验;33、灭火的原理;34、粉尘爆炸;35、点燃甲烷;36、用Mg和盐酸反响考证化学反响中的能量变化;九年级下化学演示实验1、比较黄铜片和铜片、焊锡和锡;2、蔗糖溶解;3、I2和KMnO4在水和汽油中的溶解性实验;4、水和乙醇可否互溶实验;5、清洗剂的乳化功能;6、三种不一样构成的硫酸铜溶液;仅供个人学习参照7、配制必定溶质质量分数的NaCl溶液;8、向溶液中加入酸碱指示剂;9、察看盐酸、硫酸的颜色和状态、气味;10、浓硫酸的腐化性实验;11、浓H2SO4稀释;12、把水慢慢注入浓H2SO4;13、NaOH的物理性质察看;14、生石灰和水反响;15、溶液的导电性;16、中和反响17、Na2CO3和HCl反响;18、Na2CO3溶液和澄清的石灰水反响;19、聚乙烯塑料的热塑性;九年级(上)化学研究实验1、察看和描绘——对蜡烛及其焚烧的研究;2、我们吸入的空气和呼出的气体有什么不一样;3、实验室制取O2,O2的性质实验;4、对分子运动现象的研究;5、水的净化——过滤液体;6、对证量守恒定律的研究;(铁与硫酸铜反响)7、实验室制取二氧化碳的研究;8、对焚烧条件的研究;9、自己设计、制作并使用简略灭火器;仅供个人学习参照10、酸雨危害的模拟实验;九年级(下)化学研究实验1、金属活动性的研究;(与酸反响、与盐溶液反响)2、铁的生锈条件的研究;3、物质溶解时的热现象;4、饱和溶液、不饱和溶液的研究;5、绘制溶解度曲线;6、自制指示剂;7、酸的化学性质;8、碱的化学性质;9、中和反响;10、用PH试纸测溶液的PH;11、溶液酸碱度仇家发的影响;12、粗盐提纯;13、研究初步划分氮肥、磷肥和钾肥的方法。

九年级化学演示实验计划九年级(上)化学演示实验1、水加热沸腾;2、研碎胆矾;3、胆矾溶解于水并和NaOH反应;4、石灰石和盐酸反应把产生的气体通入澄清石灰水中;5、闻气体气味的方法;6、固体颗粒的取用(锌粒);7、固体粉末的取用(Na2CO3粉末);8、液体的取用;9、Na2CO3和盐酸反应;10、酒精灯的使用;11、加热NaOH和CuSO4的混合溶液;12、洗涤玻璃仪器;13、测定空气中氧气的含量;14、带火星的木条伸入氧气中;15、硫在空气和氧气中燃烧;16、木炭在空气和氧气中燃烧;17、细铁丝在氧气中燃烧;18、用过氧化氢溶液制取氧气;19、加热KClO3和MnO2混合物制取氧气;20、电解水实验;21、品红在水中扩散实验;22、软硬水的区分23、蒸馏水的制取24、用盐酸和碳酸钠反应验证质量守恒定律;25、镁条在空气中燃烧验证质量守恒定律;26、活性炭的吸附性;27、木炭还原氧化铜;28、收集CO2并验满;29、灯火实验;30、CO2溶于水的验证;31、CO2和水的反应;32、燃烧的条件的实验;33、灭火的原理;34、粉尘爆炸;35、点燃甲烷;36、用Mg和盐酸反应验证化学反应中的能量变化;九年级下化学演示实验1、比较黄铜片和铜片、焊锡和锡;2、蔗糖溶解;3、I2和KMnO4在水和汽油中的溶解性实验;4、水和乙醇能否互溶实验;5、洗涤剂的乳化功能;6、三种不同组成的硫酸铜溶液;7、配制一定溶质质量分数的NaCl溶液;8、向溶液中加入酸碱指示剂;9、观察盐酸、硫酸的颜色和状态、气味;10、浓硫酸的腐蚀性实验;11、浓H2SO4稀释;12、把水慢慢注入浓H2SO4;13、NaOH的物理性质观察;14、生石灰和水反应;15、溶液的导电性;16、中和反应17、Na2CO3和HCl反应;18、Na2CO3溶液和澄清的石灰水反应;19、聚乙烯塑料的热塑性;九年级(上)化学探究实验1、观察和描述——对蜡烛及其燃烧的探究;2、我们吸入的空气和呼出的气体有什么不同;3、实验室制取O2,O2的性质实验;4、对分子运动现象的探究;5、水的净化——过滤液体;6、对质量守恒定律的探究;(铁与硫酸铜反应)7、实验室制取二氧化碳的探究;8、对燃烧条件的探究;9、自己设计、制作并使用简易灭火器;10、酸雨危害的模拟实验;九年级(下)化学探究实验1、金属活动性的探究;(与酸反应、与盐溶液反应)2、铁的生锈条件的探究;3、物质溶解时的热现象;4、饱和溶液、不饱和溶液的探究;5、绘制溶解度曲线;6、自制指示剂;7、酸的化学性质;8、碱的化学性质;9、中和反应;10、用PH试纸测溶液的PH;11、溶液酸碱度对头发的影响;12、粗盐提纯;13、探究初步区分氮肥、磷肥和钾肥的方法。
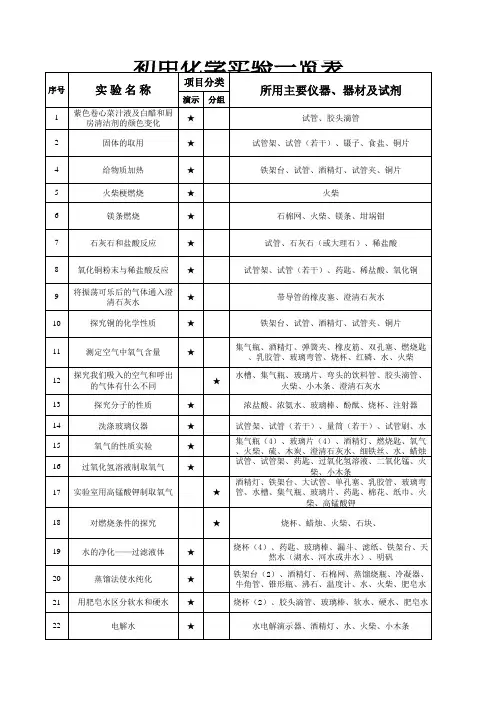
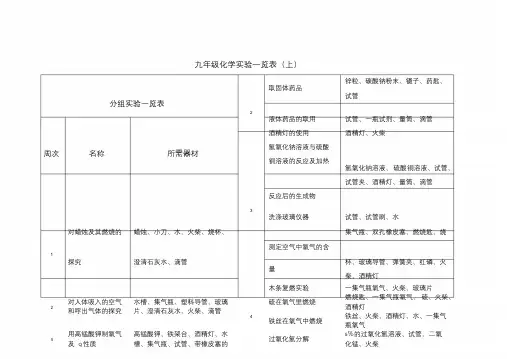
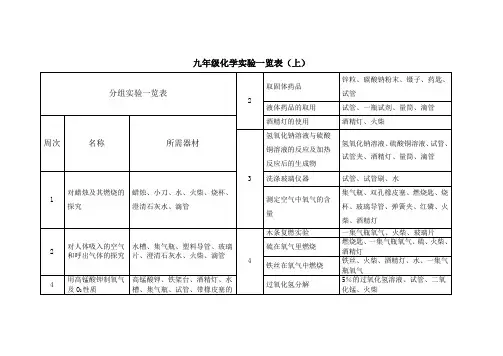
九年级化学实验一览表(上)锌粒、碳酸钠粉末、镊子、药匙、取固体药品试管分组实验一览表2液体药品的取用试管、一瓶试剂、量筒、滴管酒精灯的使用酒精灯、火柴周次名称所需器材氢氧化钠溶液与硫酸铜溶液的反应及加热氢氧化钠溶液、硫酸铜溶液、试管、试管夹、酒精灯、量筒、滴管反应后的生成物3洗涤玻璃仪器试管、试管刷、水对蜡烛及其燃烧的蜡烛、小刀、水、火柴、烧杯、集气瓶、双孔橡皮塞、燃烧匙、烧测定空气中氧气的含1探究澄清石灰水、滴管杯、玻璃导管、弹簧夹、红磷、火量柴、酒精灯木条复燃实验一集气瓶氧气、火柴、玻璃片2 对人体吸入的空气和呼出气体的探究水槽、集气瓶、塑料导管、玻璃片、澄清石灰水、火柴、滴管4硫在氧气里燃烧铁丝在氧气中燃烧燃烧匙、一集气瓶氧气、硫、火柴、酒精灯铁丝、火柴、酒精灯、水、一集气瓶氧气4 用高锰酸钾制氧气及O2 性质高锰酸钾、铁架台、酒精灯、水槽、集气瓶、试管、带橡皮塞的过氧化氢分解5%的过氧化氢溶液、试管、二氧化锰、火柴导管、药匙、石灰水、铁丝、坩铁架台、试管、水槽、集气瓶、酒锅钳加热氯酸钾制氧气精灯、带橡皮塞的导管、氯酸钾、二氧化锰、药匙铁架台、玻璃棒、滤纸、烧杯、6水的电解实验水电解器、水、火柴品红扩散烧杯、品红、水、药匙6 水的净化漏斗、滴管、明矾、药匙、浑浊用肥皂水区分软水和肥皂水、软水、硬水、烧杯、玻璃的天然水硬水棒烧瓶、硬水、碎瓷片、铁架台、冷7制取蒸馏水凝管、胶皮管、锥形瓶、牛角管、托盘天平、白磷、锥形瓶、烧杯、酒精灯、石棉网10 质量守恒定律铁钉、硫酸铜溶液、带橡皮塞的盐酸与硫酸钠反应前硫酸钠粉末、稀盐酸、托盘天平、玻璃管、砂纸后质量测定烧杯、试管10镁条燃烧前后质量测镁条、石棉网、砂纸、托盘天平、定火柴、酒精灯大理石、稀盐酸、试管、铁架台、实验室制取二氧化13石灰水、二氧化碳、火柴、带橡活性炭的吸附作用锥形瓶、红墨水、滴管、活性炭碳的研究皮塞的导管、烧杯、水13水、硫、集气瓶、玻璃片、植物酒精喷灯、试管、铁架台、石灰水、16 酸雨危害模拟实验叶子或果皮、铁架、锌粒、大理木炭还原氧化铜带橡皮塞的导管、木炭粉、氧化铜石或石灰石、燃烧匙粉末铁架台、试管、带橡皮塞的导管、制取C O2 并验满、倾倒、教师演示实验一览表集气瓶、玻璃片、石灰石、稀盐酸、溶解14烧杯、蜡烛、软塑料瓶周次名称所需器材二氧化碳与水反应小紫花、醋酸、水、二瓶CO2 气体、塑料瓶水的沸腾铁架台、试管、酒精灯、水白磷、红磷、铜片、热水、烧杯、燃烧条件探究滤纸胆矾的研碎胆矾、研钵蜡烛(3 支)、烧杯、碳酸钠、盐15蜡烛燃烧现象探究酸、火柴胆矾与氢氧化钠溶金属罐、塑料瓶、面粉、蜡烛、鼓胆矾、氢氧化钠溶液、试管、水粉尘爆炸实验1液气装置、胶皮管石灰石、稀盐酸、试管、烧杯、甲烷燃烧制取甲烷装置、烧杯、火柴石灰石与盐酸反应澄清的石灰水、铁架台、带橡皮16镁与盐酸反应镁条、稀盐酸、试管塞的导管闻气体的操作一瓶氧气、一瓶二氧化碳、火柴九年级化学实验一览表(下)分组实验一览表教师演示实验一览表周次 名称 所需器材周次名称所需器材试管、试管架、 稀盐酸、 稀硫酸、 硫酸铜、硝酸银、镁、锌、铁、 铝、铜1比较合金和纯金属 硬度1金属的活动性顺序黄铜、铜、焊锡、锡蔗糖溶解烧杯、玻璃棒、水托盘天平、烧杯、量筒、滴管、碘或高锰酸钾在水 和汽油中的溶解试管、水、汽油、碘、高锰酸钾、酒精4溶液的配制3玻璃棒、氯化钠、纸片(大小相 植物油在水、 洗涤剂植物油、洗涤剂、水、试管、橡皮塞同)中的溶解NaCL 、N H 4N O 3、NaOH 在水中溶解温度计、水、 NaCL 、N H 4NO 3、NaOH 烧杯、水、食盐、玻璃棒、硝酸钾、铁NaCL 、硝酸钾在水中酸的化学性质点滴板、稀盐酸、稀硫酸、生锈 的铁钉、紫色石蕊试液、无色酚的溶解架台、酒精灯酞试液、镁、锌、铁54相同质量的硫酸铜 试管、固体 CuSO 4、水点滴板、氢氧化钠溶液、氢氧化 在相同质量水中的 碱的化学性质钙溶液、紫色石蕊试液、无色酚 溶解酞试液用PH试纸测溶液的PH值玻璃片、PH试纸、标准比色卡、稀H2S O4、稀HCL、氢氧化钠溶液、5向溶液中加入指示剂试管、试管架、食醋、石灰水、盐酸、6自来水、玻璃棒氢氧化钠溶液、指示剂浓盐酸、浓硫酸的物 理性质浓盐酸、浓硫酸纸、小木棍、布片、玻璃片、浓硫酸、粗盐、铁架台、滤纸、烧杯、玻浓硫酸的腐蚀性7 粗盐的提纯璃棒、漏斗、蒸发皿、酒精灯、 量筒、滴管、石棉网、坩锅钳、 水6氢氧化钠的物理性烧杯、玻璃棒、分液漏斗 固体氢氧化钠、表面皿、试管、水、镊 质及溶解子生石灰的溶解 生石灰、蒸发皿、水、滴管盐酸、硫酸、氢氧化钠溶液、氢氧化钙物质的导电性8 常见化肥鉴别研钵、熟石灰、 烧杯、碳酸氢铵、磷矿粉、硫酸钾、硝酸钾7溶液、乙醇、溶液导电演示器烧杯、玻璃棒、 稀盐酸、 氢氧化钠溶液、 酸碱中和反应无色酚酞试液碳酸钠、碳酸氢钠、稀盐酸、澄清石灰碳酸钠、碳酸氢钠与盐酸反应水、试管、带橡皮塞的导管8碳酸钠与石灰水的 反应碳酸钠溶液、澄清石灰水、试管 聚氯乙烯的燃烧聚氯乙烯碎片、酒精灯、火柴、坩锅钳。

九年级化学演示实验计划九年级(上)化学演示实验1、水加热沸腾;2、研碎胆矾;3、胆矾溶解于水并和NaOH反应;4、石灰石和盐酸反应把产生的气体通入澄清石灰水中;5、闻气体气味的方法;6、固体颗粒的取用(锌粒);7、固体粉末的取用(Na2CO3粉末);8、液体的取用;9、Na2CO3和盐酸反应;10、酒精灯的使用;11、加热NaOH和CuSO4的混合溶液;12、洗涤玻璃仪器;13、测定空气中氧气的含量;14、带火星的木条伸入氧气中;15、硫在空气和氧气中燃烧;16、木炭在空气和氧气中燃烧;17、细铁丝在氧气中燃烧;18、用过氧化氢溶液制取氧气;19、加热KClO3和MnO2混合物制取氧气;20、电解水实验;21、品红在水中扩散实验;22、软硬水的区分23、蒸馏水的制取24、用盐酸和碳酸钠反应验证质量守恒定律;25、镁条在空气中燃烧验证质量守恒定律;26、活性炭的吸附性;27、木炭还原氧化铜;28、收集CO2并验满;29、灯火实验;30、CO2溶于水的验证;31、CO2和水的反应;32、燃烧的条件的实验;33、灭火的原理;34、粉尘爆炸;35、点燃甲烷;36、用Mg和盐酸反应验证化学反应中的能量变化;九年级下化学演示实验1、比较黄铜片和铜片、焊锡和锡;2、蔗糖溶解;3、I2和KMnO4在水和汽油中的溶解性实验;4、水和乙醇能否互溶实验;5、洗涤剂的乳化功能;6、三种不同组成的硫酸铜溶液;7、配制一定溶质质量分数的NaCl溶液;8、向溶液中加入酸碱指示剂;9、观察盐酸、硫酸的颜色和状态、气味;10、浓硫酸的腐蚀性实验;11、浓H2SO4稀释;12、把水慢慢注入浓H2SO4;13、NaOH的物理性质观察;14、生石灰和水反应;15、溶液的导电性;16、中和反应17、Na2CO3和HCl反应;18、Na2CO3溶液和澄清的石灰水反应;19、聚乙烯塑料的热塑性;九年级(上)化学探究实验1、观察和描述——对蜡烛及其燃烧的探究;2、我们吸入的空气和呼出的气体有什么不同;3、实验室制取O2,O2的性质实验;4、对分子运动现象的探究;5、水的净化——过滤液体;6、对质量守恒定律的探究;(铁与硫酸铜反应)7、实验室制取二氧化碳的探究;8、对燃烧条件的探究;9、自己设计、制作并使用简易灭火器;10、酸雨危害的模拟实验;九年级(下)化学探究实验1、金属活动性的探究;(与酸反应、与盐溶液反应)2、铁的生锈条件的探究;3、物质溶解时的热现象;4、饱和溶液、不饱和溶液的探究;5、绘制溶解度曲线;6、自制指示剂;7、酸的化学性质;8、碱的化学性质;9、中和反应;10、用PH试纸测溶液的PH;11、溶液酸碱度对头发的影响;12、粗盐提纯;13、探究初步区分氮肥、磷肥和钾肥的方法。
人教版九年级化学演示实验登记表1. 实验基本信息•实验编号:Chem-Exp-001•实验名称:化学演示实验•实验日期:2022年10月1日•实验地点:化学实验室2. 实验目的•通过化学实验演示,向九年级学生展示化学实验的基本原理和实验操作方法;•培养学生对化学实验的兴趣和探索精神。
3. 实验器材和药品清单序号实验器材数量清洗情况1烧杯2干净2试管5干净3酒精灯1干净4钳子1干净5管子2干净6显色剂1干净7碘1干净8洗涤剂1干净9饱和盐溶液1干净10砂纸1干净11指示剂1干净12盐酸1干净13助燃剂1干净4. 实验步骤1.实验准备:–领取实验器材和药品清单;–检查所需器材和药品是否齐全;–清洗器材,确保干净无污染。
2.演示实验操作步骤:–步骤1:将烧杯中加入10毫升饱和盐溶液;–步骤2:加热烧杯中的饱和盐溶液,并观察变化;–步骤3:取一只试管,加入适量的洗涤剂,再加入少量的酒精,摇匀;–步骤4:点燃酒精灯,将试管口倾斜放入酒精灯火焰中,观察现象;–步骤5:将碘放在试管底部,加入适量的水,摇匀后观察变化;–步骤6:用钳子夹住一根管子,将管子放入洗涤剂溶液中,观察现象;–步骤7:将砂纸用力揉搓,观察变化;–步骤8:取一只试管,加入指示剂滴至试管底部,加入适量的盐酸,观察颜色变化;–步骤9:将助燃剂加在试管底部,点燃助燃剂,观察现象。
3.实验记录:–观察并记录每个步骤的实验现象和结果;–将实验过程中的注意事项和安全措施进行记录;–适当拍摄实验现象和过程的照片作为实验记录。
5. 实验结果根据实验操作步骤和观察记录,得出以下实验结果:1.步骤2观察到饱和盐溶液加热后产生了水的蒸汽和盐的结晶。
2.步骤4观察到试管口倾斜时,酒精灯火焰会延烧至试管内,产生燃烧现象。
3.步骤5观察到碘溶液加入水后,溶液变为蓝色。
4.步骤6观察到管子放入洗涤剂溶液中,溶液会上升。
5.步骤7观察到砂纸揉搓后,砂纸表面变为暗淡。
6.步骤8观察到指示剂和盐酸混合后,溶液变为红色。
九年级化学演示实验目录一览表演示实验:上册:1、化学变化和性质2、对蜡烛及其燃烧探究3、化学实验的基本操作4、空气成分的粗略测定5、氧气的性质6、氧气的实验室制法7、水的组成8、分子运动9、水的净化(实验3-3,3-4)10、质量守恒定律探究11、木炭的吸附作用12、碳的化学性质13、二氧化碳的制取14、二氧化碳和一氧化碳(实验6-3,6-4,6-5,6-6,6-7,6-8)15、燃烧条件和灭火方法的探究16、甲烷的燃烧17、化学反应中的能量变化下册:1、比较合金与纯金属的硬度2、溶液的形成(实验9-1 9-2 9-3 9-4)3、溶质的质量分数(实验9-5 9-6)4、酸、碱与指示剂的反应5、酸的物理性质6、浓硫酸的腐蚀性7、浓硫酸的稀释(实验10-4 10-5)8、常见碱的物理性质(实验10-6 10-7)9、溶液的导电性10、中和反应11、常见盐的化学性质九年级化学学生实验目录一览表上册:1、对蜡烛及其燃烧的实验究2、对人体吸入空气和呼出气体成分的探究3、化学变化的现象4、氧气的制取和性质5、分子运动6、水的净化—过滤7、对质量守恒定律的探究8、二氧化碳的制取和性质9、对燃烧条件、灭火原理和方法探究实验10、对酸雨危害的模拟探究实验下册:1、金属的化学性质2、铁钉锈蚀条件的探究3、溶解时的吸热放热现象4、饱和溶液与不饱和溶液的探究5、配制一定溶质质量分数的溶液6、酸、碱与植物花质的反应7、酸的化学性质8、碱的化学性质9、用PH试纸测定一些液体的PH10、溶液酸碱度对头发的影响11、粗盐提纯12、复分解反应条件的探究13、探究初步区分常用氮肥、磷肥和钾肥的方法。
九年级化学演示实验计划九年级(上)化学演示实验1、水加热沸腾;2、研碎胆矾;3、胆矾溶解于水并和NaOH反应;4、石灰石和盐酸反应把产生的气体通入澄清石灰水中;5、闻气体气味的方法;6、固体颗粒的取用(锌粒);7、固体粉末的取用(Na2CO3粉末);8、液体的取用;9、Na2CO3和盐酸反应;10、酒精灯的使用;11、加热NaOH和CuSO4的混合溶液;12、洗涤玻璃仪器;13、测定空气中氧气的含量;14、带火星的木条伸入氧气中;15、硫在空气和氧气中燃烧;16、木炭在空气和氧气中燃烧;17、细铁丝在氧气中燃烧;18、用过氧化氢溶液制取氧气;19、加热KClO3和MnO2混合物制取氧气;20、电解水实验;21、品红在水中扩散实验;22、软硬水的区分23、蒸馏水的制取24、用盐酸和碳酸钠反应验证质量守恒定律;25、镁条在空气中燃烧验证质量守恒定律;26、活性炭的吸附性;27、木炭还原氧化铜;28、收集CO2并验满;29、灯火实验;30、CO2溶于水的验证;31、CO2和水的反应;32、燃烧的条件的实验;33、灭火的原理;34、粉尘爆炸;35、点燃甲烷;36、用Mg和盐酸反应验证化学反应中的能量变化;九年级下化学演示实验1、比较黄铜片和铜片、焊锡和锡;2、蔗糖溶解;3、I2和KMnO4在水和汽油中的溶解性实验;4、水和乙醇能否互溶实验;5、洗涤剂的乳化功能;6、三种不同组成的硫酸铜溶液;7、配制一定溶质质量分数的NaCl溶液;8、向溶液中加入酸碱指示剂;9、观察盐酸、硫酸的颜色和状态、气味;10、浓硫酸的腐蚀性实验;11、浓H2SO4稀释;12、把水慢慢注入浓H2SO4;13、NaOH的物理性质观察;14、生石灰和水反应;15、溶液的导电性;16、中和反应17、Na2CO3和HCl反应;18、Na2CO3溶液和澄清的石灰水反应;19、聚乙烯塑料的热塑性;九年级(上)化学探究实验1、观察和描述——对蜡烛及其燃烧的探究;2、我们吸入的空气和呼出的气体有什么不同;3、实验室制取O2,O2的性质实验;4、对分子运动现象的探究;5、水的净化——过滤液体;6、对质量守恒定律的探究;(铁与硫酸铜反应)7、实验室制取二氧化碳的探究;8、对燃烧条件的探究;9、自己设计、制作并使用简易灭火器;10、酸雨危害的模拟实验;九年级(下)化学探究实验1、金属活动性的探究;(与酸反应、与盐溶液反应)2、铁的生锈条件的探究;3、物质溶解时的热现象;4、饱和溶液、不饱和溶液的探究;5、绘制溶解度曲线;6、自制指示剂;7、酸的化学性质;8、碱的化学性质;9、中和反应;10、用PH试纸测溶液的PH;11、溶液酸碱度对头发的影响;12、粗盐提纯;13、探究初步区分氮肥、磷肥和钾肥的方法。
三亚市崖城中学九年级化学实验教学计划(2012-2013学年度第一学期)化学科组:林艳 2012年9月化学是一门以实验为基础的学科。
化学元素贯穿于整个化学教育教学之中,是化学教学的重中之重。
实验教学可以激发学生学习化学的兴趣,帮助学生形成概念,获得知识和技能,培养观察和实验能力,还有助于培养实事求是、严肃认真的科学态度和科学的学习方法。
因此,特制定本年度第一学期九年级化学实验教学计划。
一、指导思想:培养出来的学生能够适应时代,并使他们在一定程度上能够超越时代,真正能够面向未来,注重实验教学,提高学生动手操作能力,要使得学生能在实验中用探究的方法去学习,领会知识的内涵,同时在一定程度上能够学会去发明创造。
争取将实验教学工作推上一个新的台阶。
二、教学措施:第一、认真备课。
备课将按照以下步骤和要求进行。
1.备课标。
明确:(1)实验教学的任务;(2)实验教学的目的;(3)实验教学的要求;(4)实验教学规定的内容。
2.备教材。
(1)熟悉教材中实验的分布体系。
(2)掌握教材中的实验和丰富实验教学内容。
3.备教法。
教有法而无定法,实验教学的教法应牢固树立准确、示范、讲解与操作协调一致的原则。
4.备学生。
学生是教学的主体,对学生年龄特征、心理特点、认识和思维水平以及对不同年级、不同阶段的实验进行分析、研究,对实验教学将起着积极的促进作用。
5.实验教学前的准备。
(1)演示实验:a、掌握实验原理。
b、熟悉实验仪器。
c、选择实验方法。
d、设计实验程序e、实验效果的试做。
(2)学生实验:a、制定学生实验计划。
b、实验环境的准备。
c、实验器材的准备d、指导学生准备。
6.编写教案。
第二、仔细组织教学。
节课的成功与否,课堂调控是关键的一个环节。
因此,教学的开始强化课堂纪律很有必要,其次是引入新课题,让学生明确实验的目的和要求、原理、方法步骤,使学生了解观察的重点。
教师在引导指点学生观察时,讲解要与演示恰当配合,讲解要抓住重点、难点和关键,语言要精辟、简要、准确,操作要熟练、规范。
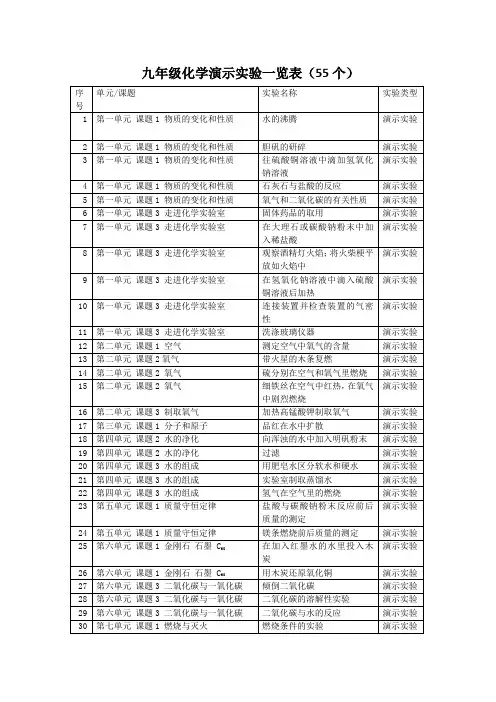
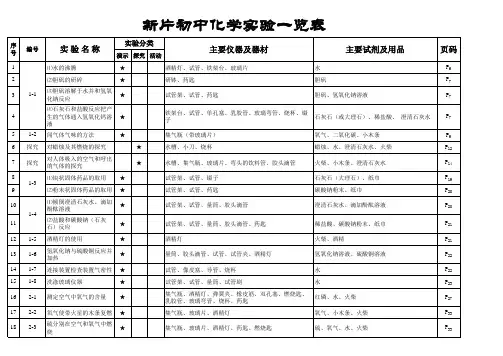
新版九年级化学演示实验一览表
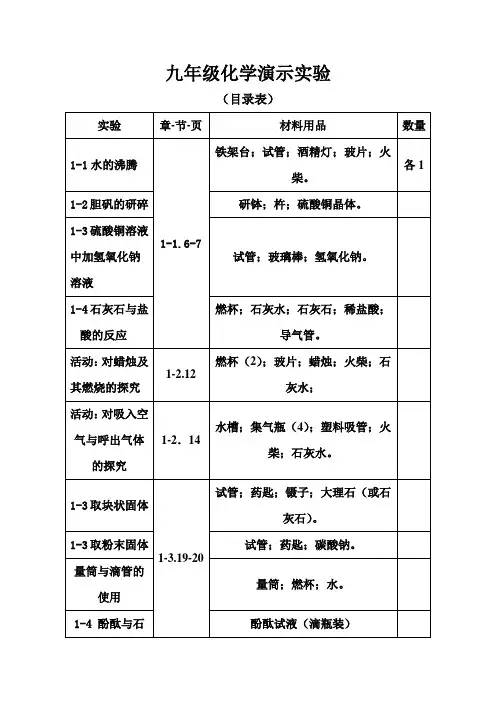
1、1-1(1)水的沸腾
(2) 胆矾的研碎
(3) 硫酸铜溶液中加氢氧化钠溶液
(4) 石灰石与盐酸的反应
2、1-2二氧化碳与氧气的性质
3、1-3(1)取块状固体
(2) 取粉末固体
4、1-4 (1)澄清的石灰水滴加酚酞溶液
(2)碳酸钠粉末与稀盐酸反应
5、1-5酒精灯的使用
6、1-6加热氢氧化钠溶液与硫酸铜溶液的反应物
7、1-7 连接装置并检查装置的气密性
8、1-8洗涤玻璃仪器
9、2-1测定空气里氧气含量
10、2-2氧气使带火星的木条复燃
11、2-3硫的燃烧
12、2-4细铁丝在氧气中燃烧
13、2-5加热高锰酸钾制氧气
14、3-1品红的扩散
15、4-1取两杯浑浊的天然水沉淀
16、4-2过滤器的制作
17、4-3用肥皂区分软硬水
18、4-4制取蒸馏水
19、4-5点燃氢气
20、5-1盐酸与碳酸钠粉末反应前后质量的测定
21、5-2镁条燃烧前后质量的测定
22、6-1木炭的吸附作用
23、6-2木炭还原氧化铜
24、6-3二氧化碳使燃着的蜡烛熄灭
25、6-4二氧化碳的溶解性
26、6-5二氧化碳与水反应
27、7-1燃烧的条件
28、7-2粉尘爆炸
29、7-3生石灰与水反应放出热量
30、7-4甲烷的燃烧
31、8-1比较合金和纯金属的硬度
32、9-1蔗糖溶解
33、9-2碘或高锰酸钾分别放入水或汽油中
34、9-3水和乙醇能够互溶吗?
35、9-4水和油的小实验
36、9-5氯化钠在水中的溶解
37、9-6硝酸钾在水中的溶解
38、9-7三种不同组成的硫酸铜溶液
39、9-8两种溶质质量分数不同的氯化钠溶液
40、10-1向溶液中加入酸碱指示剂
41、10-2观察盐酸、硫酸
42、10-3浓硫酸的腐蚀性
43、10-4浓硫酸的溶解
44、10-5观察氢氧化钠
45、10-6观察氢氧化钙
46、10-7试验物质的导电性
47、10-8中和反应
48、10-9PH试纸的使用
49、10-10测定生活中一些物质的PH
50、11-1碳酸钠与盐酸反应
51、11-2碳酸钠与石灰水反应
52、11-3硫酸铜溶液分别与氢氧化钠、氯化钡溶液的反应
53、12-1加热聚乙烯塑料碎片。