镁铝及其化合物
- 格式:ppt
- 大小:1.29 MB
- 文档页数:52

第2讲镁、铝及其重要化合物复习目标知识建构1.结合真实情景中的应用实例或通过实验探究,了解镁、铝及其重要化合物的主要性质,了解其在生产、生活中的应用。
2.结合实例认识金属性质的多样性,了解通过化学反应可以探索物质性质、实现物质的转化,认识物质及其转化在自然资源综合利用和环境保护中的重要作用。
一、镁、铝1.原子结构和存在(1)原子结构:镁、铝原子结构示意图分别为和,分别位于元素周期表的第三周期ⅡA族和ⅢA族。
(2)存在:在自然界中均以化合态的形式存在,铝是地壳中含量最多的金属元素。
2.单质的物理性质(1)相同点:均为银白色有金属光泽的固体,有良好的延展性、导电性和导热性等,密度、硬度均较小。
(2)不同点:铝的熔点比镁高,硬度比镁大。
3.单质的化学性质镁铝4.镁、铝的冶炼(1)Mg :化学方程式 MgCl 2(熔融)=====电解Mg +Cl 2↑; (2)Al :化学方程式2Al 2O 3(熔融)=====电解冰晶石4Al +3O 2↑。
【判一判】 判断下列说法是否正确,正确的打“√”,错误的打“×”。
(1)工业上制造镁粉时,可将镁蒸气在N 2中冷却( )(2)相同质量的镁条分别在足量的CO 2和O 2中完全燃烧,所得固体的质量相同( )(3)冶炼铝时常用焦炭作还原剂()(4)铝与少量NaOH溶液反应得到铝盐,与足量NaOH溶液反应生成偏铝酸盐()(5)铝制餐具可长时间存放酸性或碱性食物()(6)镁在空气中燃烧的产物固体只有MgO()答案(1)×(2)×(3)×(4)×(5)×(6)×二、镁、铝的重要化合物1.MgO与Al2O32.Mg(OH)2与Al(OH)33.明矾(1)化学式为KAl(SO4)2·12H2O,它是无色晶体,可溶于水。
(2)明矾净水的原理电离方程式为KAl(SO4)2===K++Al++2SO-4,其中Al3+发生水解反应,产生Al(OH)3胶体,能吸附水中悬浮物形成沉淀,使水澄清。
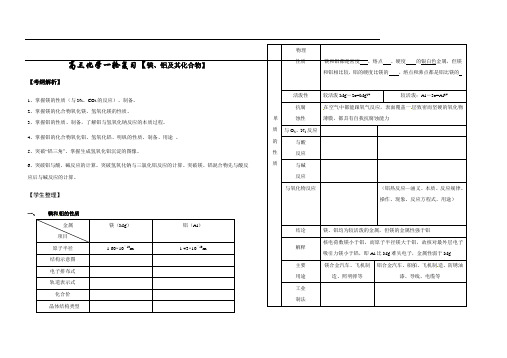
在空气中都能跟氧气反应,表面覆盖一层致密而坚硬的氧化物薄膜,都具有自我抗腐蚀能力铝合金汽车、船舶、飞机制造、防锈油漆、导线、电缆等易错点:(1)常温下,能用铝制容器盛放浓硫酸、浓硝酸的原因是二者能使铝发生“钝化”,而不是铝与浓硫酸、浓硝酸不反应。
(2)铝不但能与酸(H +)反应,还能够与碱溶液反应,表现为特殊性。
2Al +2OH -+2H 2O===2AlO -2+3H 2↑。
其反应机理应为:铝先与强碱溶液中的水反应生成H 2和Al(OH)3,然后Al(OH)3再与NaOH 反应生成H 2O 和NaAlO 2,反应中铝作还原剂,水作氧化剂,NaOH 无电子得失。
(3)铝热反应是在高温干态下进行的置换反应,铝只能与排在金属活动性顺序其后的金属氧化物反应。
铝不能与MgO 反应,铝热反应不能用来冶炼大量的金属铁、铜等(要考虑冶炼成本)。
(4)Mg 在CO 2中能够燃烧,所以活泼金属镁着火不能用干粉灭火器和泡沫灭火器灭火。
同时镁与氮气反应生成Mg 3N 2。
二、铝的重要化合物1.氧化铝(1)物理性质 色态: ;硬度: ;熔点: 。
(2)化学性质①属于两性氧化物,写出有关反应的离子方程式:,②电解 化学方程式为 2Al 2O 3(熔融)=====电解4Al +3O 2↑。
(3)用途熔点很高,是一种较好的耐火材料,天然产刚玉的成分是Al 2O 3,还可制作各种宝石。
2.氢氧化铝 (1)物理性质Al(OH)3是一种难溶于水的白色胶状物质,具有较强的吸附能力。
(2)化学性质 ①两性Al(OH)3的电离方程式为Al(OH)3既能溶于强酸又能溶于强碱,且都生成盐和水。
与强酸反应: , 与强碱溶液反应: 。
②不稳定性Al(OH)3受热分解: 。
(3)制备①向铝盐中加入氨水,离子方程式为 。
②NaAlO 2溶液中通入足量CO 2,离子方程式为 。
③NaAlO 2溶液与AlCl 3溶液混合:离子方程式为 。


镁铝及其化合物一、物理性质银白色固体、镁的硬度、熔点均低于铝,是由于二者的金属键强度不同造成的。
二、原子结构镁的第一电离能高于铝,由原子结构决定的。
三、化学性质1.与非金属反应2Mg +O2=(点燃)2MgO 4Al +3O2=(△)2 Al2O3Mg+Cl2= (点燃)MgCl2 4Al+3Cl2=(△)2AlCl3Mg + S= (△)MgS 2Al + 3S=(△)Al2S33Mg+ N2=(△)Mg3N2 不反应●镁与铝在常温下均可生成致密的氧化膜,保护金属。
●镁在空气中点燃,可与N2、O2、CO2反应。
2.与酸反应Mg + 2H+ = Mg2+ + H2↑(与硝酸反应复杂,浓度不同,还原产物不同)2Al + 6H+ === 2Al3+ + 3H2↑(常温下遇浓硝酸、冷的浓硫酸钝化)3.与沸水反应Mg +H2O=(△)Mg(OH)2+H2↑ Al不反应,铁与沸水也可反应。
4.与氧化物反应2Mg + CO2=(点燃)2MgO + C 2Al+Fe3O4=(高温)2Fe+ Al2O35.与碱反应镁不反应 2Al + 2H2O +2NaOH =2NaAlO2 + 3H2↑四、氧化镁与氧化铝(两性氧化物)1.物理性质白色固体、密度小、熔点高,用于生产耐火、耐高温材料。
2.化学性质●与水反应: MgO+H2O=Mg(OH)2 很慢不反应●与酸反应: MgO+2H+=Mg2++H2O Al2O3+ 6H+=2Al3++3H2O●与碱反应:不反应 Al2O3+ 2OH+=2AlO2-+H2O五、氢氧化铝与氢氧化镁1.物理性质氢氧化镁是难溶的中强碱,能使酚酞变红。
氢氧化铝是一种白色胶状难溶物,不能使酚酞变色。
2.化学性质●分解反应: Mg(OH)2=(△)MgO+ H2O 2Al(OH)3=(△)Al2O3+3H2O●与酸反应: Mg(OH)2+2H+=Mg2++2H2O Al(OH)3 + 3H+ = Al3+ + 3H20●与碱反应:Al(OH)3 +OH-=AlO2-+2H2O 不反应●溶解性: Mg(OH)2+2NH4+=2Mg2++2NH3↑+2H20即可溶于浓NH4Cl中 Al(OH)3不溶于氨水六、具有两性的物质1.两性氧化物如Al2O32.两性氢氧化物如Al(OH)33.单质如Al4.弱酸的铵盐如(NH4)2S、(NH4)2CO3、NH4AC。

镁铝及其化合物知识点 SANY标准化小组 #QS8QHH-HHGX8Q8-GNHHJ8-镁、铝及其化合物知识点整理Ⅰ.课标要求1.通过海水制镁的事例了解镁及化合物的性质.2.通过合金材料了解铝及化合物的性质.3.能列举合金材料的重要应用.Ⅱ.考纲要求1.掌握镁铝及化合物的性质.2.了解镁铝及化合物在生活.生活中的应用.Ⅲ.教材精讲一. Mg、Al的化学性质1.与非金属反应(1)与O2反应:常温下与空气中的O2反应生成一层致密的氧化物薄膜,所以镁、铝都有抗腐蚀的性能。
镁能在空气中燃烧:2Mg+O22MgO ,铝在纯氧中燃烧:4Al+ 3O22Al2O3(2)与卤素单质、硫等反应:Mg+ Cl 2MgCl 22Al+ 3Cl 22AlCl 32Al+ 3SAl 2S 3 (用于工业制备) Mg+ SMgS③集气瓶底部都要放一些细纱,以防止集气瓶炸裂。
2.与H 2O 反应Mg 、A1和冷水都不反应,但在加热条件下与水反应生成氢氧化物和氢气Mg+2H 2O (沸水) Mg(OH)2+H 2↑ 2A1+6H 2O2A1(OH)3+3H 2↑[特别提醒]:①镁在空气中用酒精灯火焰点燃即可燃烧,而铝在空气中需要高温点燃才能燃烧。
镁在空气中燃烧时有三个反应发生: 2Mg+O 22MgO 3Mg+N 2Mg 3N 2 2Mg+CO 22MgO+C②燃烧时都放出大量的热,发出耀眼的白光。
利用镁的这种性质来制造照明弹。
3.与酸反应置换出H2Mg、A1与浓、稀盐酸、稀硫酸、磷酸等酸反应置换出H2,其中铝在冷浓 H2SO4,冷浓硝酸中发生钝化现象。
所以可用铝制容器贮存冷的浓硫酸或浓硝酸。
4.与某些氧化物反应(1)镁与二氧化碳反应:2Mg+CO22MgO+C[特别提醒]:“CO2不能助燃”的说法是不全面的,CO2对绝大多数可燃物是良好的灭火剂,而对K、Ca、Na、Mg等可燃物却是助燃剂。
(2)铝热反应:2Al+ Fe2O32Fe+ Al2O3铝热反应可用于焊接钢轨和冶炼某些难熔金属,如:V、Cr、等。

镁、铝及其重要化合物一、镁及其重要化合物的主要性质和应用 1.镁的性质(1)物理性质:具有□01银白色金属光泽的固体,密度、硬度均较□02小,熔点较□03低,有良好的□04导电性、□05导热性和□06延展性。
(2)化学性质①与非金属反应②与CO 2反应:□102Mg +CO 2=====点燃2MgO +C③与H 2O 反应:□11Mg +2H 2O=====煮沸Mg(OH)2+H 2↑④与H +反应:□12Mg +2H +===Mg 2++H 2↑ 2.从海水中提取镁的流程 (1)流程(2)主要化学反应 ①制石灰乳□13CaCO 3=====高温CaO +CO 2↑、□14CaO +H 2O===Ca(OH)2;②沉淀Mg 2+:□15Mg 2++Ca(OH)2===Mg(OH)2↓+Ca 2+; ③制备MgCl 2:□16Mg(OH)2+2HCl===MgCl 2+2H 2O ; ④电解MgCl 2:□17MgCl 2(熔融)=====电解Mg +Cl 2↑。
3.用途生产□18合金,冶金工业上用作□19还原剂和□20脱氧剂。
4.镁的重要化合物二、铝的性质及应用 1.铝的物理性质注:铝是地壳中含量最高的金属元素。
2.铝的化学性质写出图中标号反应的化学方程式或离子方程式:④□112Al +2OH -+2H 2O===2AlO -2+3H 2↑ ⑤□122Al +Fe 2O 3=====高温Al 2O 3+2Fe(铝热反应)3.铝的制备及用途三、铝的重要化合物 1.氧化铝(1)物理性质:白色固体,难溶于水,有很高的熔点。
(2)化学性质2.氢氧化铝 (1)物理性质白色胶状不溶于水的固体,有较强的□01吸附性。
(2)化学性质(用化学方程式表示) Al(OH)3的电离方程式为②受热分解:□032Al(OH)3=====△Al 2O 3+3H 2O 。
(3)制备①向铝盐中加入氨水,离子方程式为 Al 3++3NH 3·H 2O===Al(OH)3↓+3NH +4。
第11讲金属镁、铝及及其化合物一镁、铝单质的性质1.镁、铝的结构和存在形态2.镁、铝的物理性质镁、铝都是银白色、有金属光泽的固体,密度较小,硬度较低,均具有良好的延展性、导电性和导热性等。
3.铝的化学性质特别强调:1.常温下,能用铝制容器盛放浓硫酸、浓硝酸的原因是二者能使铝发生“钝化”,而不是铝与浓硫酸、浓硝酸不反应。
2.能与铝反应产生氢气的溶液可能呈强酸性也可能呈强碱性。
4.对比掌握镁的化学性质特别强调:1.Mg在CO2中能够燃烧,所以活泼金属镁着火不能用干粉灭火器和泡沫灭火器灭火。
2.镁也可在氮气中燃烧,生成氮化镁(Mg3N2),氮化镁能与水剧烈反应生成Mg(OH)2沉淀并放出氨气。
5.从海水中提取镁(1)工艺流程(2)基本步骤及主要反应特别强调:1.由MgCl2·6H2O得到无水MgCl2,必须在HCl气流中加热,以防MgCl2水解。
2.因镁在高温下能与O2、N2、CO2等气体发生反应,故工业电解MgCl2得到的镁,应在H2氛围中冷却。
3.Mg在空气中燃烧得到的固体物质主要为MgO和少量Mg3N2及C的混合物。
4.Mg(OH)2为难溶于水的白色沉淀,故常用NaOH溶液检验Mg2+的存在。
5.由于Mg(OH)2的溶解度比MgCO3的小,故水垢的主要成分中含有的是Mg(OH)2,而非MgCO3。
6.镁的用途(1)镁合金用于制造火箭、导弹和飞机的部件;(2)镁制造信号弹和焰火;(3)MgO作耐火材料。
课堂检测011.科学家发明的透明坚硬镁铝氧化物新型材料,可以用作显示器和手机屏幕,下列关于镁、铝的说法正确的是()A.镁铝制品在空气中能稳定存在是因为铝不活泼B.浓HNO3、浓H2SO4能用铝制器皿盛装是因为铝与浓HNO3、浓H2SO4不反应C.镁、铝均能与NaOH溶液反应D.铝与Fe2O3发生铝热反应是利用了Al的还原性比Fe强答案:D2.小明家中收藏着一件清末的铝制品佛像,该佛像至今仍保存完好。