镁铝及其化合物全面版
- 格式:ppt
- 大小:1.45 MB
- 文档页数:53




第⼆节镁铝及其重要化合物完美版专题1 ⾦属及其化合物第⼆节镁铝及其重要化合物⼀、铝、镁 1.存在:。
2.物理性质:。
【问题与引⼊】(1)根据⾦属钠的性质和铝、镁的原⼦结构预测铝、镁的化学性质。
(2)根据下图镁、铝及其化合物转化关系了解镁铝的化学性质并写出相应的化学⽅程式。
3.化学性质(1)铝的化学性质①②③④(标明电⼦转移⽅向和数⽬)⑤(2)镁的化学性质①②③(标明电⼦转移⽅向和数⽬)④(标明电⼦转移⽅向和数⽬)【问题讨论与解决】⾮氧化性酸氧化性酸Al酸遇冷的浓硫酸或浓硝酸。
常温点燃O 2Al形成致密的氧化膜1)⽐较钠、镁、铝的相同点与不同点?2)说出镁、铝分别在空⽓中燃烧的现象,所得的固体产物有哪些?(⽤化学式表⽰)3)铝的化学性质活泼,为什么⽇常⽣活中⼴泛使⽤铝制品通常具有较好的抗腐蚀性能?⽽铝制餐具为何不能蒸煮或长期盛放酸碱咸物质?4)铝既能溶于强酸,⼜能溶于强碱,所以说:“铝既有⾦属性,⼜有⾮⾦属性”你认为这样说法是否恰当,为什么?5)铝分别与氧化性酸及⾮氧化性反应的本质是什么?什么物质充当氧化剂?6)向⼀个铝制易拉罐充满CO2⽓,然后往罐内注⼊⾜量的NaOH溶液,⽴即⽤胶布严封罐⼝,不多会⼉听到罐内“卡卡”作响,发现易拉罐变瘪,再过⼀会易拉罐⼜⿎起来。
①易拉罐变瘪的原因,反应的离⼦反应式;②易拉罐⼜⿎起来的原因,离⼦反应式。
【对点训练】1.关于铝及其化合物的下列说法不正确...的是A.铝及其合⾦很早就得到了⼴泛的使⽤B.不能⽤铝制品来蒸煮酸性、碱性或咸的⾷物C.铝是地壳中含量最多的⾦属元素D.铝既能与盐酸反应,⼜能与NaOH溶液反应,都产⽣氢⽓,表现还原性2.镁、铝单质的化学性质以相似为主,但也存在某些重⼤的差异性,下列物质能⽤于证明两者存在较⼤的差异性的是()A.CO2B.盐酸C.NaOH溶液D.⽔3.《优化设计》第43页例题14.Ca、Ba与Mg原⼦的最外层电⼦数相等,下列有关它们的单质及其化合物性质叙述中,错误的是A.在⽔中会有⽓体⽣成B.碳酸盐都不能溶于⽔C.硫酸盐都不能溶于⽔D.都能在⼆氧化碳⽓体中燃烧5.锂和镁的最外层电⼦数虽然不同,但它们性质相似,如它们的单质在氧⽓中反应都⽣成氧化物。



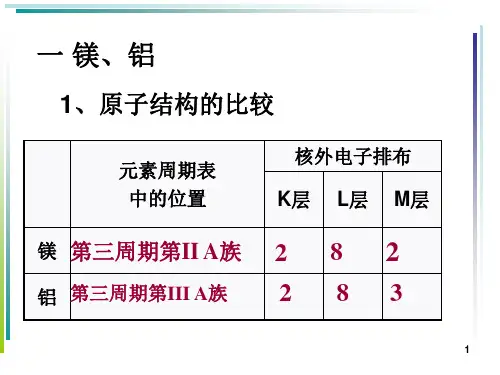
第11讲金属镁、铝及及其化合物一镁、铝单质的性质1.镁、铝的结构和存在形态2.镁、铝的物理性质镁、铝都是银白色、有金属光泽的固体,密度较小,硬度较低,均具有良好的延展性、导电性和导热性等。
3.铝的化学性质特别强调:1.常温下,能用铝制容器盛放浓硫酸、浓硝酸的原因是二者能使铝发生“钝化”,而不是铝与浓硫酸、浓硝酸不反应。
2.能与铝反应产生氢气的溶液可能呈强酸性也可能呈强碱性。
4.对比掌握镁的化学性质特别强调:1.Mg在CO2中能够燃烧,所以活泼金属镁着火不能用干粉灭火器和泡沫灭火器灭火。
2.镁也可在氮气中燃烧,生成氮化镁(Mg3N2),氮化镁能与水剧烈反应生成Mg(OH)2沉淀并放出氨气。
5.从海水中提取镁(1)工艺流程(2)基本步骤及主要反应特别强调:1.由MgCl2·6H2O得到无水MgCl2,必须在HCl气流中加热,以防MgCl2水解。
2.因镁在高温下能与O2、N2、CO2等气体发生反应,故工业电解MgCl2得到的镁,应在H2氛围中冷却。
3.Mg在空气中燃烧得到的固体物质主要为MgO和少量Mg3N2及C的混合物。
4.Mg(OH)2为难溶于水的白色沉淀,故常用NaOH溶液检验Mg2+的存在。
5.由于Mg(OH)2的溶解度比MgCO3的小,故水垢的主要成分中含有的是Mg(OH)2,而非MgCO3。
6.镁的用途(1)镁合金用于制造火箭、导弹和飞机的部件;(2)镁制造信号弹和焰火;(3)MgO作耐火材料。
课堂检测011.科学家发明的透明坚硬镁铝氧化物新型材料,可以用作显示器和手机屏幕,下列关于镁、铝的说法正确的是()A.镁铝制品在空气中能稳定存在是因为铝不活泼B.浓HNO3、浓H2SO4能用铝制器皿盛装是因为铝与浓HNO3、浓H2SO4不反应C.镁、铝均能与NaOH溶液反应D.铝与Fe2O3发生铝热反应是利用了Al的还原性比Fe强答案:D2.小明家中收藏着一件清末的铝制品佛像,该佛像至今仍保存完好。



系列二 主族金属专题8 镁铝及其化合物一、镁单质(1)镁在自然界没有单质存在,存在于各类硅酸盐和碳酸盐矿物里,如菱镁矿(MgCO 3)、白云石(CaCO 3·MgCO 3)、光卤石(KCl·MgCl 2·6H 2O)等。
海水中的镁是提取镁的主要来源,海水中的镁即使提取100万年也不会减少0.01%。
镁也是叶绿素的主要成分,在人体内镁以磷酸盐、碳酸盐的形式分布于骨头和肌肉中,缺乏会引起肌肉的颤动、脉象的混乱。
(2)强还原性:不论在固态或水溶液中都表现出强还原性,常用作还原剂。
高温下,镁夺取氧的能力特别强,甚至能在二氧化碳里燃烧,如2Mg+CO 2=====点燃2MgO+C ;也能够还原二氧化硅,2Mg+SiO 2=====点燃2MgO+Si ;常温下,由于镁表面的氧化膜导致镁不与水反应,但是加热下可以反应,Mg+2H 2O ====△Mg(OH)2+H 2↑。
(3)镁可以与大多数非金属和几乎所有的酸反应。
如2Mg+O 2=====点燃2MgO ,Mg+Cl 2=====点燃MgCl 2,Mg+S =====点燃MgS ,3Mg+N 2=====点燃Mg 3N 2(Mg 3N 2的特殊性质:Mg 3N 2+6H 2O =====3Mg (OH )2↓+2NH 3↑,导致其只能干态制取)。
镁不能和氢氟酸反应,因为MgF 2难溶会阻碍继续反应。
(4)格氏试剂:在醚的溶液中,镁能与卤代烃作用生成在有机化学中应用广泛的格氏试剂:Mg + RX =====醚RMgX(5)制取单质镁:一般是先从海水中得到氯化镁,然后电解熔融的氯化镁,MgCl 2(熔融) =====电解Mg+Cl 2↑。
二、镁的化合物(1)MgO 俗称菱苦土,是一种白色粉末。
MgO 对水呈一定惰性,特别是高温火烧后的MgO 难溶于水。
煆烧温度在923K 左右制成轻质MgO ,煆烧温度在1923K 以上制成重质MgO 。