第九章羧酸及其衍生物和取代酸
- 格式:docx
- 大小:127.12 KB
- 文档页数:8

RCOOH..第九章 羧酸及其衍生物和取代酸(一COOH )官能团的化合物,一元饱和脂肪羧酸的通式为C n H 2n O 2 。
羧基中的羟基被其它原子或基团取代的产物称为羧酸衍生物(如酰卤、酸酐、酯、酰胺等),羧酸烃基上的氢原子被其他原子或基团取代的产物称为取代酸(如卤代酸、羟基酸、羰基酸、氨基酸等)。
羧酸是许多有机化合物氧化的最终产物,常以盐和酯的形式广泛存在于自然界,许多羧酸在生物体的代谢过程中起着重要作用。
羧酸对于人们的日常生活非常重要,也是重要的化工原料和有机合成中间体。
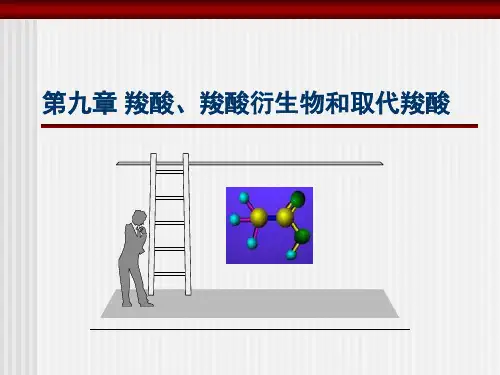
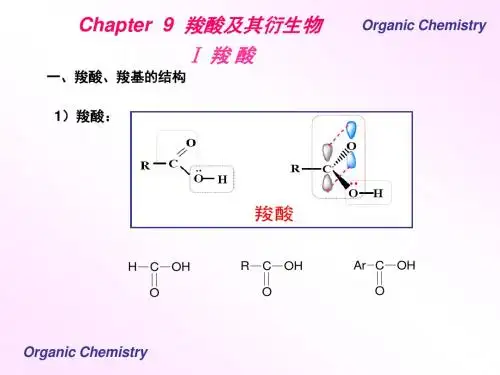
§9-1 羧酸一、羧酸的结构、分类和命名 1、羧酸的结构在羧酸分子中,羧基碳原子是sp 2杂化的,其未参与杂化的p 轨道与一个氧原子的p 轨道形成C=O 中的π键,而羧基中羟基氧原子上的未共用电子对与羧基中的C=O 形成p -π共轭体系,从而使羟基氧原子上的电子向C=O 转移,结果使C=O 和C —O 的键长趋于平均化。
X 光衍射测定结果表明:甲酸分子中C=O 的键长(0.123 nm )比醛、酮分子中C=O 的键长(0.120nm )略长,而C —O 的键长(0.136nm )比醇分子中C —O 的键长(0.143nm )稍短。
RCOOH羧基上的p -π共轭示意图2、羧酸的分类和命名 2.1.羧酸的分类根据分子中烃基的结构,可把羧酸分为脂肪羧酸(饱和脂肪羧酸和不饱和脂肪羧酸)、脂环羧酸(饱和脂环羧酸和不饱和脂环羧酸)、芳香羧酸等;根据分子中羧基的数目,又可把羧酸分为一元羧酸、二元羧酸、多元羧酸等。
例如:或OOCOOcCOOHHOOC HOOC CH 2COOHCH 2COOHCH 2HOOC CH 3CH C H C OOHCOOH HOOC脂肪羧酸 一元羧酸 脂环羧酸 芳香羧酸二元羧酸多元羧酸2.2.羧酸的命名羧酸的命名方法有俗名和系统命名两种。
俗名是根据羧酸的最初来源的命名。
在下面的举例中,括号中的名称即为该羧酸的俗名。


【圣才出](https://uimg.taocdn.com/9322be85af45b307e87197ea.webp)

有机化学羧酸及羧酸衍生物、取代羧酸练习题一、单选题1、酸性最大的是()A、乙酸B、乙二酸C、丙二酸D、丙酸正确答案:B2、下面哪个试剂不常用于制备酰卤?()A、PCl3B、PCl5C、SOCl2D、HCl正确答案:D3、从化合物CH2=CHCH2COOH反应生成CH2=CHCH2CH2OH,要用哪种还原试剂?()A、NaBH4B、LiAlH4C、Pt/H2D、Zn-Hg/浓HCl正确答案:B解析:NaBH4和LiAlH4还原能力不同4、下列二元酸受热后生成环状酸酐的是()A、丁二酸B、丙二酸C、己二酸D、乙二酸正确答案:A5、下列化合物发生醇解反应最快的是()A、CH3CONH2B、(CH3CO)2OC、CH3COClD、CH3COOC2H5正确答案:C6、下列化合物酸性最大的是()A、邻羟基苯甲酸B、间羟基苯甲酸C、对羟基苯甲酸D、苯甲酸正确答案:A7、下列可以使FeCl3显色的是()A、乙酰水杨酸B、乙酰乙酸乙酯C、乙二酸二乙酯D、α-丁酮酸正确答案:B8、糖尿病患者的代谢发生障碍,使血液和尿中酮体增加,临床上常用来测定尿中酮体中丙酮的试剂是()。
A、土伦试剂B、亚硝酰铁氰化钠和浓氨水C、费林试剂D、酸性高锰酸钾正确答案:B9、下列反应类型中,有机物不可能发生的反应类型是()。
A、消去反应B、酯化反应C、中和反应D、加成反应正确答案:A10、下列物质中,既能发生银镜反应,又能与碳酸钠溶液发生反应的是()。
A、乙酸B、甲醚C、甲酸D、甲醇正确答案:C11、下列哪一组物质不是同分异构体()。
A、丁酸和乙酸乙酯B、乙醚和丁醇C、丙酸和丙醛D、丙酮和丙醛正确答案:C12、不属于取代羧酸的是()。
A、B、C、D、正确答案:B二、判断题1、β-醇酸在受热条件下的分子内脱水生成α,β-不饱和羧酸。
正确答案:正确2、α-丁酮酸既可以发生酮式分解反应,也可以发生酸性分解反应。
正确答案:错误3、羧酸衍生物通常是指羧酸分子中羧基中的羟基被其他基团取代后的产物。




第9章羧酸及其衍生物9.1基本要求●掌握羧酸、羧酸衍生物的分类和命名。
●掌握羧基的结构和羧酸的主要化学性质:酸性与成盐、羧基中的羟基被取代的反应(酰卤的生成、酸酐的生成、酯化反应、酰胺的生成)、α- H的卤代、脱羧反应、羧基的还原。
●掌握二元羧酸受热时的特殊反应。
●熟悉饱和一元羧酸的制备反应。
●了解脂肪酸的β一氧化反应。
●掌握羧酸衍生物的水解、醇解、氨解反应。
了解亲核加成—消去反应历程。
●熟悉Claisen酯缩合反应及在合成反应上的应用。
●熟悉酰胺的主要性质:酸碱性、HNO2反应、Hofmamn 降解。
●掌握脲的结构及主要化学性质。
9.2基本知识点9.2.1 羧酸的结构特点羧酸结构的主要特点是羧基中存在着p-π共轭体系。
p-π共轭的结果,导致羧基碳上的正电性降低,使羧羰基不易发生亲核加成反应;同时还导致羧羟基氧的p电子云向羧羰基转移,增强了羧羟基O-H键的极性而使羧酸具有酸性。
9.2.2 羧酸的命名许多羧酸存在于天然产物之中,故常根据其来源而具有俗名。
羧酸的系统命名是以含羧基在内的最长碳链为主链而命名为某酸,取代基名称放在羧酸名称之前。
脂环族和芳香族羧酸以脂肪酸为母体,把脂环和芳环作为取代基来命名。
CH3(CH2)4(CH=CHCH2)4(CH2)2COOHCH2COOH花生四烯酸环己基乙酸5,8,11,14-二十碳四烯酸9.2.3 羧酸的制备羧酸制备主要有如下几种方法:1. 氧化法(1) 烃的氧化:(2)醇和醛的氧化:2. 由格氏试剂合成3. 腈的水解9.2.4 羧酸的化学性质羧酸的化学性质主要表现在四种键的断裂上:①④①处的键断裂表示酸性,酸性随R 基的吸电子诱导效应的增强而增加,反之亦然。
②处的键断裂表示羧基中的羟基被取代而生成羧酸衍生物;③处的键断裂表示脱羧,R 基团是吸电子基团则有利于脱羧;④处的键断裂表示α-H 可被卤素取代,发生α- 卤代反应。
1. 羧酸的酸性一元羧酸的酸性比无机强酸的酸性弱,但比碳酸和苯酚的酸性强,这个性质可用于鉴别羧酸和酚。
第九章羧酸及其衍生物和取代酸I学习要求1. 了解羧酸、羧酸衍生物、取代酸的结构特点和分类;了解生物体中重要羧酸及取代酸的俗名及物理性质。
2. 熟练掌握羧酸、羧酸衍生物、取代酸的系统命名。
3. 熟练掌握羧酸、羧酸衍生物、取代酸的化学性质;尤其是诱导效应对羧酸及取代酸酸性的影响。
4. 掌握个别羧酸的特殊反应(甲酸、草酸、丙酮酸、乙酰乙酸、水杨酸等)。
5. 掌握互变异构的概念以及产生互变异构的条件,理解产生互变异构的原因。
n内容提要一.羧酸的结构特点与化学性质羧基(一COOH)是羧酸的官能团,羧基中的碳原子为sp2杂化,是平面构型。
其中羰基与羟基之间存在的p-n共轭效应,使羰基的缺电子性质下降,亲核加成反应活性远不及醛、酮。
由于羰基的吸电子(-1,- C)效应和羟基氧原子的共轭什C)效应及其诱导(-I)效应,导致羧酸有一定的酸性(pK a=4~5)。
羧基的吸电子效应使羧酸的a-氢有一定的活泼性,但其活泼性小于醛、酮的a-氢。
在一定的条件下,羧基中的羟基可被取代生成酰氯、酸酐、酯和酰胺等。
羧酸是极性分子,分子间及与水分子之间均能形成氢键,其沸点比相对分子质量相同的醇的沸点高。
可以看出,在羧基中既不存在典型的羰基,也不存在典型的羟基,而是二者相互影响的统一体。
因此,根据羧基的结构特点,羧酸可发生以下主要反应:: .......... ...... ... 脱羧反应:O 亠R— CH * C---------- -氢氧键断裂显酸性H —jr Ia氢的反应.......... ................ .....亲核试剂进攻发生取代反应1. 酸性:羧酸具有酸性,其酸性比一般无机酸的酸性弱而比碳酸和苯酚强。
羧酸分子中存在有吸电子基团时,其酸性增强,连有斥电子基团时,酸性减弱。
2. 羧酸衍生物的生成:羧基中的羟基可被一成相应的羧酸衍生物酰卤、酸酐、酯和酰胺。
X、一OCOR、一OR、一NH2 等取代,生OII R—C—OH + <PCI3OR'—CPHIILC—CI° °kC—O—bR'浓HSO4R-OH -.NH3OMCPR'O- + AMC—ONH4 _H HOIIkC—NH23. 脱羧反应:饱和一元羧酸在一般条件下不易脱羧,需用无水碱金属盐与碱石灰共热。
芳香酸的脱羧比脂肪酸容易, 一般加热到熔点以上即逐渐脱羧;当脂肪酸的a- C 上连有吸电子基团时,由于诱导效应,使羧基变得不稳定,更容易脱羧;在生物体内酶的催化下, 一元羧酸容易发生脱羧反应。
二元羧酸分子中由于两个羧基的相互影响,对热比较敏感, 受热时随着两个羧基间距离不同分别发生脱羧、脱水或既脱羧又脱水。
.羧酸衍生物的性质 1.亲核取代反应一一水解、醇解、氨解O IIH OH --------- - R —C —OH +CH 3(CH 2)n-l COOH + CO 2(n=0,1)COOH (CH£nCOOH + H 2O(n=2,3)” CH 2、(CH 2) n-2 丿 C 二 O CH 2 + CO 2 + H 2O (n=4,5) 4. -H 的卤代反应:与醛、酮类似,羧酸的 比醛、酮困难,需少量碘或红磷作催化剂才能进行。
a- H 也能被卤素取代生成卤代酸,但反应 RCH 2COOH+ Cl 2 5.还原反应:羧酸不易被还原,但在 反应有较高的产率和较好的选择性。
红磷RCHCOOH+ HCl ClLiAIH 4作用下,羧酸能被顺利地还原成醇,并且 RCH 二 CHCOOH +LiAlH 41) 无水乙醚_2) H + ,H 2O 'RCH 二CHCH 2OHOR —C —A OOH_OR'R_C_OR' +HAOII H —NH2^— R —C —NH 2 +式中 A = — X 、一 OCOR 、一 OR 、一 NH 2 羧酸衍生物发生水解、醇解和氨解的活性顺序为:酰卤〉酸酐>酯>酰胺。
2.酯的还原:酯比羧酸易被还原,酯可被金属钠加乙醇还原成醇,而双键不受影响。
R —C —A HARCOOR'- Na+C 2H 5OHRCH 2OH+ R'OH △3.酯的缩合反应:酯分子中的 a- H 较活泼,在醇钠的作用下,能与另一分子的酯脱 去一分子醇生成 3 -酮酸酯。
RCOOHNaOH/CaORH + Na 2CO 3R-C-AHA[0]IIR —C —COOH +2H -2H0HR —CH —COOHR —C —COOHRCOOH + CO 2O RO II I IIRCH 2C-OR' + H-CH-C —OR"ORO II I IIRCH 2C —CH — C —OR" + R'OH4. 酰胺的主要性质:- +u+ cRCOOH(RCOO) + NH 4 (NH 3)水解H 或OH三.羟基酸的主要性质1. 酸性:羟基是一个吸电子基团, 越近,对酸性的影响就越大。
2. 脱水反应:2RCHCOOH -— OHRCHCH 2COOH — OH- O 、 R-HC C=O+2H 2O0=C O CH-R RCH 二 CHCOOH +H 2O(CH 2)nRCHC 二 0 + H 2O 0分子间脱水生成聚酯3.氧化反应:四.羰基酸的主要性质比a-酮酸更容易脱羧。
2. 氧化还原反应:OI.R —C —NH 2HO NO「RCOOH + N^ + H 2O与亚硝酸反应,用于鉴别和定量分析Br2+NaOH- RNH 2 Hofmann 降级反应,制备少一个碳原子的伯胺P 2O 5RC- N + 出0脱水反应,制备腈0H[0]LCH —COOH ---------IIR —C —COOHC 2H 5ONaH 2O 因此羟基酸的酸性比相应的羧酸要强,羟基距羧基RCH(CH 2)n COOHn>41.脱羧反应:a-酮酸和酮酸都容易脱羧而生成少一个碳原子的醛或酮,酮酸II稀 H 2SO 4R —C —COOH -IIR —C —CH 2COOHRCHO + C02 RCOCH 3 + C023. 酮式-烯醇式的互变异构现象O H OII I IICH 3- C —CH—C—OC2H5酮式OH OII二CH3-C=CH—C—OC2H5烯醇式凡具有下列结构特征者,一般都存在有互变异构现象。
O OH OII I II R—C_CH2-Y --------- R—C_CH—Y R—C—NH_Y (Y = —CHO、一COR、一COOH、一COOR、一CN 等)例题解析例1.写出下列化合物的名称或构造式:CH3 OI IICH3CHCH 2-C-OC2H5OIIO—C—NHCH 3 CH3CH2 CH3H CH2COOH(5)(7) 解:乙酰水杨酸富马酸(6)(8)草酰乙酸乙酯丁二酰亚胺(1) (3) 3-甲基丁酸乙酯N -甲基氨基甲酸-1-萘酯(2)(4)E-3-甲基-2-己烯酸3 -甲基戊二酸酐OOHO—c—CH3II3OHOOC HC=CH COOH (8)例2.将下列各组化合物的酸性由强到弱排列成序: (1)O OHOOC—C—CH2—C—OC2H5CH2— C”NHCH2—COOHIR- C_N_Y解:(1) D > C > B > A硝基的诱导效应和共轭效应方向一致,都是吸电子的。
当硝基处于间位时,其共轭效应影响不到羧基,所以对硝基苯甲酸的酸性大于间硝基苯甲酸;而对于氯原子而言,其诱导 效应为吸电子,共轭效应为供电子,对羧基的作用相反,当氯原子在间位时,其供电子的 共轭效应影响不到羧基,所以间氯苯甲酸的酸性大于对氯苯甲酸。
(2)A >C >D > B羟基具有吸电子诱导效应和供电子共轭效应。
邻位,羟基与羧基形成分子内氢键,稳定负离子,酸性相对最强。
间位,羟基的吸电子诱导效应大于其供电子共轭效应,所以间羟 基苯甲酸的酸性大于苯甲酸。
对位,羟基的供电子共轭效应大于其吸电子诱导效应,所以 对羟基苯甲酸的酸性比苯甲酸小。
例3.将下列化合物按脱羧反应由易到难排列成序。
A. CH 2(COOH )2B. N 三C — CH 2COOHC. CH 3COOHD. Cl 3C — COOHE. CH 3COCH 2COOH解:脱羧反应活性:D > B > A > E > C当a-C 上连有吸电子基团时,有利于羧基的脱羧,且取代基的吸电子能力越强,越容 易脱羧。
例4.完成下列反应或注明反应条件:COOH COOHCOOH OHCOOHOHD.CH 3CH(COOH) 2 — ol cc O(( NH 3'(CH 3CH 2CCl()C OH OHO II CH 3—C CH 3—C一(NH 2 C 0CH 3 O解:(1) CH 3CH 2COOH , PCl 3 , CH 3CH 2CONH 2(2)“—COOH 、"一COOCH 3 <^1—CONH 2 2 —COOCH 3 'Br 2+NaOH⑶ 1CH 2OH 一 CONH 2(4) |COOH OCOCH 3(5) CHO例5.由指定原料合成下列化合物:NH 2ClCOOC 2H 5 CH 2'COOC 2H 5 CH 3CHCOOHCH 3解:例6.用简便的化学方法鉴别下列各组化合物:(1)水杨酸、苯甲酸、肉桂酸 (2)草酸、丙酮酸、丙酸解:(1) 水杨酸紫色苯甲酸 I FeCl3 ” 无 1 溴水 _ 不褪色 肉桂酸」 无1 褪色⑵草酸' 丁 “ ” 银镜1 FeCb _无丙酮酸 | ------------ 银镜」 紫色 丙酸I 无CH 3CH 2OH CH 3CHCH 3OHKMnO 4/HECOOHCH 3CH 2OHClCH 2COOH CNH 2O—CH 2COOHCOOHC 2H 5OHH 2SO 4 _CH 2COOC 2H 5 COOC 2H 5H 2OHBr NaCN H 2O CH 3CHCH 3 ------------ CH 3CHCH 3 --------------- CH 3CHCH 3汴 CH 3CHCH 3Br COOHOHCN 严 一CH 2COOHr COOHCH 3(1)CH 3K ?Cr 2O 7NH 32Br 2 , NaOHCH 3COOH —p CH 2COOHNHCl6.COCOOH -■ 银镜CH 2COOH,—COOHTollens 试剂无 | KMnO 4/H + ; ------------- — 无I-褪色不褪色 .用系统命名法命名下列化合物: 1. (CH 3)2CHCH 2COOH 3. CH 3CH&CHCOOH 5. COOC 2H 5OH 8.CH 2COOH 1. 2. 3. I V练习题 COOH 6. COCH 32.gCHOC —HO4.O —C —NHCH 3 7.OA O ——CH 39. CH 3 CH 3 C N C 2H 5 10.O A NHCH3—OH 将下列化合物按酸性由强到弱的顺序排列: 醋酸、三氯乙酸、苯酚、碳酸甲酸、乙酸、草酸 苯甲酸、对氯苯甲酸、对硝基苯甲酸、对甲基苯甲酸 4. 2 -氯丙酸、2 -溴丙酸、乳酸、丙酸、丙酮酸 完成下列反应: ) 稀 H 2SO 4 )r - O ( CH 3CHCOOH1. 3)C 2H 5OH 浓 H2SO 4空(5. HOCH 2CH 2CHCOOH -CH 3SOCl 2()HNO 2NH 3)=(HOOCC-CH 2COOH---------- ( ONaOH + 12四•用简便的化学方法鉴别下列化合物:1. 丙酸、丙酮酸、B-丁酮酸2. a-氨基丙酸、a-氯丙酸、丙酮酸3. 水杨酸、苯酚、苯甲醇4. 甲酸、乙酸、甲酸乙酯五•用指定原料合成下列化合物:厂CH(COOH)2. CH 3CH2CH2OH -----------3. I OH ——4. CH 3COOH -----------------六•推导下列化合物的构造式1. 某化合物A的分子式为C5H6O3,它与等物质量的乙醇作用得到两个互为异构体的化合物B和C,B和C分别与亚硫酰氯作用后再加入乙醇得到相同的化合物D。