极性和非极性分子
- 格式:ppt
- 大小:875.50 KB
- 文档页数:25
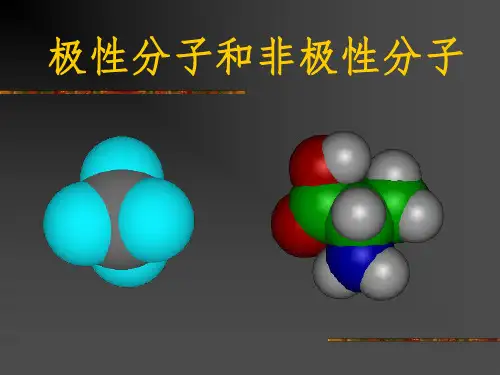

如果分子中所有的化学键都是非极性的,那么价电子就被键合原子相等地共用。
因而,在分子中电子是呈对称均匀分布的。
这种均匀分布的发生与化学键的数目和它们在空间的伸展方向无关。
具有这种特性的分子叫做非极性分子。
如H2,Cl2,N2,O2等。
像HCl和HBr这类双原子分子只有一对电子形成化学键,并且是极性键。
其电子云分布是不对称、不均衡的,被叫做极性分子。
如果分子含有多个极性键,从分子的整体来看,它可能是极性的,也可能是非极性的,这取决于分子中化学键的空间排布。
如果分子中的极性键都相同,从分子的极性的总体来说,它只取决于化学键的空间排布。
以上的看法可以从用带静电荷的棒来靠近细水流及四氯化碳流所发生的现象来证实,细的水流受到吸引而四氯化碳流不受影响。
可以说明水分子是极性分子,而四氯化碳分子尽管是由4个极性键构成但因为其排布均匀,就其总体来说是非极性分子,具有类似结构的还有CH4、C2H6等。

非极性分子与极性分子分子是由原子组成的。
当原子相互结合时,它们所形成的分子可以是极性的或非极性的。
在对分子进行分类时,需要了解一些基本的化学知识,例如化学键的类型、电子云的分布等等。
本文将介绍非极性分子和极性分子的概念,以及它们的区别。
一、什么是非极性分子?非极性分子是由原子组成的分子,其中原子之间不会产生极性化学键。
这些分子通常由相同性质的原子组成,例如氧气(O2)、氢气(H2)和氮气(N2)。
这些分子的化学键是非极性化学键,这意味着它们是由共价键组成的,共享电子对在两个原子之间平均分布,没有正负极性区。
非极性分子的化学键非常稳定,因为它们通常不与其他分子形成氢键或离子键。
这些分子的化学性质较为稳定,不易被其他物质影响。
例如在空气中,氧气、氮气和氢气都具有较高的稳定性,它们不会被其他物质影响,从而不易被氧化和/或还原。
极性分子是由两种或更多种不同原子组成的分子,其中至少一个化学键是极性化学键。
化学键的极性是由于电子云的分布不均匀所导致的。
每个原子中的电子云在分子中形成了偏移,这意味着它们的电荷分布不再对称。
正因为如此,分子在两端存在带有相反的电荷部分,并能与其他分子发生氢键或离子键。
极性分子的极性化学键会导致分子间的分子间相互作用增强,因此分子更容易被其他分子吸引。
这导致了极性分子在不同物理和化学条件下表现出不同的性质。
例如水(H2O)是一种重要的极性分子,因为其中的氧原子和氢原子之间形成了一个极性化学键。
水具有许多特殊的性质,例如可溶性高、极性化学反应性强等等。
1、化学键类型非极性分子和极性分子的显著区别在于它们的化学键类型。
非极性分子通常由非极性化学键组成,而极性分子则包括至少一个极性化学键。
2、电子云分布非极性分子和极性分子的电子云分布也是不同的。
非极性分子原子间的电子云均匀分布,而极性分子原子间的电子云分布不均匀。
3、化学性质由于极性化学键的存在,极性分子在化学方面表现出不同的性质,例如易溶于水、易发生化学反应等。


极性非极性分子判断口诀
极性分子与非极性分子判断口诀如下:
1、双原子的单质分子都是非极性分子,例如氢气,氧气。
2、双原子的化合物分子都是极性分子,如HCl,一氧化碳等。
3、多原子分子的极性和非极性具体要看其空间构型是否对称,对称的就是非极性分子,不对称的就是极性分子。
4、对于AnBm类的分子,n=1,m>1。
若A化合价等于主族数则为非极性。
5、若已知分子之间的键角,可对分子进行受力分析,合力为零的就是非极性分子。
如:CO2,C2H4等等。
扩展资料:
(1)极性分子:正电荷中心和负电荷中心不相重合的分子
(2)非极性分子:正电荷中心和负电荷中心相重合的分子
(3)分子极性的判断:分子的极性由共价键的极性及分子的空间构型两个方面共同决定
1非极性分子和极性分子的比较
2举例说明:。




极性分子:HX,CO,NO,H2O,H2S,NO2,SO2,SCl2,NH3,H2O2,CH3Cl,CH2Cl2,CHCl3,CH3CH2OH 非极性分子:Cl2,H2,O2,N2,CO2,CS2,BF3,P4,C2H2,SO3,CH4,CCl4,SiF4,C2H4,C6H6,PCl5, 溶剂极性的划分是按其偶极距和介电常数来定的.溶剂的偶极距大于2.4德拜,介电常数大于1.7为极性溶剂,小于此二值即为非极性溶剂.水是极性溶剂,乙醇,甲醇都是极性溶剂一般,极性与介电常数成反比常用溶剂的极性顺序:水(最大) > 甲酰胺> 乙腈> 甲醇> 乙醇> 丙醇> 丙酮> 二氧六环> 四氢呋喃> 甲乙酮> 正丁醇> 乙酸乙酯> 乙醚> 异丙醚> 二氯甲烷>氯仿>溴乙烷>苯>四氯化碳>二硫化碳>环己烷>己烷>煤油(最小)常用溶剂的极性顺序:水(最大) > 甲酰胺> 乙腈> 甲醇> 乙醇> 丙醇> 丙酮> 二氧六环> 四氢呋喃> 甲乙酮> 正丁醇> 乙酸乙酯> 乙醚> 异丙醚> 二氯甲烷>氯仿>溴乙烷>苯>四氯化碳>二硫化碳>环己烷>己烷>煤油(最小)物质名温度介电常数三甲基苯20 1.9苯20 2.3对二甲苯20 2.3三甲苯20 2.3间二甲苯20 2.4甲苯20 2.4三乙胺25 2.4二甲苯20 2.4萘20 2.5三甲胺25 2.5己酸71 2.6戊酸20 2.6乙醛22 2.9正丁酸20 2.9丁酸20 3乙苯24 3呋喃25 3丙酸14 3.1辛酸18 3.2脲22 3.5二乙胺20 3.7苯甲醚20 4.3乙醚20 4.3苯甲醚24 4.3苯乙酮24 17.3苯甲醛20 17.8苯乙醚21 4.5丁酸乙脂19 5.1 丁酸乙脂19 5.1 丁胺21 5.4丁酸甲酯20 5.6 乙酸20 6.2乙胺21 6.3乙酸甲酯25 6.7 甲酸乙脂25 7.1 苯胺20 7.3正丁醇19 7.8丁酸酐-7 12丁酸酐20 12吡啶20 12.5二苯甲酮20 13苯甲醇20 13丁醛26 13.4戊酮25 13.9环己醇25 15戊纯20 15.8茴香醛20 15.8乙二胺18 16甲丙酮14 16.8丁醇(1)20 17.8 环己酮20 18.2苯乙腈20 18.3丁酮20 18.5异丁醇20 18.7丙酮25 20.7丁腈21 20.7乙酸酐19 21甲醛23酒精25 24.3苯甲腈20 26乙二腈20 27丙腈20 27.7甲醇25 32.6乙二醇20 37乙腈21 37.5乙酰胺20 41丙二腈36 47甲酸16 58水20 80.4工业酒精16~31环氧乙烷25 14氯甲烷-4~12.6氧化铝9.3~11.5在结晶和重结晶纯化化学试剂的操作中,溶剂的选择**系到纯化质量和回收率的关键问题。