长期毒性作用及其试验方法
- 格式:ppt
- 大小:1.06 MB
- 文档页数:82
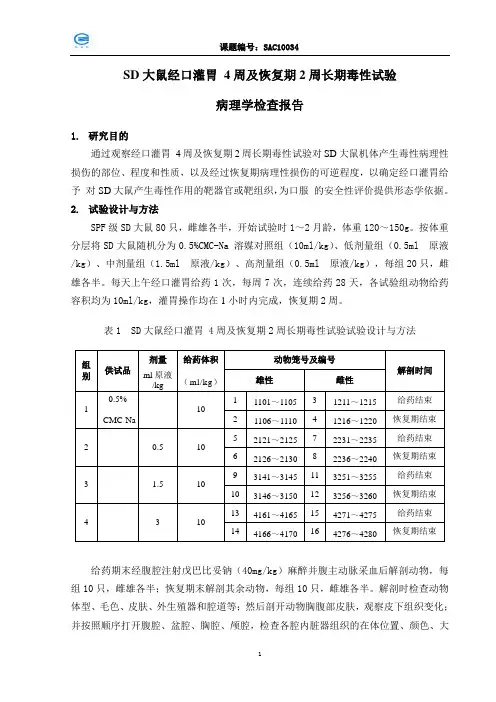
SD大鼠经口灌胃4周及恢复期2周长期毒性试验病理学检查报告1.研究目的通过观察经口灌胃4周及恢复期2周长期毒性试验对SD大鼠机体产生毒性病理性损伤的部位、程度和性质,以及经过恢复期病理性损伤的可逆程度,以确定经口灌胃给予对SD大鼠产生毒性作用的靶器官或靶组织,为口服的安全性评价提供形态学依据。
2.试验设计与方法SPF级SD大鼠80只,雌雄各半,开始试验时1~2月龄,体重120~150g。
按体重分层将SD大鼠随机分为0.5%CMC-Na 溶媒对照组(10ml/kg)、低剂量组(0.5ml原液/kg)、中剂量组(1.5ml原液/kg)、高剂量组(0.5ml 原液/kg),每组20只,雌雄各半。
每天上午经口灌胃给药1次,每周7次,连续给药28天,各试验组动物给药容积均为10ml/kg,灌胃操作均在1小时内完成,恢复期2周。
表1 SD大鼠经口灌胃 4周及恢复期2周长期毒性试验试验设计与方法组别供试品剂量给药体积动物笼号及编号解剖时间ml原液/kg (ml/kg)雄性雌性10.5%CMC-Na 101 1101~1105 3 1211~1215 给药结束2 1106~1110 4 1216~1220 恢复期结束2 0.5 10 5 2121~2125 7 2231~2235 给药结束6 2126~2130 8 2236~2240 恢复期结束3 1.5 10 9 3141~3145 11 3251~3255 给药结束10 3146~3150 12 3256~3260 恢复期结束4 3 10 13 4161~4165 15 4271~4275 给药结束14 4166~4170 16 4276~4280 恢复期结束给药期末经腹腔注射戊巴比妥钠(40mg/kg)麻醉并腹主动脉采血后解剖动物,每组10只,雌雄各半;恢复期末解剖其余动物,每组10只,雌雄各半。
解剖时检查动物体型、毛色、皮肤、外生殖器和腔道等;然后剖开动物胸腹部皮肤,观察皮下组织变化;并按照顺序打开腹腔、盆腔、胸腔、颅腔,检查各腔内脏器组织的在体位置、颜色、大小、质地,有无出血及粘连等。





慢性毒性试验测定1 目的检测受试物长期染毒对实验动物所产生的毒性作用,确定其最小观察到有害作用剂量,最大未观察到有害作用剂量及毒性作用的靶器官。
2 实验动物试验选用刚离乳的大鼠。
在试验结束时,每个剂量组每种性别的动物应不少于10只。
中间需活杀动物检查时,需相应增加实验动物数量。
3 试验分组将实验动物随机分在3个剂量组和1个阴性对照组。
阴性对照组除不接触消毒剂外,其它与实验组相同,若在试验中对受试物使用溶剂或赋形剂时,阴性对照组应给予相应剂量的溶剂或赋形剂。
试验剂量根据亚慢性试验结果选择。
高剂量应引起明显的毒性效应甚至个别动物死亡,低剂量应不引起毒性效应。
4 操作程序(1)用灌胃法或将受试物掺入饲料或饮水中喂饲。
掺入饲料的受试消毒剂的最高浓度一般不超过5%。
饲料中受试消毒剂应定期监测,观察其均匀性和稳定性。
(2)灌胃法每天给药一次。
(3)前3个月每周称量体重,3个月后每月称1次体重,调整受试物灌胃量。
如受试物掺入饲料,应定期称饲料消耗量。
如受试物溶于饮水中喂饲,需记录动物的饮水量。
(4)试验期限为一般为6个月,必要时可延长至2 年。
5 观察指标指标与亚慢性毒性试验基本相同,也可根据受试物对实验动物的亚慢性毒性作用和靶器官,可适当增加或更换一些针对性更强更灵敏的观察指标。
(1)临床观察:观察中毒表现,体重前3个月每周1次,以后每月1次。
(2)血液学检查:于试验的第3个月、6个月及以后每半年进行1次血液学检查。
(3)血液生化检查:检查时间同血液学检查。
(4)病理学检查:系统解剖:所有实验动物包括试验过程中死亡的动物都应进行完整的系统解剖和详尽的肉眼观察。
肉眼可见的异常组织都应留样作进一步组织病理学检查。
脏器重量:称取脑、肝、肾、肾上腺和睾丸重量并计算脏器系数。
组织学检查:对照组、高剂量组动物及系统解剖发现异常的组织均需作详尽的组织学检查。
当高剂量组有异常发现时,其它剂量组才进行相应检查。
检查脏器一般包括脑、心、肺、肝、脾、肾、胃、肠、肾上腺、甲状腺、垂体、睾丸(卵巢)和子宫等。




大鼠的长期毒性试验1. 目的:观察连续给予受试动物后由于积蓄而对机体产生的毒性反应及其严重程度,提供毒性反应的靶器官及其损害的可逆性,确定无毒性反应剂量,为人用安全剂量提供参考。
试验条件:2动物:应写明动物的品系,生产单位及生产合格证号,等级,周龄,性别,体重,一般选用动物品系有Wistar、SD、或其他品系的远交系动物。
应根据试验期的长短选用不同周龄的大鼠,试验期在3个月内宜用6~8周龄大鼠,超过三个月者宜用5~6周龄大鼠。
试验开始时,体重差异应不超过平均体重的20%。
实验动物应雌雄分笼饲养,每笼不宜超过5只动物,所有动物试验前至少观察一周,并记录食量和体重等基础数字。
试验报告中应写明饲料供应单位及生产合格证,若用自己配置的饲料,应提供配方及成分含量的检测报告;应写明饲养动物实验室的合格证(未获得合格证者也应注明)及等级。
受试物:应写明受试物的名称、批号、来源、纯度、保存条件及配置方法。
受试物可以是临床试验制剂。
如受试物制剂的体积较大,以不含赋形剂的制剂,如中药浸膏为宜。
固态制剂灌胃给药,可选择适当的溶媒溶解,或研磨成细粉后用1%左右羧甲基纤维素钠(或10%阿拉伯明胶)制成混悬液,但应注意临用前需要摇匀。
避免混悬不匀引起计量误差。
长期毒性试验给药周期较长,固体制剂在配成溶液或混悬液后,冰箱放置,短期内用完,一面受试药物活性降低。
3试验方法:①受试物剂量:一般设三个剂量组和一个对照组。
给受试物剂量单位一般用mg/kg、或g/kg表示。
高剂量组:应使动物产生明显的或严重的毒性反应,或个别动物死亡。
中剂量组:应相当或高于药效学试验的高剂量,应使动物产生轻微的或中等程度的毒性。
低剂量组:略高于整体动物的有效剂量,在此剂量下动物应不出现毒性反应,属基本安全剂量。
对照组:不给收拾药物仅给等容量的溶媒或赋形剂,若所用溶媒或赋形剂可能有毒时,另加一组空白对照。
如果急性毒性试验结果毒性很低,测不出LD50,也未见明显毒性反应,可设高、低两个剂量,高剂量一般为拟用于临床剂量50倍以上(有困难时,可适当减少剂量,最低不能低于临床剂量30倍)并应高于药效学试验的高剂量。

毒力测定的方法毒力测定是一种用于评估物质对生物体的毒性的方法。
它在药物研发、环境监测和食品安全等领域具有重要意义。
下面将介绍常用的毒力测定方法,包括急性毒性测定、慢性毒性测定和基因毒性测定。
1.急性毒性测定:急性毒性测定用于评估物质对生物体在短时间内的毒性影响。
常用的急性毒性测定方法包括LD50(半数致死剂量)测定和急性毒性试验。
LD50测定通过给实验动物以不同剂量的物质,观察半数动物死亡所需的剂量,来评估物质对生物体的毒性程度。
急性毒性试验通常使用小鼠、大鼠或其他实验动物,观察物质在短时间内对生物体的影响,包括行为、致死率、体重变化等。
2.慢性毒性测定:慢性毒性测定用于评估物质对生物体长期暴露后的毒性影响。
常用的慢性毒性测定方法包括慢性毒性试验和生殖毒性试验。
慢性毒性试验通过给实验动物长期饮食或注射物质,观察其对生物体的影响,包括生长发育、行为、器官功能等。
生殖毒性试验主要评估物质对生殖能力和胎儿发育的影响,包括种鼠试验和胚胎毒性试验。
3.基因毒性测定:基因毒性测定用于评估物质对基因组的损伤和突变的影响。
常用的基因毒性测定方法包括细菌突变试验、小鼠骨髓细胞染色体畸变试验和激光束微单带凝胶电泳(COMET)试验。
细菌突变试验通常使用大肠杆菌或沙门氏菌等细菌,观察物质对细菌基因的突变作用。
小鼠骨髓细胞染色体畸变试验通过观察物质对小鼠骨髓细胞的染色体损伤和畸变,评估其对基因组的影响。
COMET试验则通过电泳法测定细胞DNA的断裂和损伤程度,进一步评估物质对基因组的损伤和突变作用。
毒力测定方法在实验过程中应严格遵守伦理原则和实验操作规范。
同时,需要根据实际需求选择合适的物质浓度和实验动物,确保测定结果准确可靠。
此外,还应结合其他相关的生物学指标和实验数据,综合评估物质的毒性。
总而言之,毒力测定方法是评估物质对生物体毒性的重要手段。
各种毒力测定方法在研究领域和监测实践中得到了广泛应用,对保护人类健康和环境安全具有重要意义。