分叉病变PCI后的抗栓治疗策略(2020完整版)
- 格式:doc
- 大小:23.00 KB
- 文档页数:4

冠状动脉分叉病变的定义、分型、评估方法和治疗策略牛雪凝;李广平【摘要】冠状动脉分叉病变是经皮冠状动脉介入治疗的难题之一,虽然药物支架的出现降低了术后再狭窄率,但是在进行介入治疗之前对于冠状动脉分叉病变的分型及分支血管受累情况进行预判仍极为重要,但目前尚未对其治疗策略达成共识。
为了能更好地评估分叉病变的严重程度、选择最适合的治疗方法,需要对冠状动脉分叉病变形成原因及其定义、病理生理学意义有充分的认识。
【期刊名称】《临床荟萃》【年(卷),期】2014(000)007【总页数】4页(P826-829)【关键词】冠状动脉狭窄;危险性评估;放射学;介入性【作者】牛雪凝;李广平【作者单位】天津医科大学第二医院心脏科,天津心脏病学研究所,天津300211;天津医科大学第二医院心脏科,天津心脏病学研究所,天津 300211【正文语种】中文【中图分类】R543.5在经皮冠状动脉介入治疗(percutaneous coronary intervention,PCI)领域中,冠状动脉分叉病变是目前具有挑战性的病变类型之一。
与简单冠状动脉病变的PCI治疗相比,分叉病变介入治疗手术远期心血管事件发生率、术后再狭窄率及手术费用较高,而临床预后较差、手术成功率较低[1]。
目前关于冠状动脉分叉病变的分型、评估方法和治疗策略仍有不同意见。
我们在回顾冠状动脉分叉病变的定义、分型及定量测量的基础上,对其治疗的新观点综述如下。
冠状动脉分叉处容易发生动脉粥样硬化,内皮功能紊乱、血液涡流形成及血管壁受到剪切力增加是其形成的重要原因[2]。
欧洲分叉病变俱乐部将分叉病变定义为:病变邻近或累及较大分支口部,该分支血管对于患者有明显功能价值(与症状有关、存在大量存活心肌、提供侧支循环以及对左心功能意义重大等),在介入治疗过程中不可丢失[3]。
治疗分叉病变最具有挑战性的是,在处理主支血管病变时,由于“铲雪”效应引起斑块移行、支架嵴移位等原因易导致邻近分支血管受累。

【指南与共识】冠心病合并心房颤动患者抗栓管理中国专家共识2020摘要冠心病与心房颤动(房颤)合并存在临床并不少见。
冠心病患者需要进行抗血小板治疗以减少心肌缺血事件,而血栓栓塞高风险的房颤患者则需口服抗凝药物以减少卒中等血栓栓塞事件。
冠心病与房颤合并存在时,联合应用抗血小板与抗凝治疗可有效减少缺血及血栓栓塞事件,但会增加出血风险。
针对冠心病合并房颤患者,如何选择最佳的抗栓方案一直是临床研究的热点。
近年来,欧美等国家和地区相继发布了急性冠状动脉综合征和/或经皮冠状动脉介入治疗合并房颤患者的抗栓治疗专家共识并及时更新,而我国尚缺乏相应的抗栓治疗指南或共识。
该共识依据已发表的临床研究证据,结合国内外相关指南、共识以及专家建议等,着眼于解决不同类型冠心病合并房颤患者抗栓治疗临床实践中的问题,对指导我国冠心病合并房颤患者的治疗意义重大。
冠心病与心房颤动(房颤)具有多种相同的危险因素,两种疾病常合并存在。
冠心病患者合并房颤的比例为6%~21%,房颤患者合并冠心病的比例为20%~30%。
冠心病患者需要进行抗血小板治疗以减少心肌缺血事件,而血栓栓塞高风险的房颤患者则需口服抗凝药物(oral anticoagulant,OAC)治疗以减少卒中等血栓栓塞事件。
冠心病与房颤合并存在时,联合应用抗血小板与抗凝治疗可有效减少缺血及血栓栓塞事件,但增加出血风险。
冠心病合并房颤患者如何选择最佳的抗栓方案一直是临床研究的热点问题。
近年来,欧洲及北美相继发布了急性冠状动脉综合征(acute coronary syndromes,ACS)和/或经皮冠状动脉介入治疗(percutaneous coronary intervention,PCI)合并房颤患者抗栓治疗的专家共识,并均已陆续更新至第3版。
我国虽已发表了一系列冠心病或房颤相关指南或共识,但尚缺乏针对冠心病合并房颤患者抗栓治疗的指南或共识。
本共识依据已发表的临床研究证据,结合国内外相关指南或共识以及专家建议,着眼于解决不同类型冠心病合并房颤患者抗栓治疗临床实践中的问题。


冠脉分叉病变的介入治疗策略目录➢分叉病变的基本概念➢分叉病变介入治疗的基本方法➢分叉病变的评估及治疗策略➢分叉病变介入治疗的临床问题及技术细节➢分叉病变介入治疗的新型辅助技术一、分叉病变的基本概念➢分叉病变占所有PCI的15%-20%, 30%-45%是真分叉病变;PMV:主干血管近段;MB:主干血管远段;SB:分支血管;POC:汇合多边区;Carina:分叉嵴➢冠脉分叉部血流方向发生改变,导致局部形成涡流或湍流;➢分叉嵴对侧低剪切应力区易形成斑块;➢分叉嵴对侧低剪切应力区湍流场可抑制药物支架再内膜化和损伤新生内膜,高剪切应力区则容易激活血小板。
1, 1, 1 1 , 1, 01, 0 , 10, 1, 11, 0, 00, 1, 00, 0, 1MBDistalMBProximal SB分叉病变的分型Medina 分型分叉病变的分型陈氏分型二、分叉病变介入治疗的基本方法分叉病变介入治疗的基本方法➢单支架技术✓Crossover✓开口精确定位➢双支架技术✓C rush✓C ulotte✓T支架✓V支架➢必要时支架技术单支架技术➢单支架Crossover✓简单Crossover✓支架过渡Crossover➢分支开口精确定位:✓常见用于前降支开口精确定位,也可用于其他分叉病变。
找到真正的开口是关键!✓Szabo技术单支架技术的主要难点在于分支保护!双支架技术➢Crush技术:包括经典Crush、Mini-Crush、DK-Crush 、Step-Crush、Rreversed-Crush等;➢Culotte技术:包括经典Culotte、Mini- Culotte、DK-Culotte等;➢T支架技术:包括经典T支架及改良T支架;➢V支架技术:包括V支架以及Kissing-Stent(SKS )。
Crush技术经典Crush技术Crush技术➢适应症:✓需双支架策略及分支与主支夹角<70°。
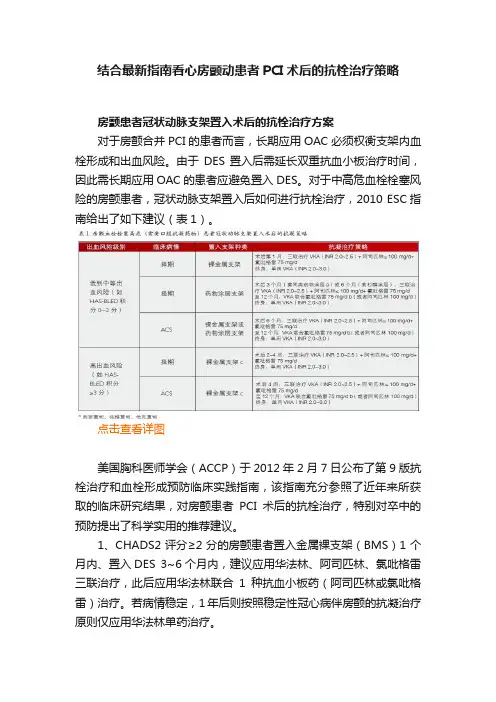
结合最新指南看心房颤动患者PCI术后的抗栓治疗策略房颤患者冠状动脉支架置入术后的抗栓治疗方案对于房颤合并PCI的患者而言,长期应用OAC必须权衡支架内血栓形成和出血风险。
由于DES置入后需延长双重抗血小板治疗时间,因此需长期应用OAC的患者应避免置入DES。
对于中高危血栓栓塞风险的房颤患者,冠状动脉支架置入后如何进行抗栓治疗,2010 ESC指南给出了如下建议(表1)。
点击查看详图美国胸科医师学会(ACCP)于2012年2月7日公布了第9版抗栓治疗和血栓形成预防临床实践指南,该指南充分参照了近年来所获取的临床研究结果,对房颤患者PCI术后的抗栓治疗,特别对卒中的预防提出了科学实用的推荐建议。
1、CHADS2评分≥2分的房颤患者置入金属裸支架(BMS)1个月内、置入DES 3~6个月内,建议应用华法林、阿司匹林、氯吡格雷三联治疗,此后应用华法林联合1种抗血小板药(阿司匹林或氯吡格雷)治疗。
若病情稳定,1年后则按照稳定性冠心病伴房颤的抗凝治疗原则仅应用华法林单药治疗。
2、CHADS2评分0~1分者,建议在支架置入术后1年内进行双联抗血小板药物(阿司匹林与氯吡格雷)治疗,无需进行三联治疗。
1年后若病情稳定则参照稳定性冠心病伴房颤的治疗原则进行抗凝治疗。
3、伴房颤的急性冠状动脉综合征(ACS)患者、未进行支架置入术且CHADS2评分≥1分时,建议华法林联合1种抗血小板药物治疗1年。
1年后若病情稳定则参照稳定性冠心病伴房颤的治疗原则进行抗凝治疗。
对于CHADS2评分为0分者本指南也作出了相同的推荐建议,即华法林联合1种抗血小板药物治疗1年。
不稳定性心绞痛与支架置入术后的患者应用双联抗血小板治疗可显著降低不良心血管事件风险。
当房颤患者合并上述情况时,在华法林治疗基础上加用双联抗血小板药物治疗亦可减少血栓栓塞事件的发生。
现有证据提示,与仅应用双联抗血小板药物治疗者相比,短期(如1个月)加用华法林并不会显著增加出血事件风险,但长期应用三联抗栓药物的安全性尚有待论证。





2020版:药物球囊应用国际专家共识解读(全文)目前药物洗脱支架(DES)仍然是冠心病的主流介入治疗方法,但药物球囊(DCB)已成为某些冠脉病变新的治疗措施之一,越来越多的证据显示其在一些特殊病人群体及特殊部位的病变中具有更大的优势。
除了指南推荐的DCB可用于支架内再狭窄(ISR)外,最近的随机临床研究显示,DCB治疗原位小血管病变和伴高出血风险患者具有良好的疗效和安全性。
此外,对于冠脉其它原位病变可能亦具有良好的治疗前景(例如,分叉病变、大血管疾病、急性冠脉综合征、糖尿病)。
根据最近发布的大量临床试验数据,DCB国际共识小组对DCB使用建议进行了阐述,总结了DCB 的历史背景及发展历程、技术建议、可能的适应症和未来前景。
由于在输送球囊的设计、所用药物的剂量、制剂和药物释放动力学之间有非常重要的相关性,因此不同的DCB之间具有“类效应”现象似乎并不存在。
文章于近期发表在美国心脏病学会杂志的心血管病介入治疗子刊上,以下对共识的主要内容进行阐述及讨论。
该国际共识较既往DCB共识更新主要包括以下内容:1.不存在DCB 之间的“类效应”:由于球囊的设计、药物种类、药物剂量剂型、药物释放动力学及塑形剂不同,不同DCB之间疗效存在差别;2.DCB使用适应症的拓展:首次提出每例PCI从开始都应该以使用单纯DCB策略为目标,提出了从病变到临床两种适应症范畴,但目前DCB除应用于ISR和小血管原位病变外的其它病变尚需更多的临床证据;3.强调更加充分的病变预处理的重要性:预处理球囊与血管直径比有原来的0.8:1提高到1:1,以达到即刻的最大管腔获得;4.双联抗血小板(DAPT)时程大大缩短:对于稳定性冠心病或仅基于病变因素考虑,术后仅需要1个月DAPT。
对于出血极高危病人或需要近期外科手术患者,可考虑术后即采用单联抗血小板治疗(SAPT);5.雷帕霉素类DCB产品已获欧盟审批上市,但其临床疗效尚待进一步验证。
鉴于DES远期仍有较高的不良事件发生率及需要较长的DAPT时程,如能在不使用永久植入物的情况下防止再狭窄,应该是一种最佳的治疗方式。

左主干分叉病变的介入治疗策略(全文)冠状动脉左主干病变通过造影的检出率为5%-7%,一旦左主干出现狭窄或者闭塞,将会引起大面积心肌缺血,乃至恶性心律失常、心源性休克以及猝死等致命并发症。
因此,冠状动脉搭桥手术(CABG)一直是治疗左主干病变的金标准。
随着EXCEL和NOBEL临床研究数据的公布,证明对选择性无保护左主干病变行PCI治疗是安全和有效的。
由于超过80%的左主干病变会累及到左主干末端分叉,目前对于左主干末端分叉病变的最佳介入治疗策略还没有定论,而且左主干分叉病变的PCI治疗一直是临床的难点,所以本文将近年来左主干分叉病变的介入治疗策略做一综述。
一、左主干分病变病例的选择左主干病变治疗方法要依据目前的指南推荐。
目前欧洲的心肌血运重建指南已将SYNTAX评分<22分的左主干病变作为Ⅰb类推荐,将SYNTAX评分为23~32分者作为Ⅱa类推荐,将SYNTAX评分>32分,推荐进行冠脉搭桥手术。
美国的心肌血运重建指南,将SYNTAX评分<22分的左主干病变作为Ⅱa类推荐,将SYNTAX评分为23~32分者作为Ⅱb类推荐。
对左主干病变进行介入治疗时,应当由心脏团队进行决策,由经验丰富的术者完成。
可以通过使用SYNTAX、SYNTAXⅡ、NERS和EuroSCorE评分系统评估患者病变和临床的复杂性。
DEFINITION研究所提出的标准适用于左主干末端分叉病变。
二、术前左主干病变的影像学和功能学评估当左主干合并弥漫病变时,由于缺乏正常的参考血管段,单纯的根据冠脉造影检查评估左主干病变,容易造成误判。
与冠脉造影相比,IVUS 和OCT具有极高的分辨率,能够精确的评估左主干的病变、指导支架的置入以及术后的优化,改善患者的临床预后。
IVUS和OCT检查可以明确左主干斑块分布、组织特性、钙化弧度和狭窄的严重性。
FFR是评估左主干狭窄病变和相应分支病变血流动力学意义的重要诊断工具。
目前左主干介入干预的标准是:(1)造影显示左主干直径狭窄≥70%;(2)通过IVUS 或者OCT检查测得最小管腔面积(MLA)≤6.0mm2;(3)FFR≤0.80。
左主干分叉病变介入治疗策略(全文)左主干病变属于临床上较为严重的冠脉病变类型,一旦出现狭窄甚至闭塞,将引起大面积的心肌梗死,乃至恶性心律失常、心源性休克乃至猝死等致命并发症,因此既往左主干病变患者多选择外科手术治疗。
但随着新一代药物涂层支架(DES)、生物可吸收支架(BVS)的问世,经皮冠状动脉介入(PCI)治疗左主干分叉病变逐渐被临床所接受,而左主干病变的治疗策略选择一直是介入治疗的难点问题。
近年来数项研究结果表明,PCI与冠状动脉旁路移植术(CABG)在安全性及有效性方面无显著差异。
近期公布的SYNTAX研究左主干亚组5年随访结果[1]表明,PCI 组与CABG组在主要不良心脑血管事件(MACCE)事件上无显著差异(36.9%vs 31.0%;p=0.12)。
而新版ESC/EACTS心肌血运重建指南[2]中将PCI的推荐级别提升为B级,与CABG相同等级推荐。
目前国际临床上关于左主干远端尤其是分叉病变的最佳介入治疗的策略及方法还没有定论,本文将就近年来左主干分叉病变的介入治疗策略做一简要叙述。
一.左主干病变的影像学评价:左主干病变属于较为复杂的冠脉病变,单纯根据造影图像判断其病变性质具有较大的人为差异,因此手术策略的选择也是千差万别。
术中应用血管影像学评价手段可以在支架置入前判断斑块大小、位置与性质,并在支架放置后评价扩张情况,有效避免上述问题,这也恰恰契合当前提倡的精准诊疗技术思路。
血管内超声(IVUS)技术可准确评价左主干病变严重程度,其具有图像精准、径向穿透力较强的特点。
Kang等[7]在一项研究中采用了IVUS指导下的左主干介入治疗策略,共纳入403名左主干病变患者,在分析其介入治疗数据后,研究者发现支架后最小管腔面积可预测术后支架内再狭窄发生率,其最小界值在回旋支(LCX)开口、前降支(LAD)开口、二者交汇处和左主干近端分别为5.0mm2、6.3 mm2、7.2 mm2、8.2 mm2,应用上述界值在两年随访中可有效预测MACE事件的发生。
急性心肌梗死合并多支血管病变的PCI策略(全文)在急性心肌梗死患者中合并多支血管病变的比例高达40%-60%1,2,这部分患者病情往往更危重,并发心源性休克﹑死亡﹑心衰的风险更高,预后更差。
在应激状态下,非罪犯血管一旦缺血加重或闭塞,可造成心肌缺血或坏死面积的进一步扩大,诱发和加重恶性心血管事件的发生3,因此如何进行血运重建策略是目前介入领域关注的热点。
针对急性心肌梗死合并多支血管病变,目前血运重建策略主要包括以下三种:仅处理罪犯血管﹑急诊完全血运重建和分阶段完全血运重建,每一种策略均存在各自的优缺点。
在急性心肌梗死合并多支血管病变血运重建策略的早期研究中,大部分的研究均倾向于仅罪犯血管血运重建更能带来获益,急诊完全血运重建显著增加患者脑卒中和死亡的发生率4-7。
在众多的研究中,以2010年的APEX-AMI和2011年的HO RIZONS-AMI研究最具代表性和说服力。
前者共纳入5745例患者,研究发现,在对急性心肌梗死患者罪犯血管直接植入支架(PCI)的同时对非罪犯血管行血运重建者术后3个月的死亡﹑复合终点事件(死亡﹑心力衰竭及休克)的发生率均显著高于仅罪犯血管PCI组(12.5%vs 5.6%;17.4%vs 12.0%)6。
2011年的HO RIZONS-AMI研究得出的结果与其基本一致,后者的随访时间延长至PCI术后一年,研究发现,急诊完全冠脉血运重建显著增加一年死亡率(9.2%vs 2.3%)7。
基于上述代表性的研究,2012年ESC指南建议仅对罪犯血管行急诊PCI(IIa),除非合并心源性休克或对罪犯血管行血运重建治疗后仍持续存在心肌缺血症状时才对非罪犯血管行血运重建(IIb)9。
2013年ACCF/AHA冠脉介入指南不推荐对血流动力学稳定的急性心肌梗死患者行非罪犯血管血运重建(III,C)8。
然而近年来,越来越多的大型多中心前瞻性研究给出了与以上不一样的结论。
PRAMI研究是一项旨在评价对STEMI患者非罪犯血管进行预防性血运重建的效果,该研究共纳入465例急性心肌梗死合并多支血管病变行急诊PCI的患者,随机分为仅处理罪犯血管组和处理罪犯血管的同时对非罪犯血管进行处理的完全血运重建组,随访23个月。
分叉病变PCI后的抗栓治疗策略(2020完整版)
欧洲介入杂志近日刊登了多国专家编写的分叉病变PCI后的抗栓治疗策略,其中有来自中国的陈绍良教授,晨读将主要内容整理后分享给大家。
分叉病变约占PCI病例的15-20%,是围术期和长期不良事件的高危因素,这主要和支架内血栓(ST)形成有关。
据统计分叉病变的ST发生率在1.5-2%,而非分叉病变PCI的ST<1%。
病例研究发现ST主要的病理机制是支架贴壁不良(33%),支架膨胀不全(19%)和孤立的支架未覆盖(19%)。
分叉病变也因冠脉解剖部位不同风险也有很大的差异,比如左主干分叉风险就很大。
DEFINITION II 研究还定义了“复杂分叉病变”。
所以分叉病变的抗栓治疗要权衡患者缺血和出血风险,欧洲分叉俱乐部也对减少相应不良事件对术式做了推荐,推荐大部分分叉病变行“provisional”的单支架术式,而左主干分叉可以采用DK-Crush的双支架术式(IIb)。
在双支架术式中最后的球囊对吻和POT非常重要,可以最小化支架贴壁不良,减少支架内血栓的风险。
也提倡腔内影像学进行指导。
一、抗栓药物的选择
在ACS患者,替格瑞洛和普拉格雷优先于氯吡格雷推荐,尽管自发的出血风险有增加,但临床净获益更多。
如果是血栓高危的稳定型冠心病PCI患者,比如复杂左主干,专家建议使用替格瑞洛或普拉格雷。
译者按:作者认为分叉病变双支架最好选择起效快和强有力的P2Y12抑制剂,因为支架内血栓都出现在PCI急性和早期阶段。
二、双抗血小板(DAPT)持续时间和风险分层
国际的指南认为分叉病变是支架内血栓的一个危险因素,不管患者是ACS还是稳定型冠心病,都建议更长时间(>12个月)的DAPT(IIb)。
复杂病变(包括分叉病变双支架)PCI,与3-6个月DAPT比,≥12个月DAPT的患者复合终点事件有明显的下降。
延长DAPT事件,出血事件也相应增加,需要进行缺血和出血风险评估。
比如下图的DAPT和PRECISE-DAPT评分,来决定DAPT的维持时间。
三、鉴别高危出血(HBR)患者
ARC-HBR新近出版了一个鉴别HBR的共识,用来评估1年的BARC 3-5级出血风险≥4%和颅内出血≥1%的患者。
HBR患者至少满足1个主要标准或2个次要标准。
这类患者建议分叉病变选“Provisional”单支架术式,腔内影像学指导,从而可以选择更短的DAPT时间。
四、P2Y12抑制剂单抗的作用
在TWILIGHT-COMPLEX研究亚组中有10.7%是分叉病变双支架病例,该研究总体结果发现,DAPT1个月后替格瑞洛单抗治疗在“复杂”和“非复杂”PCI患者中的BARC 2、3、5级出血风险相似。
但分叉病变还需要针对性的研究来进行确认。
五、P2Y12抑制剂转换及停用
通常在复杂PCI后的早期可将P2Y12抑制剂升级(如氯吡格雷转换到普拉格雷),比如在血栓性病变、长和分叉病变,来加强血小板的抑制。
如果是HBR患者分叉病变支架后,因为出血风险大,可考虑将替格瑞洛或普拉格雷降级。
如果分叉病变双支架术式的患者需要外科手术停用抗血小板药时,可以用坎格瑞洛静脉桥接。
六、联合口服抗凝药
最近的一个荟萃分析指出,PCI后一个口服抗凝药+一个抗血小板药物(DAT)与一个口服抗凝药+双抗血小板药物(TAT)相比出血风险显著减少(RR 0.33),但DAT比TAT的支架内血栓(RR1.59)和心梗风险更高。
PIONEER AF-PCI和REDUAL PCI 研究的亚组分析结果显示基于NOAC的DAT比基于华法林的DAT出血风险更小,而血栓风险相似,无论是否是复杂PCI。
总结
分叉病变PCI的抗栓策略需要考虑多种因素,如临床表现(ACS还是稳定型冠心病)、基线的出血风险和支架术式等等。
尽可能在PCI中使用腔内影像学进行指导,最优的抗栓治疗策略还需要针对分叉病变PCI的研究。