2018人教版高中化学必修2第四章第一节《开发利用金属矿物和海水资源》(第1课时)ppt课件38页
- 格式:ppt
- 大小:2.23 MB
- 文档页数:38

第一节开发利用金属矿物和海水资源第1课时知识点一、金属的冶炼(1)热分解法对于不活泼金属,可以直接用加热分解的方法将金属从其化合物中还原出来,2HgO=2Hg+O2↑Ag2O=(2)热还原法在金属活动性顺序表中处于中间位置的金属,通常是用还原剂(C、CO、H2、活泼金属等)将金属从其化合物中还原出来,例如:Fe2O3+CO 高温WO3+H2高温(湿法炼铜)Fe+CuSO4= Fe2O3+Al高温【演示实验】课本P81实验4-1镁条的作用:氯酸钾的作用:现象:结论:化学方程式:铝热剂:应用:①焊接钢轨②冶炼高熔点金属(3)电解法活泼金属较难用还原剂还原,通常采用电解熔融的金属化合物的方法冶炼活泼金属,例如:NaCl(熔融)电解4NaOH(熔融)电解4Na+O2+2H2OMgCl2(熔融)电解Al2O3电解[思考] 工业上制备金属铝,采用电解熔融的Al2O3(加冰晶石时)而不电解熔融的AlCl3;工业上制备金属镁,则采用电解熔融的MgCl2,而不电解MgO的原因?[归纳小结]结论:金属活动顺序表中不同金属冶炼方法的选择K Ca Na Mg Al Zn Fe Sn Pb(H)Cu Hg Ag例题:冶炼金属一般有下列四种方法:①焦炭法,②水煤气(或H2或CO)法,③活泼金属置换法,④电解法。
四种方法在工业上均有应用。
古代有(Ⅰ)火烧孔雀石法炼铜,(Ⅱ)湿法炼铜,现代有(Ⅲ)铝热法炼铬,(Ⅳ)从光卤石(KCl•MgCl2•6H2O)中炼镁,对它们的冶炼方法分析不正确的是()A.(Ⅰ)用①B.(Ⅱ)用②C.(Ⅲ)用③D.(Ⅳ)用④巩固练习1.我国古代的湿法冶金术是世界闻名的。
我国在世界上最先应用湿法冶金术冶炼的金属是()A、FeB、CuC、AgD、Hg2.在冶金工业上,均不能用化学还原剂制得的一组金属是()A、Na Mg AlB、Na K Zn FeC、Zn Fe Cu AgD、Mg Al Zn Fe3.下列冶炼方法中,可将化合物中的金属元素还原为金属单质的是()_____________ ________________ ________A、加热Al2O3B、加热CaCO3C、电解熔融NaClD、氯化钠与铝粉高温共热4.铝能用于冶炼难熔的金属(如:钒、铬、锰等),这是因为铝具有什么性质()A、金属性和非金属性B、导电性C、熔点低D、还原性,在冶炼反应中放出大量热5.下列金属冶炼的反应原理,错误的是()A、2NaCl(熔融)电解2 Na+Cl2↑B、MgO+H2高温Mg+H2OC、Fe3O4+4CO 高温3Fe+4CO2D、2HgO高温2Hg+O2↑6..石灰在工农业生产和建筑业上有着重要用途。





第一节《开发利用金属矿物和海水资源》第一课时“开发利用金属矿物”教学设计一、教学内容分析本节课是高中化学必修2(人教版)第四章《化学与自然资源的开发利用》第一节《开发利用金属矿物和海水资源》第一课时的教学内容。
以金属活动顺序表、氧化还原反应为依托,探究金属的冶炼原理、金属资源的回收和利用。
化学研究和应用的一个重要的目标就是开发和利用自然界中可能的物质资源和能源资源,为人类生存和社会发展提供必要的物质和能源基础;同时,应注意到这一过程必须同自然环境相互协调,走可持续发展的道路。
帮助学生认识和体会化学在自然资源开发和利用中的意义和作用,揭示化学与可持续发展的重要关系,树立资源保护意识和合理开发意识。
二、学生情况分析学生在必修1中已学习了氧化还原反应的基本理论,掌握了钠、铝、铁、铜等金属元素及其重要化合物的性质,并且对金属冶炼知识也有了一定的了解,通过元素化合物知识的学习,已经掌握了化学学科的基本思想,以及比较、分类、归纳、推理等基本方法,在此前提下进一步系统学习工业上金属冶炼的方法。
三、教学策略与设计本节课的教学拟采用“问题引领,思考归纳”;“观看音像资料、阅读课本、思考、比较、讨论、总结”;“实验呈现”等方法;首先通过PPT课件创设问题情境,引导学生发现问题,形成认知冲突。
然后通过思考归纳,完成“冶炼的定义及原理”的学习任务;再通过提出问题、观看音像资料、阅读课本和观察实验,尽可能多的提供学生参与教学互动的活动空间,引导学生分析归纳,得出结论,完成“金属冶炼的方法与选择”的学习任务;四、教学目标及重、难点知识与技能(1)知道金属元素在自然界的存在形态;(2)了解金属冶炼的原理和方法;(3)知道铝热反应及其应用。
过程与方法(1)通过铝热反应的实验,学会金属冶炼的原理;(2)学会运用氧化还原概念归纳一般金属冶炼的实质和方法。
情感态度与价值观(1)通过了解金属回收的意义,培养学生的资源环保意识(2)通过联系知识与生产实践的关系,激发学生对化学学科的兴趣热爱教学重点:了解化学方法在金属矿物开发及海水资源开发中的作用。


海水资源的开发利用学习目标:了解海水资源开发和利用的前景及化学在其中可以发挥的作用;体验工业生产的复杂性、艰苦性。
学习方法:教师指导下学生的合作、探究学习。
学习过程一、学前准备:1、你亲密接触过大海吗?你的感受如何?2、你对大海了解多少?请从报刊、书籍、网络等多渠道、全方位了解海洋。
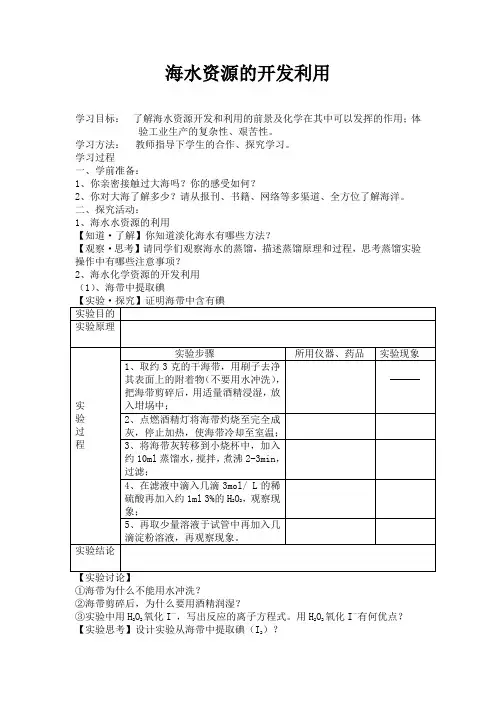
二、探究活动:1、海水水资源的利用【知道·了解】你知道淡化海水有哪些方法?【观察·思考】请同学们观察海水的蒸馏,描述蒸馏原理和过程,思考蒸馏实验操作中有哪些注意事项?2、海水化学资源的开发利用(1)、海带中提取碘①海带为什么不能用水冲洗?②海带剪碎后,为什么要用酒精润湿?③实验中用H2O2氧化I—,写出反应的离子方程式。
用H2O2氧化I—有何优点?【实验思考】设计实验从海带中提取碘(I2)?(2)、海水中提取溴是海水提溴中关键的化学反应,你能否设计【探究·感受】将Br - 转变为Br2一个实验方案模拟这一生产过程?写出有关反应的方程式。
【思考·交流】该过程的目的是获得溴单质,第一步已经得到了溴单质,为什么还要将其转变为氢溴酸之后再进一步氧化为溴单质?三、链接相关知识:海水中提取食盐(必修1)【复习·思考1】比如你就是盐场的技术人员,你如何提取海水中的NaCl?【复习·思考2】如何对粗盐提纯?粗盐中含有哪些杂质离子?为除去这些杂质离子,应加入哪些除杂试剂?除杂试剂在量上有什么要求?在加入顺序上有什么要求?四、知识拓展:镁是一种用途很广的金属材料,目前世界上60%的镁从海水中提取。
流程如下,请写出有关反应方程式。
五、学习体会:1、本节课你有哪些收获?2、你认为老师上课过程中还有哪些需要注意或改进的地方?。

人教版化学必修2第四章第一节《开发利用金属矿物和海水资源》第四章第一节开发利用金属矿物和海水资源☆金属的存在有什么规律吗引言少数化学性质不活泼的金属,在自然界中能以游离态存在,如金和铂以及少量的银和铜,较活泼的铁只能存在于陨石中,而化学性质活泼的金属,在自然界中总是以化合态存在.但在实际生产和生活中应用的金属材料却往往是纯金属或合金,这就需要把金属从金属矿物中提炼出来,这就叫做金属的冶炼.一、金属矿物物开发利用1.你知道从金属矿物中提炼金属,一般要经过哪些步骤金属冶炼的步骤:矿石富集金属冶炼金属精炼2.要将化合态的金属矿物转化为金属单质,有哪些方法其实质是什么金属冶炼的一般方法:(1).热分解法.(2).热还原法.(3).电解法.金属冶炼的实质:利用还原的方法,使金属化合物中的金属离子得到电子变成金属原子.解说不活泼的金属汞和银的氧化物不稳定,受热易分解生成金属单质和氧气;较活泼的金属如铁等和不活泼金属铜的氧化物稳定,受热不易分解,需用还原剂(焦炭、一氧化碳、氢气、铝)来还原;活泼金属如钠、铝等氧化物非常稳定,加热或热还原剂均无法使其分解,只能用最强的还原手段即电解法使其氯化物、氧化物还原。
不活泼金属的冶炼△2HgO===2Hg+O2↑△2Ag2O===4Ag+O2↑活泼金属常用电解法冶炼MgCl2(熔融)===Mg+Cl2↑电解2Al2O3(熔融)===4Al+3O2↑冰晶石电解2NaCl(熔融)===2Na+Cl2↑冰晶石:Na3AlF6电解实验4-1铝热反应表4-1常见金属的冶炼原理金属冶炼原理Fe2O3+3CO===2Fe+3CO2(高炉炼铁)高温Fe2O3+2Al===2Fe+Al2O3(铝热法炼铁)Cu2S+O2===2Cu+SO2(火法炼铜)Fe+CuSO4===FeSO4+Cu(湿法炼铜)高温MgO+C===Mg+CO↑电解MgCl2(熔融)===Mg+Cl2↑电解2Al2O3(熔融)===4Al+3O2↑冰晶石高温高温FeCuMgAlNa2NaCl(熔融)===2Na+Cl2↑电解4NaOH(熔融)===4Na+O2↑+2H2O电解请结合金属活泼性顺序表总结金属冶炼方法的一般规律:金属的活动顺序金属原子失电子能力金属离子得电子能力主要冶炼方法KCaNaMgAlZnFeSnPbCuHgAgPtAu强弱电解法热还原法弱强热分解法二、海水资源的开发利用1、海水资源的广阔性海洋约占地球表面积的71%。
第四章第一节开发利用金属矿物和海水资源(第一课时)金属矿物的开发利用【学习目标】1.了解金属元素在自然界的存在形态。
2.掌握金属冶炼的原理和方法。
3.了解废旧金属回收利用的意义【学习重点】了解化学方法在金属冶炼中的作用【预习案】先预习课本标注要点,对疑难问题特殊标记。
再观看微课。
完成以上任务后回答下列问题。
【问题1】金属元素在自然界中的存在形态?【问题2】金属冶炼的定义是什么?【问题3】初中我们学过哪些化学反应可以制取金属单质?(写出相关反应方程式)【问题4】依据金属活泼性不同,金属冶炼可以采用哪些方法?【预习检测】1.下列各组物质中,均能使Fe2O3还原成铁单质的是()A.CO、O2、H2 B.CO、CO2、C C.CO2、CO、C D.Al、C 、H22.判断正误(正确的打√,错误的打╳)(1)在自然界中金属都以化合态形式存在()(2)在金属化合物中金属元素都显正价()(3)金属冶炼过程中,金属化合物得到电子发生氧化反应()(4)金属的活动性越强,即金属失电子能力越强()【探究案】探究一:常见金属的冶炼方法【交流研讨1】从石器、青铜器时代到铁器时代,人类冶炼金属和使用金属的顺序是一种历史的巧合还是历史的必然?之所以有先后,主要取决于什么?【交流研讨2】归纳常见金属的冶炼与金属活动顺序表的关系:ol ,消耗铝最少的是8.以辉铜矿Cu 2S 为原料冶炼铜,其反应原理可表示为Cu 2S +O 2错误!ol O 2参加反应时,上述反应转移电子总物质的量为4 mol被分离、回收后氧化生成SO 3,作为制取硫酸的原料91Al 与Fe 3O 4发生铝热反应的化学方程式为________________________________________________________________________,该反应中氧化剂是____________,还原剂是__________________________________。
第1课时金属矿物的开发利用1.了解金属在自然界中的存在形式。
2.掌握金属的冶炼方法。
3.掌握铝热反应原理及实验。
4.了解金属回收和资源保护的意义。
5.认识和体会化学在自然资源开发和利用中的意义和作用。
1.金属活动性顺序为K、Ca、Na、Mg、Al、Zn、Fe、Sn、Pb(H)、Cu、Hg、Ag、Pt、Au_。
2.金属的存在(1)地壳中含量最高的金属元素是铝,其次是铁。
(2)金、铂等少数金属以游离态的形式存在,绝大多数金属以化合态的形式存在于自然界中。
3.金属冶炼的含义:将金属矿物中的金属从其化合物中还原出来用于生产和制造各种金属材料的过程。
4.常见金属的冶炼方法(1)冶炼铝的方法:电解法,化学方程式:。
(2)冶炼铁的方法:热还原法、铝热法,化学方程式:Fe 2O 3+3CO=====高温2Fe +3CO 2 、Fe 2O 3+2Al=====高温2Fe +Al 2O 3。
(3)冶炼银的方法:热分解法,化学方程式:2Ag 2O=====△4Ag +O 2↑。
(4)冶炼铜的方法:火法炼铜、湿法炼铜,化学方程式:Cu 2S +O 2=====高温2Cu +SO 2 、Fe +CuSO 4===FeSO 4+Cu 。
5.金属资源的合理开发利用 (1)提高金属矿物的利用率。
(2)减少金属的使用量。
(3)加强金属资源的回收和再利用。
(4)使用其他材料代替金属材料。
[新知探究]1.金属冶炼的实质是用还原的方法使金属化合物中的金属离子得到电子变成金属原子。
2.金属冶炼的方法有哪些?完成下表。
续表3.工业上冶炼镁、铝的原理是什么?可否电解熔融MgO 和AlCl 3制取镁、铝,为什么? 提示:MgCl 2(熔融)Mg +Cl 2↑,2Al 2O 3(熔融)=====电解冰晶石4Al +3O 2↑。
MgO 的熔点远高于MgCl 2,而AlCl 3属于共价化合物,熔融状态不导电,故工业上冶炼Mg 、Al 是电解熔融的MgCl 2、Al 2O 3而不是电解MgO 和AlCl 3。
- 1 -第四章 化学与可持续发展第一节 开发利用金属矿物和海水资源一、金属矿物的开发利用1、金属的存在:除了金、铂等少数金属外,绝大多数金属以化合态的形式存在于自然界。
2、金属冶炼的涵义:简单地说,金属的冶炼就是把金属从矿石中提炼出来。
金属冶炼的实质是把金属元素从化合态还原为游离态,即M +n (化合态) M 0(游离态)。
3、金属冶炼的一般步骤: (1)矿石的富集:除去杂质,提高矿石中有用成分的含量。
(2)冶炼:利用氧化还原反应原理,在一定条件下,用还原剂把金属从其矿石中还原出来,得到金属单质(粗)。
(3)精炼:采用一定的方法,提炼纯金属。
4、金属冶炼的方法(1)电解法:适用于一些非常活泼的金属。
2NaCl (熔融) 电解2Na +Cl 2↑ MgCl 2(熔融) 电解Mg +Cl 2↑ 2Al 2O 3(熔融) 电解4Al +3O 2↑(2)热还原法:适用于较活泼金属。
Fe 2O 3+3CO 高温2Fe +3CO 2↑ WO 3+3H 2 高温 W +3H 2O ZnO +C 高温Zn +CO ↑常用的还原剂:焦炭、CO 、H 2等。
一些活泼的金属也可作还原剂,如Al ,Fe 2O 3+2Al 高温2Fe +Al 2O 3(铝热反应) Cr 2O 3+2Al 高温2Cr +Al 2O 3(铝热反应)(3)热分解法:适用于一些不活泼的金属。
2HgO △2Hg +O 2↑ 2Ag 2O △4Ag +O 2↑5、 (1)回收金属的意义:节约矿物资源,节约能源,减少环境污染。
(2)废旧金属的最好处理方法是回收利用。
(3)回收金属的实例:废旧钢铁用于炼钢;废铁屑用于制铁盐;从电影业、照相业、科研单位和医院X 光室回收的定影液中,可以提取金属银。
二、海水资源的开发利用1、海水是一个远未开发的巨大化学资源宝库 海水中含有80多种元素,其中Cl 、Na 、K 、Mg 、Ca 、S 、C 、F 、B 、Br 、Sr 11种元素的含量较高,其余为微量元素。