第二章烃和卤代烃复习课
- 格式:ppt
- 大小:606.00 KB
- 文档页数:29

第2讲卤代烃考点三:卤代烃的结构与性质1.概念:烃分子里的氢原子被取代后生成的产物。
官能团为,饱和一元卤代烃的通式为。
2.物理性质状态:除CH3Cl、CH3CH2Cl、CH2=CHCl等少数为气体外,其余为液体或固体。
沸点:比同碳原子数的烷烃沸点要;同系物沸点,随碳原子数增加而。
溶解性:卤代烃难溶于水,易溶于有机溶剂。
密度:一氟代烃、一氯代烃的密度比水小,其余的密度比水。
3.化学性质(1)水解反应①反应条件为强碱(如NaOH)水溶液、加热。
②C2H5Br在碱性(如NaOH溶液)条件下发生水解反应的化学方程式。
(2)消去反应①概念:有机化合物在一定条件下,从一个分子中脱去一个或几个小分子(如H2O、HBr等),生成含(如双键或三键)化合物的反应。
②反应条件为强碱(如NaOH)的乙醇溶液、加热。
③溴乙烷在NaOH的乙醇溶液中发生消去反应的化学方程式。
4.卤代烃对环境的影响:氟氯烃在大气平流层中会破坏臭氧层,是造成臭氧空洞的主要原因。
5.卤代烃的获取方法(1)取代反应(写出化学方程式):乙烷与Cl2:;苯与Br2:;C2H5OH与HBr:。
(2)不饱和烃的加成反应丙烯与Br2的加成反应: CH3-CH=CH2+Br2―→。
【题例解析】考向一:卤代烃的两种重要反应类型1.下列化合物在一定条件下,既能发生消去反应,又能发生水解反应的是 ( )A.CH3ClB.C.D.【答案】B【归纳总结】1.卤代烃水解反应和消去反应的比较反应类型水解反应(取代反应)消去反应反应条件强碱的水溶液、加热强碱的醇溶液、加热断键方式反应本质和通式卤代烃分子中-X 被水中的-OH 所取代,生成醇:RCH 2-X+NaOH ――→H 2O△RCH 2OH+NaX 相邻的两个碳原子间脱去小分子HX产物特征引入—OH ,生成含—OH 的化合物消去HX ,生成含碳碳双键或碳碳三键的化合物2.卤代烃水解反应和消去反应的规律 (1)水解反应①卤代烃在NaOH 的水溶液中一般能发生水解反应。





第二章 烃和卤代烃单元复习
【教学目标】
1.对各类烃进行归钠、整理,构建知识体系。
2.培养学生对知识的整合能力。
【预习任务】
1.结合课本P44内容,掌握下列网络:
乙炔有机物
烃
烃的衍
生物
【自主检测】
1.下列叙述中,错误的是()
A.苯与浓硝酸、浓硫酸共热并保持55-60℃反应生成硝基苯
B.苯乙烯在合适条件下催化加氢可生成乙基环己烷
C.乙烯与溴的四氯化碳溶液反应生成1,2-二溴乙烷
D.甲苯与氯气在光照下反应主要生成2,4-二氯甲苯
2.下列说法正确的是( )
A.乙烯的结构简式可以表示为CH2CH2
B.苯、乙醇和乙酸都能发生取代反应
C.溴乙烷都能使硝酸银产生白色溶液沉淀
D .液化石油气和天然气的主要成分都是甲烷
3.下列烷烃在光照下与氯气反应,只生成一种一氯代烃的是( ) (A)CH 3CH 2CH 2CH 3 (B)CH 3CH(CH 3)2
(C)CH 3C(CH 3)3 (D)(CH 3)2CHCH 2CH 3
4.煤的气化是煤高效、洁净利用的方向之一。
下图为加热某地煤样所得煤气组成及体积分数随温度变化的曲线图。
由图可知该煤气中( )
t / ℃
(A)只含有碳、氢两种元素
(B)所含的有机物是CH 4、C n H m 、CO (C)CO 体积分数小于CH 4体积分数 (D)氢气体积分数最大。
课题烃和卤代烃专题复习教学目标了解烷烃,烯烃,炔烃,苯,卤代烃物理性质,掌握各自化学性质和特征反应,理解机理,掌握其运用重点掌握烃和卤代烃的化学性质,理解机理,掌握运用难点烃和卤代烃的化学性质作业剩余教案题目加以巩固知识回顾(一)烷烃(1)烷烃的通式 C n H2n+2(2)烃的物理性质:①密度:所有烃的密度都比水小②状态:常温下,碳原子数小于等于4的气态③熔沸点:碳原子数越多,熔、沸点越高;碳原子数相同,支链越多,熔沸点越低;④烷烃都不溶与水、易溶于有机溶剂(3)各类烃及卤代烃的结构特点和化学性质二、有机化学的主要反应类型1、取代反应2、加成反应3、消去反应4、氧化反应5、还原反应6、聚合反应7、酯化反应 8、水解反应(二)烯烃复习 [以乙烯为主体](1)(单)烯烃的通式__________(2)烯烃的物理性质的变化规律与烷烃一样,C1到C4均为气体,其他为非气态,熔沸点都随碳原子个数增加而增大,密度都小于水(3)烯烃的化学性质(与乙烯类似)(各举一例写出方程式)1)氧化反应①燃烧②与酸性KMnO4溶液反应:能使酸性KMnO4溶液褪色。
2)加成反应(可与H2、X2、HX、H2O加成)3)加聚反应【另注:乙烯为稍有气体的烯烃,是重要化工石油原料】(5)二烯烃的化学性质(各举一例写出方程式)1)二烯烃的加成反应:2) 加聚反应:(6)二烯烃的命名针对练习1.乙烷中混有少量乙烯气体, 欲除去乙烯可选用的试剂是()A.氢氧化钠溶液B.酸性高锰酸钾溶液C.溴水 D.碳酸钠溶液2.将15克甲烷与乙烯的混合气通入盛有溴水(足量)的洗气瓶, 反应后测得溴水增重7克, 则混合气中甲烷和乙烯的体积比为()A.2∶1 B.1∶2 C.3∶2 D.2∶33.下列变化中,由加成反应引起的是:A.乙炔通入酸性高锰酸钾溶液中,高锰酸钾溶液褪色B.乙烯在氧气中燃烧生成二氧化碳和水C.在光照条件下,C2H6与Cl2反应生成了油状液体D.在催化剂作用下,乙烯与水反应生成乙醇(三)、炔烃(1)炔烃的通式__________(2)炔烃的化学性质(与乙炔类似)(各举一例写出方程式)1)、氧化反应:a.可燃性:b.被KMnO4氧化:能使紫色酸性高锰酸钾溶液褪色。
烃和卤代烃2.直馏汽油和裂化汽油的区别3.各种工业制气的主要成分考点三:苯的同系物与苯在结构和性质上的异同1.相同点(1)分子里都含有一个苯环;(2)都符合通式C n H2n-6(n≥6);(3)燃烧时都能产生带浓烟的火焰,苯和苯的同系物燃烧反应的通式为:(4)都能发生取代反应;(5)均能发生加成反应,且1 mol苯或苯的同系物均能与3 mol H2加成。
2.不同点(1)甲基对苯环的影响①苯的同系物比苯更容易发生苯环上的取代反应,苯主要发生一元取代,而苯的同系物能发生邻、对位取代,如苯与浓H2SO4、浓HNO3混合加热主要生成,甲苯与浓HNO3、浓H2SO4混合加热在30℃时主要生成邻硝基甲苯和对硝基甲苯两种一元取代产物;在一定条件下易生成2,4,6三硝基甲苯(TNT)。
②苯的同系物发生卤代反应时,在光照和催化剂条件下,卤素原子取代氢的位置不同,如:、。
(2)苯环对甲基的影响烷烃不易被氧化,但苯环上的烷基易被氧化。
苯的同系物能使酸性高锰酸钾溶液褪色,而苯不能被酸性高锰酸钾溶液氧化,用此法可鉴别苯和苯的同系物。
考点四:有机烃在有机合成中的桥梁作用1.卤代烃的主要化学性质2.卤代烃的消去反应规律(1)没有邻位碳原子的卤代烃不能发生消去反应。
例如CH3Cl。
(2)有邻位碳原子,但邻位碳原子上没有氢原子的卤代烃也不能发生消去反应。
例如:(3)卤代烃发生消去反应,也可生成炔烃,如(4)卤代烃和醇发生消去反应的条件不同,如:3.卤代烃在有机合成中的经典路线通过烷烃、芳香烃与X2发生取代反应,烯烃、炔烃与X2、HX发生加成反应等途径可向有机物分子中引入-X;而卤代烃的水解和消去反应均消去-X。
卤代烃发生取代、消去反应后,可在更大的空间上与醇、醛、酸、酯相联系。
引入卤素原子常常是改变物质性能的第一步反应,卤代烃在有机物的转化、合成中具有“桥梁”的重要地位和作用。
其合成路线如下:(1)一元合成路线RCH=CH2―→一卤代烃―→一元醇―→一元醛―→一元羧酸―→酯(2)二元合成路线RCH=CH2―→二卤代烃―→二元醇―→二元醛―→二元羧酸―→酯(链酯、环酯、聚酯)(R代表烃基或H)4.卤代烃一元取代物与二元取代物之间的转化关系考点五:典型烃的空间结构1.烃的典型代表物的分子结构特点:(1)甲烷分子(CH4)为正四面体结构,最多有3个原子共平面;(2)乙烯的平面结构。
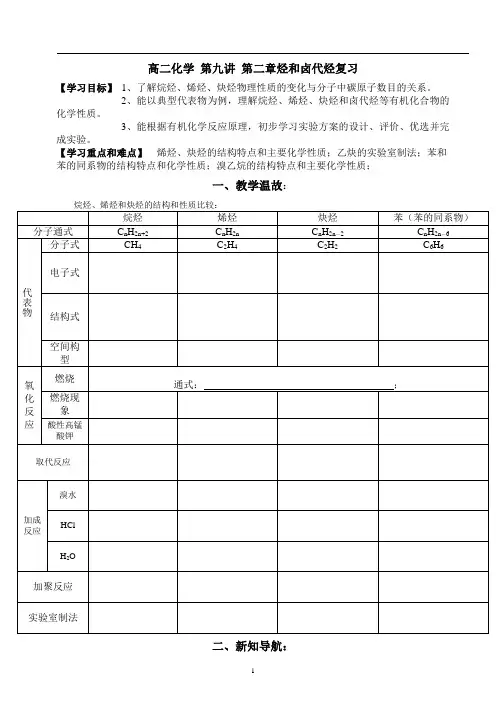
高二化学第九讲第二章烃和卤代烃复习【学习目标】1、了解烷烃、烯烃、炔烃物理性质的变化与分子中碳原子数目的关系。
2、能以典型代表物为例,理解烷烃、烯烃、炔烃和卤代烃等有机化合物的化学性质。
3、能根据有机化学反应原理,初步学习实验方案的设计、评价、优选并完成实验。
【学习重点和难点】烯烃、炔烃的结构特点和主要化学性质;乙炔的实验室制法;苯和苯的同系物的结构特点和化学性质;溴乙烷的结构特点和主要化学性质;一、教学温故:烷烃、烯烃和炔烃的结构和性质比较:烷烃烯烃炔烃苯(苯的同系物)分子通式C n H2n+2C n H2n C n H2n-2C n H2n-6代表物分子式CH4C2H4C2H2C6H6电子式结构式空间构型氧化反应燃烧通式:;燃烧现象酸性高锰酸钾取代反应加成反应溴水HCl H2O加聚反应实验室制法二、新知导航:芳香烃卤代烃烃和卤代烃链烃二.有机物完全燃烧前后气体体积的变化 1、气态烃(C x H y )在100℃及其以上温度完全燃烧时气体体积变化规律与氢原子个数有关①若y 4,燃烧前后体积不变,△V=0②若y 4,燃烧前后体积增大,△V=14-y③若y 4,燃烧前后体积减少,△V=41y-2、气态烃(C x H y )完全燃烧后恢复到常温常压时气体体积的变化直接用烃类物质燃烧的通式通过差量法确定即可。
三.有机物完全燃烧耗氧量比较1、有机物的质量一定时:烃类物质(CxHy)完全燃烧的耗氧量与 成正比;2、有机物物质的量一定时,烃类物质(CxHy)完全燃烧的耗氧量取决于 ;三、经典范例:【例1】描述CH 3-CH =CH -C ≡C -CF 3分子结构的下列叙述中,正确的是( ) A. 6个碳原子有可能都在一条直线上 B. 6个碳原子不可能都在一条直线上 C. 6个碳原子有可能都在同一平面上 D. 6个碳原子不可能都在同一平面上 解析:依据基团的结构,将原题中的结构简式改写为如图所示的立体结构,并将碳原子编号。