高中化学:分子极性
- 格式:pdf
- 大小:127.56 KB
- 文档页数:3

高三化学分子结构与化学反应知识点概述化学是一门研究物质的组成、结构、性质以及变化规律的基础自然科学。
在高中化学的学习中,分子结构与化学反应是两个核心知识点,对于理解化学的本质和探索化学世界具有重要的意义。
本文将对这两个知识点进行详细的阐述和解析。
一、分子结构分子是化学中最基本的单位,分子结构则决定了分子的性质。
分子结构主要包括以下几个方面:1.原子组成:分子由原子组成,不同种类的原子以一定的比例结合形成分子。
例如,水分子(H₂O)由两个氢原子和一个氧原子组成。
2.空间构型:原子在分子中的空间排列形式称为分子的空间构型。
它决定了分子的形状和性质。
例如,甲烷(CH₄)的空间构型为正四面体,而乙烯(C₂H₄)的空间构型为平面结构。
3.化学键:原子之间的连接称为化学键。
化学键的类型有离子键、共价键和金属键。
其中,共价键又分为单键、双键和三键。
例如,氢气(H₂)中的氢原子之间是共价单键,氮气(N₂)中的氮原子之间是共价三键。
4.分子极性:分子极性取决于分子的空间构型和化学键的类型。
极性分子中正负电荷的中心不重合,而非极性分子中正负电荷的中心重合。
例如,水(H₂O)是极性分子,而二氧化碳(CO₂)是非极性分子。
二、化学反应化学反应是物质在原子、离子或分子层面上发生的转化,产生新的物质。
化学反应的本质是旧键的断裂和新键的形成。
化学反应主要包括以下几个方面:1.反应类型:根据反应的物质变化和能量变化,化学反应可以分为合成反应、分解反应、置换反应、复分解反应等。
每种反应类型都有其特定的特点和规律。
2.反应速率:化学反应速率是指反应物浓度变化的速度。
影响反应速率的因素有反应物浓度、温度、催化剂等。
反应速率可用反应物浓度的变化量与时间的比值表示。
3.化学平衡:在封闭系统中,正反应速率达到相等时,反应体系中各种物质的浓度或含量不再发生变化的状态称为化学平衡。
化学平衡常数K表示平衡时反应物和生成物的浓度比。
4.氧化还原反应:氧化还原反应是指电子的转移。


高中化学选修3分子极性的判断技巧与重要物质的用途STEP1、共价键的极性判断化学键有无极性,是相对于共价键而言的。
从本质上讲,共价键有无极性取决于共用电子对是否发生偏移,有电子对偏移的共价键即为极性键,无电子对偏移的共价键即为非极性键。
从形式上讲,一般来说,由同种元素的原子形成的共价键即为非极性键,由不同种元素的原子形成的共价键即为极性键。
在学习共价键的极性判断时,一定要走出这样一种误区“由同种元素的原子形成的共价键一定为非极性键”。
对于化合物来说,象H3C-CH3中的“C-C”键、CH2=CH2中的“C=C”键、Na2O2中的“O-O”键等具有结构对称的分子中同种元素原子间形成的共价键的确是非极性键。
但象CH3CH2OH、CH3COOH等结构不对称的分子中的“C-C”键却不是非极性键,而是极性键。
对于单质来说,象在H2、O2、N2、P4、C60、金刚石、石墨等共价单质中的共价键的确是非极性键。
但在O3分子中的“O-O”键却不是非极性键,而是极性键。
这是因为O3分子结构呈“V”型(或角型),键长为127.8pm(该键长正好位于氧原子单键键长148 pm与双键键长112 pm之间),与SO2结构相似,可模仿SO2把O3称作“二氧化氧”,所以O3分子中的“O-O”键是极性键,其分子是极性分子。
二、分子的极性判断分子是否存在极性,不能简单的只看分子中的共价键是否有极性,而要看整个分子中的电荷分布是否均匀、对称。
根据组成分子的原子种类和数目的多少,可将分子分为单原子分子、双原子分子和多原子分子,各类分子极性判断依据是:1、单原子分子:分子中不存在化学键,故无极性分子或非极性分子之说,如He、Ne等稀有气体分子。
2、双原子分子:对于双原子分子来说,分子的极性与共价键的极性是一致的。
若含极性键就是极性分子,如HF、HI等;若含非极性键就是非极性分子,如I2、O2、N2等。
3、多原子分子:⑴以非极性键结合的多原子单质分子,都是非极性分子,如P4等。


第2课时分子的极性与手性分子目标与素养:1.初步认识分子的极性、手性分子等概念。
(微观探析)2.认识分子的空间构型与分子极性的关系。
(宏观辨识)一、分子的极性1.极性分子与非极性分子(1)极性分子:正电荷重心和负电荷重心不相重合的分子。
(2)非极性分子:正电荷重心和负电荷重心相重合的分子。
2.分子极性的判断方法分子的极性是由分子中所含共价键的极性与分子的空间构型两方面共同决定的。
判断分子极性时,可根据以下原则进行:(1)只含有非极性键的双原子分子或多原子分子大多是非极性分子,如O2、H2、P4、C60。
(2)含有极性键的双原子分子都是极性分子,如HCl、HF、HBr。
(3)含有极性键的多原子分子,空间结构中心对称的是非极性分子;空间结构中心不对称的是极性分子。
3.分子的极性对物质溶解性的影响——相似相溶规则非极性分子构成的物质一般易溶于非极性溶剂,极性分子构成的物质一般易溶于极性溶剂。
二、手性分子1.观察比较下图所示两种分子的结构(1)相同点是分子组成相同、都是CHFClBr,从平面上看相似。
(2)不同点是在空间上不同,它们构成实物和镜像关系。
(3)具有完全相同的组成和原子排列的一对分子,如同左手与右手一样互为镜像,却在三维空间里不能重叠,互称为手性异构体。
有手性异构体的分子叫做手性分子。
2.手性分子的判断判断一种有机物是否具有手性异构体,关键是看其含有的碳原子是否连有4个不同的原子或基团,即有机物分子中是否存在手性碳原子,如,R1、R2、R3、R4互不相同,含有手性碳原子,该有机物分子具有手性。
3.手性分子的重要用途由于手性分子对生命及生理活动有其特殊的活性,化学工作者期望可以找到对癌症和一些目前的疑难杂症有治疗作用的手性药品;同时也期望早日实现“手性分子”的合成和分离的工业化;期望能制造出可以利用的“手性分子”作为高分子聚合物的单体,用以合成易降解的高分子化合物,减少环境污染。
(1)手性异构体(又称对映异构体、光学异构体)的两个分子互为镜像关系,即分子形式的“左撇子和右撇子”。
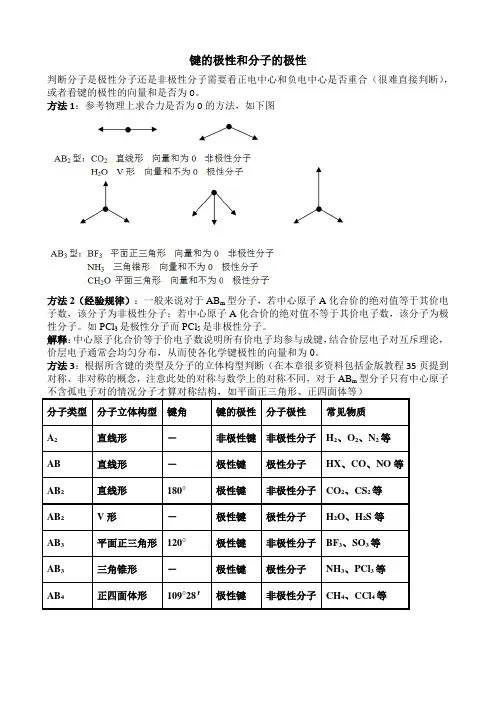
键的极性和分子的极性判断分子是极性分子还是非极性分子需要看正电中心和负电中心是否重合(很难直接判断),或者看键的极性的向量和是否为0。
方法1:参考物理上求合力是否为0的方法,如下图方法2(经验规律):一般来说对于AB m型分子,若中心原子A化合价的绝对值等于其价电子数,该分子为非极性分子;若中心原子A化合价的绝对值不等于其价电子数,该分子为极性分子。
如PCl3是极性分子而PCl5是非极性分子。
解释:中心原子化合价等于价电子数说明所有价电子均参与成键,结合价层电子对互斥理论,价层电子通常会均匀分布,从而使各化学键极性的向量和为0。
方法3:根据所含键的类型及分子的立体构型判断(在本章很多资料包括金版教程35页提到对称、非对称的概念,注意此处的对称与数学上的对称不同,对于AB m型分子只有中心原子化学键类型和物质类别的关系:1.不含有化学键的物质:稀有气体分子。
2.只含非极性键的物质:同种非金属元素构成的单质。
H2、P4、金刚石等3.只含极性键的物质:一般是不同非金属元素构成的共价化合物。
HCl、NH3等4.含非极性键和极性键的物质:H2O2、C2H2、CH3CH3、C6H6等5.只含离子键的物质:活泼金属与活泼非金属元素形成的化合物。
MgCl2、K2O等6.含离子键和非极性键的物质:Na2O2、CaC2等7.含离子键和极性键的物质:NaOH等8.含离子键、极性键和非极性键的物质:CH3COONa等9.只含金属键的物质:金属和合金(第三章内容)10.含金属键和共价键的物质:石墨(第三章内容)分子极性与键的极性的关系:1.只含非极性键的物质一定是非极性分子(除O3外的单质分子。
O3分子是V形结构,存在一个大π键,从而导致整个分子正电中心与负电中心不重合。
有时候题中会考查O3的分子构型,可根据O3与SO2互为等电子体判断)。
2. AB型的双原子分子只含一个极性键,一定是极性分子。
3.只含极性键的AB m型分子可能是极性分子(如H2O、NH3等),也可能是非极性分子(如CO2、BF3、CCl4等)。



《分子极性》高中化学教案设计一、教学目标1. 让学生理解分子的概念,知道分子是由原子通过共价键连接而成的粒子。
2. 让学生了解极性分子的概念,能判断常见分子的极性。
3. 让学生掌握极性分子和非极性分子的性质差异。
4. 培养学生运用分子极性理论分析解释化学现象的能力。
二、教学重点与难点1. 教学重点:分子极性的判断方法,极性分子和非极性分子的性质差异。
2. 教学难点:分子极性判断的原理,极性分子和非极性分子在实际应用中的例子。
三、教学方法1. 采用问题驱动法,引导学生探究分子极性的判断方法。
2. 利用多媒体课件,展示分子的结构模型,增强学生的直观感受。
3. 通过小组讨论,培养学生的合作能力和口头表达能力。
4. 运用实例分析,让学生将理论知识与实际应用相结合。
四、教学准备1. 多媒体课件:分子结构模型、极性分子和非极性分子的图片及实例。
2. 教学用具:黑板、粉笔、分子模型。
3. 课前准备:让学生预习相关知识,了解分子极性的基本概念。
五、教学过程1. 导入新课利用多媒体课件展示一个水分子模型,引导学生回顾分子的概念。
提问:同学们能说出哪些是由分子构成的物质吗?2. 探究分子极性的判断方法提问:我们如何判断一个分子是否具有极性呢?引导学生思考并讨论。
讲解:分子极性的判断方法。
举例说明极性分子(如HCl)和非极性分子(如CO2)。
3. 极性分子和非极性分子的性质差异提问:同学们能想到哪些极性分子和非极性分子在性质上的差异吗?讲解:极性分子和非极性分子在溶解性、熔点、沸点等方面的性质差异。
4. 实例分析提问:同学们能举例说明极性分子和非极性分子在实际应用中的差异吗?讲解:实例分析,如溶解现象、分子间作用力等。
5. 课堂小结总结本节课所学内容,让学生明确分子极性的判断方法和极性分子与非极性分子的性质差异。
6. 布置作业让学生完成课后练习,巩固所学知识。
六、教学活动1. 案例分析:通过具体案例分析,让学生了解分子极性在现实生活中的应用,如溶剂的选择、分子间相互作用等。

高中化学分子的极性与非极性解析极性分子和非极性分子:(1)极性分子:正电荷中心和负电荷中心不相重合的分子(2)非极性分子:正电荷中心和负电荷中心相重合的分子(3)分子极性的判断:分子的极性由共价键的极性及分子的空间构型两个方面共同决定非极性分子和极性分子的比较:举例说明:分子极性的判断方法:An型分子(以非极性键结合形成的单质分子)一般是非极性分子(O3例外),AB型分子一定是极性分子。
对于ABn型分子是极性分子还是非极性分子,通常有以下判断方法。
1.根据分子的立体构型判断判断ABn型分子是否有极性,关键是看分子的立体构型.如果分子的立体构型为直线形、平面三角形、正四面体形、三角双锥形、正八面体形等空间对称的结构,致使正电中心与负电中心重合,这样的分子就是非极性分子。
若为V形、三角锥形、四面体形(非正四面体形)等非对称结构,则为极性分子。
比如H2O分子中虽然2个H原子轴对称,但整个分子的空间构型是不对称的:,负电中心在a点,正电中心在b 点,二者不重合,因此是极性分子。
2.根据实验现象判断将液体放入适宜的滴定管中,打开活塞让其缓慢流下,将用毛皮摩擦过的橡胶棒靠近液流,流动方向变化(发生偏移)的是极性分子.流动方向不变的是非极性分子。
3.根据中心原子最外层电子是否全部成键判断ABn型分子中的中心原子A的最外层电子若全部成键(没有孤电子对),此分子一般为非极性分子,如CO2、CCl4等;分子中的中心原子最外层电子若未全部成键(有孤电子对),此分子一般为极性分子,如H2O、PCl3等。
4.判断ABn型分子极性的经验规律若中心原子A的化合价的绝对值等于该元素所在的主族序数,则为非极性分子;若不等,则为极性分子。
如BF3、CO2、CH4、SO3等分子中,B、C、S等元素的化合价的绝对值等于其主族序数,是非极性分子;H2O、NH3、SO2、PCl3等分子中,O、N、S、P等元素的化合价的绝对值不等于其主族序数,是极性分子。

《分子极性》高中化学教案设计一、教学目标1. 让学生理解分子极性的概念及其与分子结构和性质的关系。
2. 培养学生运用价层电子对互斥理论分析分子极性的能力。
3. 通过对分子极性的学习,提高学生的科学思维能力和解决问题的能力。
二、教学内容1. 分子极性的定义及判断方法。
2. 常见极性分子与非极性分子的实例分析。
3. 分子极性与分子性质的关系。
三、教学重点与难点1. 教学重点:分子极性的判断方法,分子极性与分子性质的关系。
2. 教学难点:价层电子对互斥理论在分子极性判断中的应用。
四、教学方法1. 采用问题驱动的教学方法,引导学生通过实例分析分子极性。
2. 利用多媒体课件,形象直观地展示分子结构和极性判断过程。
3. 结合小组讨论,培养学生的合作交流能力和科学思维。
五、教学过程1. 导入:通过生活中的实例,如溶解现象,引出分子极性的概念。
2. 新课导入:介绍分子极性的定义及判断方法。
3. 实例分析:分析常见极性分子和非极性分子的实例,让学生加深对分子极性的理解。
4. 理论讲解:讲解价层电子对互斥理论在分子极性判断中的应用。
5. 小组讨论:让学生分组讨论分子极性与分子性质的关系,分享讨论成果。
6. 总结与拓展:总结本节课的主要内容,布置课后习题,引导学生进一步思考。
六、教学评估1. 课堂提问:通过提问了解学生对分子极性概念的理解程度。
2. 实例分析:观察学生在分析常见极性分子和非极性分子时的判断准确性。
3. 课后习题:布置与分子极性相关的习题,检验学生对知识的掌握情况。
七、教学反思1. 反思教学内容:检查教学内容是否全面,难易程度是否适中。
2. 反思教学方法:思考教学方法是否有效,学生参与度是否较高。
3. 反思教学效果:评估学生对分子极性的理解和应用能力,发现问题并及时调整。
八、教学拓展1. 分子极性与溶解性:讲解分子极性对溶解性的影响,拓展学生知识视野。
2. 分子极性与分子间作用力:探讨分子极性对分子间作用力的影响,加深学生对分子极性的理解。
第三节分子的性质第1课时键的极性和分子的极性范德华力和氢键学业要求素养对接1.知道分子极性与分子中键的极性、分子的空间结构密切相关。
2.能说明分子间作用力(含氢键)对物质熔、沸点等性质的影响。
3.能列举含有氢键的物质及其性质特点。
微观探析:键的极性和分子的极性。
模型认知:运用分子间作用力(含氢键)理论模型解释物质的性质。
[知识梳理]一、键的极性和分子的极性1.键的极性2.分子的极性3.键的极性和分子极性的关系(1)只含非极性键的分子一般是非极性分子。
(2)含有极性键的分子有没有极性,必须依据分子中极性键的极性的向量和是否等于零而定,等于零时是非极性分子。
【自主思考】1.乙烯分子中共价键极性如何?乙烯是极性分子还是非极性分子?提示乙烯分子中C—H是极性共价键,C===C是非极性共价键,乙烯分子空间对称,是非极性分子。
二、范德华力及其对物质性质的影响1.概念分子之间普遍存在的相互作用力。
2.特征范德华力很弱,约比化学键的键能小1~2数量级。
3.影响因素(1)组成和结构相似的物质,相对分子质量越大,范德华力越大。
(2)分子的极性越大,范德华力越大。
4.对物质性质的影响范德华力主要影响物质的物理性质,如熔、沸点。
范德华力越大,物质的熔、沸点越高。
【自主思考】2.Cl2、Br2、I2三者的组成和化学性质均相似,但状态却为气、液、固的原因是什么?提示Cl2、Br2、I2的组成和结构相似,由于相对分子质量逐渐增大,所以范德华力逐渐增大,故熔、沸点升高,状态由气体变为液体、固体。
三、氢键及其对物质性质的影响1.概念已经与电负性很大的原子(如N、F、O)形成共价键的氢原子与另一个分子电负性很大的原子之间的作用力。
2.表示方法氢键通常用A—H…B—表示,其中A、B为N、O、F,“—”表示共价键,“…”表示形成的氢键。
3.分类氢键可分为分子内氢键和分子间氢键两类。
存在分子内氢键,存在分子间氢键。
前者的沸点低于后者。
4.特征氢键不属于化学键,属于一种较弱的作用力,比化学键弱,但比范德华力强。
分子概述 如果分子的构型不对称,则分子为极性分子。
如:氨气分子,HCl分子等。
区分极性分子和非极性分子的方法: 非极性分子的判据:中心原子化合价法和受力分析法1、中心原子化合价法: 组成为ABn型化合物,若中心原子A的化合价等于族的序数,则该化合物为非极性分子.如:CH4,CCl4,SO3,PCl52、受力分析法: 若已知键角(或空间结构),可进行受力分析,合力为0者为非极性分子.如:CO2,C2H4,BF33、非极性分子: 同种原子组成的双原子分子都是非极性分子。
不是非极性分子的就是极性分子了! 高中阶段知道以下的就够了: 极性分子:HX,CO,NO,H2O,H2S,NO2,SO2,SCl2,NH3,H2O2,CH3Cl,CH2Cl2,CHCl3,CH3CH2OH 非极性分子:Cl2,H2,O2,N2,CO2,CS2,BF3,P4,C2H2,SO3,CH4,CCl4,SiF4,C2H4,C6H6,PCl5,汽油 简单判断方法 对于AnBm型 n=1 m>1 若A化合价等于主族数 则为非极性有机极性判断弱极矩μ 有机化合作大多难溶于水,易溶于汽油、苯、酒精等有机溶剂。
原因何在?中学课本、大学课本均对此进行了解释。
尽管措词不同,但中心内容不外乎是:有机化 合物一般是非极性或弱极性的,它们难溶于极性较强的水,易溶于非极性的汽油或弱极性的酒精等有机溶剂。
汽油的极性在课本中均未做详细说明,故而在教学中常 常做如下解释:所有的烷烃,由于其中的O键的极性极小,以及结构是对称的,所以其分子的偶极矩为零,它是一非极性分子。
烷烃易溶于非极性溶剂,如碳氢化合 物、四氯化碳等。
以烷烃为主要成分的汽油也就不具有极性了。
确切而言,上述说法是不够严格的。
我们知道,分子的极性(永久烷极)是由其中正、负电荷的“重心”是否重合所引起的。
根据其分子在空间是否绝对对称来判定极性,化学键极性的向量和——弱极 矩μ则是其极性大小的客观标度.分析1 常见烷烃中,CH4、C2H6分子无极性,C3H8是 折线型分子,键的极性不能相互完全抵消,其μ≠为0.084D。
高中化学:分子极性
一、分类:按照分子的极性,可把分子分为两类。
1、非极性分子:正负电荷重心重合,分子对外不显示电负性的分子。
例如:
等。
疏水分子是指不溶于水的分子。
非极性分子是指原子间以共价键结合,分子里电荷分布均匀,正负电荷中心重合的分子。
水分子是极性分子,根据相似相溶原理,非极性分子很难溶于水。
但疏水分子也可能是极性很大的分子,例如各类脂肪酸,所以疏水分子不一定是非极性分子!
2、极性分子:正负电荷重心不重合,分子对外显示电负性的分子。
例如
HCl、H
2O
2等。
二、掌握常见分子极性及其空间构型:常见分子极性及其空间构型可用下表表示。
三、了解常见分子空间构型及其键角:中学常见分子空间构型及其键角列举如下:(1)等双原子单质分子为直线形,夹角为180°。
(2)为平面形,夹角为104.5°。
(3)为三角锥形,夹角为107°18”。
(4)S为平面形,夹角为92°。
(5)为正四面体形,夹角为109°28”。
(6)为四面体形,夹角不确定。
(7)为直线形,夹角为180°。
(8)为平面形,夹角为120°。
(9)为平面形,夹角为60°。
(10)为正四面体形,夹角为109°28”。
(11)为直线形,夹角为180°。
(12)为平面形,夹角为120°。
②③④⑤
注意:中学常见的四面体物质有①CH
4
⑥⑦⑧⑨等。
其中是正四面体的有①、⑤、⑥、
⑦、⑧、⑨共6种。
四、分子极性判断规律。
①双原子单质分子都是非极性分子。
如等。
②双原子化合物分子都是极性分子。
如HCl、HBr、HI等。
③多原子分子极性要看空间构型是否对称,对称的是非极性分子,否则是极性分
O、等是极性分子;
子。
如H
2
等是非极性分子。
④形分子极性判断:若A原子的最外层电子全部参与成键,这种分子一般为非极性分子。
如等。
若A原子的最外层电子没有全部参与成键,这种分子一般为极性分子。
如等。