高中化学 课时分层作业12 分子的极性与手性分子(含解析)苏教版选修3
- 格式:doc
- 大小:125.50 KB
- 文档页数:6




4.1.3 分子的极性和手性分子A组1.下列叙述正确的是()A.含有非极性键的分子一定是非极性分子B.非极性分子中一定含有非极性键C.由极性键形成的双原子分子一定是极性分子D.键的极性与分子的极性有关答案:C解析:分子的极性与分子的空间结构有关,分子结构对称,正负电荷重心重合的分子为非极性分子,否则为极性分子,与分子中含有极性键或非极性键(键的极性)无关,故A、B、D错误;C选项,由极性键形成双原子分子,正负电荷重心不重合,一定是极性分子,正确。
故选C。
2.下列化合物中,化学键的类型和分子的极性(极性或非极性)皆相同的是()A.CO2和SO2B.CH4和PH3C.BF3和NH3D.HCl和HI答案:D3.根据物质溶解性“相似相溶”的一般规律,能说明碘、溴单质在CCl4中比在水中溶解度大的是() A.溴、碘单质和CCl4中都含有卤素B.溴、碘是单质,CCl4是化合物C.Br2、I2是非极性分子,CCl4也是非极性分子,而水为极性分子D.以上说法都不对答案:C解析:根据相似相溶规则,溶质和溶剂极性相同的分子,溶解度大,极性不同,溶解度小。
4.下列分子中,不含手性碳原子的是()答案:B5.X、Y为两种不同元素,由它们组成的下列物质的分子中,肯定有极性的是() A.XY4B.XY3C.XY2D.XY答案:D解析:当分子为对称结构时,正负电荷重心重合,分子为非极性,当XY4为正四面体,XY3为平面三角形,XY2为直线形时,分子没有极性;XY为不同原子构成的双原子分子,正负电荷重心不重合,肯定为极性分子。
故选D。
6.下列叙述正确的是()A.NH3是极性分子,分子中氮原子处在3个氢原子所组成的三角形的中心B.CCl4是非极性分子,分子中碳原子处在4个氯原子所组成的正方形的中心C.H2O是极性分子,分子中氧原子不处在2个氢原子所连成的直线的中央D.CO2是非极性分子,分子中碳原子不处在2个氧原子所连成的直线的中央答案:C7.经验规律(“相似相溶规则”):一般来说,由极性分子组成的溶质易溶于极性分子组成的溶剂,非极性分子组成的溶质易溶于非极性分子组成的溶剂。

第2课时分子的极性与手性分子目标与素养:1.初步认识分子的极性、手性分子等概念。
(微观探析)2.认识分子的空间构型与分子极性的关系。
(宏观辨识)一、分子的极性1.极性分子与非极性分子(1)极性分子:正电荷重心和负电荷重心不相重合的分子。
(2)非极性分子:正电荷重心和负电荷重心相重合的分子。
2.分子极性的判断方法分子的极性是由分子中所含共价键的极性与分子的空间构型两方面共同决定的。
判断分子极性时,可根据以下原则进行:(1)只含有非极性键的双原子分子或多原子分子大多是非极性分子,如O2、H2、P4、C60。
(2)含有极性键的双原子分子都是极性分子,如HCl、HF、HBr。
(3)含有极性键的多原子分子,空间结构中心对称的是非极性分子;空间结构中心不对称的是极性分子。
3.分子的极性对物质溶解性的影响——相似相溶规则非极性分子构成的物质一般易溶于非极性溶剂,极性分子构成的物质一般易溶于极性溶剂。
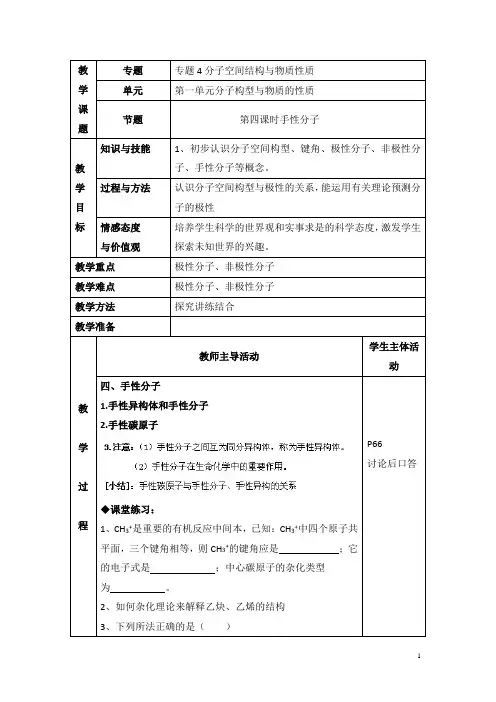
二、手性分子1.观察比较下图所示两种分子的结构(1)相同点是分子组成相同、都是CHFClBr,从平面上看相似。
(2)不同点是在空间上不同,它们构成实物和镜像关系。
(3)具有完全相同的组成和原子排列的一对分子,如同左手与右手一样互为镜像,却在三维空间里不能重叠,互称为手性异构体。
有手性异构体的分子叫做手性分子。
2.手性分子的判断判断一种有机物是否具有手性异构体,关键是看其含有的碳原子是否连有4个不同的原子或基团,即有机物分子中是否存在手性碳原子,如,R1、R2、R3、R4互不相同,含有手性碳原子,该有机物分子具有手性。
3.手性分子的重要用途由于手性分子对生命及生理活动有其特殊的活性,化学工作者期望可以找到对癌症和一些目前的疑难杂症有治疗作用的手性药品;同时也期望早日实现“手性分子”的合成和分离的工业化;期望能制造出可以利用的“手性分子”作为高分子聚合物的单体,用以合成易降解的高分子化合物,减少环境污染。
(1)手性异构体(又称对映异构体、光学异构体)的两个分子互为镜像关系,即分子形式的“左撇子和右撇子”。
[课后练习]一、选择题1.分子有极性分子和非极性分子之分。
下列对极性分子和非极性分子的认识正确的是()A.只含非极性键的分子一定是非极性分子B.含有极性键的分子一定是极性分子C.非极性分子一定含有非极性键D.极性分子一定含有极性键2.把下列液体分别装在酸式滴定管中,并使其以细流流下,当用带有静电的玻璃棒接近液体细流时,细流可能发生偏转的是()l4B. C2H5OHC.CS2D.CH2Cl23.以极性键结合的多原子分子,分子是否有极性取决于分子的空间构型。
下列分子属极性分子的是()A. H2OB.CO2C.BCl3D. NH34.(06年全国卷II)下列叙述正确的是()A. NH3是极性分子,分子中N原子处在3个H原子所组成的三角形的中心B. CCl4是非极性分子,分子中C原子处在4个Cl原子所组成的正方形的中心C. H2O是极性分子,分子中O原子不处在2个H原子所连成的直线的中央D. CO2是非极性分子,分子中C原子不处在2个O原子所连成的直线的中央5.SiCl4的分子结构与CCl4类似,对其做出如下推断:①SiCl4晶体是分子晶体;②常温常压SiCl4不是气体;③SiCl4分子是由极性键构成的非极性分子;④SiCl4熔点高于CCl4。
其中正确的是()A.只有①B.只有①②C.只有②③D.①②③④6.下列关于天然气水合物中两种分子极性的描述正确的是()A 两种都是极性分子B 两种都是非极性分子C CH4是极性分子,H2O是非极性分子D H2O是极性分子,CH4是非极性分子7.根据“相似相溶”的规律,下列溶剂可以用来从溴水中萃取溴的是()(1)酒精(2) CCl4(3)液氨(4)苯(5)直馏汽油A.(1)(2)(4)(5)B.(2)(4)(5)C.(1)(3)(5)D.(1)(3)(4)8.下列现象不能用“相似相溶”规律解释的是()A.氯化氢易溶于水B.氯气易溶于NaOH溶液C.碘易溶于CCl4 D.碘难溶于水9.NH3、H2S等是极性分子,CO2、BF3、CCl4等是极性键构成的非极性分子。


课时分层作业(十二)(建议用时:40分钟)[基础达标练]1.下列分子中,属于极性分子的是( )A.CO2B.BeCl2C.BBr3D.COCl2D2.下列比较正确的是( )A.熔沸点:C(CH3)4>CH3(CH2)3CH3B.熔沸点:H2S>H2OC.I2的溶解度:水>苯D.因为CS2为非极性分子,故硫易溶于CS2中D [A项中两分子互为同分异构体,C(CH3)4为非极性分子,CH3(CH2)3CH3为极性分子,故熔沸点应为C(CH3)4<CH3(CH2)3CH3。
B项H2O分子间存在氢键,熔沸点应为H2O>H2S。
C项中I2在苯中的溶解度大于在水中的溶解度。
]3.下列粒子中不存在非极性键的是( )A.C2H4B.H2O2C.NH+4D.C2H5OHC4.下列分子中,属于含有极性键的非极性分子的是( )A.H2O B.Cl2C.NH3D.CCl4D [H2O分子中O—H键为极性键,整个分子的电荷分布不对称,是极性分子。
Cl2是双原子单质分子,属于含非极性键的非极性分子。
NH3分子中N—H键是极性键,分子构型是三角锥型,电荷分布不对称,是极性分子。
CCl4分子中C—Cl键是极性键,分子构型呈正四面体型,电荷分布对称,是非极性分子。
]5.实验测得BeCl2为共价化合物,两个Be—Cl键间的夹角为180°,则BeCl2属于 ( ) A.由极性键构成的极性分子B.由极性键构成的非极性分子C.由非极性键构成的极性分子D.由非极性键构成的非极性分子B [Be—Cl键由不同元素的原子形成,两种原子吸引电子能力不同,为极性键。
由于两个Be—Cl键间的夹角为180°,分子空间构型为直线形,分子内正负电荷重心重合,共价键的极性抵消,分子没有极性。
由此可见,BeCl2属于由极性键构成的非极性分子。
]6.膦(PH3)又称磷化氢,在常温下是一种无色有大蒜臭味的有毒气体,电石气的杂质中常含有磷化氢。


[课后练习]一、选择题1.下列说法中不正确的是()A.共价化合物中不可能含有离子键B.有共价键的化合物,不一定是共价化合物C.离子化合物中可能存在共价键D.原子以极性键结合的分子,肯定是极性分子2.下列四种分子中,只含极性键而没有非极性键的是()A.CH4B.CH3CH3C.CH2=CH2D.CH≡CH3.下列分子中,属于含有极性键的非极性分子的一组是()A.CH4、CCl4、CO2B.C2H4、C2H2、C6H6C.Cl2、H2、N2D.NH3、H2O、SO24.下列现象不能用“相似相溶”规律解释的是()A.氯化氢易溶于水B.氯气易溶于NaOH溶液C.碘易溶于CCl4 D.碘难溶于水5.下列物质易溶于苯的是()A.NH3 B.HF C.I2D.Br26.下列分子中,属于含有极性键的非极性分子的一组是()A.CH4、CCl4、CO2B.C2H4、C2H2、C6H6C.Cl2、H2、N2D.NH3、H2O、SO27.瑞典皇家科学院2001年10月10日宣布,2001年诺贝尔化学奖授予“手性碳原子的催化氢化、氧化反应”研究领域作出贡献的美、日三位科学家。
下列分子中含有“手性碳原子”的是()A.CBr2F2B.CH3CH2OH C.CH3CH2CH3D.CH3CH(OH)COOH 8.下列有机物分子中带“*”碳原子就是手性碳原子。
该有机物分别发生下列反应,生成的有机物分子中含有手性碳原子的是()A.与乙酸发生酯化反应 B.与NaOH水溶液反应C.与银氨溶液作用只发生银镜反应D.催化剂作用下与H2反应9.已知氯化铝易溶于苯和乙醚,其熔点为190℃,则下列结论错误的是()A.氯化铝是电解质B.固体氯化铝是分子晶体C.可用电解熔融氯化铝的办法制取金属铝D.氯化铝为非极性分子10.根据“相似相溶”的规律,下列溶剂可以用来从溴水中萃取溴的是()(1)酒精(2) CCl4(3)液氨(4)苯(5)直馏汽油A.(1)(2)(4)(5)B.(2)(4)(5)C.(1)(3)(5)D.(1)( 3)(4)11.根据“相似相溶”规律,你认为下列物质在水中溶解度较大的是()A .乙烯B .二氧化碳 C.二氧化硫 D.氢气二、填空题12.我们可把共价键按分为极性键和非极性键,而共价键产生极性的根本原因是,故此有人这样判断键的极性:凡是同种元素原子间形成的共价键属极性键,凡是异种元素原子间形成的共价键属非极性键。
课时分层作业(15)分子的极性和手性分子1.已知带静电的有机玻璃棒靠近纯水的细流,水流方向发生改变,则用带静电的有机玻璃棒靠近下列物质的细流时,细流方向也发生偏转的是() A.苯B.二硫化碳C.过氧化氢D.四氯化碳C[苯的空间结构对称,为非极性分子,电荷分布均匀,用带静电的有机玻璃棒靠近苯的细流时,细流的方向不发生偏转,故A错误;二硫化碳的空间结构对称,为非极性分子,电荷分布均匀,用带静电的有机玻璃棒靠近二硫化碳的细流时,细流的方向不发生偏转,故B错误;过氧化氢的空间结构不对称,为极性分子,电荷分布不均匀,用带静电的有机玻璃棒靠近过氧化氢的细流时,细流的方向会发生偏转,故C正确;四氯化碳分子的空间结构对称,为非极性分子,电荷分布均匀,用带静电的有机玻璃棒靠近四氯化碳的细流时,细流的方向不发生偏转,故D错误。
]2.在半导体生产或灭火剂的使用中,会向空气中逸散气体,如:NF3、CHClFCF3、CF4等。
它们虽然是微量的,有些却是强温室气体。
下列推测不正确的是()A.NF3分子呈三角锥形B.CF4在CCl4中溶解度比在水中的大C.CHClFCF3存在手性碳原子D.CHClFCF3中没有非极性键D[NH3分子中价层电子对个数=3+12(5-3×1)=4,所以氮原子杂化方式为sp3,含有1对孤电子对,为三角锥形,NF3分子结构与氨气分子相似,所以NF3分子呈三角锥形,故A正确;有机物一般难溶于水,易溶于有机物,CF4、CCl4均属于有机物,所以CF4在有机物CCl4中溶解度比在水中的大,故B正确;碳原子连有4个不同的基团,则具有手性,则CHClFCF3存在手性碳原子,故C 正确;根据原子成键规律,CHClFCF3分子中存在碳碳非极性共价键,故D错误。
]3.下列叙述中,不正确的是()A.HF、HCl、HBr、HI的稳定性依次增强B.臭氧是空间结构为V形的极性分子,在水中的溶解度大于氧气C.硝酸根离子中所有原子都在一个平面上D.CH2OHCH(OH)CHO为手性分子A[同主族元素从上到下,非金属性逐渐减弱,非金属性:F>Cl>Br>I,故HF、HCl、HBr、HI的稳定性依次减弱,A项错误;臭氧是空间结构为V形的极性分子,氧气是非极性分子,水是极性分子,根据“相似相溶规则”可知,臭氧在水中的溶解度大于氧气,B项正确;硝酸根离子中,中心原子是氮原子,价电子对数为5+1+0×32=3,没有孤电子对,空间结构为平面三角形,所有原子都在一个平面上,C项正确;碳原子连接四个不同的原子或原子团时,该碳原子为手性碳原子,CH2OHCH(OH)CHO中有一个手性碳原子,属于手性分子,D 项正确。
第三课时 分子的极性 手性分子[学习目标] 1.初步认识分子的极性、手性分子等概念。
2.认识分子的空间构型与分子极性的关系。
自主学习区一、分子的极性 1.极性分子和非极性分子2.键的极性和分子极性的关系双原子分子的极性取决于□03成键原子之间的共价键是否有极性,以□04极性键结合的双原子分子是极性分子,如HCl 、CO 、NO 等;以□05非极性键结合的双原子分子是非极性分子,如H 2、O 2、N 2等。
同种原子形成的双原子分子都是□06非极性分子。
以极性键结合的多原子分子(AB m ,A 为中心原子,B 为配位原子),分子是否有极性取决于□07分子的空间构型。
如CO 2、BF 3、CH 4等分子,虽然分子中的共价键都是极性键,但由于配位原子对称地分布在中心原子周围,整个分子的正、负电荷重心□08相重合,所以这些分子都是□09非极性分子。
二、相似相溶规则一般情况下,由极性分子构成的物质易溶于□01极性溶剂,由非极性分子构成的物质易溶于□02非极性溶剂。
三、手性分子 1.手性异构体具有完全相同的□01组成和□02原子排列方式的一对分子,如同左手和右手一样互为□03镜像,却在三维空间里□04不能重叠,互称手性异构体。
2.手性分子有□05手性异构体的分子叫做手性分子。
3.手性碳原子连接□06四个不同的原子或基团的碳原子称为手性碳原子。
1.如何判断多原子分子的极性?提示:多原子分子,如果为单质,为非极性分子;如果为化合物,则看分子的空间构型,若整个分子正负电荷重心重合则为非极性分子,若整个分子正负电荷重心不重合则为极性分子。
2.CH 4、CH 3Cl 、CCl 4分别是极性分子还是非极性分子? 提示:CH 4和CCl 4为非极性分子,CH 3Cl 为极性分子。
3.互为手性异构的两个分子是同一种分子吗?提示:不是。
虽然互为手性异构的两个分子有极大的相似性,但两个分子不能重合,即结构不完全相同,不属于同种分子。
课时分层作业(十二)(建议用时:40分钟)[基础达标练]1.下列分子中,属于极性分子的是( )A.CO2B.BeCl2C.BBr3D.COCl2D2.下列比较正确的是( )A.熔沸点:C(CH3)4>CH3(CH2)3CH3B.熔沸点:H2S>H2OC.I2的溶解度:水>苯D.因为CS2为非极性分子,故硫易溶于CS2中D [A项中两分子互为同分异构体,C(CH3)4为非极性分子,CH3(CH2)3CH3为极性分子,故熔沸点应为C(CH3)4<CH3(CH2)3CH3。
B项H2O分子间存在氢键,熔沸点应为H2O>H2S。
C项中I2在苯中的溶解度大于在水中的溶解度。
]3.下列粒子中不存在非极性键的是( )A.C2H4B.H2O2C.NH+4D.C2H5OHC4.下列分子中,属于含有极性键的非极性分子的是( )A.H2O B.Cl2C.NH3D.CCl4D [H2O分子中O—H键为极性键,整个分子的电荷分布不对称,是极性分子。
Cl2是双原子单质分子,属于含非极性键的非极性分子。
NH3分子中N—H键是极性键,分子构型是三角锥型,电荷分布不对称,是极性分子。
CCl4分子中C—Cl键是极性键,分子构型呈正四面体型,电荷分布对称,是非极性分子。
]5.实验测得BeCl2为共价化合物,两个Be—Cl键间的夹角为180°,则BeCl2属于 ( ) A.由极性键构成的极性分子B.由极性键构成的非极性分子C.由非极性键构成的极性分子D.由非极性键构成的非极性分子B [Be—Cl键由不同元素的原子形成,两种原子吸引电子能力不同,为极性键。
由于两个Be—Cl键间的夹角为180°,分子空间构型为直线形,分子内正负电荷重心重合,共价键的极性抵消,分子没有极性。
由此可见,BeCl2属于由极性键构成的非极性分子。
]6.膦(PH3)又称磷化氢,在常温下是一种无色有大蒜臭味的有毒气体,电石气的杂质中常含有磷化氢。
以下关于PH3的叙述不正确的是( )A.PH3分子中有未成键的孤电子对B.PH3是极性分子C.它的分子构型是平面三角形D.磷原子采用sp3杂化方式C [PH3分子中含有3个σ键和一个孤电子对,故杂化轨道的数目为4,采取sp3杂化方式,分子构型为三角锥型,与NH3相似。
]7.微波炉加热时,电炉内的微波场以极高的频率改变电场的方向,使水分子迅速摆动而产生热效应。
在高频改变方向的电场中水分子会迅速摆动的原因是( )A.水分子具有极性共价键B.水分子中有共用电子对C.水由氢、氧两元素的原子组成D.水分子是极性分子D [水分子在不断改变方向的电场中迅速摆动,说明水分子显示电性作用,其根本原因是水分子属于极性分子。
]8.(双选)下列描述中正确的是 ( )A.CS2为V形的极性分子B.ClO-3的空间构型为平面三角形C.SF6中有6对完全相同的成键电子对D.SiF4和SO2-3的中心原子均为sp3杂化CD [依据价层电子对互斥理论可知,CS2为直线形的非极性分子,A错误;由价层电子对互斥理论可知,ClO-3的中心原子的孤电子对数是1/2×(8-3×2)=1,所以ClO-3是三角锥型,B错误;硫原子最外层有6个电子,和氟原子之间有6个完全相同的成键电子对,C正确;SiF4和SO2-3的空间构型分别为正四面体型和三角锥型,但中心原子均采用的是sp3杂化,D正确。
] 9.下列说法正确的是( )A.HOCH2CH(OH)CH2OH与CH3CHClCH2CH3都是手性分子B.NH+4和CH4的空间构型相似C.BF3与都是平面三角形分子D.CO2和H2O都是直线形分子B [手性分子是化学中结构上镜像对称而又不能完全重合的分子,连有四个不同原子或基团的碳原子称为手性碳原子,HOCH2CH(OH)CH2OH不是手性分子,A项错误;NH+4和CH4的空间构型都是正四面体型,B项正确;BF3是平面三角形,苯是平面结构,C项错误;CO2是直线形分子,而H2O是V形分子,D项错误。
]10.下列有机物中含有两个手性碳原子的是( )B [由有机物的结构可以看出,A、C、D三项中没有手性碳原子;B项中每个与氯原子相连的碳原子都是手性碳原子。
]11.(1)CrO2Cl2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断CrO2Cl2是________(填“极性”或“非极性”)分子。
(2)在①苯、②CH3OH、③HCHO、④CS2、⑤CCl4五种有机溶剂中,碳原子采取sp2杂化的分子有________(填序号),CS2分子的空间构型是________。
CO2与CS2相比,________的熔点较高。
[解析](1)CCl4、CS2是非极性溶剂,根据相似相溶原理,CrO2Cl2是非极性分子。
(2)苯、CH3OH、HCHO、CS2、CCl4分子中碳原子的杂化方式分别是sp2、sp3、sp2、sp、sp3。
CS2、CO2分子的空间构型都是直线形,其结构相似,所以相对分子质量越大,范德华力越大,熔点越高。
[答案](1)非极性(2)①③直线形CS212.3氯2丁氨酸的结构简式为:一个3氯2丁氨酸分子中含有________个手性碳原子。
其中一对对映异构体用简单的投影式表示为:则另一对对映异构体的简单投影式为和________。
[解析]根据手性碳原子周围连接四个不同的原子或基团这一规律可以判断该物质的手性碳原子个数;参照例子可以知道对映体关系就像我们照镜子一样,其另一种就是该种在镜子中的“镜像”。
[答案] 2[能力提升练]13.毒奶粉事件仍时有发生,这主要是奶粉中含有有毒的三聚氰胺()。
下列关于三聚氰胺分子的说法中正确的是( )A.所有氮原子均采取sp3杂化B.一个三聚氰胺分子中共含有15个σ键C.属于极性分子,故极易溶于水D.三聚氰胺分子中同时含有极性键和非极性键B [三聚氰胺分子中,处于环上的氮原子采取sp2杂化,A选项错误;由三聚氰胺分子的结构知,它是对称结构,为非极性分子,而水为极性溶剂,故三聚氰胺在水中的溶解度不大,C选项错误;三聚氰胺分子中不存在由同种元素的原子形成的共价键,故不存在非极性键,D 选项错误。
]14.中所含的手性碳原子数为( )A.1个B.2个C.3个D.4个B [手性碳原子是指所连的四个原子或基团均不相同的碳原子,据此可知分子中标有“*”的碳原子为手性碳原子:。
]15.在HF、H2O、NH3、CS2、CH4、N2中:(1)以非极性键结合的非极性分子是____________________;(2)以极性键相结合,具有直线形结构的非极性分子是________;(3)以极性键相结合,具有三角锥型结构的极性分子是________;(4)以极性键相结合,具有四面体形结构的非极性分子是________;(5)以极性键相结合,具有V形结构的极性分子是________;(6)以极性键相结合,而且分子极性最大的是______________________。
[解析]该题要求判断键的极性、分子的空间构型与分子的极性之间的关系,实质是要掌握分析分子极性的正确思路或方法,简言之,就是要明确常见分子的空间构型及其对称性。
另外,分子极性强弱与成键原子的电负性有关,HF分子中元素的电负性相差最大,所以键的极性最强,则HF分子的极性也最大。
[答案](1)N2(2)CS2(3)NH3(4)CH4(5)H2O (6)HF16.试用有关知识解释下列现象。
(1)有机物大多难溶于水,而乙醇与乙酸可与水互溶:________________________________________________________________________________________________________________。
(2)乙醚(C2H5OC2H5)的相对分子质量远大于乙醇,但乙醇的沸点却比乙醚的高很多,原因是__________________________________。
(3)从氨合成塔里H2、N2、NH3的混合物中分离出NH3,常采用加压使NH3液化的方法:___________________________________________________________________________________________。
(4)水在常温下,其组成的化学式可用(H2O)m表示:______________________________________________________________________________________________________________________________________________________________________。
[答案](1)乙醇分子中的醇羟基、乙酸分子中的羧羟基均可与水形成分子间氢键,相互结合成缔合分子,故表现为互溶(2)乙醇分子之间形成的氢键作用远大于乙醚分子间的范德华力,故乙醇的沸点比乙醚的高很多(3)NH3分子间可以形成氢键,而N2、H2的分子间作用力很小,故可采用加压液化的方法从混合物中分离NH3(4)常温下,液态水中水分子间通过氢键缔合成较大分子团,而不是以单个分子形式存在,所以可用(H2O)m表示。