紫外–可见吸收光谱原理
- 格式:docx
- 大小:36.52 KB
- 文档页数:1
紫外吸收光谱分析一概述紫外可见吸收光谱法是利用某些物质的分子吸收10~800nm光谱区的辐射来进行分析测定的方法,这种分子吸收光谱产生于价电子和分子轨道上的电子在电子能级间的跃迁,广泛用于有机和无机物质的定性和定量测定。
该方法具有灵敏度高、准确度好、选择性优操作简便、分析速度好等特点。
分子的紫外可见吸收光谱法是基于分子内电子跃迁产生的吸收光谱进行分析的一种常用的光谱分析法。
分子在紫外-可见区的吸收与其电子结构紧密相关。
紫外光谱的研究对象大多是具有共轭双键结构的分子。
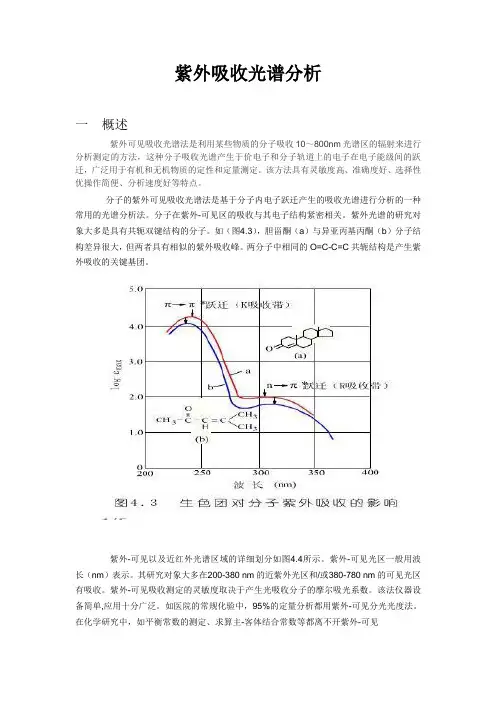
如(图4.3),胆甾酮(a)与异亚丙基丙酮(b)分子结构差异很大,但两者具有相似的紫外吸收峰。
两分子中相同的O=C-C=C共轭结构是产生紫外吸收的关键基团。
紫外-可见以及近红外光谱区域的详细划分如图4.4所示。
紫外-可见光区一般用波长(nm)表示。
其研究对象大多在200-380 nm的近紫外光区和/或380-780 nm的可见光区有吸收。
紫外-可见吸收测定的灵敏度取决于产生光吸收分子的摩尔吸光系数。
该法仪器设备简单,应用十分广泛。
如医院的常规化验中,95%的定量分析都用紫外-可见分光光度法。
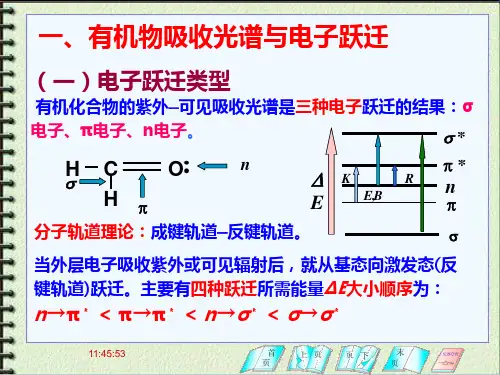
在化学研究中,如平衡常数的测定、求算主-客体结合常数等都离不开紫外-可见二基本原理紫外可见吸收光谱的基本原理是利用在光的照射下待测样品内部的电子跃迁,电子跃迁类型有:(1)σ→σ* 跃迁指处于成键轨道上的σ电子吸收光子后被激发跃迁到σ*反键轨道(2)n→σ* 跃迁指分子中处于非键轨道上的n电子吸收能量后向σ*反键轨道的跃迁(3)π→π* 跃迁指不饱和键中的π电子吸收光波能量后跃迁到π*反键轨道。
(4)n→π* 跃迁指分子中处于非键轨道上的n电子吸收能量后向π*反键轨道的跃迁。
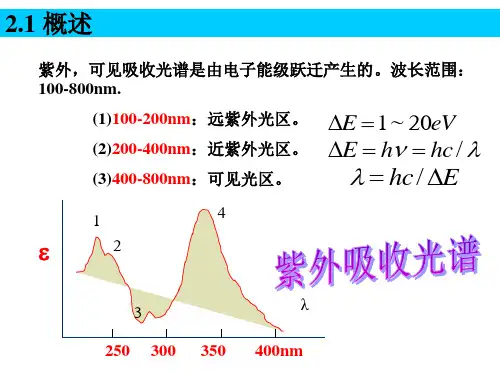
电子跃迁类型不同,实际跃迁需要的能量不同:σ→σ* ~150nmn→σ* ~200nmπ→π* ~200nmn→π* ~300nm吸收能量的次序为:σ→σ*>n→σ*≥π→π*>n→π*特殊的结构就会有特殊的电子跃迁,对应着不同的能量(波长),反反映在紫外可见吸收光谱图上就有一定位置一定强度的吸收峰,根据吸收峰的位置和强度就可以推知待测样品的结构信息三特点1、紫外可见吸收光谱所对应的电磁波长较短,能量大,它反映了分子中价电子能级跃迁情况。






紫外–可见吸收光谱原理
紫外-可见吸收光谱是一种常用的光谱分析技术,用于分析物
质的化学结构和浓度。
它基于物质对紫外-可见光的吸收特性。
紫外-可见光谱是通过将被测物质溶解在适当的溶剂中,然后
用一束紫外-可见光照射样品,并测量样品对光的吸收来进行的。
紫外-可见吸收光谱的原理基于被测物质分子电子的激发和跃迁。
当物质处于基态时,其分子处于低能级的电子轨道上。
当紫外-可见光照射被测物质时,光子的能量能够被物质中的电
子吸收,使其跃迁到高能级的轨道上。
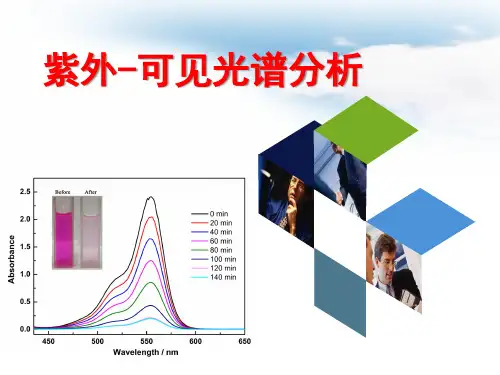
这种电子跃迁导致了紫外-可见光谱的吸收峰。
每种物质都有其特定的吸收特性,这是由其分子结构和化学键决定的。
不同的分子或化学键对不同波长的光具有不同的吸收能力。
通过测量光通过样品后的强度变化,可以得到吸收光谱。
紫外-可见吸收光谱通常以波长(nm)为单位进行测量。
在可
见光范围内,波长较长的光产生红色的吸收峰,而波长较短的光产生紫色的吸收峰。
在紫外光范围内,波长较长的光产生较低能级的吸收峰,而波长较短的光产生较高能级的吸收峰。
通过分析样品吸收光谱的形状和位置,可以确定样品中的物质种类和浓度。
此外,紫外-可见吸收光谱还可以用于分析反应
动力学、鉴定物质和定量测量等应用。