紫外可见光吸收光谱共56页
- 格式:ppt
- 大小:9.05 MB
- 文档页数:56


紫外和可见光吸收光谱1.紫外光谱及其产生⑴紫外光的波长范围紫外光的波长范围为4-400nm。
200-400为近紫外区,4-200nm为远紫外区。
由于波长很短的紫外光会被空气中氧和二氧化碳吸收,研究远紫外区的吸收光谱很困难,一般的紫外光谱仅仅是用来研究近紫外区的吸收。
⑵紫外光谱当把一束光通过有机化合物时,某一波长的光可能吸收很强,而对其他波长的光可能吸收很弱,或者根本不吸收。
当化合物吸收一定波长的紫外光时,电子发生跃迁,所产生的吸收光谱叫做紫外吸收光谱,简称紫外光谱。
⑶电子跃迁的种类在有机化合物分子中,由于化合物的价电子有三种类型,即σ键电子、π键电子和未成键的 n 电子,在电子吸收光谱中,电子跃迁主要是经下三种。
①σ-σ*跃迁σ电子是结合得最牢固的价电子,在基态下,电子在成键轨道中,能级最低,而σ*态是最高能级。
σ-σ*跃迁需要相当高的辐射能量。
在一般情况下,仅在200nm以下约~150nm才能观察到,即在一般紫外光谱仪工作范围之外,只能用真空紫外光谱仪才可观察出来(在无氧和二氧化碳的情况下)。
所以测紫外光谱时,常常用烷烃作溶剂。
② n电子的跃迁n 电子是指象N,S,O,X 等原子上未共用的电子。
它的跃迁有两种方式。
第一种方式:n-π* 跃迁未共用电子激发跃入π*轨道,产生吸收带,称为R带(基团型的,Radikalartig德文),由n-π*引起的,在200 nm以上。
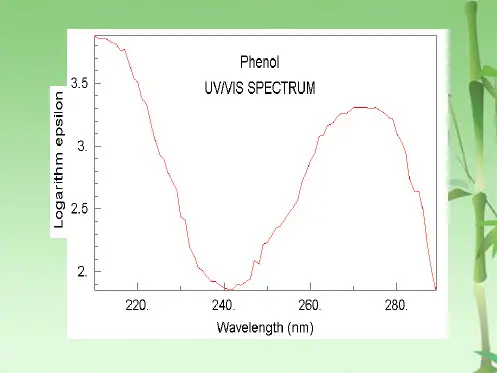
如:醛酮分子中羰基在275-295nm处有吸收带,为C=O中n-π*跃迁吸收带。
第二种方式是n→σ*跃迁,这种跃迁所需的能量大于n-π*,故醇醚均在远紫外区才出现吸收带。
~ 200nm。
如甲醇λmax183nm。
③π→π*跃迁乙烯分子中π电子吸收光能量,跃迁到π*轨道。
吸收带在远紫外区。
当双键上氢逐个被烯基取代后,由于共轭作用,π→π*能级减小。
吸收带向长波递增。
由共轭双键产生的吸收带称为K带,其特征是摩尔消光系数大于104。
在近紫外区吸收,CH2=CH2 λmax162nm,CH2=CH-CH=CH2 λmax217nm。