食品中辣椒素类物质含量测定操作规程
- 格式:docx
- 大小:23.81 KB
- 文档页数:4


中药材干辣椒中辣椒素和二氢辣椒素含量测定方法研究目的对中药材干辣椒中辣椒素和二氢辣椒素的反相高效液相色谱色谱法定量检测方法的优化。
方法采用ThermoC18色谱柱(250mm×4.6mm,5um),流动相为甲醇-水(65:35),流速为1.0mL/min检测波长280nm,柱温40℃。
结果辣椒素及二氢辣椒素在20min内就得到更好的分离和准确的结果,线性范围r=0.9999平均回收率为95.64%。
结论通过对流动相比例改变的检测得到该方法准确,简单,快速、分离效果优。
规避了《中国药典》中流动相甲醇-水(50:50)流动相黏度大,压力高189PA,耗时长(60min)后出峰,具拖尾因子较大,峰型较差,伤柱子。
可作为中药材中辣椒素及二氢辣椒素的含量测定方法。
标签:干辣椒;辣椒素;二氢辣椒素辣椒(Capsicum frutescens L.)属茄科辣椒属,又名海椒、辣子、番椒、辣茄等,为植物辣椒的干燥成熟果实。
收载于《中国药典》2015年版一部中,呈圆锥形、类圆锥形、略弯曲。
表面橙红色、红色或深红色,光滑或较皱缩,显油性。
基部微圆,常有绿棕色、具有5裂齿的宿萼及果柄。
辣椒素及二氢辣椒素属香草胺类生物碱,是辣椒果实中的主要呈辣物质,辛、热,归心、脾经。
温中散寒,开胃消食,用于寒滞腹痛,呕吐,泻痢,冻疮。
为了高效提取辣椒中辣椒素及二氢辣椒素,本研究通过对《中国药典》辣椒中的辣椒素、二氢辣椒素的提取方法和增加甲醇流动相比列进行选择和优化,报道如下。
1 仪器与材料1.1 仪器安捷伦1260高效液相色谱仪(带紫外检测器)、ThermoC18色谱柱(250mm×4.6mm,5um)、BP211D电子分析天平(北京赛多利斯)、电热恒温水浴锅、超声波清洗器,DHG-9101-2A电热恒温干燥箱1.2 材料药材为本地干燥尖辣椒(云南文山州砚山县嫁依镇)对照品辣椒素(批号110839-201205 97.5%中国食品药品检定研究院)二氢辣椒素(批号11166-201303 98.5%中国食品药品检定研究院)试剂甲醇为色谱纯,四氢呋喃为分析纯,水为UP水。
·实验研究·紫外分光光度法测定姜中姜辣素类化合物的含量 贵阳中医学院药学系(550002) 张明昶 李 健 蒙继昭 姜为姜科植物的根状茎,具有温中散寒,驱风止痛等作用。
主要有效成分是姜辣素及挥发油。
因此,可通过测定姜中姜辣素类化合物的含量,鉴定姜及姜制品的品质。
姜辣素的测定方法现有报道均利用酚类测定方法,即将酚类还原铁氰化铁成普鲁士蓝[1]或还原F o 2lin -酚试剂呈蓝色反应(钼蓝和钨蓝混合物)[2]而进行酚类物质含量测定。
此类方法需显色,操作条件比较烦琐,其中反应液引起腾氏兰沉淀可影响比色测定结果的准确性。
本文提出用紫外分光光度法测定姜辣素的含量,克服了上述缺点,方法简单可行。
1 仪器、试剂111 仪器DU -70紫外分光光度计(美国贝克曼公司),TC Q -250超声波清洗器(北京医疗设备二厂)。
112 试剂 分析纯无水乙醇、正丁醇、甲醇等。
2 供试液的制备211 香草醛标准溶液 精密称取香草醛标准品0105g ,用无水乙醇溶解并定容至100ml ,再准确吸取4ml ,用无水乙醇稀释至100ml ,得20μg Πml 香草醛标准溶液。
212 样品供试液 取生姜适量,清洗,切碎,置60℃烘箱内烘干8小时,磨细过80目筛。
精密称取姜粉015g ,置于具塞瓶中,准确加入无水乙醇100ml ,摇匀后精密称重,60℃水超声提取30min ,冷至室温,称重,用无水乙醇补足失重,摇匀过滤,弃去初滤液,收集续滤液密闭备用。
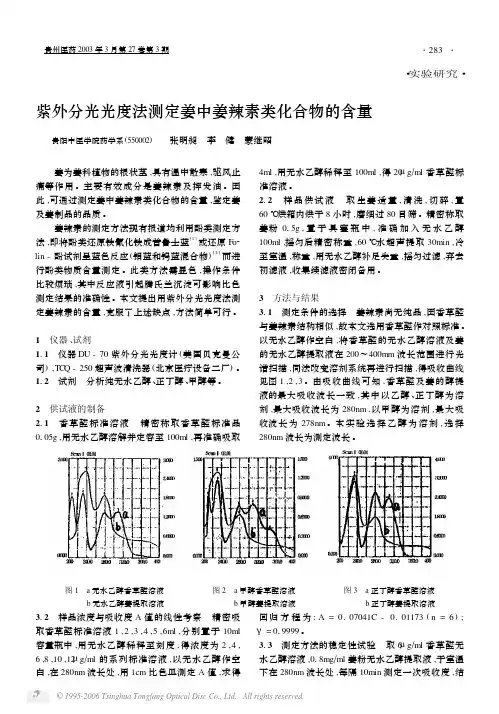
3 方法与结果311 测定条件的选择 姜辣素尚无纯品,因香草醛与姜辣素结构相似,故本文选用香草醛作对照标准。
以无水乙醇作空白,将香草醛的无水乙醇溶液及姜的无水乙醇提取液在200~400mm 波长范围进行光谱扫描,同法改变溶剂系统再进行扫描,得吸收曲线见图1,2,3。
由吸收曲线可知,香草醛及姜的醇提液的最大吸收波长一致,其中以乙醇、正丁醇为溶剂,最大吸收波长为280nm ,以甲醇为溶剂,最大吸收波长为278nm 。

食物中的激素含量测定实验为了保障食品安全以及人们的健康,对食物中激素含量进行准确测定非常重要。
本实验旨在使用适当的方法测定食物中的激素含量,为相关研究提供数据支持。
一、实验材料和仪器1. 实验材料:- 食物样品(例如:肉类、蔬菜等)- 氨基甲酸乙酯- 激素标准品2. 仪器:- 电子天平- 气相色谱仪(GC)- 注射器和样品瓶- 蒸馏瓶二、实验步骤1. 样品准备:- 选择适当数量和种类的食物样品,并将其称量并记录质量。
- 将样品切碎并加入蒸馏瓶中,加入适量的氨基甲酸乙酯,盖上瓶盖,摇匀混合。
- 将混合溶液放置于恒温水浴中,使样品中的激素溶解于溶剂中。
2. 提取激素:- 将提取溶液进行离心处理,以分离出食物残渣和溶液层。
- 使用注射器将溶液层吸取出来,并放入样品瓶中。
3. 准备样品:- 取出一定量的激素标准品。
- 使用注射器分别取出样品和标准品,注入气相色谱仪中进行分析。
4. GC分析:- 将样品和标准品注入气相色谱仪进行分析。
- 通过峰面积或峰高值来计算激素的含量。
5. 数据处理:- 根据GC分析结果,计算食物样品中激素的含量。
- 将测定结果进行统计和图表展示,以便进一步分析。
三、安全措施1. 在实验过程中,注意遵循实验室的安全操作规程,佩戴个人防护装备,如实验手套和眼镜。
2. 使用化学品时,注意正确的操作方法,避免接触皮肤和吸入气体。
3. 使用实验仪器时,遵守使用说明书,确保操作正确和安全。
四、实验结果和讨论通过以上实验步骤,我们可以得到食物样品中激素的准确含量数据。
根据实验结果,可以进一步分析不同食物样品中激素的差异,并对食品安全和健康问题作出评估。
在实验过程中,我们使用了气相色谱仪作为分析工具,它能够对样品中的激素进行有效的分离和定量。
此外,通过合理的样品准备和提取方法,可以确保激素在样品中的溶解和提取效果。
在数据处理方面,我们使用了峰面积或峰高值来计算激素的含量。
这是一种常见且准确的方法,可以通过与标准品进行比较来确定样品中激素的含量。

成绩:江西科技师范大学生物工程综合实训题目:ELISA法测定辣椒粉中的苏丹红Ⅰ含量院(系):生命科学学院班级:09级生物工程1班学生姓名:刘翔学号:20094230指导老师:裘雪梅2012年11月20日ELISA法测定辣椒粉中的苏丹红Ⅰ含量摘要:本实验是采用ELISA方法测定辣椒粉中的苏丹红Ⅰ含量。
实验通过对苏丹红Ⅰ进行修饰,与载体蛋白交联得到免疫抗原和包被抗原并用牛奶封闭,在酶标二抗的连接下加入底物显色液,用2mol/L的H2SO4终止,并测定其OD450值,得到最佳实验结果为:当抗原浓度为2ug/ml,抗体浓度为1:2000时效果最佳。
并用此修饰的苏丹红Ⅰ对样品辣椒粉进行测定其苏丹红Ⅰ含量。
关键词:ELISA;苏丹红Ⅰ;辣椒粉Abstract: This experiment was measured by ELISA Sudan Ⅰcontent in the chili powder.Experimental modified by Sudan Ⅰobtained with a carrier protein cross-linking to the immunizing antigen and envelope antigen and blocked with milk, the chromogenic substrate solution is added to the under HRP resistance connection termination with 2mol/L H2SO4, and measuring OD450values, the best experimental results as follows: When the concentration of antigen 2ug/ml, antibody concentration of 1:2000 when the best results. Sudan Ⅰand modified sample chili powder Determination of Sudan Ⅰcontent.Key Word : ELISA;sudan I;chili powder引言“苏丹红”是一种化学染色剂,并非食品添加剂。

辣椒红⾊素的分离提取及测定辣椒红素综述辣椒辣椒红⾊素⼜名辣红素,是从辣椒中提取的⼀种天然⾊素,属于叶黄素类共轭多烯烃含氧衍⽣物,主要成分为辣椒红素、辣椒⽟红素、⽟⽶黄质⼀胡萝⼘素、隐辣质等,辣椒红⾊素作为从成熟辣椒果⽪中提取的天然红⾊素的主要成分,是⽬前国际上公认的最好的红⾊素。
我国早在“七五”期间就将辣椒红⾊素列为重点开发的4种天然⾊素之⼀。
理化性质:纯品为深红⾊液体,⽆辣味,其显⾊强度强于其他天然⾊素。
辣椒红⾊素不溶于⽔,易溶于⼄醇、酮、油脂等有机溶剂,因其极性较强,在超临界⼆氧化碳中⼏乎不溶解。
具有如下稳定性:1.光对稳定性的影响在室内光线下,稳定性较好,放置4周,⾊素⽆褪⾊现象。
但如直接暴露在室外强光之下则很容易褪⾊。
2.温度对稳定性的影响温度对辣椒红⾊素有⼀定影响。
温度越⾼⾊素损失愈多,加热⾄70℃以上则损失更明显。
3. pH值对稳定性的影响辣椒红⾊素的耐酸、耐碱性好。
pH值在3—12之间时⾊泽稳定不变。
4.⾦属离⼦对稳定性的影响cu、Fe对辣椒红⾊素具有明显的破坏作⽤,Sn、A1+在浓度较⾼,即⼤于400 mg/kg时对红⾊素的⾊价有影响,⽽Fe3+、Na+、K+、M矿等对红⾊素的影响可以忽略。
提取⽅法⽐较:辣椒红素是从红辣椒果⽪中得到的深红⾊天然红⾊素,⾊泽优良、性质稳定,⼴泛⽤于⾷品、化妆品、饲料等领域,另外还具有抗癌功能。
⽬前,辣椒红⾊素提取⽅法⼤致可归为油溶法、溶剂提取法、超临界CO2流体萃取法、超声波溶剂提取法、溶剂微波提取法和酶法提取六类。
国内外辣椒红⾊素的提取⽅法主要有油溶法、有机溶剂法和超临界CO 流体萃取法三种。
油溶法因油与⾊素难分离不易得到纯净的辣椒红⾊素,所以该种⽅法现已基本停⽌使⽤;溶剂法使⽤较普遍,通常⽤丙酮、⼄醇、正⼰烷等有机溶剂浸提。
超临界CO2流体萃取法是⼀种新型的分离技术,⼯艺简单、能耗低、萃取溶剂⽆毒、易回收、所得产品具有⾮常⾼的纯度。
提取⽬的及社会需求:辣椒红⾊素在国内外市场需求量很⼤。

辣椒中辣椒素的高效液相色谱法测定2008年第6期现代科学仪器ModernScientificInstruments辣椒中辣椒素的高效液相色谱法测定李如华韩振泰(中国林科院森林生态环境与保护研究所国家林业局森林生态环境重点实验室北京100091)摘要辣椒素的化学组成主要为辣椒碱和二氢辣椒碱.辣椒碱具有镇痛,消炎,促进食欲,改善消化,抗菌,杀虫及对神经递质的选择性等药理作用.辣椒碱可以治愈和缓和一些难治愈慢性神经疼痛,可为这些疾病的治疗提供一条新的途径,是一个很有发展潜力的药物本文采用高效液相色谱法,通过对流动相,检测波长等分离条件的优化,建立了辣椒素的分析方法.经实验证实,本方法操作简单,重复性好,准确度高,可以对辣椒素的工业化生产提供帮助J.方法回收率90%~92%,相对偏差:2.5%,相关系数:r=0.9956.关键词辣椒素;二氢辣椒碱;高效液相色谱中图分类号Q946.88 DeterminationofCapsaicinoidsinHotPepperbyRP—HPLCLiRuhua,HanZhentai (ResearchInstituteofForestryEnvironmentandProtection,CAF;KeyLaboratoryofForestr yEcologyandEnvironment,StateForestryAdministration,Beijing,100091,China) AbstractThechemicalcompositionofCapsaicinoidsiscapsaicinanddihydrocapsaicin.Cap saicinhastheeffectsofAnalgesia,antiphlogosis,increasingtheappetite,improvingthedigestion,antibact erial,disinfectionsandSOon.CapsaicinoidsCallcureandmitigatesomechronicneuralache,provideanewwayf orthesediseasetreatments.Capsaicinoidsisthemedicinewithhighdevelopmentpotentials.Inthispaper,byt heHPLCmethod andwiththeoptimizationofmobilephaseanddetectionwavelength,theanalysismethodofC apsaicinoidswases—tablished.Experimentsprovedthatthemethodhasthecharacteristicsofsimpleoperation,go odreproducibility, highaccuracyandcanprovidehelptotheindustrialproductionofCapsaicinoids-4j.TheReco veryrate.relativedeviationandcorrelationcoefficientofthemethodare90%~92%.2.5%and0.9956respectively.KeywordsCapsaicinoids;Dihydrocapsaicin;HPLC辣椒是一种药食同源的蔬菜,含有生物碱,色素,维生素,有机酸,矿物质等成分j.辣椒所独具的特性是辣味,其成分为辣椒素类物质.辣椒素是辣椒果实中结构为N一香草基酞胺类的生物碱.辣椒素的化学组成主要为辣椒碱(Capsaicin,C),二氢辣椒碱(Dihydrocapsaicin,DC),二者约占整个辣椒素的90%,其它为二者的同系物.辣椒素类提取物通常是混合物J,晶体颜色为白色(或微黄,微红),没有固定的熔点,通常熔点范围为57℃一66℃,沸点范围为210~C一220℃,易溶于低级醇和丙酮,氯仿,石油醚等有机溶剂,由于其酚羟基表现出弱酸性,因而能溶于强碱J.辣椒素属于酰胺类化合物,因而可发生水解生成香草基胺和癸烯酸.辣椒素的结构通式:收稿日期:2008—07—29作者简介:李如华,男,大学本科.1实验部分1.1仪器与试剂液相分析仪:Waters244高效液相色谱仪,Wa—ters486紫外检测器,M510泵,浙大色谱工作站.甲醇为优级并经0.5m滤膜过滤.水为重蒸水并经0. 451xm滤膜过滤.辣椒碱标样:天然,Sigma公司. 1.2色谱条件色谱柱:250am×4.6mmODS柱;流动相:75%的甲醇/水溶液;流速:1mL/min;检测器:220nm.1.3标准样品配制准确称取50mg辣椒碱标样,用甲醇定容至1O mL,备用.1.4辣椒碱样品配制准确称取60—200mg辣椒碱样品,用甲醇定容至10mL.68?现代科学仪器ModemScientificInstruments2008年12月2实验结果与讨论2.1流动相的选择和优化实验前我们对辣椒碱的HPLC法进行了调研,目前所采用的流动相主要有以下几种体系.张继敏等人采用稀磷酸(pH3.1~3.5)溶液/乙腈(50:50)为流动相,这与美国药典USP2003磷酸水溶液(1:1000, v/V)/乙腈(600:400)相似;赵仁邦等人采用甲醇作流动相.用甲醇作流动相,价格低廉,且避免了使用酸性溶液.为此,我们选择以甲醇作流动相进行实验.实验发现,用纯甲醇作流动相,辣椒碱和二氢辣椒碱的色谱峰未完全分开.于是,我们分别配制85%,75%,70%的甲醇溶液作流动相.实验结果显示,随着流动相中水的含量增加,辣椒碱和二氢辣椒碱的t逐渐增加,当流动相为85%的甲醇/水溶液时,辣椒碱和二氢辣椒碱基本分开;当流动相为75%的甲醇/水溶液时,辣椒碱和二氢辣椒碱可实现基线分离;但当水的含量增加至40%时,即60%的流动相对辣椒碱样品溶解性降低.因此,我们认为,流动相以70—75%的甲醇溶液较为合适.此时样品各组分能实现基线分离(如图1).图1辣椒碱标样图谱图2辣椒提取物样品图谱2.2检测波长的影响我们用标准样品,在图1的条件下,测定了不同检测波长下的辣椒素和二氢辣椒素的峰面积,其结果见表1. 表1不同检测波长下的辣椒素和二氢辣椒素的峰面积蝗面积l波长选择波长(m)图3检测波长对峰面积的影响根据表1,我们绘出了保留时间t为17.3min的辣椒碱组分的检测波长对峰面积的影响趋势,如图3所示.由图3看出,当波长在220nm时,辣椒碱的峰面积最大,此时灵敏度最高.2.3定量分析2.3.1重复性实验在上述优化条件下,即流动相为75%的甲醇/水溶液,检测波长为220am,连续钡定七次标样,测定结果见表2.经计算,平均测定相对偏差为2.5%.表2计算相对误差2.3.2标准曲线通过测量不同浓度的标样,得出辣椒碱,二氢辣椒碱的峰面积与浓度的关系,(见表3),即可绘出标准曲线,如图4,图5所示.结果表明,辣椒碱在0,25 —5mg/mL浓度范围内,浓度与峰面积具有良好的线性关系.蝗面积浓度/mL)图4辣椒碱标准曲线直线回归方程:Y=2.0927+2.801X,蝗面积维度/mL)图5二氢辣椒碱标准曲线直线回归方程:Y=0.6805+2.2141X.2.3.3样品测定表4样品中的辣椒碱含量测定表5样品中的二氢辣椒碱含量测定3结论本文建立了辣椒素的高效液相色谱分析方法.其优化条件是:色谱柱250cm×4.6mmODS柱;流动相75%的甲醇/水溶液;流速1mL/min;UV220nm.平均相对偏差为2.5%,辣椒碱在0.25—5mg/mL浓度范围内,浓度与峰面积具有良好的线性关系.经实验证实,本方法操作简单,重复性好,准确度高,满足分析要求.参考文献[1]彭书练,单扬,丁芳林.辣椒碱的制取,纯化及应用研究.辣椒杂志, 2005,3:40~41[2]张甫生,庞杰,徐秋兰,陈梅芳.辣椒红色素的研究进展.辣椒杂志, 2003,2:37[3]江和源,段文华,尉蕊仙.分子蒸馏技术及其应用.西部粮油科技, 2003.6:41—43[4]杨村,于宏奇,冯武文.分子蒸馏技术.北京:化工工业出版社, 2003,1:1—55,110—111[5]张志栋.辣椒碱的研究进展.天津药学,1997,9:25—26[6]伍明,任仲皎,王杰.天然辣椒红色素的提取新工艺.精细化工, 1994.11:30—33[7]阳勇.重庆大学学报.2004,12[8]张世文.吉首大学学报.2002,2。

食品中辣椒素含量检测方法的研究进展引言:辣椒作为一种常见的调味品和食材,不仅赋予食物丰富的香辣味道,还富含多种营养成分,如辣椒素。
辣椒素对人体具有多种好处,如增强食欲、促进新陈代谢、提高免疫力等,因此深受人们喜爱。
然而,食品中辣椒素含量的检测方法一直是食品科学领域的热门研究课题。
本文将综述近年来国内外食品中辣椒素含量检测方法的研究进展,并探讨其方法优缺点及发展前景。
一、传统的辣椒素含量检测方法1. 化学分析法:化学分析法是最早被采用的辣椒素含量检测方法。
常用的方法有高效液相色谱法、气相色谱法以及比色法等。
这些方法具有操作简单、准确度高的特点,但也存在着一些缺点,如耗时长、需要大量的试剂和仪器设备等。
2. 生化分析法:生化分析法是通过辣椒中辣椒素的生化反应来检测其含量。
例如,采用辣椒素酶法来测定辣椒素含量。
这种方法具有灵敏度高、操作简单等优点,但对试剂的纯度要求较高,且容易受到其他物质的干扰。
二、近年来的新型辣椒素含量检测方法1. 光谱分析法:光谱分析法是近年来辣椒素含量检测方法的研究热点之一。
这种方法通过采用紫外-可见光谱仪、红外光谱仪等,测定不同波长下辣椒素的吸收光谱,进而计算其含量。
相比于传统方法,光谱分析法具有快速、无污染、对样品无破坏性的优点,因此受到了广泛关注。
2. 生物传感器法:生物传感器法是一种基于生物反应的辣椒素含量检测方法。
如利用酶生物传感器来测定辣椒素。
通过将酶与电极结合,当酶与辣椒素发生反应时,可通过测定电流或电压变化等来计算其含量。
这种方法具有快速、灵敏、无污染等优点,但需要较高的装备和技术条件。
3. 分子印迹技术:分子印迹技术是一种基于辣椒素与特定配位体之间的识别和结合性质的检测方法。
通过制备具有选择性的分子印迹聚合物进行辣椒素的吸附和检测。
这种方法具有选择性强、重复性好等特点,但对印迹聚合物的合成和制备条件要求较高。
三、方法之间的比较与评估不同的辣椒素含量检测方法各有优劣,适用于不同的实际应用场景。
食品安全国家标准食品添加剂辣椒红1 范围本标准适用于以辣椒(Capsicum annuum L)果皮及其制品为原料,经萃取、过滤、浓缩、脱辣椒素等工艺制成的食品添加剂辣椒红。
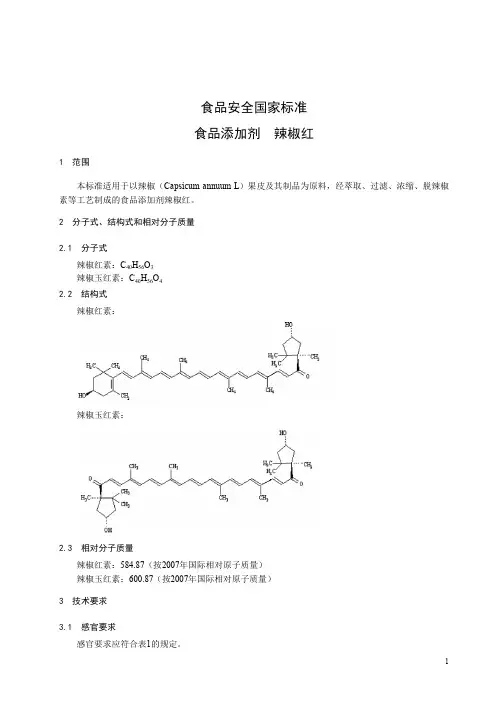
2 分子式、结构式和相对分子质量2.1 分子式辣椒红素:C40H56O3辣椒玉红素:C40H56O42.2 结构式辣椒红素:辣椒玉红素:2.3 相对分子质量辣椒红素:584.87(按2007年国际相对原子质量)辣椒玉红素:600.87(按2007年国际相对原子质量)3 技术要求3.1 感官要求感官要求应符合表1的规定。
GB 10783—201X3.2 理化指标理化指标应符合表2的规定。
表2 理化指标附录A 检验方法A.1 一般规定本标准所用试剂和水,在没有注明其他要求时,均指分析纯试剂和符合GB/T 6682规定的三级水。
试验中所用标准溶液、杂质标准溶液、制剂及制品,在没有注明其他要求时,均按GB/T 601、GB/T 602、GB/T 603的规定配制。
试验中所用溶液在未注明用何种溶剂配制时,均指水溶液。
A.2 鉴别试验 A.2.1 溶解性溶于乙醇,易溶于植物油、丙酮、乙醚、三氯甲烷,几乎不溶于水,不溶于甘油。
A.2.2 显色反应在1滴试样中加2~3滴三氯甲烷和1滴硫酸,应呈现暗蓝色。
A.2.3 最大吸收峰样品溶解在正己烷中,在约470nm 处有最大吸收峰。
A.3 吸光度的测定 A.3.1 试剂和材料丙酮。
A.3.2 仪器和设备A.3.2.1 分光光度计,附1 cm 比色皿。
A.3.3 分析步骤准确称取0.1g 试样(精确至0.000 2g ),用丙酮稀释于100mL 容量瓶中,再精确吸取稀溶液10mL ,稀释至100 mL ,用分光光度计在460nm 波长处,用丙酮作参比液,于1cm 比色皿中测定其吸光度。
注:被测比色液的吸光度范围宜控制在A=0.30~0.70范围内。
A.3.4 结果计算吸光度nm E cm 460%11按公式(A.1)计算:1001460%11⨯⨯=m f A nm E cm ………………………………(A.1) 式中:A ——实测试样溶液的吸光度; f ——稀释倍数;m ——试样质量,单位为克(g )。
红辣椒中辣椒红素的提取、分离及鉴定一、实验目的1、学习从红辣椒中提取辣椒红素的原理和方法。
2、掌握萃取、干燥、浓缩、薄层层析、柱层析等基本操作。
3、学习色谱分离方法的原理与操作,学习红外光谱鉴定有机化合物的方法。
二、实验原理红辣椒中含有辣椒红素、辣椒玉红素和β-胡萝卜素等几种色泽鲜艳的色素,其中以辣椒红素为主。
这几种物质都是由8个异戊二烯单元组成的四萜类化合物,难溶于水和乙醇,易溶于石油醚、氯仿和二氯甲烷。
最大吸收波长λmax=470nm。
在实验室中,常用二氯甲烷作溶剂从红辣椒中提取辣椒红素。
二氯甲烷沸点为39.8℃。
用二氯甲烷提取的物质除上述几种物质外还有辣椒素等,可利用辣椒红色素易于溶于正己烷而辣椒素较难溶于正己烷的性质将两者进行分离。
得到辣椒红素、辣椒玉红素和β-胡萝卜素等的混合物,可通过薄层层析和柱层析将它们分离。
在薄层层析中,有三个斑点,R f值约为0.6的较大红色斑点为辣椒素,R f值稍大的较小红色斑点为辣椒玉红素,R f值最大的黄色斑点是β-胡萝卜素。
柱层析时,以硅胶为吸附剂,以二氯甲烷为洗脱剂可比较容易得将3种物质分开。
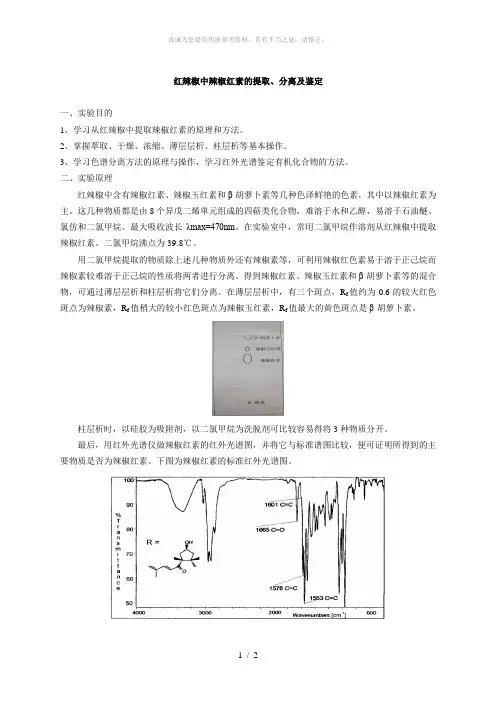
最后,用红外光谱仪做辣椒红素的红外光谱图,并将它与标准谱图比较,便可证明所得到的主要物质是否为辣椒红素。
下图为辣椒红素的标准红外光谱图。
三、仪器、试剂及实验材料1、仪器:50m圆底烧瓶1个、25ml锥形瓶3个、50ml量筒、50ml烧杯2个、研钵、载玻片、球形冷凝管、层析板、层析缸、层析柱、抽滤瓶、布氏漏斗、蒸馏装置一套。
2、实验材料及试剂:干红辣椒、二氯甲烷、正己烷、硅胶G、硅胶(60~200目)。
四、实验步骤1、预处理:称5g干红椒,将干红辣椒去蒂、去籽,研磨成粉末。
2、色素提取:装好回流装置。
在50ml 圆底烧瓶中,加入3g磨细的红辣椒粉和25ml 二氯甲烷,再放2粒沸石,回流30min。
冷却至室温后抽滤,除去固体物,得鲜红色滤液。
将滤液用蒸馏法蒸去溶剂,即得粗产品。

含量测定的操作规程有哪些含量测定是一种常见的分析方法,可以用于确定物质中某种成分的含量。
在进行含量测定之前,需要设计一个详细的操作规程,以确保实验结果的准确性和可重复性。
下面是一个大致的含量测定操作规程,供参考。
1. 实验前准备工作- 仔细阅读样品的相关信息,了解其特性和测定目的。
- 回顾相关的理论知识,了解测定方法的原理和操作步骤。
- 准备好实验所需的仪器设备和试剂材料,确保其齐全和正确。
2. 样品处理- 根据样品特性和测定目的,选择合适的样品处理方法。
例如,可以进行溶解、煮沸、萃取等操作。
- 根据需要,对样品进行适当的预处理,如干燥、研磨、过筛等。
3. 样品测定- 设置合适的实验条件,包括温度、pH值、溶剂选择等。
- 准备好测定容器,如试管、比色皿、烧杯等。
- 使用准确的量取工具,如天平、量筒、移液器等,量取适量的样品和试剂。
- 根据测定方法的要求,按照特定的操作步骤,将样品和试剂添加到测定容器中。
- 进行反应、混合、摇匀等处理,确保反应均匀和充分。
- 根据测定方法的要求,对反应体系进行适当的处理,如加热、冷却、过滤等。
- 使用相关仪器对反应体系进行测定,如使用吸光度计、电解质测定仪等。
- 记录测定结果,并进行数据处理和分析。
4. 质量控制- 在进行含量测定之前,建议进行质量控制步骤,以确保实验结果的准确性和可靠性。
- 比对样品处理和测定步骤,确保每个步骤都符合操作规程。
- 使用标准样品进行验证,检查测定方法的准确性和可重复性。
- 进行质量控制记录,包括待测样品的信息、实验条件、测定结果等。
5. 安全措施- 特别要注意实验操作的安全性,遵守实验室的操作规范和安全要求。
- 使用适当的个人防护装备,如实验衣、手套、护目镜等。
- 谨慎操作化学试剂,避免接触皮肤和吸入有害气体。
- 当有需要时,使用通风设备或操作在安全柜中。
这只是一个大致的含量测定操作规程,实际操作中可能会有所变化,具体的操作规程应根据实验目的、样品特性、测定方法等因素进行详细设计和调整。
辣椒红色素的提取、分离及鉴定一、实验目的1. 了解从红辣椒中提取辣椒红素的原理和方法;2. 进一步熟悉回流、抽滤、薄层层析、柱层析等基本操作;3. 学习红外光谱鉴定有机化合物的方法。
二、实验原理红辣椒中含有辣椒红素、辣椒玉红素和ß-胡萝卜素等几种色泽鲜艳的色素,其中以辣椒红素为主。
这几种物质都是有8个异戊二烯单元组成的四萜类化合物,难溶于水和乙醇,易溶于石油醚、氯仿和二氯甲烷。
其中极性较大的红色组分主要是辣椒红素和辣椒玉红素,占总量的50%-60%;另一类是极性较小的黄色组分,主要成分是β-胡萝卜素和玉米黄质。
辣椒红素不仅色泽鲜艳、热稳定性好、而且耐光、耐热、耐酸碱、耐氧化、无毒副作用,是高品质的天然色素,可用作食品的添加剂,也广泛用于化妆品、保健药品等行业,其结构式如下:在实验室中,常用二氯甲烷(沸点39.75℃)作溶剂从红辣椒中提取辣椒红素。
用二氯甲烷提取的混合物可通过薄层层析和柱层析将它们分离。
在薄层层析中,有三个斑点,R f 值约为0.6的较大红色斑点为辣椒红素,R f值稍大的较小红色斑点为辣椒玉红素,R f值最大的黄色斑点是ß-胡萝卜素。
柱层析时,以硅胶为吸附剂,以二氯甲烷为洗脱剂,可对比标准样品图谱较容易地将3种物质分开。
红辣椒色素的薄层层析图最后,用紫外光谱测样品的λmax并用红外光谱仪做辣椒红素的红外光谱图,并将它与标准谱图比较,便可证明所得到的主要物质是否为辣椒红素。
辣椒红素的紫外可见吸收光谱图辣椒红素的标准红外光谱图三、实验仪器及试剂材料:干红辣椒(或辣椒粉)仪器:研钵、25ml锥形瓶3个、50ml量筒、50ml烧杯2个、50mL圆底烧瓶、沸石、电热套、球形冷凝管、布氏漏斗、抽滤瓶、蒸馏装置、滤纸、玻璃板、毛细管、层析缸、层析柱红外光谱仪等。
试剂:二氯甲烷、硅胶G、硅胶(60~200目)、0.1mol/L乙酸钠、无水硫酸钠等。
四、实验步骤1.实验材料前处理称取5.00g干红辣椒,去蒂、去籽后研磨成粉末。
高效液相色谱法测定火锅底料中辣椒素类物质
尼海峰;但晓容;李栋钢
【期刊名称】《中国调味品》
【年(卷),期】2014(000)011
【摘要】为了测定火锅底料中的辣味物质(辣椒素及二氢辣椒素),建立了高效液相色谱快速检测方法:色谱柱为C18 InertSustain (4.6 mm ×250 mm,5μm),流动相为甲醇和水(V/V,65∶35),流速1.0 mL/min,柱温30℃,进样量10μL,检测波长280 nm。
辣椒素类物质的提取采用超声波辅助提取。
结果表明:火锅底料中的辣椒素类物质含量在0.256~0.816 g/kg 之间,斯科维尔系数在3948~12583 SHU。
【总页数】5页(P115-119)
【作者】尼海峰;但晓容;李栋钢
【作者单位】四川天味食品集团股份有限公司,成都 610200;四川天味食品集团股份有限公司,成都 610200;四川天味食品集团股份有限公司,成都 610200【正文语种】中文
【中图分类】TS207.3
【相关文献】
1.高效液相色谱法测定辣椒制品中的辣椒素类物质 [J], 孙胜枚
2.麻辣火锅底料中常用配料对辣椒素类物质的影响 [J], 唐毅;张丽;李杨梅;王森;陈小容
3.高效液相色谱法测定豆瓣中辣椒素类物质含量 [J], 贾洪锋;彭德川;梁爱华;何江红;陈祖明;贺稚非
4.高效液相色谱法测定高含水量辣椒制品中的辣椒素类物质 [J], 王穗萍;夏延斌;彭进;熊科;郑瑶瑶;杨峰
5.冻干浓缩对高效液相色谱法测定杭椒类辣椒中辣椒素类物质的影响 [J], 吕晓菡; 杨静; 陈建瑛; 傅鸿妃; 祝彪; 聂智星
因版权原因,仅展示原文概要,查看原文内容请购买。
辣椒及辣椒制品中辣椒素类物质的测定及辣度表示方法操作规程
1 目的
对公司产品的辣椒素类物质含量测定制定标准操作规程,检验室操作人员按本规程操作,保证公司辣椒素类物质含量检测结果准确。
2 范围
第一法液相色谱法适用于辣椒油树脂、辣椒及其为原料生产食品中的辣椒素、二氢辣椒素含量的测定第二法适用于辣椒和辣椒精油中辣椒素类物质总量的测定;
第一法液相色谱法
3 依据
GB/T 21266-2007《辣椒及辣椒制品中辣椒素类物质测定及辣度表示方法》、NY/T 1381-2007 《辣椒素的测定高效液相色谱法》、GB 28314-2012《食品安全国家标准食品添加剂辣椒油树脂》附录A.3。
4 实验原理
试样经甲醇溶液提取,过微孔滤膜,进样,用反相色谱分离,紫外可见光检测器检测,外标法定量。
5 仪器和设备
5.1 高效液相色谱仪:带紫外可见光检测器。
5.2 天平:感量±0.0001g、±0.01g。
5.3 超声波提取器。
5.4 组织捣碎机、电动粉碎机。
5.5恒温水浴锅。
5.6 滤膜:0.45µm有机滤膜
6 实验步骤
6.1 样品制备
6.1.1半固态、固态样品
取一独立包装样品,将样品混合均匀,静置,取上清液。
6.1.1液态样品
取一独立包装样品,将样品振摇1min,使其混合均匀。
6.2 操作步骤
称取一定质量的试样(精确至0.001g)于具塞锥形瓶中,加入甲醇20mL,在55℃水浴条件下,用超声波提取30min,然后放入冰水浴中冷却20min,收集滤液。
将滤渣连同滤纸重新用20mL甲醇超声提取30min后重复上述步骤,收集滤液。
再加入甲醇10mL重复一次。
将三次收集的滤液合并至50mL容量瓶,用甲醇定容。
经0.45µm有机相滤膜过滤后进行色谱分析。
(1)火锅底料类称取3g左右,定容于50mL容量瓶;
(2)辣椒段、粉等(二荆条、新一代等)称取1g样品,定容于50mL容量瓶。
(3)辣椒油树脂、水辣粉等称取0.5g,定容于100mL容量瓶。
注:对于含水量高的样品,过滤时加入无水硫酸钠1-2g。
7 色谱参考条件
色谱柱:C18色谱柱(250mm×4.6mm),粒径5µm。
流动相:甲醇+水=70+30,用前过0.45µm滤膜,脱气。
流速:0.8mL/min。
检测波长:280nm。
柱温箱温度:30℃。
8 试液的测定
将制备好的试液在7 色谱条件下测定,做单点或多点校准,以峰面积积分值定量。
9 结果计算及表述
试样中辣椒素、二氢辣椒素含量以质量分数w计,单位以mg/g表示,按照下式进行计算:
W=
A×V×ρs m×A s×1000
A—试样中辣椒素、二氢辣椒素的峰面积积分值;
A S—标准工作溶液中辣椒素、二氢辣椒素的峰面积积分值;
ρS—标准工作溶液中辣椒素、二氢辣椒素的质量浓度,单位为mg/L(ug/mL);
V—试样最终定容体积,单位为毫升(mL);
m—试样质量,单位为克(g);
计算结果保留三位有效数字。
10 精密度
在重复性条件下获得的两次独立测定结果的绝对差值不得超过算术平均值的10%。
11 斯科维尔指数(SHU)的计算
斯科维尔指数X的计算如下:
X = W×0.9×(16.1×103)+ W×0.1×(9.3×103)
第二法紫外分光光度法
依据
GB/T 30389-2013 《辣椒及其油树脂总辣椒碱含量的测定分光光度法》
13 原理
在波长248nm和296nm处测定辣椒萃取物或辣椒油树脂的甲醇溶液的紫外吸收,根据吸收值计算样品中总辣椒碱的含量。
14 试剂
除特别说明以外,试剂为分析纯,水为蒸馏水、去离子水或纯度相当的蒸馏水。
活性碳;甲醇(光谱纯);甲醇溶液(7+3):70体积甲醇和30体积水混合而成;盐酸溶液(1mol/L);氢氧化钠溶液(1mol/L)。
15 仪器
容量瓶:25mL,100mL,250mL;
紫外分光光度计(可测220nm~370nm的紫外吸收,配1cm石英比色皿)
振摇式混合器,膜过滤器(孔径0.45μm)
分析天平:感量0.1mg
16 试样制备
16.1 取辣椒样品约200g,将其研磨粉碎,称取1g混匀的粉状样品,精确至0.001g,加入甲醇75mL超声萃取30min。
16.2 辣椒油树脂样品,称取0.5g~1g混匀的辣椒油树脂,精确至0.0001g,移入250ml容量瓶中
17 试样分析测试
17.1 辣椒或辣椒粉
在16.1得到的萃取物中加入0.5~0.9g活性碳,活性碳与萃取物的比例为1:10 ,然后加入约30ml蒸馏水,磁力或振摇30min,放置5min,膜过滤或滤纸过滤入100mL容量瓶中,用甲醇定容到100mL(略显淡黄色不影响测定)。
17.2 辣椒油树脂
在试样16.2中加入0.05g~0.1g活性碳,活性碳与辣椒油树脂的比例为1:10,然后加入约90mL甲醇溶液,磁力或振摇30min,放置5min,膜过滤或滤纸过滤入100mL容量瓶中,用甲醇溶液(70%)定容到100mL (略显淡黄色不影响测定)。
18 吸光度测定用稀释液的制备
18.1 将3mL水、2mL盐酸加入25mL容量瓶中,用甲醇稀释至刻度,此溶液标记为“空白酸液A”。
18.2 将3mL水、2mL氢氧化钠溶液(1mol/L)加入到25mL容量瓶中,用甲醇稀释至刻度,此溶液标记为“空白碱液B”。
18.3 取1个25mL容量瓶,加入1mL滤液(18.1或18.2)、2.7mL水和2mL盐酸(1mol/L),用甲醇稀释至刻度。
18.4 取1个25mL容量瓶,加入1mL滤液(18.1或18.2)、2.7mL水和2mL氢氧化钠(1mol/L),用甲醇稀释至刻度。
19 吸光度测定
用70%甲醇溶液调零点和100%透过率。
将空白碱液B放入测量池后重新调零点,然后分别在248nm和296nm处测定样品的吸光度值A s、A s,;再将空白酸液A放入测量池重新调零点,然后分别在248nm和296nm 处测定样品的吸光度值A b、A
b
,。
20 结果计算
20.1 在248nm处,总辣椒素含量的质量分数W248,数值以%表示,按下式(1)计算:
ω248=(A s−A b)×d 314×m
式中:
W248——总辣椒素含量(质量分数),%;
A s——样品碱溶液的吸光度值;
A b——样品酸溶液的吸收值;
d——稀释因子(本标准为25×100)
M——试样的质量,g。
当吸光度值大于0.8时,稀释重测。
20.2 在296nm处,总辣椒素含量的质量分数W296,数值以%表示,按下式(2)计算:
ω296=(A s,−A
b
,)×d 127×m
式中:
W296——总辣椒素含量(质量分数),%;
A s,——样品碱溶液的吸光度值;
A
b
,——样品酸溶液的吸收值;
d——稀释因子(本标准为25×100)
M——试样的质量,g。
当吸光度值大于0.8时,稀释重测。
20.3 在248nm和296nm处测得的总辣椒素含量的差不得大于10%,否则重测。
实验结果以平行测定结果的算术平均值为准。
在重复性条件下获得的两次独立测定结果的绝对差值不大于算术平均值的10%。
21 注意事项
1、吸光度值控制在0.2到0.8之间。
2、本方法可用于测定牛油或清油底料的麻味物质含量,方法同辣椒样品,牛油超声提取时温度控制在
50℃以上。