废渣中铟的回收与利用.
- 格式:doc
- 大小:638.01 KB
- 文档页数:40

铟是稀散金属之一,地壳上没有单独的铟矿床,主要富集于硫化矿,特别是闪锌矿内。
含铟原料的世界储量按金属量计约为2985t,其探明储量中约17.7%集中分布在美国,18.4%分布在加拿大,日本和秘鲁各占约4%。
我国铟的储量居世界第一,广西大厂是我国重要的铟基地,矿产资源丰富,开发矿山产出的高铟锌精矿中铟的含量高达0.095%。
1冶炼过程中铟在产物中的分布目前生产的大多数铟是从铅、锌、铜、锡等矿石冶炼过程中回收的副产品。
在从较难挥发的锡和铜内分离铟的过程中,铟多数富集在烟道灰和浮渣内,在从挥发性的锌和镉中分离铟时,铟则富集于炉渣及滤渣内。
我国生产铟主要是从铅、锌冶炼的副产品中提取。
1.1铟在铅冶炼中的分布铟在铅精矿中的含量一般为0.005%左右。
铅精矿在烧结时约3%的铟进入烟尘,在鼓风炉熔炼过程中,铟几乎平均分配于粗铅、炉渣和烟灰中,粗铅火法精炼熔析除铜时,粗铅中的铟大部分进入铜浮渣,用苏打—铁屑法在反射炉处理此渣时,部分铟挥发随烟气进入收尘系统。
铟在铅冶炼产物中的分布为(%):烟尘34~38、炉渣31.3~35.7、苏打渣1.1、冰铜6.5、返回物7.1~8.8、无名损失33.1~48.2。
1.2铟在锌湿法冶炼中的分布锌精矿含铟一般为0.003%~0.013%(广西大厂矿除外),在湿法炼锌中,当锌精矿进行焙烧时,由于矿石中的铟被氧化成难挥发的氧化铟,故矿石中95%以上的铟留在焙砂中。
当采用常规浸出时,80%~100%的铟留在浸出渣中,采用回转窑挥发处理渣,有60%~70%的铟进入氧化锌烟灰中,采用此种方法时,铟在锌冶炼产物中的分布为(%):氧化锌烟尘55~65、回转窑渣20~25、铜镉渣~5、损失~5。
当采用热酸浸出—黄钾铁矾法炼锌时,95%以上的铟进入浸出液中,而在随后的沉矾过程中,铟又进入矾渣,铟在此法各产物中的分布为(%):铁矾渣90~93、高浸渣3~5、铜镉渣l~2、损失2~3。
当采用热酸浸出—针铁矿法炼锌时,铟的提取方法是:在还原预中和的上清液中,加入氧化锌粉经两段中和沉铟,其铟渣即为提取铟的原料。

铟的生产工艺铟的提取工艺以萃取-电解法为主,这也是现今世界上铟生产的主流工艺技术。
其原则工艺流程是:含铟原料→富集→化学溶解→净化→萃取→反萃取→锌(铝)置换→海绵铟→电解精炼→精铟。
世界上铟产量的90%来自铅锌冶炼厂的副产物。
铟的冶炼回收方法主要是从铜、铅、锌的冶炼浮渣、熔渣及阳极泥中通过富集加以回收。
根据回收原料的来源及含铟量的差别,应用不同的提取工艺,达到最佳配置和最大收益。
常用的工艺技术有氧化造渣、金属置换、电解富集、酸浸萃取、萃取电解、离子交换、电解精炼等。
当前较为广泛应用的是溶剂萃取法,它是一种高效分离提取工艺。
离子交换法用于铟的回收,还未见工业化的报导。
在从较难挥发的锡和铜内分离铟的过程中,铟多数集中在烟道灰和浮渣内。
在挥发性的锌和镉中分离时,铟则富集于炉渣及滤渣内。
在ISP炼铅锌工艺中,精矿中的铟较大部分富集于粗锌精馏工序产出的粗铅中,回收富铟粗铅的铟,一直采用碱煮提铟工艺,存在生产能力小、生产成本高、金属回收率低等缺点。
为了简化铟的提取流程,降低生产成本,提高金属回收率,针对原有的提铟生产工艺,本项目通过条件试验、循环实验及综合试验,研究开发了“富铟粗铅电解-铅电解液萃铟”提取工艺,确定了新工艺的最佳工艺参数。
工艺流程为:粗铅熔化铸成极板,装入电解槽通电进行电解,阳极中的铟溶解进入电解液,当铟富集到一定浓度后,抽出电解液进行萃取、反萃,富铟反萃液经pH调节、置换、压团熔铸后得到粗铟。
分离提取铟的几种新技术:这些新技术使用的主要分离材料包括液膜、螯合树脂、浸渍树脂和微胶囊。
在合适的条件下,运用这些技术可对铟进行有效地分离回收。
这些新技术为分离回收铟提供了新的选择。

铁矾渣提铟及铁资源利用新工艺研究的开题报告一、课题背景和意义随着环保和资源节约意识的提高,资源循环利用逐渐成为一种趋势。
铟是一种稀有金属,具有高效的光电转换性能,是太阳能电池、液晶显示器、LED等电子产品的重要材料。
然而,根据目前的铟产量和需求预测,在不久的将来,铟资源将成为一种非常紧俏的物质。
因此,提高铟资源的回收率和开发利用新的铟资源是非常必要的。
目前,铟的主要来源是来自金属硫化物和磷酸盐矿物。
除了这些矿物外,铁矾渣中也含有较多的铟资源。
铁矾渣是一种含铁废弃物,具有很高的铁和含量,而且每年的产量相当庞大。
对于铁矾渣的铟资源回收和铁资源利用,是很有研究意义和工程价值的。
二、研究内容和工作计划本研究旨在开发一种新的铁矾渣提铟技术,同时实现铁资源的有效利用。
具体的研究内容和计划如下:1、铁矾渣的化学成分分析:利用XRD、SEM等分析手段分析铁矾渣的化学成分和物相组成。
2、铟的萃取和分离:选取萃取剂和条件,优化工艺参数,实现铟的高效萃取和分离。
并进行萃取后相分离和铟纯化处理。
3、铁的资源利用:利用还原焙烧或浸出法,将萃剂和残留液中的铁提取出来,返还高质量的铁资源。
4、工艺流程优化:根据实验结果,对工艺流程进行优化调整,使得工艺更加有效、稳定,同时实现文理经济效益的统一。
5、技术经济评价:对新技术进行技术经济评价,研究加工规模、投资回收期、制约成本等重要经济指标,为实际生产应用提供参考。
三、预期成果本研究通过对铁矾渣的性质和成分分析,探讨了铁矾渣提铟和铁资源利用的新工艺。
对萃取剂、工艺参数等进行优化调控,实现了对铟的高效从铁矾渣中回收率,同时通过铁的资源利用,返还了大量高质量的铁资源。
通过实验结果,建立了一套完整的铁矾渣提铟工艺流程,促进了对铟资源的回收和铁资源的循环利用。
同时,对新工艺进行经济评价,为实际工业生产应用提供了参考。
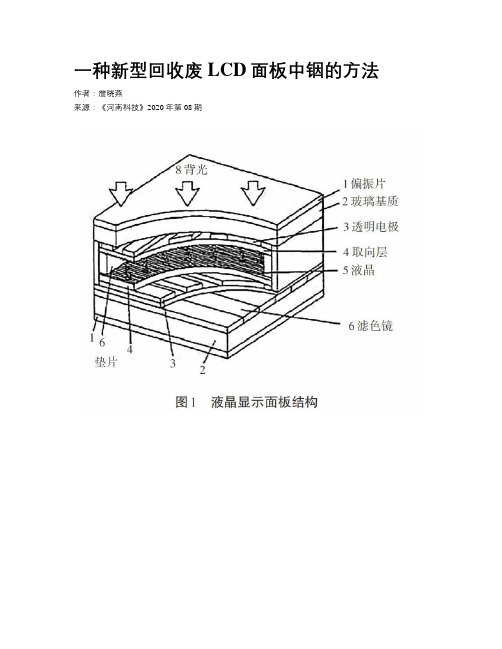
一种新型回收废LCD面板中铟的方法作者:詹晓燕来源:《河南科技》2020年第08期摘要:作为废LCD面板中的一种稀有金属,铟具有较大的回收利用价值。
目前,主流的回收方法是首先进行酸浸出,然后分离富集得到铟。
YZND公司开发了一种方法,首先采用物理法实现含液晶铟富集物和玻璃偏光片层的分离,然后采用真空裂解法将铟精矿和液晶分离,完成铟的回收,同时分离得到玻璃和偏光片,并实现了液晶的无害化处理,此方法具有环保和资源双重意义。
关键词:LCD面板;铟回收;物理分离;真空裂解中图分类号:X76;TF843.1 文献标识码:A 文章编号:1003-5168(2020)08-0125-03A New Method for Recycling Indium in Waste LCD PanelsZHAN Xiaoyan(Jiangsu Zhihuan Technology Co., Ltd.,Yangzhou Jiangsu 225009)Abstract: As a rare metal in waste LCD panels, indium has great recycling value. The current mainstream recycle method to obtain indium is acid leaching firstly, separating and enriching secondly. YZND company has developed a new method to recycle indium which separates the liquid crystal indium-containing enrichment and the glass-polarizer layer physicaly, and then uses vacuum pyrolysis method to separate the indium concentrate and the liquid crystal. The method can recycle glass and polarizer at the same time, and treat liquid crystal harmlessly which has double significance in environmental protection and resource utilization.Keywords: LCD panels;indium-recycle;physical separation;vacuum pyrolysis铟作为一种稀有金属,单价比黄金还贵。


铟的回收可行性报告第二章市场预测2.1 市场需求预测铟的应用领域很广,由于铟的延展性极好、蒸汽压低,又能够粘附在多种材料之上,所以它被广泛用作高空仪器和宇航设备中的垫片或内衬层材料。
铟箔常用作超声波线性阻滞的接触器。
铟的最为重要的应用是在半导体工业技术和无线电电子技术这两大领域。
在原子能工业中,铟用于制造中子的指示剂。
金属铟易于在金属表面形成牢固的涂层,具有良好的抗腐蚀性能,特别是能阻止碱性溶液的腐蚀作用。
铟的最富发展前景的应用领域是口腔医学,往制作牙科镶补物的材料中添加少量的金属铟,可以显著提高这些镶补物的抗腐蚀能力和硬度,含铟的氟化合物曾被掺入牙膏中,因为它具有预防龋齿的作用。
由高纯氧化铟和氧化锡的玻璃态复合物(ITO )在离子电视和液晶电视屏工业中用来制作透明导体的电极,还用作某些气体测量的敏感元件。
ITO (铟锡氧化物)主要使用于手提便携电脑及各类平板显示器。
随着平板显示器的越来越畅销,2002 年全球ITO的需求增长10%〜15%,世界消费铟达到约425吨,其中镀膜(主要为ITO )占73%。
2.2 价格现状与预测2005 年4 月初,世界金属铟(MWNYDealer)市场价格曾达到1000〜1070 美元/公斤的水平;后来缓慢下降,从4 月18 至5 月30 日,降至980〜1050 美元/公斤;从6 月初至7 月初,再降至900〜980美元/公斤;最近价格水平是850〜950美元/公斤。
ISuppli 的数据显示,2004 年全球笔记本电脑面板的出货量将达到4650 万个,比2003年增长16.3%,2005 年将上升到5500 万个,增长18.3%,2008年将接近8500 万个。
2004年台式液晶电脑面板出货量为6900 万个,2005 年将上升到1 亿个以上,到2008 年将超过1.5 亿个以上。
笔记本电脑和台式液晶电脑曾经创造了LCD 面板需求的两次浪潮,LCD 电视面板可能会带来第三次需求浪潮。
沉淀分离法回收真空炼锌渣中铟的研究王吉华;阮琼【摘要】从炼锌副产物中回收铟,大多采用萃取法将铟从酸浸液中富集分离出来,存在易乳化、废水酸度高、废水量大等缺点.针对真空渣等铟含量较高的物料提出沉淀富集分离的方法.用碳酸钠中和酸浸液至pH5.0,可将铟、锡完全沉淀而与锌、铁等元素分离.铟、锡混合沉淀用盐酸溶解,再将Sn2氧化为Sn4+,调整溶液pH为2.0,进行铟、锡分离,得到的氯化铟溶液经置换、碱熔等工艺处理,可得99.3%的粗铟.【期刊名称】《云南冶金》【年(卷),期】2016(045)001【总页数】4页(P34-37)【关键词】真空炼锌渣;铟;锡;沉淀【作者】王吉华;阮琼【作者单位】云南师范大学化学化工学院,云南昆明 650500;云南师范大学化学化工学院,云南昆明 650500【正文语种】中文【中图分类】TF801.3铟是一种重要的战略储备物资,由于其具有十分独特而优良的物理和化学性能,被广泛用于能源、电子、光电、航空、核工业和现代信息产业等高科技领域,需求量较大。
铟属于地壳中的稀有元素,不能独立成矿,而是很分散地分布于其它矿物中,大部分分散于闪锌矿中,所以锌冶炼的副产物是回收铟的主要原料。
目前,从锌冶炼副产物中回收铟的工艺主要是经过:硫酸浸出、萃取、反萃、置换、碱熔、除杂、电解精炼等过程[1-3]。
酸浸萃取工艺是在高酸环境下把铟浸出,从浸出液中用萃取剂萃取铟。
该工艺操作过程简单、铟的回收率较高,但也存在对浸出液的质量和组分要求高、废水量大、废水酸度高、废水处理成本高等不足之处,特别是对于铟含量比较高的物料,按传统工艺处理,萃取时很容易出现乳化现象,废水量大、废水酸度高等缺陷非常明显[4]。
本试验所用原料为火法炼锌中的下脚料硬锌、锌渣等经真空蒸馏回收锌后剩余的残渣(简称真空渣),其组成见表1。
根据物料的组成,本试验提出硫酸二次浸出、沉淀富集铟、除杂、置换、碱熔的工艺制得粗铟,铟含量可达99.3%。
浅析锌冶炼过程中铟的富集与回收技术作者:刘旭升来源:《中国新技术新产品》2017年第14期摘要:铟作为制造电光源、半导体、轴承合金、低熔合金等材料的重要原料,是一种质地柔软、可拉成细丝的性能独特的金属,随着科技的发展和进步,铟在社会发展中的应用日趋广泛。
本文主要通过对锌冶炼过程中铟的走向与分布的了解,在此基础上对冶炼渣及副产品中铟的富集与回收方式进行了分析和研究,总结了不同技术方式的特点,并对铟富集回收的发展方向做出了展望。
关键词:铟;冶炼锌;萃取;浸出;富集回收中图分类号:TF843 文献标识码:A根据美国地质局的调查资料信息,世界铟的已探明储量为1.1万t,而我国铟储量占世界铟储量的73%,其主要分布于内蒙、云南、广西等地区。
由于因矿物主要伴生存在于硫化锌类的矿物当中,并在硫化锑矿、硫化铜矿、氧化铅矿、锡矿、方铅矿等矿物中伴生存在,因此,从锌冶炼中进行铟的富集和回收就成为目前主要的铟收集方法。
一、阐述锌冶炼过程中铟的走向与分布当前,在锌冶炼中我国主要采取的工艺方法包括湿法与火法两种,其中,湿法又分为常规浸出法与热酸浸出法、直接浸出法3类,而在实际的锌湿法冶炼过程中通常将湿法与火法相互结合;火法主要是铅锌密闭的鼓风炉熔炼方法(简称ISP),另外还有竖罐炼锌、电炉炼锌等。
(一)锌湿法冶炼中铟的走向和分布在采用黄钾铁矾法来进行锌的湿法冶炼过程中,超过95%的铟会溶入到浸出液当中,并在之后的沉矾阶段中会随着沉淀物一同进入到铁矾当中去,从而实现铟的富集,因此铁矾渣能够当做铟的提取原料。
此外,在采用此法进行锌冶炼时,还需在还原预中和上清液当中进行中和剂的添加,以实现铟的沉淀,从而使铟渣成为铟提取的原料;或是直接于上清液当中进行萃取剂的添加,以实现铟的萃取回收。
(二)锌火法冶炼中铟的走向和分布闪锌矿作为锌冶炼中的通常处理矿物,考虑到其同方铅矿之间的共生关系,因此在进行锌冶炼的实际操作中通常会伴有铅冶炼情况的发生。
1 摘 要 本文首先对含铟废渣进行主要组分鉴定,然后采取合适的方法对主要组分的含量进行测定,最后对铟废渣中铟的回收进行了条件和工艺的研究,研究酸度,时间,温度等因素对铟浸出率的影响,及铟置换的工艺的条件探索。对酸度影响铟浸出率研究,采取了酸度分别为20 g/L、40 g/L、60 g/L进行研究,对浸出时间影响铟浸出率研究,采取了浸出时间分别为1 h、2 h、3 h、4 h进行研究,对温度影响铟浸出率的研究,采取了温度分别为70℃、75℃、80℃、85℃进行研究,对液固比影响浸出率采取分别为1:10、1:9、1:8进行研究,研究结果表明,在反应温度为85℃,反应时间为4h,液固比为1:10 酸度为40g/L (H2SO4), 加聚丙稀酰胺 ,可以高效只置换出酸液中的铟,并一次浸出率达到77%,取得较大的生产效果和经济效益。 关键词:铟,测定,浸出,萃取
2
Abstract This paper sludge containing indium main components identified, then take the appropriate method to determine the contents of the main components. Finally, the recovery of indium indium sludge process and the conditions for the study, research acidity, time, temperature on the rate of leaching and its behavior toward impurities, and the replacement process on the condition of indium. Effects of acidic leaching rate, a pH of 20 g/L,40 L,60 L for a study on the impact of leaching rate of leaching time, a time for the 1st and 2nd h leaching. Research conducted a three-hour incubation, the leaching rate of temperature, a temperature of 70 ° C, 75 ° C,80 ° C, 85 ° C for a study on the ratio of liquid to solid take affect leaching rate of 1:10,1:9,1 :8 study results show that the reaction temperature of 85 ° C and the reaction time of 4 hours, the liquid-to-solid ratio of 1 :10 acidity of 40g/L. (H2SO4), plus polyacrylamide, the replacement acid can be highly effective only in the indium, and a leaching rate of 77%, greater effectiveness and cost-effective production。
Keywords:Indium ,Determination,leaching,extraction 3
目 录 摘 要 ...................................................................................................................................... 1 Abstract .................................................................................................................................... 2 第一章 前 言 ........................................................................................................................ 4 1.1 金属铟的用途 .................................................................................................................... 4 1.2 国内外市场分析 ................................................................................................................ 4 1.3 铟资源在我国的分布与冶金特性 .................................................................................... 5 1.4 铟的回收技术研究进展 .................................................................................................... 5 第二章 铟渣的成分分析 ...................................................................................................... 8 2.1 实验原料与试剂 ................................................................................................................ 8 2.2 实验设备及仪器 ................................................................................................................ 8 2.3 组分的鉴定 ........................................................................................................................ 9 2.4 铟渣中组分含量测定 ...................................................................................................... 9 2.4.1 用邻二氮菲法测定铟渣中的铁 .................................................................................. 9 2.4.2 EDTA 容量法测定铝量 .............................................................................................. 11 2.4.3 EDTA 容量法测锌含量 ................................................................................................ 11 2.4.4 铟的测定 ...................................................................................................................... 12 2.4.5 结果小结 ...................................................................................................................... 12
第三章 浸出工艺实验条件 ...................................................................................................... 13 3.1 实验原理 ............................................................................................................................ 13 3.2 物料的组成 ........................................................................................................................ 13 3.3 试剂的配制 ...................................................................................................................... 13 3.4 铟回收工艺流程图 ............................................................................................................ 13 3.5 试验过程 ............................................................................................................................ 14 3.6 结果处理与计算 ................................................................................................................ 16 3.7 小 结 ............................................................................................................................ 18 第四章 结 论 ...................................................................................................................... 19 第五章 致 谢 ...................................................................................................................... 20 参考文献 .................................................................................................................................... 21 附件(英) ................................................................................................................................ 32 附件(中) ................................................................................................ 错误!未定义书签。