2020慢性胰腺炎的内镜治疗
- 格式:doc
- 大小:60.50 KB
- 文档页数:16

胰腺疾病内镜介入诊治新技术近年来胰腺疾病的发病率有逐渐上升趋势,但传统的诊疗方法在胰腺疾病的诊治方面存在许多不足:如对早期胰腺癌诊断困难,往往使病人失去手术根治性切除的机会,进展期胰腺癌对放疗、化疗等传统治疗方法的疗效非常有限;在胆源性重症急性胰腺炎、慢性胰腺炎等疾病的治疗方面也存在很大局限。
近年来,随着内镜介入技术的发展与创新,内镜下微创介入诊治技术为胰腺良恶性疾病的诊断和治疗提供了新的途径和方法,并已经成为一个介于传统内科学和外科学之间的临床诊疗体系,具有安全、有效、简便、并发症低等优点,使胰腺疾病的诊治技术发生了一个质的飞跃,在一定程度上已取代传统的外科手术,成为胰腺疾病诊治中的一个重要手段。
本文拟对该领域近年发展起来的新技术作一简要介绍。
1治疗性ER C P技术治疗性E RCP主要包括内镜鼻胆/胰管引流术、胆/胰管支架内引流术、十二指肠乳头括约肌切开术(E S T)、O dd i括约肌球囊扩张术、胰管括约肌切开术(E PS)、经内镜胆/胰管碎石和取石术、胆/胰管扩张术等。
经过近20年来的不断发展和完善,治疗性E RCP技术已经逐步成熟,并替代了许多难度较大的外科手术,成为胰腺疾病重要的治疗技术与方法[1,2]。
近10年来,众多研究对疑有胆源性急性胰腺炎患者实行早期(发病后24~72小时内)E RCP检查及治疗已达成共识。
绝大多数学者认为,胆源性重症急性胰腺炎的患者应在48小时内行急诊E RCP,以解除胆源性梗阻因素,使胆胰管内压力迅速下降,从而阻断急性胰腺炎的病理过程,使胰腺和全身病理损害减轻或逆转,并减少并发症的发生。
早期内镜治疗胆源性急性胰腺炎的临床意义还表现在阻断轻症急性胰腺炎的重症化上。
S ch m id t等[3]的研究表明,胆胰共同通道的梗阻可加重胰腺炎,超过48小时常致胰腺的广泛出血和坏死。
Fio cca[4]等在比较了重症急性胆源性胰腺炎24小时内行E RCP与先保守治疗,72小时再行E RCP的治疗效果后,推荐急性胆源性胰腺炎发病后24小时内一旦确诊应立即行E RCP及E ST,以降低术后并发症的发生率和病死率。




慢性胰腺炎诊断标准慢性胰腺炎是一种常见的胰腺疾病,临床上常见的症状包括腹痛、消化不良和体重下降。
对于慢性胰腺炎的诊断,医生需要根据一系列的临床表现和检查结果来进行判断。
本文将介绍慢性胰腺炎的诊断标准,帮助医生更好地诊断和治疗患者。
一、临床表现。
慢性胰腺炎的临床表现多样,常见的症状包括腹痛、恶心、呕吐、消化不良、腹泻、体重下降等。
腹痛是慢性胰腺炎最常见的症状,常呈顽固性、持续性,并可放射至背部。
消化不良表现为脂肪泻、脂肪泻和腹胀等。
此外,患者还可能出现黄疸、糖尿病等并发症。
二、影像学检查。
影像学检查是慢性胰腺炎诊断的重要手段,包括腹部超声、CT、MRI等检查。
影像学检查可以帮助医生观察胰腺的形态、结构和密度,发现胰腺的炎症、囊肿、钙化等病变。
此外,影像学检查还可以排除其他疾病,如胆囊炎、胆管结石等。
三、实验室检查。
实验室检查是慢性胰腺炎诊断的重要依据,包括血清淀粉酶、血清脂肪酶、血清胰蛋白酶等指标。
血清淀粉酶和脂肪酶的升高是慢性胰腺炎的特征性表现,有助于诊断和评估疾病的严重程度。
此外,实验室检查还可以检测血糖、血清钙、血清镁等指标,帮助评估患者的营养状况和并发症。
四、内镜检查。
内镜检查是慢性胰腺炎诊断的重要手段,包括内镜超声、内镜逆行胰胆管造影等检查。
内镜检查可以直接观察胰腺的病变,包括炎症、囊肿、钙化等,并可以进行组织活检,明确诊断。
此外,内镜检查还可以进行治疗性操作,如引流、扩张等,缓解患者的症状。
五、诊断标准。
根据临床表现、影像学检查、实验室检查和内镜检查的结果,慢性胰腺炎的诊断需要符合以下标准,1)符合慢性胰腺炎的临床表现;2)影像学检查显示胰腺的病变;3)实验室检查显示血清淀粉酶或脂肪酶的升高;4)内镜检查显示胰腺的病变。
只有同时符合以上标准,才能确诊慢性胰腺炎。
六、结语。
慢性胰腺炎是一种临床常见的疾病,诊断需要综合临床表现、影像学检查、实验室检查和内镜检查的结果。
只有全面了解患者的病情,才能做出准确的诊断和制定有效的治疗方案。

年ERCP术后胰腺炎治疗的药物选择策略胰腺炎是一种胰腺疾病,其特征是急性或慢性的胰腺炎症反应。
胆道结石或梗阻是胰腺炎的常见原因之一。
ERCP(内镜下胆道引流术)是一种常用于解除胆道梗阻的介入治疗方法。
然而,ERCP术后胰腺炎的发生率较高,因此需要合理的药物选择策略来进行治疗。
本文将探讨年ERCP术后胰腺炎治疗的药物选择策略。
1. 胰排特(丙氨酸胰酶)胰排特是丙氨酸胰酶,是一种治疗胰腺疾病的常用药物。
它可以通过补充胰酶,帮助消化食物,减轻胰腺负担,促进胰腺功能的恢复。
在ERCP术后胰腺炎治疗中,胰排特可以起到改善胰腺消化功能的作用,有助于缓解炎症反应。
2. 肠溶性片剂由于ERCP术后胰腺炎患者的消化功能受到一定程度的损害,因此在药物选择上应优先考虑使用肠溶性片剂。
肠溶性片剂可以延迟药物在胃内释放,直接进入小肠,避免了酸性环境对药物的影响,提高药物的吸收率和生物利用度。
因此,在ERCP术后胰腺炎治疗中,选用肠溶性片剂可以增加药物的疗效。
3. 胰泰隆(索拉非尼)胰泰隆是一种多靶点酪氨酸激酶抑制剂,可以抑制肿瘤的生长和血管生成,对于胰腺炎的治疗也具有一定的作用。
研究发现,胰泰隆可以减轻胰腺炎引起的炎症反应,降低炎症介质的释放,减少胰腺组织的坏死和纤维化。
因此,在年ERCP术后胰腺炎的治疗中,胰泰隆可以作为辅助药物使用,帮助缓解炎症反应。
4. 耐汉(罗格列酮)耐汉是一种胰高血糖素样肽-1(GLP-1)受体激动剂,常用于治疗2型糖尿病。
研究发现,耐汉可以通过促进胰岛素的分泌,调节血糖水平,对于控制胰腺炎引起的高血糖有一定的作用。
在ERCP术后胰腺炎治疗中,耐汉可以作为辅助药物使用,帮助控制胰腺炎引起的高血糖,维持血糖的稳定。
5. 静脉营养支持在严重的ERCP术后胰腺炎患者中,可能存在不良的肠道吸收功能,导致营养不良和体重下降。
此时,可以考虑给予静脉营养支持,通过静脉途径输入充足的营养物质,维持患者的营养状态,促进患者的康复。


如对您有帮助,可购买打赏,谢谢自身免疫性胰腺炎的治疗方法
导语:大家肯定都知道什么是胰腺,胰腺对于我们人体有着非常重要的作用,我们的胰腺起到了中和胃酸和蛋白质等功能,如果我们的胰腺出现了问题,那
大家肯定都知道什么是胰腺,胰腺对于我们人体有着非常重要的作用,我们的胰腺起到了中和胃酸和蛋白质等功能,如果我们的胰腺出现了问题,那么将给我们的身体带来多方面的麻烦,胰腺容易出现的一种病症就是胰腺炎,自身免疫性胰腺炎是胰腺炎里面的一种,下文我们介绍一下自身免疫性胰腺炎的治疗方法。
1.外科治疗
胰腺结石病例和难治性疼痛及合并假性囊肿时进行手术治疗,此外肿瘤形成性胰腺炎和胰腺癌不能鉴别时也要进行手术治疗。
肿瘤形成性胰腺炎中含有自身免疫性胰腺炎,这个类型的胰腺炎多,明显的胆管狭窄,不能抑制的黄疸,胰腺无法切除时,可行胆管空肠吻合术。
2.内镜治疗
急性期由于胰腺炎症末端胆管变细,胆汁流出不畅,在内镜下进行内造瘘术和外造瘘术,改善肿大的胰腺。
3.药物治疗
急性期对急性胰腺炎要给予治疗,禁食,高热量静脉输液,抗胰酶制剂治疗。
在缓解期,药物可静脉和口服交替使用,如出现腹痛等临床症状可应用镇静药。
胰腺进行性萎缩时胰腺的外分泌功能低下,可给消化酶治疗。
慢性胰腺炎一般不用类固醇激素治疗,但是,当有其他自身免疫性疾病和自身免疫性胰腺炎时,类固醇治疗是有效的。
一般经口服给药,从每天30~40mg开始,观察治疗症状反应,每间隔2周左右逐渐减量
预防疾病常识分享,对您有帮助可购买打赏。

慢性胰腺炎疼痛的内镜治疗进展
刘宏;邓明明
【期刊名称】《西南军医》
【年(卷),期】2009(11)6
【摘要】@@ 内窥镜治疗胰腺炎疼痛是保持胰管通畅,降低胰管内压力或内脏神经阻滞等方法来缓解慢性胰腺炎的疼痛.由于具有损伤小、痛苦少、恢复快、疗效确切等优点,近年已在理论和实践上得到迅速发展,成为慢性胰腺炎疼痛的治疗新策略.【总页数】4页(P1106-1109)
【作者】刘宏;邓明明
【作者单位】泸州医学院消化内科,四川,泸州,646000;泸州医学院消化内科,四川,泸州,646000
【正文语种】中文
【中图分类】R657.5+1
【相关文献】
1.慢性胰腺炎的内镜治疗进展 [J], 高峻
2.慢性胰腺炎内镜治疗进展 [J], 唐艳萍;李方儒
3.慢性胰腺炎内镜治疗进展 [J], 李兆申
4.儿童慢性胰腺炎内镜治疗进展 [J], 吕彦玮;王丹;胡良皞
5.慢性胰腺炎疼痛的药物治疗进展 [J], 杨振;王腾;胡良皞
因版权原因,仅展示原文概要,查看原文内容请购买。

慢性胰腺炎内镜治疗的研究进展谭学明;张银;马丽梅;何晓露(综述);范志宁(审校)【期刊名称】《中国微创外科杂志》【年(卷),期】2015(15)5【摘要】消化内镜治疗慢性胰腺炎( chronic pancreatitis ,CP)已有10多年的历史,常见方法有内镜下胰管括约肌切开术、内镜下胰管扩张和胰管支架植入术、超声内镜引导下腹腔干神经节的阻滞等。
内镜治疗CP可以有效缓解疼痛,改善胰腺的功能,从一定程度上可替代外科治疗。
多数CP伴有胰胆管的其他病变特征,包括胰管结石、胆总管狭窄、胰腺假性囊肿等,病情发展均可引起相应的症状并与CP互为因果。
综合考虑治疗效果、并发症发生率及患者术后生活质量等,内镜下治疗可以作为CP及其伴发症的首选治疗方案。
%There have been more than10 years since endoscopy was used to treat the chronic pancreatitis , including endoscopic pancreatic sphincterotomy , dilatation of pancreatic duct , endoscopic pancreatic stent deployment , etc. Endoscopic management could relieve the pain caused by chronic pancreatitis effectively , and improve the pancreatic functions .In other words , it could substitute the surgical therapy to some extent .Most cases with chronic pancreatitis were accompanied with other diseases , such as pancreatic duct stones , stricture of common biliary duct , and pancreatic pseudocyst , which also caused these symptoms and interacted as both causes and effected with chronic pancreatitis .Considering the efficacy of treatment , complication incidence and quality of life of patients, we find thatendoscopic management can be chosen as the first treatment method for chronic pancreatitis and its co -morbidities .【总页数】6页(P455-459,464)【作者】谭学明;张银;马丽梅;何晓露(综述);范志宁(审校)【作者单位】南京医科大学第二附属医院消化医学中心,南京 210029;南京医科大学第二附属医院消化医学中心,南京 210029;南京医科大学第二附属医院消化医学中心,南京 210029;南京医科大学第二附属医院消化医学中心,南京 210029;南京医科大学第二附属医院消化医学中心,南京 210029【正文语种】中文【中图分类】R657.5+1【相关文献】1.慢性胰腺炎流行病学特征与内镜治疗研究进展 [J], 郝峻烽;胡良皞;李兆申2.《2018年欧洲胃肠内镜学会指南更新:慢性胰腺炎的内镜治疗》摘译 [J], 李家速; 李宛桐3.慢性胰腺炎的内镜治疗 [J], 刘雨;胡良皞4.儿童慢性胰腺炎内镜治疗进展 [J], 吕彦玮;王丹;胡良皞5.内镜治疗慢性胰腺炎患者疗效观察 [J], 王叶;蓝宇;高岩因版权原因,仅展示原文概要,查看原文内容请购买。
2022慢性胰腺炎的治疗推荐建议(第一部分)慢性胰腺炎(chronicpancreatitis,CP)是指胰腺实质持续性炎症,导致腺体广泛纤维化、腺泡和胰岛细胞萎缩,致使胰腺的内分泌、外分泌功能受损,且常有钙化及假性囊肿形成。
典型症状为反复腹痛、消化不良、腹泻、消瘦等,晚期可出现胰腺囊肿、糖尿病或黄疸。
因本病缺乏简便而特异的诊断方法,故诊断困难,常被误诊。
2021版日本慢性胰腺炎指南修订版基于2019年日本慢性胰腺炎诊断标准进行了修订,主要针对慢性胰腺炎的诊断和治疗提供指导建议。
本文对指南「诊断」部分的要点进行了梳理。
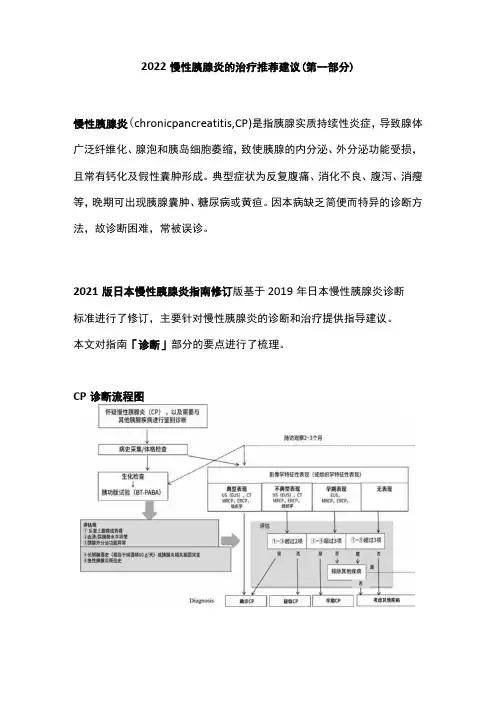
CP诊断流程图★①~⑤中两项阳性且提示早期CP的影像学结果的病例中排除其他疾病时,需对早期CP的疑似病例进行仔细随访。
BT-PABA,胰功肽试验CT,X线计算机体层摄影CP,慢性胰腺炎ERCP z内镜下逆行胆胰管造影术EUS,内镜超声MRCP z磁共振胰胆管造影术US,超声检查诊断要素包括影像学特征性表现、组织学特征性表现和5个评估要素。
如果患者内镜超声(EUS)x内镜下逆行胆胰管造影术(ERCP)或磁共振胰胆管造影术(MRCP)具有早期CP的特征性表现且5个评估项目中符合任意3项,则诊断为早期CP o 腹部超声可用于诊断结石、胰管扩张和胰腺萎缩,但如果患者身体状况较差,通常难以观察到这些特征。
一项系统性综述发现,腹部超声的敏感度为67%(95%CI53-78%),明显低于其他诊断成像方法。
美国的一项研究发现,当根据内镜超声(EUS)诊断CP的标准系统Rosemont分类评估胰管和实质中的发现时,敏感度增加到81%,特异度增加到97%o CT可用于诊断CP,但难以诊断早期CP。
尽管腹部CT的诊断能力劣于EUS,但据报告,腹部CT可用于CP的诊断。
在对用于CP的各种诊断成像方法的系统综述中,腹部CT的敏感度为75%,特异度为91%,表明其具有极好的诊断能力。
当怀疑早期CP时,CT很难发现胰腺实质的细微改变,应加用EUS评估。
胰腺炎的症状与治疗胰腺炎,对于我们来说陌生又熟悉。
陌生是因为由于胰腺所在的位置原因导致我们常把胰腺炎和其它疾病混淆,熟悉是因为我们大家都知道胰腺是人体的第二大消化器官,它所分泌的胰液是人体最重要的消化液。
那么胰腺炎是什么呢?一、你知道什么是胰腺炎吗?胰腺炎分为急性和慢性两种。
急性胰腺炎是常见的急腹症之一,通俗地讲胰腺炎就是在人体胰腺部位的炎症,其发病仅次于急性阑尾炎、急性胆囊炎胆石症、肠梗阻,多见于青壮年,女性发病率高于男性;由于胰腺因胰蛋白酶的自身消化作用而引起的疾病我们称之为胰腺炎,胰腺炎患者常出现腹痛、腹胀、发热、恶心、呕吐等症状,并且在化验尿和血的过程中会出现淀粉酶含量升高等现象。
现代人吃饭的不规律很容易引起急性胰腺炎,那么当我们患上胰腺炎时身体又会给我们传达怎样的信号呢?二、急性胰腺炎的症状急性胰腺炎患者多有胆道疾病史或暴饮暴食的症状。
急性胰腺炎若为出血坏死型其死亡率极高,但也很少见1、突然的腹痛突发的腹痛是急性胰腺炎最主要的症状,常位于中上腹部,有时也会向腰背部呈束带状放射,前倾坐位或弯腰时可以减缓疼痛,仰卧位时疼痛加重。
急性胰腺炎的患者大约有95%的比例都会出现此症状,常在饱餐后或大量饮酒后发作,轻一点的为钝痛,严重者呈现持续性绞痛或刀割样痛,一般的止痛剂无效,少数患者仅有胰区压痛或无痛,属于无痛性急性胰腺炎。
2、恶心、呕吐约有三分之二的急性胰腺炎患者起病就会恶心、呕吐,有些甚至会呕吐出胆汁,并且患者在呕吐过后并不会消除腹痛症状。
3、发烧大多数急性胰腺炎患者会伴随有38℃一39℃,状态持续3-5天不等的发烧,坏死出血型患者体温多在40℃左右,逐日升高或持续不退,可能怀疑有胰腺或腹腔的继发感染。
4、脱水患者还会出现脱水的现象,代谢性碱中毒对于频繁呕吐的患者来说也是可发生的。
低钙血症、代谢性酸中毒、低血钾、血糖升高、低血镁等问题也是也伴随重症胰腺炎患者而发生。
5、休克休克多见于出血坏死型病患,多表现为冒冷汗、四肢冰冷、脸色泛白等症状,一般是突发或者间接发生的,休克的发生原因可能是胰腺组织及腹腔内出血、胰液的外溢刺激了腹膜或者由于组织坏死,蛋白质分解引起的机体中毒等,若不及时抢救可以致人死亡。
慢性胰腺炎的症状及治疗,带你了解专业知识我们每个人都生活在复杂的环境中,所有人的身体都有可能会出现一些疾病,所以要懂得这些疾病的相关知识,比如慢性胰腺炎这种疾病,最起码要懂得相应的症状表现以及治疗方法。
★一、慢性胰腺炎表现1.腹痛是主要临床症状。
腹痛剧烈,起始于中上腹,也可偏重于右上腹或左上腹,放射至背部。
累及全胰则呈腰带状向腰背部放射痛。
饮酒诱发的胰腺炎常在醉酒后12~48小时期间发病,出现腹痛。
胆源性胰腺炎常在饱餐之后出现腹痛。
2.恶心、呕吐常与腹痛伴发呕吐剧烈而频繁。
呕吐物为胃十二指肠内容物,偶可伴咖啡样内容物。
3.腹胀早期为反射性肠麻痹,严重时可由腹膜后蜂窝织炎刺激所致。
邻近胰腺的上段小肠和横结肠麻痹扩张。
腹胀以上腹为主,腹腔积液时腹胀更明显,患者排便、排气停止,肠鸣音减弱或消失。
4.腹膜炎体征水肿性胰腺炎时,压痛只限于上腹部,常无明显肌紧张。
出血坏死性胰腺炎压痛明显,并有肌紧张和反跳痛,范围较广或延及全腹。
5.其他初期常呈中度发热,约38℃。
合并胆管炎者可伴寒战、高热。
胰腺坏死伴感染时,高热为主要症状之一。
黄疸可见于胆源性胰腺炎,或者由于胆总管被水肿的胰头压迫所致。
★二、慢性胰腺炎治疗1.治疗原则去除病因,控制症状,纠正改善胰腺内外分泌功能不全及防治并发症。
2.非手术治疗(1)一般治疗戒烟戒酒,调整饮食结构,避免高脂饮食,可补充脂溶性维生素及微量元素,营养不良者可给予肠内或肠外营养支持。
(2)胰腺外分泌功能不全治疗患者出现脂肪泻、体重下降及营养不良表现时,需要补充外源性胰酶制剂,改善消化吸收功能障碍。
首选含高活性脂肪酶的微粒胰酶胶囊,建议进餐时服用,正餐给予(3~4)万U脂肪酶的胰酶,辅餐给予(1~2)万U脂肪酶的胰酶。
效果不佳可增加剂量或联合服用质子泵抑制剂。
(3)胰腺内分泌功能不全治疗根据糖尿病进展程度及并发症情况,一般首选二甲双胍控制血糖,必要时加用促胰岛素分泌药物,对于症状性高血糖、口服降糖药物疗效不佳者选择胰岛素治疗。
超声内镜引导下胰管穿刺引流术的临床应用对于慢性胰腺炎、胰肠吻合口狭窄、胰腺肿瘤压迫等原因导致的胰液排出受阻、上游胰管高压的患者,传统治疗方案主要是内镜逆行胰管造影(endoscopic retrograde pancreatography, ERP)并支架植入、外科手术切除并重建、经皮穿刺胰管引流3种。
其中外科手术创伤大,经皮穿刺引流并发症发生率高,因此对于ERP治疗失败的症状性胰管高压患者,一种新的可选择的治疗方案——超声内镜引导下胰管穿刺引流术(endoscopic ultrasound guided pancreatic duct drainage,EUS-PDD)越来越受到临床医师的关注。
近5年来,随着治疗性超声内镜的发展、新的配套器械设备的出现以及多个中心临床数据的发表,人们对于EUS-PDD有了更新的认识。
本文结合笔者团队的临床实践及文献报道,重点讨论EUS-PDD在慢性胰腺炎合并症状性胰管高压、胰肠吻合口狭窄等方面的临床应用及其进展,以期为临床医师进一步认识、选择、应用该技术提供参考。
一. 概述得益于治疗性超声内镜的发展,特别是在超声内镜引导下胰腺囊性肿物穿刺引流术广泛应用的基础上,EUS-PDD应运而生,于2002年由Francois等首先报道。
EUS-PDD是指在线阵超声内镜引导下,经胃或肠向主胰管穿刺、造影、置入导丝并建立引流道的一种治疗方式。
目前临床常用的术式主要有两种,即应用会师技术经十二指肠乳头或胰肠吻合口引流术(EUS-guided rendezvous, EUS-RV)以及直接经胃或肠壁引流术(EUS-guided transmural drainage, EUS-TMD)。
前者是指导丝经穿刺点从胰管上游向下游方向越过狭窄段、通过乳头或吻合口进入肠腔,从而指导和辅助内镜下逆行建立引流道并支架植入;后者是指经胃或肠与主胰管之间直接建立引流道并支架植入,支架远端指向胰头者称顺行支架植入(anterograde),指向胰尾者称逆行支架植入(reterograde)。
中医辨证分型治疗慢性胰腺炎慢性胰腺炎由于多种因素引发的节段性、局限性、弥漫性慢性炎症,会导致患者的胰管组织以及胰腺实质出现不可逆损害,并导致胰腺分泌功能出现障碍,就现阶段来看,关于胰腺炎的病理原因、生理原因、发病原理还不清楚,治疗慢性胰腺炎的常见方式有内镜疗法、外科手术疗法、药物疗法等,手术疗法虽然有效率较高,但是往往会给患者造成较大的损伤。
而中医辨证分型疗法可以有效缓解患者的症状,成效更加理想。
1 慢性胰腺炎的中医发病原因与机制慢性胰腺炎的特点以胰腺组织纤维化、胰腺实质消失、慢性炎症为主,在中医范畴内,慢性胰腺炎属于胁痛、腹痛、腹泻以及胃脘痛范畴,病位与肝、胆、脾胃相关。
牛春风的研究显示,慢性胰腺炎病机虚实夹杂,病程长多为肝郁脾虚,病程短则与肝脾郁热有关,慢性胰腺炎病变与一般腹泻相似,病变位置集中在大小肠与脾胃中,多由于脾虚湿盛有关。
李厚根的研究显示,慢性胰腺炎的发病原因主要由于饮食不节、情志不畅引发,慢性胰腺炎的临床表现多种多样,但是其病变位置主要在脾胃。
总而言之,慢性胰腺炎的发病机制与肝脾不调、脾胃虚弱相关,其标则为食积、血瘀、气滞、湿热、痰浊。
2 中医辨证分型治疗慢性胰腺炎的方式在中医角度而言,慢性胰腺炎属于胃脘痛、腹泻、胁痛、腹痛范畴,根据中医辨证治疗理论,对于慢性胰腺炎的治疗可以采取如下的措施:2.1 肝脾论治疗法研究显示,偏食者为肝胆郁热、胃和失调,可使用金钱草、茵陈、制大黄、炒山栀、柴胡、黄岑等进行治疗;对于偏虚者,为气血瘀滞、脾馁肝横导致,可采用益气祛瘀、扶脾柔肝法进行治疗,常用药物有炒白术、炒党参、佛手片、茯苓、姜半夏等。
李厚根等对78 例慢性胰腺炎患者采用升阳益胃法进行治疗,取得了良好的效果,升阳益胃汤药物组方有党参、炒白术、生甘草、泽泻、云苓、陈皮、生黄芪等,治疗有效率达到了93.7%。
其治疗机理包括几个方面,即消导和中,疏肝理气;行气活血,清泻脾胃,出了升阳益胃汤外,常用的药方还有大承气汤、柴胡疏肝散、柴芍六君子汤等等。
2020慢性胰腺炎的内镜治疗慢性胰腺炎是胰腺进行性、炎症性疾病,病理特征为胰腺组织不可逆的纤维化,可出现主胰管狭窄、胰管结石等特征性病理改变,病程中常伴发胰腺内、外分泌功能下降。
胰管结石和主胰管狭窄可导致胰液引流不畅,引起胰管高压,患者反复发作腹痛,生活质量降低。
慢性胰腺炎的治疗方式包括内镜治疗、外科手术治疗和药物保守治疗。
随着近年来内镜技术的发展,内镜治疗创伤小、安全性高、疗效尚可,已成为慢性胰腺炎一线治疗手段。
目前内镜治疗主要用于解除胰管结石导致的胰管梗阻、改善主胰管狭窄、引流胰腺假性囊肿、处理慢性胰腺炎继发良性胆管狭窄,以及进行腹腔神经丛阻滞以缓解腹痛。
1胰管结石的内镜治疗胰管结石是矿物质在胰管中积聚,可能导致胰管梗阻,从而继发胰管高压,激活炎症反应过程,加重胰腺组织纤维化。
胰管结石分为阳性和阴性结石。
以钙盐为主要成分的是X线不可穿透的阳性结石;以蛋白栓成分为主的是X线可穿透的阴性结石。
绝大部分(>95%)胰管结石为阳性结石[1]。
本中心前期研究[2]发现,慢性胰腺炎确诊后胰管结石发生率逐渐增高,慢性胰腺炎确诊15年时,胰管结石发生率为75.3%。
胰管结石的内镜治疗目的是去除结石,解除梗阻。
最直接的方法为逆行进入胰管,通过取石球囊、取石篮去除结石。
胰括约肌切开术可促进较大结石排出,但此方法有一定局限性。
当结石直径大、位置分散、结石嵌顿或狭窄上游有结石时,取石常会失败[3]。
结石可能导致取石网篮嵌顿,结石碎片可能导致取石球囊破裂,括约肌切开术也可能导致术后出血、胰腺炎、穿孔或括约肌狭窄等并发症[4-5]。
上述内镜治疗方法无法处理直径大于5 mm的结石,此类较大结石常需辅助技术或辅助设备进行碎石。
经内镜机械碎石可在特殊设计的导管或者取石篮内粉碎结石,该方法常有一定效果,但可能发生严重并发症[6]。
其他导管内碎石技术比如液电碎石和激光碎石亦被应用于胰管结石的治疗[7-8]。
SpyGlass是一种新型的子镜系统,不同于以往胆管镜及胰管镜系统。
随着SpyGlass系统的发展,胆管镜检查的技术不断进步,第一代SpyGlass 系统是一个可重复使用的单操作光纤镜,包括一个用于辅助仪器和冲洗功能的通道,其外工作直径为3.3 cm,长度为230 cm,可与标准十二指肠镜配合使用,其附件端口允许使用活检钳和液电或激光碎石探头等工具,但图像清晰度欠佳。
2015年,第二代SpyGlass系统问世,提供了4倍的分辨率和更宽阔视野的数字图像,且图像的清晰度更好。
此外,它还包括一个全新设计的附件通道,更容易使用[9]。
SpyGlass系统可用于导管内乳头状瘤可视化诊断、胰管狭窄评估、胰管结石可视化诊断及去除。
一项应用SpyGlass监测肿瘤生长13年的研究[10]显示,79例患者行胰管镜评估胰管病变,其检测肿瘤生长的敏感度为87%,应用SpyGlass可视化引导下的组织活检后,敏感度升至91%。
Attwell等[11]采用SpyGlass可视化引导下激光碎石术治疗胰管结石,79%患者结石完全清除,89%患者腹痛改善、止痛药使用减少、住院次数减少。
在一项慢性胰腺炎患者内镜治疗的研究[12]中,共行内镜治疗280次,其中15例患者接受了30次SpyGlass可视化引导下胰管镜检查及治疗,结果分别有73%(11/15)和27%(4/15)患者结石完全清除和部分清除,有13次内镜治疗后发生了并发症。
上述导管内碎石技术有一定优势,但也存在并发症,且治疗费用相对较高,因此不作为一线治疗手段。
体外震波碎石术(ESWL)联合内镜被证明是清除胰管结石的有效方法[13]。
有证据[14]表明单纯ESWL对疼痛性钙化性慢性胰腺炎有较好疗效,且花费较低。
2018版欧洲胃肠内镜学会(ESGE)慢性胰腺炎内镜治疗指南[15]推荐直径大于5 mm的胰头/体部阳性结石应用ESWL治疗,阴性结石或直径小于5 mm的阳性结石应用经内镜逆行胰胆管造影(ERCP)治疗。
一项荟萃分析[16]报道,ESWL治疗的患者,分别有70%和22%主胰管结石被完全清除或部分清除,治疗后2年,52.7%患者腹痛完全缓解,33.4%患者有轻中度腹痛,ESWL治疗后88.2%患者生活质量改善。
上海长海医院消化内科是国内率先开展ESWL治疗慢性胰腺炎的机构,截止目前已进行六千余例次ESWL治疗慢性胰腺炎患者,安全性和有效性较好,在本中心前期报道[13]中,214例慢性胰腺炎患者接受了473次ESWL治疗,最终72.4%患者胰管结石完全清除,90.8%慢性胰腺炎患者获得成功胰管减压,经过平均18.5个月随访后,各有71.3%和24.0%患者疼痛完全缓解与部分缓解,ESWL治疗明显改善了患者生活质量。
在另一报道[17]中,1470例次ESWL术后并发症发生率为6.7%,中至重度并发症发生率为1.1%,除1例患者发生胰瘘,未见其他罕见并发症;1例发生肝包膜下血肿的患者行经皮血肿穿刺引流,其余患者均经过密切观察和保守治疗恢复,可见ESWL具有良好的安全性。
本中心也通过这项报道在国际上首次提出ESWL术后并发症的分类,包括ESWL术后急性胰腺炎、出血、感染、石街(ESWL术后主胰管内较多胰腺结石排在一起,形成一长串胰腺结石,导致胰管梗阻,胰液引流不畅,患者出现保守治疗无法缓解的腹痛,常需急诊ERCP治疗)、穿孔,其中ESWL术后急性胰腺炎最常见,在1470次ESWL治疗后发生率为4.4%,感染发生率为1.4%,石街、穿孔、出血相对少见,发生率分别为0.4%、0.3%、0.3%。
ESWL术后罕见并发症包括:ESWL术后肝包膜下血肿形成[18]、肠系膜血肿形成[19]、结肠血肿形成[20]。
上述ESWL治疗并发症的发生大多缘于冲击波对周围脏器的损伤,目前冲击波打击频率是恒定的,在碎石过程中,胰腺位置随着人体呼吸运动而变化,并且患者在麻醉过程中也可能发生不自主肢体运动,如果结石位置随人体运动发生变化,冲击波即可能打到正常组织,导致损伤发生;另外,冲击波所途经的器官也会受到影响,从而发生出血、穿孔等并发症。
目前对不同形态、不同理化特性胰管结石的ESWL治疗均为同质化治疗,其碎石参数(冲击波能量、频次、入射角度)设置相同,临床发现不同患者之间疗效差异大,治疗成本与风险增加;此外,同一患者伴发多个胰管结石时,不同结石的治疗紧迫性和先后顺序是依据医师个人经验判断,缺乏相应的标准和规范;目前碎石治疗方案中碎石时长达60 min,碎石过程中结石位置随呼吸运动变化,存在大量“空打”现象(空打率>40%),造成碎石效率较低,严重时出现脏器损伤,患者进行镇静麻醉后身体有自主或不自主运动,结石会移出碎石区域,故每3 min需要进行X线定位,对医生和患者造成的辐射量大。
综合上述问题,本学科团队与上海交通大学、同济大学、深圳慧康医疗器械有限公司联合,试图制订结石个性化治疗流程,减少“空打”现象,降低患者辐射剂量,全面评估结石危害系数、碎石参数、治疗风险等,并且利用红外线探测患者体位变化或结石位置变化,建立胰管结石自动追踪系统,提高冲击波打击精确度,减少对周围脏器的损伤。
1996年一项日本的研究[21]报道了单行ESWL治疗胰管结石,79%(22/28)患者在44个月随访时腹痛缓解。
后来大部分研究均报道了ERCP联合ESWL治疗,并发现二者联合可提高胰管结石清除率。
在既往研究[22]中,初始内镜取石失败的患者经过ESWL治疗后,超过80%患者再次ERCP取石成功。
一项回顾性研究[23]发现,尝试ERCP治疗前先行ESWL碎石是结石成功清除的独立影响因素。
因此,单纯采用ERCP治疗时需选择性应用,可用于预期取石成功率较高的患者或难以进行ESWL治疗的患者,如阴性结石、直径<5 mm的胰管结石或难以用X线定位结石的情况。
ESWL术后是否必须行内镜治疗?Vaysse等[24]研究结果显示,单行ESWL治疗与ESWL联合内镜治疗的患者腹痛缓解率无明显差异。
一项随机对照临床研究[14]发现,主胰管直径的减小和腹痛发作频率的降低在单行ESWL组和ESWL联合内镜组无明显差异,ESWL联合内镜治疗的患者住院时间更长,治疗费用更高。
上述两项研究发现ESWL后辅助内镜治疗较单行ESWL并未带来更多获益,但目前ESWL术后是否需行ERCP尚无定论。
本中心在开展相应的临床研究,比较单行ESWL与ESWL 联合ERCP治疗的效果,通过大宗随机对照临床研究有望得出更确切的结论。
总之,上述内镜技术在胰管结石患者中疼痛缓解率可达65%[25]。
直径<5 mm的胰管结石可尝试直接取石,直径>5 mm的胰管结石首选ESWL治疗,无法开展ESWL的机构可尝试胰管镜下SpyGlass机械碎石等。
内镜导管内机械碎石术不推荐使用。
外科手术不是单纯取石的主流观点,其常用于可疑恶性病变、胆管狭窄、内镜治疗后腹痛症状持续无法缓解的患者。
2主胰管狭窄的内镜治疗慢性胰腺炎患者常见主胰管狭窄。
通常主胰管狭窄是良性的,恶性主胰管狭窄需考虑恶性疾病。
主胰管狭窄可导致胰管高压,引起腹痛等症状。
显著的主胰管狭窄定义为出现以下任一表现:主胰管上游直径不小于 6 mm;在狭窄上游插入6F导管时造影剂无法流出;从狭窄上游插入的鼻胰管中连续注入1 L盐水持续12~24 h引起腹痛[15]。
主胰管狭窄的主要治疗目标是减轻胰管内压力以缓解腹痛、持续扩张狭窄,治疗方法包括胰管括约肌切开术、狭窄段扩张和放置胰管支架。
Weber等[26]研究纳入了19例胰管狭窄慢性胰腺炎患者,进行内镜胰管括约肌切开、胰管扩张、胰管支架植入治疗,17例患者初始治疗完全成功,且初始治疗完成后疼痛完全或部分缓解,在随访5年时,57%(8/14)患者无胰管狭窄复发,50%(7/14)患者腹痛完全缓解。
一项前瞻性非随机研究[27]报道,在42例显著主胰管狭窄的慢性胰腺炎患者中,接受了临时胰管支架植入的患者随访5年时疼痛复发率为15%,而未接受胰管支架植入的患者疼痛复发率为50%。
植入单根塑料支架常被用作主胰管狭窄初始内镜治疗方法。
植入单根塑料胰管支架后,主胰管狭窄的缓解率可达50%[28]。
一项荟萃分析[29]显示,内镜治疗的536例主胰管狭窄慢性胰腺炎患者即时腹痛缓解率为74.4%(95%可信区间:62.4%~84.0%),长期腹痛缓解率为67.5%(95%可信区间:51.5%~80.2%)。
单根胰管支架放置1年仍存在有症状的显著主胰管狭窄或有症状的显著主胰管狭窄复发定义为难治性主胰管狭窄[15]。
对于这部分难治性主胰管狭窄患者,ESGE推荐可考虑外科手术或多根塑料支架治疗,但需多学科团队讨论权衡不同治疗方案的利弊。
在多支架治疗48例难治性主胰管狭窄的长期随访研究[30]中,患者平均植入胰管塑料支架3枚,支架移除后平均随访9.5年,74.4%(32/43)患者症状完全缓解,25.6%(11/43)在支架移除26.4个月发生了胰腺炎复发或胰性腹痛,其中8例患者未见狭窄复发,3例患者存在狭窄复发。