吉非替尼合成工艺研究
- 格式:pdf
- 大小:679.18 KB
- 文档页数:2
化学抗肿瘤药物经过半个多世纪的发展,已经进入靶向治疗药物时代。
小分子靶向药物在临床上的应用日益增多,在一些肿瘤类别中已经进入一线用药地位,比如肾癌、慢粒白、多发性骨髓瘤等。
本文对小分子靶向治疗药物做一综述。
小分子靶向治疗药物简介一、受体酪氨酸激酶抑制剂作为抗肿瘤药物靶点的酪氨酸激酶有两类,一类是受体酪氨酸激酶(RTKs),另一类是非受体酪氨酸激酶(nrRTKs)。
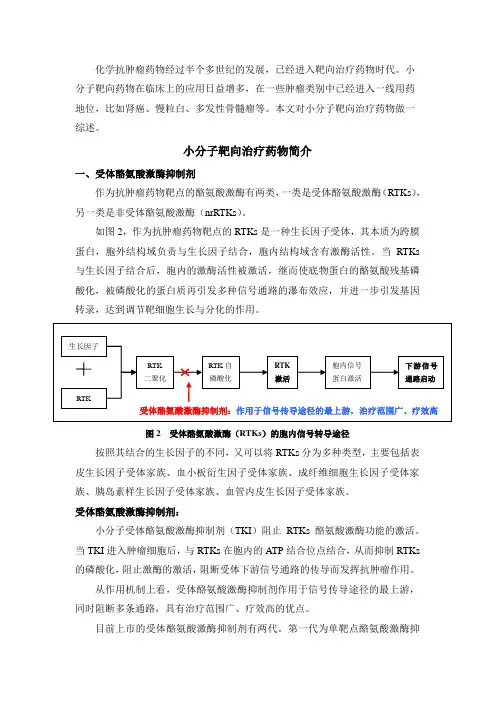
如图2,作为抗肿瘤药物靶点的RTKs是一种生长因子受体,其本质为跨膜蛋白,胞外结构域负责与生长因子结合,胞内结构域含有激酶活性。
当RTKs 与生长因子结合后,胞内的激酶活性被激活,继而使底物蛋白的酪氨酸残基磷酸化,被磷酸化的蛋白质再引发多种信号通路的瀑布效应,并进一步引发基因转录,达到调节靶细胞生长与分化的作用。
图2 受体酪氨酸激酶(RTKs)的胞内信号转导途径按照其结合的生长因子的不同,又可以将RTKs分为多种类型,主要包括表皮生长因子受体家族、血小板衍生因子受体家族、成纤维细胞生长因子受体家族、胰岛素样生长因子受体家族、血管内皮生长因子受体家族。
受体酪氨酸激酶抑制剂:小分子受体酪氨酸激酶抑制剂(TKI)阻止RTKs酪氨酸激酶功能的激活。
当TKI进入肿瘤细胞后,与RTKs在胞内的ATP结合位点结合,从而抑制RTKs 的磷酸化,阻止激酶的激活,阻断受体下游信号通路的传导而发挥抗肿瘤作用。
从作用机制上看,受体酪氨酸激酶抑制剂作用于信号传导途径的最上游,同时阻断多条通路,具有治疗范围广、疗效高的优点。
目前上市的受体酪氨酸激酶抑制剂有两代。
第一代为单靶点酪氨酸激酶抑制剂,如吉非替尼、厄洛替尼。
表已上市的酪氨酸激酶抑制剂注:EGFR:表皮生长因子受体,属HER家族;VEGFR:血管内皮生长因子;PDGFR:血小板衍生因子;HER2:HER家族的一种受体;Abl-Bcr:一种非受体酪氨酸激酶;Raf:酪氨酸激酶的下游信号通路中的一种蛋白;Flt-3:Src:一种非受体酪氨酸激酶;c-kit:Ret:胶质细胞源性神经营养因子的受体吉非替尼为EGFR酪氨酸激酶抑制剂,主要用于非小细胞肺癌,对酪氨酸激酶基因编码区突变型肿瘤的有效率高达80%以上。


表皮生长因子受体酪氨酸激酶抑制剂的研究进展一、本文概述表皮生长因子受体(EGFR)酪氨酸激酶抑制剂(TKIs)是一类针对EGFR信号通路的关键药物,广泛应用于非小细胞肺癌、结直肠癌、头颈癌等多种癌症的治疗。
本文旨在综述近年来EGFR TKIs的研究进展,包括其作用机制、药物研发、临床应用以及面临的挑战等方面。
通过深入了解EGFR TKIs的研究现状和发展趋势,有望为癌症治疗提供新的思路和方法,进一步改善患者的生活质量和预后。
本文将从EGFR TKIs的作用机制出发,阐述其如何通过抑制EGFR 的酪氨酸激酶活性来阻断癌细胞的增殖和转移。
接着,我们将回顾EGFR TKIs的药物研发历程,介绍目前市场上主流的EGFR TKIs药物及其特点。
在此基础上,我们将重点关注EGFR TKIs在临床试验中的应用情况,包括其疗效、安全性以及耐药性等问题。
我们将探讨EGFR TKIs面临的挑战和未来发展方向,包括如何克服耐药性、提高治疗效果以及拓展新的适应症等。
通过本文的综述,我们希望能够为相关领域的研究者和临床医生提供有价值的参考信息,推动EGFR TKIs在癌症治疗中的进一步应用和发展。
二、EGFR-TK抑制剂的分类与机制表皮生长因子受体酪氨酸激酶抑制剂(EGFR-TK抑制剂)是近年来癌症治疗领域的重要突破,其通过抑制表皮生长因子受体(EGFR)的酪氨酸激酶活性,从而阻断细胞的生长、增殖和转移过程。
根据药物的作用机制和化学结构,EGFR-TK抑制剂主要分为两大类:可逆性抑制剂和不可逆性抑制剂。
可逆性抑制剂,如吉非替尼和厄洛替尼,能够与EGFR的ATP结合位点形成可逆性结合,从而竞争性地抑制酪氨酸激酶的活性。
这类药物对于EGFR敏感突变的非小细胞肺癌具有较好的疗效,但在长期治疗过程中,患者往往会出现耐药现象。
不可逆性抑制剂,如阿法替尼和奥希替尼,能够与EGFR的ATP 结合位点形成共价键,导致EGFR的永久性失活。

回生口服液对吉非替尼治疗晚期非小细胞肺癌凝血功能和生活质量的影响杨轩璇;石红兵;胡文蔚;吴骏【期刊名称】《临床荟萃》【年(卷),期】2012(027)023【总页数】4页(P2093-2096)【关键词】癌,非小细胞肺;中成药;回生口服液;吉非替尼【作者】杨轩璇;石红兵;胡文蔚;吴骏【作者单位】常州市第一人民医院肿瘤内科,江苏常州 213003;常州市第一人民医院肿瘤内科,江苏常州 213003;常州市第一人民医院肿瘤内科,江苏常州 213003;常州市第一人民医院肿瘤内科,江苏常州 213003【正文语种】中文【中图分类】R734.2非小细胞肺癌(NSCLC)是我国常见恶性肿瘤之一,其发病率占肺癌80%左右,而且起病隐匿,确诊时60%~70%已属晚期,大部分已失去根治手术和局部放疗的机会。
吉非替尼(gefitinib,易瑞沙)是一种口服的表皮生长因子受体(EGFR)酪氨酸激酶拮抗剂,单药对于中晚期NSCLC患者具有一定的有效率和疾病控制率,但也存在着一定的不良反应。
回生口服液作为一种抗肿瘤中成药广泛应用于临床已有20多年的历史,有直接杀伤肿瘤细胞和增强免疫细胞活性等作用。
我们采用回生口服液联合吉非替尼治疗中晚期NSCLC,取得了较好的临床疗效,现将结果报告如下。
1.1 病例选择2008年9月至2011年2月在我院治疗的晚期NSCLC患者69例,所有患者均有明确的细胞学或病理学诊断,随机分为两组。
对照组36例,男14例,女22例,年龄37~75岁,中位年龄55.1岁;其中腺癌27例,鳞癌8例,其他1例。
研究组33例,男12例,女21例,年龄38~74岁,中位年龄54.7岁;其中腺癌24例,鳞癌7例,其他2例。
两组患者治疗前血常规、肝肾功能、心电图均基本正常,卡氏(Karnofsky,KPS)评分≥60分,预计生存期超过6个月。
两组临床资料经统计学检验,差异无统计学意义(P>0.05),具有可比性。

贝达喹啉合成工艺研究贝达喹啉(Bedaquiline)是一种针对耐药多药性肺结核(MDR-TB)的新型抗结核药物。
它的研发对于解决MDR-TB问题具有重要意义。
下面是关于贝达喹啉合成工艺的研究,详细介绍了其合成路线和工艺参数。
贝达喹啉的合成路线主要包括七个关键步骤:1)嘧啶环的连接;2)芳香杂环的引入;3)蒸发过程中的固化;4)三方合成;5)酉反应;6)催化还原反应;7)异构化。
第一步是嘧啶环的连接。
通过一系列的加和、溶解和蒸发步骤,将4-氨基-2-氯嘧啶和氧乙基苯合成为3-氨基-7-氧乙基-2-(3-甲基-噻吩-2-基)-4H-1,4-联吡啉-1-氧化物。
第二步是芳香杂环的引入。
将3-氨基-7-氧乙基-2-(3-甲基-噻吩-2-基)-4H-1,4-联吡啉-1-氧化物与苯硼酸,通过钯催化交叉偶联反应,合成芳香噻吩衍生物。
第三步是蒸发过程中的固化。
将芳香噻吩衍生物通过溶解、过滤和蒸发等步骤得到固态晶体,这是后续反应的重要中间体。
第四步是三方合成。
通过一系列的步骤,包括加热反应、溶剂挥发和结晶等,将固态晶体与还原剂和硅氧烷反应,生成吉那菲环。
第五步是酉反应。
吉那菲环与气相酉反应,提供稳定的分子结构。
第六步是催化还原反应。
通过添加催化剂,将吉那菲环催化还原,得到具有脱氢基团的贝达喹啉。
最后一步是异构化。
通过一系列的步骤,贝达喹啉进行异构化反应,得到最终的产物贝达喹啉。
通过对贝达喹啉合成工艺的研究,我们可以优化工艺参数以提高合成效率和产量。
例如,选择合适的溶剂和反应条件,可以最大程度地提高产率。
此外,优化催化剂的选择和使用方法,可以使反应更加高效。
此外,为了确保贝达喹啉的合成工艺符合药品生产标准,我们还需要进行质量控制研究。
质量控制研究包括对原料、中间体和最终产品的理化性质进行检测,以确保合成过程中的质量稳定性和纯度。
总之,贝达喹啉合成工艺的研究对于提高MDR-TB的治疗效果具有重要意义。
通过优化合成路线和工艺参数,可以提高贝达喹啉的产量和纯度,为广大患者提供更好的治疗选择。

胡粉青,李翠柏,党菱婧,等. 槲皮素体外抗肺癌作用研究进展[J]. 食品工业科技,2022,43(18):416−424. doi: 10.13386/j.issn1002-0306.2021080017HU Fenqing, LI Cuibai, DANG Lingjing, et al. Research Progress of Anti-lung Cancer Effect of Quercetin in Vitro [J]. Science and Technology of Food Industry, 2022, 43(18): 416−424. (in Chinese with English abstract). doi: 10.13386/j.issn1002-0306.2021080017· 专题综述 ·槲皮素体外抗肺癌作用研究进展胡粉青1,李翠柏1,党菱婧1,邹 澄2,赵 庆3,邵曰凤1,*(1.德宏职业学院,云南芒市 678400;2.昆明医科大学药学院,云南昆明 650599;3.云南中医药大学中药学院,云南昆明 650599)摘 要:槲皮素是一个含有邻二酚羟基和间二酚羟基的黄酮醇类化合物。
为了探析槲皮素体外抗肺癌现状,本文通过国内知网、万方,输入“槲皮素”、“肺癌”、“槲皮素衍生物”等,国外SpringerLink 、PubMed 数据库查阅了“lung cancer ”、“ quercetin ”、“quercetin derivative ”等主题词,检索了近年槲皮素及其衍生物在抗肺癌方面研究的相关数据,综述了其新制剂、衍生物和作用机制。
槲皮素抗肺癌新制剂有纳米粒、纳米乳、纳米胶束、脂质体和其他制剂。
从已合成的120余个槲皮素衍生物中发现了11个对肺癌作用强于槲皮素的化学成分。
通过诱导细胞凋亡、抑制酶的活性、阻滞细胞周期、逆转肿瘤耐药性等作用发挥抗肺癌作用,以期为槲皮素及其衍生物在肺癌方面研究开发利用提供依据。




湖南省娄底市部分学校2022-2023学年高三三模化学试题学校:___________姓名:___________班级:___________考号:___________一、单选题1.化学为推动人类文明和社会进步做出了重要贡献。
下列说法错误的是 A .我国科学家研究的由2CO 到淀粉的全合成有利于实现“碳中和” B .“神舟飞船”返回舱外层材料的酚醛树脂球属于有机高分子材料 C .服装中含有的“Gore -Tex”聚四氟乙烯薄膜面料的单体是卤代烃 D .“光刻技术”的光敏树脂在曝光条件下发生分子间聚合成像是物理变化2.白磷(P 4,结构见图)与Cl 2反应得 PCl 3,PCl 3可继续与Cl 2 反应:PCl 3(g)+Cl 2(g)= PCl 5(g) ΔH <0。
固态 PCl 5中含有4PCl +、6PCl -两种离子。
下列关于 H 2O 、P 4、PCl 3和 4PCl +的说法正确的是A .H 2O 很稳定是因为分子间含有氢键B .PCl 3的空间构型为平面三角形C .P 4与4PCl + 中的键角相同D .H 2O 、PCl 3与4PCl +的中心原子都是sp 3杂化3.下列说法正确的是A .金刚石经锤易碎,原因是共价键具有方向性,外力作用下原子易错位而断裂B .乙醛能与水任意比互溶,原因是其水溶液中形成了3种氢键C .含钙化合物中的钙元素常显正二价,原因是钙的第二电离能小于其第一电离能D .碳原子的轨道表示式为,原因是违反了泡利原理4.宏观辨识与微观探析是化学学科核心素养之一,下列用于解释事实的方程式书写正确的是A .泡沫灭火器喷出白色泡沫用于灭火: 2A13++32-3CO +3H 2O=2Al(OH)3↓+3CO 2↑B .用饱和Na 2CO 3溶液处理锅炉水垢中的CaSO 4: Ca 2++2-3CO =CaCO 3↓C .缠有铜丝的铁钉放入滴有酚酞的NaCl 溶液,铜丝附近溶液变红:O 2+4e -+2H 2O =4OH -A.用装置甲检验该条件下铁发生了吸氧腐蚀B.用装置乙可以来加热熔融的烧碱固体Fe OH胶体和氯化铁溶液C.用装置丙可分离()3D.用装置丁可分离苯(沸点80.1℃)和溴苯(沸点156.2℃)二、未知8.部分含N及Cl物质的分类与相应化合价关系如图所示,下列推断不合理的是A.可以通过a的催化氧化反应制备eB.工业上通过_a→b→c→d→e来制备HNO3C.浓的a′溶液和浓的c′溶液反应可以得到b′D.加热d′的固态钾盐可以产生O2三、单选题9.根据下列图示所得出的结论正确的是)3CaCO AgCl 和2Ag CrO 沉淀显深红色,则由图丙可知,在用标准 A .AB .BC .CD .D11.某反应A(g)+B(g)C(g)+D(g)−−→的速率方程为m n v=k c (A)c (B)⋅⋅,其半衰期(当剩下列说法正确的是A .该反应的速率方程中的m=n=1B .该反应的速率常数-2-1k=6.410min ⨯C .表格中的-3112c =0.75,v =v =6.410⨯D .在过量的B 存在时,反应掉93.75%的A 所需的时间是375min12.有机物液流电池因其电化学性能可调控等优点而备受关注。

新药破解耐药困局本土患者尚求而不得我国肺癌发病率和死亡率均高,每年肺癌新增病例约73万例,全球每年大约有1/3的新发肺癌患者来自中国,而其中EGFR基因突变型肺癌最为常见。
生机令人欣慰的是,经过医药公司和研究机构的不懈努力,针对非小细胞肺癌的治疗出现了突破性的变革,先后出现了第一代、第二代肺癌靶向药,并在欧美国家进入临床治疗,效果显著。
自2005年第一代肺癌靶向药吉非替尼进入中国市场,我国非小细胞肺癌治疗也进入了靶向治疗时代。
十余年来,晚期肺癌患者中位生存期增加了2.4倍,从此前的14.1个月延长至33.5个月。
靶向治疗无论是在延长生存时间还是提高生活质量上,都给晚期肺癌患者带来了新的希望。
然而,伴随耐药性的出现,新的问题随之而来。
1突变靶向药是针对癌细胞的某一个蛋白、某一个分子起作用的,所以只抑制肿瘤生长的一条通路。
当一条通路受到抑制时,肿瘤细胞会自寻新的“生路”,选择其他通路合成自身生长所需要的物质,久而久之可使分子靶向药物失去作用,从而产生耐药性。
研究显示,60%的产生获得性耐药的患者表皮生长因子受体基因发生第2个位点突变(T790M),即表皮生长因子受体基因存在2个突变位点。
据广东省肺癌研究所所长、中国临床肿瘤学会(CSCO)理事长吴一龙教授介绍,非小细胞肺癌患者中有部分患者存在表皮生长因子受体基因突变,称为EGFR突变,这类患者在接受第一代、第二代EGFR抑制剂类靶向药物治疗之后,在经过一个比较长的有效期(多为9~11个月)之后会出现疾病进展,这种情况称为获得性耐药。
肿瘤出现耐药性,现有的治疗则失效。
在没有新一代靶向药物的情况下,患者只能转而接受化疗。
但由于这样的治疗欠缺针对性,患者的无恶化存活期只有约6个月,并且治疗副作用大,患者生活质量下降。
2转机针对这一部分耐药患者的治疗,医学界也一直在努力研究新药,并成功研发出针对获得性耐药中2/3情形的EGFR-T790M突变,能够直接抑制耐药基因癌细胞的新一代靶向药物。