小鼠氧化型低密度脂蛋白 ox-LDL ELISA试剂盒说明书
- 格式:doc
- 大小:41.00 KB
- 文档页数:3

说明书版本号:V1.0货号HOEM0601-01HOEM0601-02HOEM0601-03产品名称低密度脂蛋白胆固醇(LDL-C)检测试剂盒(直接法)预期用途本试剂盒用于体外测定人血清中低密度脂蛋白胆固醇(LDL-C)的含量。
低密度脂蛋白胆固醇用于冠心病和动脉粥样硬化的诊断。
动脉粥样硬化(AS)斑块中沉淀的脂质主要是低密度脂蛋白(LDL),在各类脂质中,LDL被认为是主要的致病因素,而高密度脂蛋白(HDL)可能起保护作用,血清总胆固醇(TC)大致反映LDL胆固醇(LDL-CHO)水平,但也受HDL-C水平的影响,因此在AS脂类危险因素判别中,TC偏高时,测定LDL-C有重要临床意义。
检验原理反应分两步进行:第一步:R1中聚阴离子与LDL形成复合物,在表面活性剂1作用下,不与胆固醇酶试剂反应。
而其它脂蛋白(CM,VLDL-C,HDL-C)则被酶试剂水解产生过氧化氢,在缺乏偶联剂时被消耗而不显色。
第二步:R2中表面活性剂2使LDL释放胆固醇,在胆固醇酶试剂与偶联剂作用下参与Trinder反应而显色,吸光度与样本中低密度脂蛋白胆固醇浓度成正比。
主要组成成分组成浓度试剂1(R1):Tris缓冲液100mmol/L(pH7.5)聚阴离子化合物0.5mmo1/LN-乙基-N-(2-羟基-3-磺丙基)间甲苯胺(TOOS)1mmol/L4-氨基安替比林0.5mmo1/L胆固醇酯酶800U/L胆固醇氧化酶500U/L表面活性剂适量试剂2(R2):Tris缓冲液100mmol/L(pH7.0)过氧化物酶30KU/L表面活性剂适量储存条件及有效期未开封试剂避光保存于2~8℃,有效期12个月;试剂开封后避光保存于2~8℃,在无污染情况下有效期1个月;试剂不可冰冻。
样本要求1.新鲜无溶血的血清2.样本中血红蛋白≤600mg/dL、甘油三酯≤1000mg/dL、胆红素≤20mg/dL时未观察到明显干扰。
3.稳定性:2~8℃保存可稳定7天。

小而密低密度脂蛋白胆固醇测定试剂盒1.性能指标1.1外观外观应符合表1要求。
表1 试剂盒内各组成的外观性状1.2装量液体试剂装量要求不低于标示量。
1.3水分含量校准品质控品的水分含量应不超过5%。
1.4试剂空白吸光度在主波长,1cm光径下,试剂空白吸光度≤0.20。
1.5分析灵敏度测定1.17mmol/L人血清样本时,试剂与样本反应产生的吸光度值应≥0.05。
1.6线性范围1.6.1试剂盒在[0.20,3.00] mmol/L 范围内,线性相关系数r≥0.990。
1.6.2在[0.20,1.20] mmol/L 范围内,线性绝对偏差应不超过±0.12 mmol/L;在(1.20,3.00] mmol/L 范围内,线性相对偏差应不超过±10%。
1.7精密度1.7.1重复性变异系数(CV)应≤5%。
1.7.2批间差试剂盒批间相对极差R 应≤10%。
1.8准确度回收率应在90%~110%。
1.9分析特异性当抗坏血酸≤60mg/dL,胆红素≤15mg/dL、血红蛋白≤500mg/dL、脂肪乳剂≤1.5%时,对试剂检测结果的偏差影响在±10%以内。
1.10量值溯源应明确分析物的量值溯源。
1.11校准品赋值结果及其不确定的的表示方式应使用规范的表示方式,主要表示方式可选择:a)赋值结果±扩展不确定度;b)赋值结果,扩展不确定度。
1.12校准品正确度≤1。
量值传递的正确度应符合En1.13质控品赋值准确度在用校准品校准后的生化分析仪上测试定值质控品,结果应在制造商指定的赋值范围内。
1.14校准品均匀性1.14.1瓶内均匀性:CV 瓶内应不大于10%。
1.14.2瓶间均匀性:CV 瓶间应不大于10%。
1.15质控品均匀性1.15.1瓶内均匀性:CV 瓶内应不大于10%。
1.15.2瓶间均匀性:CV 瓶间应不大于10%。

小而密低密度脂蛋白胆固醇(sd LDL-C)测定试剂盒
(过氧化物酶法)
2性能指标
2.1外观和性状
外观和性状应符合表2要求。
表2 试剂盒内各组成的外观性状
2.2装量
不同规格装量要求不低于其标示量。
2.3试剂空白吸光度
试剂以生理盐水为空白样本时,在37±1℃,主波长600 nm,光径1 cm下,吸光度A≤0.05。
2.4分析灵敏度
试剂(盒)测试1.00 mmol/L被测物时,吸光度值差值ΔA≥0.02。
2.5线性范围
2.5.1 在[0.10,2.59] mmol/L 区间内,其线性相关系数r≥0.990。
2.5.2 相对偏差或绝对偏差应符合表 3 要求。
表3 相对偏差或绝对偏差
2.6测量精密度
2.6.1重复性
试剂盒批内精密度 CV(%)应≤10%。
2.6.2批间差
试剂盒批间相对极差(R)应≤10%。
2.7准确度
以校准品为检测样本时,相对偏差(Bias%)应在±10.0%以内。
2.8校准品含水量
含水量应不超过 10.0%
2.9校准品正确度
E n 绝对值应≤1。
2.10质控品准确度
相对偏差(Bias%)应在±15.0%以内。
2.11校准品均一性
CV
瓶间值应≤10.0%;CV
瓶内
值应≤10.0%。
2.12质控品均一性
CV 值应≤10.0%。

REV20190712仅供研究,不用于临床诊断。
客服热线: 400-7060-959﹡技术支持邮箱: **************公司官网: 目录简介 ........................................................................................................................................................... - 3 -检测原理 ................................................................................................................................................... - 3 -试剂盒组分 ............................................................................................................................................... - 4 -储存条件 ................................................................................................................................................... - 5 -其他实验材料(不提供,但可协助购买) : ............................................................................................. - 5 -注意事项 ................................................................................................................................................... - 5 -样本收集处理及保存方法 ....................................................................................................................... - 6 -试剂准备 ................................................................................................................................................... - 6 -操作步骤 ................................................................................................................................................... - 8 -操作流程图 ............................................................................................................................................... - 8 -操作要点提示 ........................................................................................................................................... - 9 -结果判断 ................................................................................................................................................... - 9 -结果重复性 ............................................................................................................................................. - 10 -灵敏度 ..................................................................................................................................................... - 10 -特异性 ..................................................................................................................................................... - 10 -参考文献 ................................................................................................................................................. - 10 -该产品由北京四正柏生物科技有限公司研制。
大鼠低密度脂蛋白(LDL)酶联免疫分析(ELISA)试剂盒使用说明书厦门慧嘉生物科技有限公司本试剂仅供研究使用目的:本试剂盒用于测定大鼠血清,血浆及相关液体样本中低密度脂蛋白(LDL)含量。
实验原理:本试剂盒应用双抗体夹心法测定标本中大鼠低密度脂蛋白(LDL)水平。
用纯化的大鼠低密度脂蛋白(LDL)抗体包被微孔板,制成固相抗体,往包被单抗的微孔中依次加入低密度脂蛋白(LDL),再与HRP标记的低密度脂蛋白(LDL)抗体结合,形成抗体-抗原-酶标抗体复合物,经过彻底洗涤后加底物TMB显色。
TMB在HRP酶的催化下转化成蓝色,并在酸的作用下转化成最终的黄色。
颜色的深浅和样品中的大鼠低密度脂蛋白(LDL)呈正相关。
用酶标仪在450nm波长下测定吸光度(OD值),通过标准曲线计算样品中大鼠低密度脂蛋白(LDL)浓度。
样本处理及要求:1.血清:室温血液自然凝固10-20分钟,离心20分钟左右(2000-3000转/分)。
仔细收集上清,保存过程中如出现沉淀,应再次离心。
2.血浆:应根据标本的要求选择EDTA、者柠檬酸钠或肝素作为抗凝剂,混合10-20分钟后,离心20分钟左右(2000-3000转/分)。
仔细收集上清,保存过程中如有沉淀形成,应该再次离心。
3.尿液:用无菌管收集,离心20分钟左右(2000-3000转/分)。
仔细收集上清,保存过程中如有沉淀形成,应再次离心。
胸腹水、脑脊液参照实行。
4.细胞培养上清:检测分泌性的成份时,用无菌管收集。
离心20分钟左右(2000-3000转/分)。
仔细收集上清。
检测细胞内的成份时,用PBS(PH7.2-7.4)稀释细胞悬液,细胞浓度达到100万/ml左右。
通过反复冻融,以使细胞破坏并放出细胞内成份。
离心20分钟左右(2000-3000转/分)。
仔细收集上清。
保存过程中如有沉淀形成,应再次离心。
5.组织标本:切割标本后,称取重量。
加入一定量的PBS,PH7.4。
用液氮迅速冷冻保存备用。
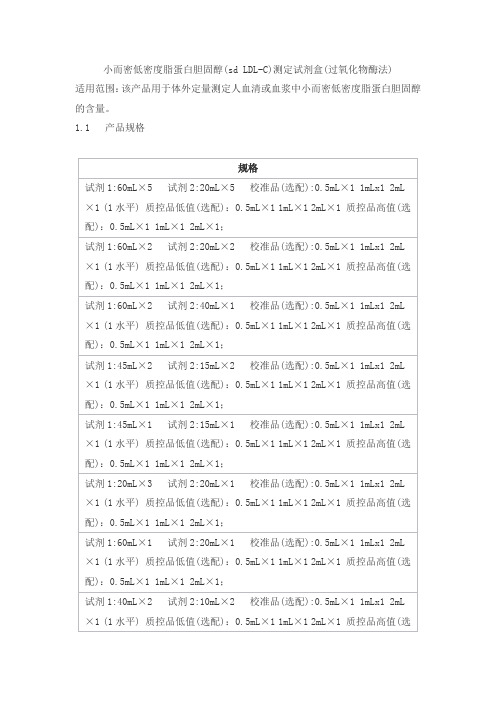
小而密低密度脂蛋白胆固醇(sd LDL-C)测定试剂盒(过氧化物酶法)适用范围:该产品用于体外定量测定人血清或血浆中小而密低密度脂蛋白胆固醇的含量。
1.1 产品规格1.2 组成成分1.2.1 试剂组成试剂1:Tris 缓冲液 100mmol/L胆固醇酯酶(CHE) 1600U/L胆固醇氧化酶(CHO) 600U/L磷脂酶 2700U/L过氧化氢酶 1200U/L2-羟基-3-间甲苯胺丙磺酸钠 2mmol/L试剂2:Tris 缓冲液 100mmol/L过氧化物酶(POD) 5000U/L4-氨基安替比林4mmol/L1.2.2校准品的组成校准品为冻干品,校准品组成是在磷酸盐缓冲液中加入含一定浓度的小而密低密度脂蛋白胆固醇纯品,稳定剂<5%。
1个水平校准品目标浓度为1.1 mmol/L(42.5 mg/dL),浓度有批特异性,具体定值详见瓶签。
1.2.3质控品的组成两水平冻干质控品,在20g/L牛血清中加入小而密低密度脂蛋白胆固醇纯品,稳定剂<5%。
靶值范围分别为:0.259 ~ 1.036 mmol/L(10.0~40.0 mg/dL)、1.036 ~2.072 mmol/L(40.0~80.0 mg/dL)。
2.1 外观试剂 1 为无色到淡褐色液体,目测不得有任何沉淀及絮状悬浮物;试剂 2 为淡黄色到黄色液体,目测不得有任何沉淀及絮状悬浮物;校准品为白色或淡黄色粉末状物质,复溶后为无色或淡黄色液体,目测不得有任何沉淀及絮状悬浮物;质控品为白色或淡黄色粉末状物质,复溶后为无色或淡黄色液体,目测不得有任何沉淀及絮状悬浮物。
2.2 净含量液体试剂的净含量不得低于标示体积。
2.3 空白吸光度试剂空白吸光度应≤0.1。
2.4 分析灵敏度浓度为2.59 mmol/L(100.0 mg/dL)时,吸光度变化应≥0.05。
2.5 线性测试血清样本,试剂线性在[0.1,2.59] mmol/L([4.0,100.0] mg/dL)范围内,线性相关系数(r)应不小于0.99;测定结果在[0.1,0.777] mmol/L([4.0,30.0] mg/dL)时绝对偏差不超过±0.078 mmol/L (± 3 mg/dL);在(0.777,2.59]mmol/L ((30,100.0] mg/dL)范围内的相对偏差不超过±10%。
氧化低密度脂蛋白的检测方法氧化低密度脂蛋白(oxLDL)是低密度脂蛋白(LDL)在体内经过氧化后的产物,与动脉粥样硬化和心血管疾病的发展有密切关系。
因此,检测oxLDL的水平对于心血管疾病的预防和治疗具有重要意义。
以下是几种常用的oxLDL检测方法:1. 酶联免疫吸附试验(ELISA):这是检测oxLDL最常用的方法之一。
通过使用特异性抗体识别和结合oxLDL,然后通过酶标记的二抗和底物的颜色变化来定量oxLDL的浓度。
ELISA方法具有较高的特异性和灵敏度,适合于临床和研究实验室的需要。
2. 免疫荧光法:通过使用特异性抗体,这些抗体对oxLDL有很高的亲和力,并且被荧光染料标记。
当抗体与oxLDL结合时,可以通过荧光显微镜或流式细胞仪检测到荧光信号,从而实现对oxLDL的定性和定量分析。
3. 流式细胞术:这种方法可以用来检测血液样本中含有oxLDL的细胞。
通过使用针对oxLDL的荧光标记抗体,可以在流式细胞仪上对单个细胞进行分析,从而评估oxLDL的水平和其在细胞中的分布。
4. 电化学发光法:这是一种灵敏度高、特异性强的检测方法,利用电化学发光标记的抗体与oxLDL的结合来测量oxLDL的浓度。
该方法适合于高通量筛选和大规模临床样本的分析。
5. 高效液相色谱法(HPLC):HPLC可以用于分离和定量oxLDL中的特定氧化产物,如氧化脂质和胆固醇氧化物。
这种方法需要复杂的样品准备和专业的操作,但提供了关于oxLDL氧化程度的详细信息。
6. 直接检测氧化标志物:还可以通过检测与LDL氧化相关的标志物,如丙二醛修饰的LDL(MDA-LDL)、4-羟基壬烯醛(4-HNE)修饰的LDL等,间接评估oxLDL的水平。
每种方法都有其优点和局限性,选择适合的方法通常取决于实验目的、样本类型、设备可用性以及成本等因素。
在临床和研究应用中,多种方法的结合使用可以提供更全面的信息,有助于更好地理解oxLDL在心血管疾病中的作用。
氧化型低密度脂蛋白
氧化型低密度脂蛋白是一种重要的血清脂质,总量低于普通低密度脂蛋白(LDL)。
它可以对血液中的油脂、脂肪酰胺和脂肪酸结合形成脂蛋白,并被用于转运到体内细胞的胆固醇。
它也是一种复合物,由脂肪酰胺结合的高度磷脂酰肌醇构成。
氧化型低密度脂蛋白是血脂流动性和负载特性的重要指标,可以帮助医生确定患者的血脂水平。
据估计,氧化型低密度脂蛋白水平正常的人群中,大多数情况下血清氧化型低密度脂蛋白的水平较低。
当血清水平超过正常范围时,则存在患有动脉粥样硬化症(atherosclerosis)的风险。
如果血清氧化型低密度脂蛋白水平较高,可能表明有心血管疾病的风险,成年人可能会患有冠心病,而儿童可能会患有斑块性心肌病。
氧化型低密度脂蛋白的水平受到多种因素的影响,包括遗传因素、营养因素、药物因素、饮食因素和其他因素。
一般来说,年龄和性别会影响氧化型低密度脂蛋白的水平,其中男性的水平要高于女性。
此外,正常的体重、合理的饮食和良好的心理健康状态也会促进氧化型低密度脂蛋白水平的正常。
氧化型低密度脂蛋白可以通过血液检测测定,药物治疗和行为干预可以降低氧化型低密度脂蛋白水平,减少心血管疾病的发生。
最常用的是降低胆固醇的药物治疗,其他如饮食干预、运动干预和血压管理等也可以调节氧化型低密度脂蛋白的水平。
这些措施的及早采取可以降低血脂异常的风险,预防心血管疾病的发生。
总而言之,氧化型低密度脂蛋白是一种重要的血清脂质,水平的正常是保持血脂平衡和预防心血管疾病的关键。
因此,对氧化型低密度脂蛋白的测定和监测十分重要,应采取合理的血脂管理措施,保持血脂水平正常,远离心血管疾病的危险。
兔氧化低密度脂蛋白(oxLDL)ELISA试剂盒使用说明最近更新时间:2014-09-24详细介绍:兔氧化低密度脂蛋白(oxLDL)ELISA试剂盒使用说明本试剂仅供研究使用标本:血清或血浆试验原理:兔氧化低密度脂蛋白(oxLDL)ELISA试剂盒是固相夹心法酶联免疫吸附实验(ELISA).已知oxLDL浓度的标准品、未知浓度的样品加入微孔酶标板内进行检测。
先将oxLDL 和生物素标记的抗体同时温育。
洗涤后,加入亲和素标记过的HRP。
再经过温育和洗涤,去除未结合的酶结合物,然后加入底物A、B,和酶结合物同时作用。
产生颜色。
颜色的深浅和样品中oxLDL的浓度呈比例关系。
试剂盒内容及其配制试剂盒成份(2-8℃保存) 96孔配置 48孔配置配制96/48人份酶标板 1块板(96T)半块板(48T)即用型塑料膜板盖 1块半块即用型标准品:400mmol/L 1瓶(0.6ml) 1瓶(0.3ml)按说明书进行稀稀空白对照 1瓶(1.0ml) 1瓶(0.5ml)即用型标准品稀释缓冲液 1瓶(5ml) 1瓶(2.5ml)即用型生物素标记的抗oxLDL抗体 1瓶(6ml) 1瓶(3.0ml)即用型亲和链酶素-HRP 1瓶(10ml) 1瓶(5.0ml)即用型洗涤缓冲液 1瓶(20ml) 1瓶(10ml)按说明书进行稀释底物A 1瓶(6.0ml) 1瓶(3.0ml)即用型底物B 1瓶(6.0ml) 1瓶(3.0ml)即用型终止液 1瓶(6.0ml) 1瓶(3.0ml)即用型自备材料1.兔氧化低密度脂蛋白(oxLDL)ELISA试剂盒蒸馏水。
2.加样器:5ul、10ul、50ul、100ul、200ul、500ul、1000ul。
3.振荡器及磁力搅拌器等。
安全性1.避免直接接触终止液和底物A、B。
一旦接触到这些液体,请尽快用水冲洗。
2.实验中不要吃喝、抽烟或使用化妆品。
3.不要用嘴吸取试剂盒里的任何成份。
操作注意事项1.试剂应按标签说明书储存,使用前恢复到室温。
1
小鼠氧化型低密度脂蛋白(ox-LDL)酶联免疫分析(ELISA)
试剂盒使用说明书
厦门慧嘉生物科技有限公司
本试剂仅供研究使用 目的:本试剂盒用于测定小鼠血清,血浆及相
关液体样本中氧化型低密度脂蛋白(ox-LDL)的含量。
实验原理:
本试剂盒应用双抗原夹心法测定标本中小鼠氧化型低密度脂蛋白(ox-LDL)水平。用纯化
的小鼠氧化型低密度脂蛋白(ox-LDL) 抗体包被微孔板,制成固相抗体,往包被抗原的微孔
中依次加入氧化型低密度脂蛋白(ox-LDL),再与HRP标记的氧化型低密度脂蛋白(ox-LDL)
抗体结合,形成抗体-抗原-酶标抗体复合物,经过彻底洗涤后加底物TMB显色。TMB在
HRP酶的催化下转化成蓝色,并在酸的作用下转化成最终的黄色。颜色的深浅和样品中的
氧化型低密度脂蛋白(ox-LDL)呈正相关。用酶标仪在450nm波长下测定吸光度(OD值),
通过标准曲线计算样品中小鼠氧化型低密度脂蛋白(ox-LDL)浓度。
试剂盒组成:
试剂盒组成 48孔配置 96孔配置 保存
说明书 1份 1份
封板膜 2片(48) 2片(96)
密封袋 1个 1个
酶标包被板 1×48 1×96 2-8℃保存
标准品:270μg/L 0.5ml×1瓶 0.5ml×1瓶 2-8℃保存
标准品稀释液 1.5ml×1瓶 1.5ml×1瓶 2-8℃保存
酶标试剂 3 ml×1瓶 6 ml×1瓶 2-8℃保存
样品稀释液 3 ml×1瓶 6 ml×1瓶 2-8℃保存
显色剂A液 3 ml×1瓶 6 ml×1瓶 2-8℃保存
显色剂B液 3 ml×1瓶 6 ml×1瓶 2-8℃保存
终止液 3ml×1瓶 6ml×1瓶 2-8℃保存
浓缩洗涤液 (20ml×20倍)×1瓶 (20ml×30倍)×1瓶 2-8℃保存
样本处理及要求:
1. 血清:室温血液自然凝固10-20分钟,离心20分钟左右(2000-3000转/分)。仔细收集上
清,保存过程中如出现沉淀,应再次离心。
2. 血浆:应根据标本的要求选择EDTA或柠檬酸钠作为抗凝剂,混合10-20分钟后,离心
20分钟左右(2000-3000转/分)。仔细收集上清,保存过程中如有沉淀形成,应该再次
离心。
2
3. 尿液:用无菌管收集,离心20分钟左右(2000-3000转/分)。仔细收集上清,保存过程
中如有沉淀形成,应再次离心。胸腹水、脑脊液参照实行。
4. 细胞培养上清:检测分泌性的成份时,用无菌管收集。离心20分钟左右(2000-3000转/
分)。仔细收集上清。检测细胞内的成份时,用PBS(PH7.2-7.4)稀释细胞悬液,细胞
浓度达到100万/ml左右。通过反复冻融,以使细胞破坏并放出细胞内成份。离心20分
钟左右(2000-3000转/分)。仔细收集上清。保存过程中如有沉淀形成,应再次离心。
5. 组织标本:切割标本后,称取重量。加入一定量的PBS,PH7.4。用液氮迅速冷冻保存备
用。标本融化后仍然保持2-8℃的温度。加入一定量的PBS(PH7.4),用手工或匀浆器
将标本匀浆充分。离心20分钟左右(2000-3000转/分)。仔细收集上清。分装后一份待
检测,其余冷冻备用。
6. 标本采集后尽早进行提取,提取按相关文献进行,提取后应尽快进行实验。若不能马上
进行试验,可将标本放于-20℃保存,但应避免反复冻融.
7. 不能检测含NaN3的样品,因NaN3抑制辣根过氧化物酶的(HRP)活性。
操作步骤
1. 标准品的稀释与加样:在酶标包被板上设标准品孔10孔,在第一、第二孔中分别加标
准品100μl,然后在第一、第二孔中加标准品稀释液50μl,混匀;然后从第一孔、第二
孔中各取100μl分别加到第三孔和第四孔,再在第三、第四孔分别加标准品稀释液50μl,
混匀;然后在第三孔和第四孔中先各取50μl弃掉,再各取50μl分别加到第五、第六孔
中,再在第五、第六孔中分别加标准品稀释液50ul,混匀;混匀后从第五、第六孔中各
取50μl分别加到第七、第八孔中,再在第七、第八孔中分别加标准品稀释液50μl,混
匀后从第七、第八孔中分别取50μl加到第九、第十孔中,再在第九第十孔分别加标准
品稀释液50μl,混匀后从第九第十孔中各取50μl弃掉。(稀释后各孔加样量都为50μl,
浓度分别为180μg/L,120μg/L ,60μg/L,30μg/L, 15μg/L)。
2. 加样:分别设空白孔(空白对照孔不加样品及酶标试剂,其余各步操作相同)、待测样
品孔。在酶标包被板上待测样品孔中先加样品稀释液40μl,然后再加待测样品10μl(样
品最终稀释度为5倍)。加样将样品加于酶标板孔底部,尽量不触及孔壁,轻轻晃动混
匀。
3. 温育:用封板膜封板后置37℃温育30分钟。
4. 配液:将30(48T的20倍)倍浓缩洗涤液用蒸馏水30(48T的20倍)倍稀释后备用。
5. 洗涤:小心揭掉封板膜,弃去液体,甩干,每孔加满洗涤液,静置30秒后弃去,如此
重复5次,拍干。
6. 加酶:每孔加入酶标试剂50μl,空白孔除外。
7. 温育:操作同3。
8. 洗涤:操作同5。
9. 显色:每孔先加入显色剂A50μl,再加入显色剂B50μl,轻轻震荡混匀,37℃避光显色
15分钟.
10. 终止:每孔加终止液50μl,终止反应(此时蓝色立转黄色)。
11. 测定:以空白空调零,450nm波长依序测量各孔的吸光度(OD值)。 测定应在加终止
液后15分钟以内进行。
注意事项:
1. 试剂盒从冷藏环境中取出应在室温平衡15-30分钟后方可使用,酶标包被板开封后如未
用完,板条应装入密封袋中保存。
2. 浓洗涤液可能会有结晶析出,稀释时可在水浴中加温助溶,洗涤时不影响结果。
3. 各步加样均应使用加样器,并经常校对其准确性,以避免试验误差。一次加样时间最好
3
控制在5分钟内,如标本数量多,推荐使用排枪加样。
4. 请每次测定的同时做标准曲线,最好做复孔。如标本中待测物质含量过高(样本OD值
大于标准品孔第一孔的OD值),请先用样品稀释液稀释一定倍数(n倍)后再测定,计
算时请最后乘以总稀释倍数(×n×5)。
5. 封板膜只限一次性使用,以避免交叉污染。
6. 底物请避光保存。
7. 严格按照说明书的操作进行,试验结果判定必须以酶标仪读数为准.
8. 所有样品,洗涤液和各种废弃物都应按传染物处理。
9. 本试剂不同批号组分不得混用。
10. 如与英文说明书有异,以英文说明书为准。
计算:
以标准物的浓度为横坐标,OD值为纵坐标,
在坐标纸上绘出标准曲线,根据样品的OD
值由标准曲线查出相应的浓度;再乘以稀释
倍数;或用标准物的浓度与OD值计算出标
准曲线的直线回归方程式,将样品的OD值
代入方程式,计算出样品浓度,再乘以稀释
倍数,即为样品的实际浓度。
(此图仅供参考)
试剂盒性能:
1.样品线性回归与预期浓度相关系数R值为0.990以上。
2.批内与批见应分别小于9%和11%
检测范围:0.45 nmol/ml-30 nmol/ml
灵敏度:0.11 nmol/ml
(外文文献一篇)
保存条件及有效期:
1.试剂盒保存:;2-8℃。
2.有效期:6个月