雅博司(门冬氨酸鸟氨酸注射液)说明书(精)
- 格式:doc
- 大小:1.12 MB
- 文档页数:7

异甘草酸镁联合门冬氨酸鸟氨酸治疗化疗药物性肝损伤临床疗效观察李晓芳;王海雄;裴毅【摘要】Objective:To investigate the clinical effect of magnesium isoglycyrrhizinate combined with L - ornithine - L -aspartate in the treatment of patients with chemotherapeutics - induced liver injury. Methods:All 160 patients with chemothera-peutic drug - induced liver injury were randomly divided into two groups. Patients in combination group(n = 80)were treated intravenously with magnesium isoglycyrrhizinate combined with L - ornithine - L - aspartate for 2 weeks,and the patients in control group(n = 80)were treated with L - ornithine - L - aspartate alone. The serum levels of glutamic - pyruvic transaminase (ALT),glutamic - oxaloacetic transaminase(AST)and total bilirubin(TBIL)were observed. Results:At the end of 2 week treatment,the serum levels of ALT and AST in control group were significantly lower than pre - treatment(P ﹤ 0. 05);serum levels of ALT and AST in combination group were significantly lower than pre - treatment(P ﹤ 0. 01). The serum levels of ALT and AST in combination group were significantly lower than control group after threatment(P ﹤ 0. 05). The total effective rate in combination group were significantly higher than control group(P ﹤ 0. 01). Conclusion:Magnesium isoglycyrrhizinate com-bined with L - ornithine - L - aspartate is effective for chemotherapeutics - induced liver injury.%目的:探讨异甘草酸镁联合门冬氨酸鸟氨酸对化疗药物性肝损伤的临床疗效。

1. 乐派 0.3 i.v.drip q.d 加替沙星(第四代)2. 凯泽 0.4 i.v.drip q.d 加替沙星 100ml:0.2/袋3. 海超 0.4 i.v.drip q.d 加替沙星 100ml:0.2/袋4. 圣迪锋 0.4+N.S 100ml i.v.drip q.d 加替沙星5. 来立信 0.4 i.v.drip q.d 左氧氟沙星(第三代) 100:0.2/袋6. 利复星 0.4 i.v.drip q.d 左氧氟沙星 100:0.2/袋7. 左克 0.4 i.v.drip q.d 左氧氟沙星8. 可乐必妥 0.4 i.v.drip q.d 左氧氟沙星 100:0.2/袋9. 丽珠强派 0.4+N.S 100ml i.v.drip q.d 盐酸左氧氟沙星 0.1g/瓶10. 奎泰 0.3 i.v.drip q.d11. 拜复乐 0.4 p.o q.d 盐酸莫西沙星(第四代) 0.4/片11. 诺佳 0.4+5%Glucose 500ml i.v.drip q.d 依诺沙星12. 科奇 0.4+5%Glucose 500ml i.v.drip q.d 天门冬氨酸洛美沙星2ml:0.1/支13.天方罗欣 0.2-0.4 i.v.drip q.d 氟罗沙星 100:0.2/袋作用特点:主要对 G-细菌作用较强,而且具有一定抗结核作用。
不用于儿童和孕妇。
不良反应: 1.胃肠道反应(常与剂量有关):如恶心、呕吐等。
2.少数有中枢兴奋作用(本要有脂溶性);3.过敏反应4.静脉炎(可不处理)。
5.曾经有报导科奇可诱发癫痫。
处理:可嘱慢滴。
1. 仙力素2.0+N.S 100ml i.v.drip q.12h 头孢 1.0/瓶(一代)2. 新亚星 2.5+N.S 100ml i.v.drip q.12h 头孢呋辛钠舒巴坦钠 2.5/瓶(二代)能够透过血脑屏障3. 泰吡信 2.0+N.S 100ml i.v.drip q.8h 头孢匹胺钠 1.0/支4. 益保世灵 2.0+N.S 100ml i.v.drip q.12h 头孢唑亏 1.0/瓶5. 可赛舒 2.5+N.S 100ml i.v.drip q.12h 头孢曲松钠舒巴坦钠 1.5/瓶(三代)6. 康利必欣 3.0+N.S 100ml i.v.drip q.d 头孢哌酮舒巴坦钠 1.5/支7. 新瑞普欣 3.0+N.S 100ml i.v.drip q.8h 头孢哌酮舒巴坦钠 1.5/瓶 (三代)8. 海舒必 3.0+N.S 100ml i.v.drip q.12h 头孢哌酮舒巴坦钠 1.5/瓶9. 利君哌舒 2.0+N.S 100ml i.v.drip q.12h 头孢哌酮舒巴坦钠 1.0/瓶10. 威哌 4.0+N.S 100ml i.v.drip q.d 头孢哌酮舒巴坦钠 4.0/瓶11. 铃兰欣 4.0+N.S 100ml i.v.drip q.12h 头孢哌酮舒巴坦钠 0.5/瓶 (三代)12. 凯复定 2.0+N.S 100ml i.v.drip q.12h 头孢拉定 1.0/瓶(三代)13. 舒秦 3.0+N.S 100ml i.v.drip q.12h 头孢他定 1.5/瓶14. 海灵 4.0+N.S 100ml i.v.drip q.d 头孢他定 2.0/瓶15. 舒普深 3.0+N.S 100ml i.v.drip q.d 头孢三代16. 凯帝龙 2.0-4.0+N.S 100ml i.v.drip q.d17. 施复捷口服头孢丙烯 0.25/片18. 全泽复口服头孢地尼 2# tid 0.1/片19. 美爱克口服头孢妥仑匹酯 0.1/片20. 可服乐口服头孢克络21. 曼宁胶囊头孢克络缓释片22. 西力欣口服头孢呋辛23. 马斯平 4.0+N.S 100ml i.v.drip q.8h 头孢吡肟(四代) 1.0/支24. 信力威 2.0+N.S 250ml i.v.drip q8d 头孢吡肟炭青酶烯类:25. 泰能 0.5 +N.S 100ml i.v.drip q.8h 亚胺培南/西司他丁钠 0.5/支26. 美平 0.5+N.S 100ml i.v.drip q.6h-q.8h 美罗培南 0.5/瓶(二代)27. 倍能 0.5 +N.S 100ml i.v.drip q.8h 美罗培南28. 海正美特 0.5 +N.S 100ml i.v.drip q.8h 美罗培南广谱,强效作用特点:从一代到三代,对 G-菌及厌氧菌的作用越来越强,对 G+菌作用越来越弱。

门冬氨酸鸟氨酸注射液的处方与工艺优化研究王璐璐;陈少华;相莉;郑稳生【摘要】Objective To develop an injection formulation for ornitbinaspaetant injection. Methods The appearance, color, pH, drug content and related substances of the injection were used as indicators for screening the formulation. Results The optimum pH for the injection formulation was 6.0-7.0 according to the stability. Pressing steam sterilization was performed at 115 for 30 minutes. The prepared product was stable when stored at room temperature in light-resistant container for 12 months. Conclusion The developed injection formulation was stable and suitable for industrial production.%目的:研究门冬氨酸鸟氨酸注射液的处方及制备工艺。
方法通过考察门冬氨酸鸟氨酸注射液的性状、色泽、pH、含量及有关物质,得到优选处方。
结果本品最适pH值为6.0~7.0,以115℃热压蒸汽灭菌30min作为本品的灭菌方法。
本品在室温避光放置12个月,各项质量指标均在合格范围内。
结论本品处方设计合理,工艺可行,质量稳定。
【期刊名称】《中国医药指南》【年(卷),期】2014(000)036【总页数】2页(P51-52)【关键词】门冬氨酸鸟氨酸注射液;制备工艺;稳定性【作者】王璐璐;陈少华;相莉;郑稳生【作者单位】中国医学科学院药物研究所药物传输技术及新型制剂北京市重点试验室,北京 100050;中国医学科学院药物研究所药物传输技术及新型制剂北京市重点试验室,北京 100050;中国医学科学院药物研究所药物传输技术及新型制剂北京市重点试验室,北京 100050;中国医学科学院药物研究所药物传输技术及新型制剂北京市重点试验室,北京 100050【正文语种】中文【中图分类】R917门冬氨酸鸟氨酸(Ornithine Aspartate,OA)最先于20世纪70年代在德国用于临床,1991年收载德国药典,并被美国FDA批准用于治疗肝性脑病。

静脉用药常用药物:(一).止痛和镇静药:安定 10mg/2ml50ml纯安定(250mg)微泵,1-2ml/h(5-10mg/h)开始,随调。
0.1-0.2mg/kg 静注 q2-4h。
咪唑安定/力月西10mg/2ml/支50mg 配至50ml,负荷量0.03mg/kg,,维持0.03~0.2mg/kg.h(1.5-10ml/h), 据镇静情况调整。
芬太尼 0.1mg/2ml/支0.3mg +N.S.至50ml, 3-5ml/h(15~25ug/h) 持续泵入。
2-5ug/kg IV q1-2h或以2-5ug/kg/h维持杜冷丁/哌替啶50mg/ml/支1mg/kg IM/IV q2-4h, 50-100mg/次, 200-400mg/日;极量: 150mg/次。
吗啡10mg/1ml10mg+NS9ml。
50mg+NS40ml/微泵,1-2ml/h(10-40ug/kg/h)。
0.05-0.1mg/kg静注/肌注q1-2h。
异丙酚10mg/ml首剂 40mg 维持 40mg/h。
单次静注25~50mg,连续输注:0.5~3mg/kg.h。
万可松/维库溴胺4mg/支体重×3 +N.S.至50ml,1-2ug/kg/min(1~2ml/h)持续泵入氟哌啶醇5mg肌注(二)抗心律失常药:心律平/普罗帕酮70mg/20ml/支70mg 加GS/N.S.配至20ml,静推,10-20min重复,极量5支。
可达龙/胺碘酮5% 150mg/3ml首剂150 mg + NS 20 ml,维持 300 mg + NS 44ml <=6 ml(35mg/h)。
静点:300mg-450mg+500ml液体。
150mg+5%GS100ml静滴负荷量,继之1mg/min-vp,6h后可减至0.5mg/min。
一般不静推,只用5%GS配液。
利多卡因 100mg/5ml/支,400mg/20ml50mg-100mg静推;200-400mg 配至500ml 液体静滴。

梁瑞你好,有关生产工艺方面,还需药厂大力配合,需要每一步骤的详细描述,参数)下文红色标记为需要药厂提供,以及和药厂讨论的内容)3.2.P.2.3 生产工艺的开发对于本品种,配液、除热原、灌装、灭菌为关键步骤,实验对关键步骤,关键参数进行考察。
(审评中心要求对关键步骤及其关键工艺进行考察,实际操作中是否是这样的?有不妥处咱们再讨论)3.2.P.2.3.1配液(这是我们做的一个其他产品,工厂进行的相关实验研究和参数考察,不知是否与此产品及工厂工艺相配,作参考)生产环境要求:生产设备:取样:混合10分钟时停机,请验,QA员按检验需用量从三维运动混合机的上中下三层(上下两层按三个点、中层按四个点)分别取样;然后再开机继续混合至15,20,25分钟时停机,请验及取样方法同上;最后再开机继续混合至25分钟时停机,请验及取样方法同上。
QA员将30个样品送检。
(注:请验,每层填写一张请验单,注明取样点编号;样品口袋外壁贴有取样点编号的标签),取样位置:参见下图1门冬氨酸鸟氨酸胶囊工艺验证数据(批号)生产工艺的选择和优化混合时间为分钟,符合验证标准。
确定混合工艺步骤的目标值及范围3.2.P.2.3.2 除热原(具体的除热原的工艺、参数及验证包括活性炭的处理、用量,吸附时浓度、温度、搅拌方式、速度和时间;初滤及精滤的滤材种类和孔径、过滤方式、滤液的温度与流速工艺验证)3.2.P.2.3.3 灌装(灌装设备、参数如履带转速,灌装速度,考察其对装量差异,灌装效果的影响,进行验证)鉴于本品种的特殊性,灌装是一个难题,这个最好在报批前解决,因为如果决定,设备是不能换的。
生产环境要求:。
生产设备:。
3.2.P.2.3.4 灭菌(这个是我们实验室进行的实验,还需药厂生产规模的灭菌工艺验证)3.2.P.2.3.4.1灭菌方法选择蒸汽法:是在高压灭菌器中使用高压蒸汽进行灭菌的方法。
因微生物在湿热的环境中,一些重要的蛋白发生变性和凝固,使微生物死亡,从而达到灭菌的目的。

ECHO临床病例征集项目模板E xperience in SNM C &H epa-Merz O ption药品一般信息⏹通用名:门冬氨酸鸟氨酸注射液⏹有效成分含量:每10ml 含有门冬氨酸鸟氨酸5g ⏹规格:每安瓿10ml ,每盒含5安瓿⏹适应症:各种原因引起的血氨升高、肝性脑病⏹生产企业:德国Merz 公司⏹销售企业:卫材(中国)药业有限公司作用机制激活尿素循环促进谷氨酰胺合成降低血氨浓度参与三羧酸循环,为肝细胞供能参与核酸合成,促进肝细胞修复生成谷胱甘肽,保肝解毒临床获益我国约有40%住院肝硬化患者合并肝性脑病(HE ),对HE 的及时诊断和积极治疗可显著改善患者生活质量、预防疾病进展,改善预后。
雅博司的临床疗效:⏹快速降低血氨浓度,有效改善各级别肝性脑病患者神经生理症状⏹起效迅速,缩短肝性脑病患者临床恢复时间,减少及预防肝昏迷的发生⏹降氨醒脑的同时修复肝细胞损伤、改善肝功能,从根本上治疗引起肝性脑病的基础疾病⏹疗效确切,国内外临床指南推荐使用⏹德国原研品质,更少日治疗费用,更适用重症及补液限制患者雅博司®修复受损肝细胞改善肝脏功能雅博司®临床使用方法注射溶液可以和常用的各种注射用溶液混合而不发生任何问题。
最大溶解度每500mL溶液中不要溶解超过60mL本药物。
滴注速度输入速度最大不要超过每小时5g该药物(10mL,一支);个别患者可能出现轻微胃肠道反应(如恶心呕吐),一般不必停药,调慢滴速大多可自行恢复。
禁忌症不适用于肾功能严重受损患者(肌酐水平>3mg/100mL,即265.2μmol/L)雅博司®临床推荐剂量适应症推荐剂量和疗程血氨升高轻微型HE20g/天,静脉滴注,连续7天,根据血氨水平调整用药疗程Ⅰ、Ⅱ级HEⅢ、Ⅳ级HE每小时5g,连续静滴,至患者苏醒。
患者转醒后建议保持20g/天继续治疗7天。
慢性肝损伤(肝硬化、慢性病毒性肝20g/天,静脉滴注,连续7天,根据病情调整用药剂量及疗程炎、非酒精性脂肪肝)急性肝损伤(酒精性肝病、病毒性肝10g/天,静脉滴注,连续7天,根据病情调整用药剂量及疗程炎、药物性肝损伤、外伤手术相关肝损伤等)根据病情的严重程度,酌情增加剂量,但是每天最多不应该超过100g(20支)。
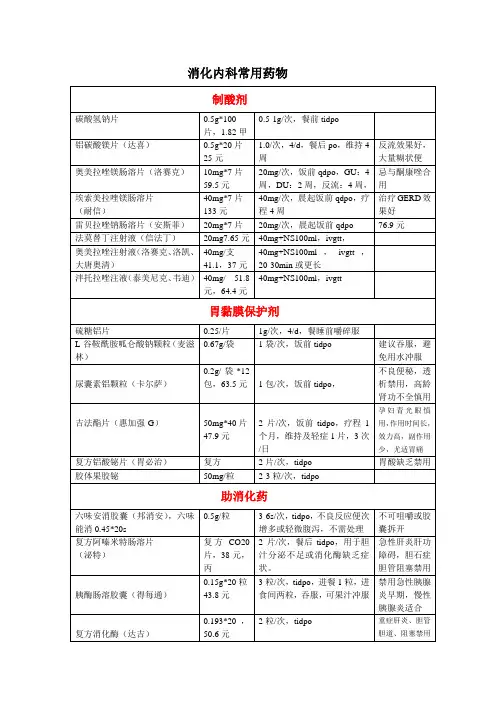

消化内科经常使用药目录能增进食物消化,用于消化道分泌功能减弱,消化不良,多为消化液中成份或增进消化液分泌的药物达吉胶囊(复合消化酶胶囊)含有胃蛋白酶、木瓜酶淀粉酶、熊去氧胆酸、纤维素酶、胰酶、胰脂酶用法:(成人)一日三次,餐后口服1-2 粒,或遵医嘱注意事项:可能发生口内不快感,偶有呕吐,软便多酶片:含胰蛋白酶、胰脂肪酶、胰淀粉酶、胃蛋白酶用法:口服,一次~3片,一日3次或遵医嘱注意事项:酸性条件下易破坏,故服历时切勿嚼碎;放置日久,效劳降低,宜用新制品;铝制剂可能阻碍本品疗效,故不宜合用六味安消胶囊:粒要紧成份为土木香、大黄、诃子、山柰、寒水石(煅)、碱花。
具有和胃健脾,导滞消积,行血止痛的功能。
用于胃痛胀满,消化不良,便秘,痛经。
用法:口服,每次~6粒,每日~3次注意事项:不宜与四环素类抗生素合用谷参肠安胶囊(复方谷氨酰胺):胶囊粒要紧成份为茯苓、甘草、谷氨酰胺等,有甘温益气、健脾养胃,爱惜及增进肠粘膜修复,增强肠道免疫屏障功能,调剂消化系统功能,适用于食欲不振、消化吸收不良、食后腹胀、肠道溃疡、急慢性肠炎、慢性腹泻等疾病;增进创伤及手术后肠道功能恢复及重建。
用法:餐前口服,每次~4粒,每日3次注意事项:勿将胶囊内药物倾出服用,妊妇慎用止吐药昂丹斯琼ondansetron 针剂4mg/支用法:遵医嘱注意事项:有壮大的中枢止吐作用,对肿瘤化疗、放疗引发的呕吐有极佳作用;对晕动病及多巴胺兴奋剂去水吗啡引发的呕吐无效,不良反映轻,可有头痛、头晕、便秘或腹泻。
胃复安(甲氧氯普胺)metoclopramide 针剂10mg/支用法:遵医嘱注意事项:可引发从食道至近段小肠滑腻肌运动,发挥促胃肠动力作用,大剂量静脉注射或长期利用,可引发锥体外系反映,可引发男性乳房发育、溢乳等。
吗丁啉motilium多潘立酮片剂10mg/片用法:每次片,3次/日,餐前15~30分钟服用注意事项:不良反映轻,偶见腹部痉挛、口干、皮疹、头痛等莫沙比利:片剂5mg/片用法:每次片,3次/日注意事项:不良反映要紧有腹泻、腹痛、口干、皮疹及头晕等,偶见嗜酸性粒细胞增多,甘油三酯升高、ALT、AST、ALP、γ-GT升高。

门冬氨酸鸟氨酸治疗脂肪肝疗效Meta分析张志华;顾天翊;陈柳莹;陆伦根【摘要】Objective To evaluate the efficacy of ornithine aspartate in the treatment of patients with fatty liver. Methods According to the inclusion and exclusion criteria,China National Knowledge Infrastructure (CNKI),Wanfang database,PubMed,EMBASE and Cochrane library up to July 20,2017 were screened for randomized controlled trial of ornithine aspartate in the treatment of patients with fatty liver. The Cochrane handbook was used to assess the risk bias,and the Jadad 7 subscales was used to document the quality score. Meta analysis by using RevMan 5.3 was made. Results A total of 727 Chinese patients with fatty liver were enrolled in the 9 Chinese clinical trials. The results of Meta analysis showed that total clinical efficiency rate in L-ornithine-L-aspartate treatment was much higher as compared to that in the control [OR=3.71,95% CI(1.85,7.46),P=0.0002];the decreased serum total cholesterol level was [MD=-3.04,95% CI(-3.76,-2.31),P<0.00001],and the decreased serum triglyceride level was [MD=-1.60,95%CI(-2.55,-0.65),P=0.0009];the total effective rate in L-ornithine-L-aspartate treatment was[OR=11.99,95%CI(2.36,60.91),P=0.003];the decreased serum ALT was [MD=-34.04,95%CI(-61.73,-6.35),P=0.02],and the decreased serum AST level was[MD=-9.48, 95% CI(-24.66,5.70),P=0.22];the decrease total serum bilirubin was [MD=-14.92,95% CI(-20.70,-9.15),P<0.00001]. Conclusion The application of L-ornithine-L-aspartate in the treatment of patients withfatty liver has a better therapeutic effect,which might improve the indexes of liver function and blood lipids. The efficacy of L-ornithine L-aspartate in the treatment of patients with fatty liver needs to be confirmed by multi-center,well-designed randomized clinical trials in the future.%目的评价门冬氨酸鸟氨酸治疗脂肪肝患者的疗效.方法检索中国知网(CNKI)、万方、维普、PubMed、EMBASE、Medline和Cochrane library自建库至2017年7月20日发表的门冬氨酸鸟氨酸治疗脂肪肝患者的临床随机对照试验,应用Cochrane 手册进行风险偏倚评价,采用Jadad 7分量表进行文献质量评分.应用RevMan5.3进行Meta分析.结果纳入符合要求的9篇中文文献,共计727例脂肪肝患者.Meta 分析结果显示,门冬氨酸鸟氨酸治疗脂肪肝患者临床总有效率显著高于常规对照组[OR=3.71,95%CI(1.85,7.46),P=0.0002];降低总胆固醇合并效应值MD=-3.04,95%CI-3(.76,-2.31),P<0.0000,降低甘油三酯(TG)合并效应值MD=-1.60,95%CI (-2.55,-0.65),P=0.0009;降低血清ALT合并效应值MD=-34.04,95%CI(-61.73,-6.35),P=0.02;降低AST合并效应值MD=-9.48,95%CI(-24.66,5.70),P=0.22;相比异甘草酸镁治疗,门冬氨酸鸟氨酸治疗脂肪肝患者的临床总有效率显著升高[OR=4.06,95%CI(1.91,8.65),P=0.0003].结论门冬氨酸鸟氨酸治疗脂肪肝患者具有较好的治疗效果,可以改善肝功能指标,降低血脂水平.门冬氨酸鸟氨酸治疗脂肪肝患者的疗效尚需更多设计良好的临床试验证实.【期刊名称】《实用肝脏病杂志》【年(卷),期】2018(021)002【总页数】4页(P233-236)【关键词】脂肪肝;门冬氨酸鸟氨酸;疗效;Meta分析【作者】张志华;顾天翊;陈柳莹;陆伦根【作者单位】200080上海市上海交通大学附属第一人民医院消化科;200080上海市上海交通大学附属第一人民医院消化科;200080上海市上海交通大学附属第一人民医院消化科;200080上海市上海交通大学附属第一人民医院消化科【正文语种】中文目前,防治脂肪肝的主要措施包括去除病因、治疗原发病、调节饮食结构、运动和药物治疗等,但至今仍缺乏理想的特效药物[1,2]。

注射用门冬氨酸鸟氨酸Zhusheyong Mendong’ansuan Niao’ansuanOrnithine Aspartate for Injection本品为门冬氨酸鸟氨酸的无菌冻干品。
按平均装量计算,含门冬氨酸鸟氨酸(C 5H 12N 2O 2•C 4H 7NO 4)应为标示量的90.0%~110.0%。
【性状】 本品为白色或类白色的粉末或疏松块状物。
【鉴别】 (1)取本品约10mg ,加水2ml 使溶解,加茚三酮约2mg ,加热,溶液显蓝紫色。
(2)在有关物质检查项下记录的色谱图中,供试品溶液两主峰的保留时间应分别与系统适用性试验溶液中的门冬氨酸与鸟氨酸色谱峰的保留时间一致。
【检查】 酸度 取本品0.5g ,加水20ml 溶解后,依法测定(中国药典2010年版二部附录Ⅵ H ),pH 值应为6.0~7.0。
溶液的澄清度与颜色 取本品5瓶,分别加水适量使溶解并稀释制成每1ml 中含门冬氨酸鸟氨酸25mg 的溶液,溶液应澄清无色;如显浑浊,与1号浊度标准液(中国药典2010年版二部附录 B Ⅸ)比较,均不得更浓;如显色,与黄色2号标准比色液(中国药典2010年版二部附录 A Ⅸ第一法)比较,均不得更深。
有关物质 取装量差异项下的内容物适量(约相当于门冬氨酸鸟氨酸0.4g ),精密称定,置100ml 量瓶中,加0.02mol/L 磷酸二氢钾缓冲液40ml 使溶解,用乙腈稀释至刻度,摇匀,作为供试品溶液;精密量取供试品溶液适量,用流动相稀释制成每1ml 中约含门冬氨酸鸟氨酸8μg 的溶液,作为对照溶液;另精密称取马来酸、富马酸、精氨酸、3-氨基-2-哌啶酮(杂质Ⅰ)与门冬氨酸缩合物(杂质Ⅱ)对照品各适量,分别加流动相溶解并定量稀释制成每1ml 中约含4µg 的溶液,作为各杂质对照品溶液。
照门冬氨酸鸟氨酸有关物质检查项下的方法测定。
供试品溶液的色谱图中如有与上述各杂质对照品溶液主峰保留时间相同的色谱峰,按外标法以峰面积分别计算各已知杂质的含量:马来酸、富马酸和精氨酸的量均不得过标示量的0.1%,杂质Ⅰ不得过标示量的0.4%,杂质Ⅱ不得过0.15%;供试品溶液的色谱图中如有其他杂质峰,其他最大杂质峰面积不得大于对照溶液两主峰面积之和(0.2%);杂质总量不得过标示量的1.0%。

门冬氨酸钾镁注射液英文名:Potassium Aspartate and Magnesium Aspartate Injection汉语拼音:Men Dong An Suan Jia Mei Zhu She Ye【成份】本品为复方制剂,其组份为:每1ml中含门冬氨酸应为79-91mg、钾10.6-12.2mg、镁3.9-4.5mg。
辅料名称:注射用水。
【性状】本品为无色的澄明液体。
【适应症】电解质补充药。
用于低钾血症,低钾及洋地黄中毒引起的心律失常,病毒性肝炎,肝硬化和肝性脑病的治疗。
【规格】10ml/支【用法用量】静脉滴注一次10~20ml,加入5%或10%葡萄糖注射液500ml中缓慢滴注,一日1次。
【不良反应】(1)滴注太快时可能出现恶心、呕吐、血管疼痛、面色潮红、血压下降等症状。
(2)极少数可出现心率减慢,减慢滴速或停药后即可恢复。
(3)大计量可致腹泻。
【禁忌】高血钾、高血镁、肾功能不全及房室传导阻滞者慎用。
【注意事项】(1)本品未经稀释不得进行注射;滴注速度应缓慢。
(2)用于防治低钾血症时,需同时随访血镁浓度。
(3)除洋地黄中毒外,其他房室传导阻滞患者慎用。
(4)肾功能损害患者,活动性消化道溃疡患者慎用。
【孕妇及哺乳期妇女用药】无特殊禁忌。
【儿童用药】儿童酌减。
【老年患者用药】无特殊禁忌。
【药物过量】药物过量所致的高血钾、高血镁症,可用氯化钙、葡萄糖酸钙拮抗。
【药理毒理】门冬氨酸作为体内草酰乙酸的前体,在三羧酸循环中起重要作用,并参与鸟氨酸循环,使氨和二氧化碳结合生成脲素。
对细胞亲和力强,可作为钾、镁离子的载体,助其进入细胞内,提高细胞内钾、镁的浓度,加速肝细胞三羧酸循环,对改善肝功能、降低血清胆红素浓度有一定作用。
经肾脏代谢排出体外。
【药代动力学】未进行该项实验且无可靠参考文献。
【药物相互作用】不宜与保钾利尿药合用。
【贮藏】遮光,密闭保存。
【包装】安瓿包装,5支/盒,10支/盒。
保肝药:能改善肝脏功能,促进肝细胞再生,增强肝脏解毒功能等作用的药物。
《临床用药须知》1. 解毒保肝类此类药物能为肝脏提供巯基或葡萄糖醛酸,可以增强肝脏的氧化、还原、水解等化学反应解毒功能,或者络合重金属将有毒物质转变成水合物,通过尿液或胆汁排出体外,减少有害物质对肝脏的损害,起到保护肝脏的作用。
1.1注射用还原型谷胱甘肽(阿拓莫兰)1.8g,45.14元注射用还原型谷胱甘肽(双益健)0.9g, 26.04元适应症:化疗患者:包括用顺氯铵铂、环磷酰胺、阿霉素、红比霉素、博来霉素化疗,尤其是大剂量化疗时。
放射治疗患者。
各种低氧血症:如急性贫血,成人呼吸窘迫综合症,败血症等。
肝脏疾病:包括病毒性、药物毒性、酒精毒性 (包括酒精性脂肪肝、酒精性肝纤维化、酒精性肝硬化、急性酒精性肝炎) 及其他化学物质毒性引起的肝脏损害。
亦可用于有机磷、胺基或硝基化合物中毒的辅助治疗;解药物毒性 (如肿瘤化疗药物,抗痨药物,精神神经科药物,抗抑郁药物,扑热息痛等)。
1.2注射用硫普罗宁(凯西莱)0.1g,17.24元适应症:改善各类急慢性肝炎的肝功能。
用于脂肪肝、酒精肝、药物性肝炎损伤及重金属解毒。
用于降低放化疗的不良反应,并可预防放化疗所致的外周白细胞减少。
用于老年性早起白内障和玻璃体混浊。
1.3葡醛内酯片(肝泰乐) 0.1g,0.1元适应症:用于急慢性肝炎的辅助治疗。
1.4 水飞蓟宾葡甲胺片(西利宾胺)50mg, 1.05元适应症:用于急、慢性肝炎,初期肝硬化,中毒性肝损害的辅助治疗。
2. 促肝细胞再生类此类药物能加速修复肝细胞,使受损的肝功能和酶活力恢复正常,从而促进肝细胞的再生。
2.1 促肝细胞生长素注射液(威佳) 2ml:30ug, 33.52元注射用促肝细胞生长素120mg,72.21元适应症:用于亚急性重症肝炎(病毒性;肝功衰竭早期或中期)的辅助治疗。
2.2 多烯磷脂酰胆碱注射液(易善复)5ml:232.5mg, 26.14元多烯磷脂酰胆碱注射液5ml:232.5mg, 25.28元多烯磷脂酰胆碱胶囊(易善复)228mg, 1.93元适应症:辅助改善中毒性肝损伤(如药物、毒物、化学物质和酒精引起的肝损伤等)以及脂肪肝和肝炎患者的食欲不振、右上腹压迫感。
肝性脑病(HE)是肝硬化患者严重并发症,为死亡主因之一,发病机制尚未完全阐明。
多年来研究证明,氨中毒假说是HE主要发病机理。
近年来的临床研究表明门冬氨酸-鸟氨酸对肝硬化并发肝性脑病具有一定疗效,为进一步探讨门冬氨酸-鸟氨酸对肝性脑病临床疗效,我们对56例肝性脑病患者进行治疗,现报道如下。
1 材料与方法1.1 一般资料1.1.1 对2006年9月~2009年6月间我院消化科符合肝性脑病诊断标准[1]住院患者56例,其中男36例,女20例,平均年龄(58.4±13.3)岁。
随机分为治疗组28例和对照组28例。
两组年龄、性别、病因、病程、肝功能Child-Pugh分级以及肝性脑病临床分期等均有可比性。
1.1.2 治疗方法 治疗组在常规治疗的基础上加用门冬氨酸-鸟氨酸(瑞苷,武汉启瑞药业有限公司提供,2.5g/支)10.0g加入葡萄糖或生理盐水250mL,1次/日,12h/次,静脉滴注5d,至患者完全清醒后减半;而对照组仅采用常规治疗。
1.1.3 观察项目 测定两组患者治疗前、后血清氨的含量,观察门冬氨酸-鸟氨酸对肝性脑病疗效,包括神志转清醒时间和数字连接试验(NCT)及数字符号试验(DS)。
1.1.4 统计学处理 计数资料以均数±标准差(x ±s )表示,采用SPSS10.05软件,做t 检验并比较分析。
2 结果2.1 血氨变化 肝性脑病患者血氨含量明显增加,且与肝性脑病临床程度有关(r=0.724,P <0.05),如表1;治疗后两组患者血氨含量明显下降(P <0.05),且治疗组比对照组明显下降(P <0.01),见表2。
2.2 神志转清时间 从治疗至完全清醒时间,治疗组为3.5~12.6h,平均为(7.53±3.40h);而对照组为9.7~45.5h,平均(11.67±8.12h),两组比较(P <0.05),详见表2。
2.3 智力试验 清醒后5d行NCT和DS。