盐酸麻黄碱注射液说明书
- 格式:doc
- 大小:13.00 KB
- 文档页数:2
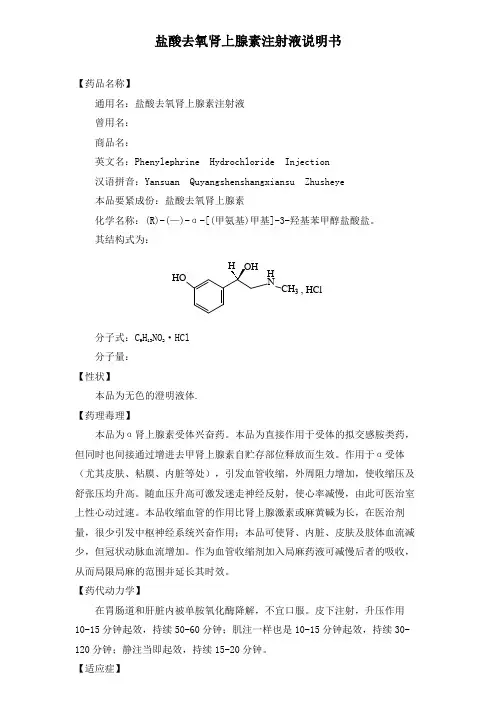
盐酸去氧肾上腺素注射液说明书【药品名称】通用名:盐酸去氧肾上腺素注射液曾用名:商品名:英文名:Phenylephrine Hydrochloride Injection汉语拼音:Yansuan Quyangshenshangxiansu Zhusheye本品要紧成份:盐酸去氧肾上腺素化学名称:(R)-(—)-α-[(甲氨基)甲基]-3-羟基苯甲醇盐酸盐。
其结构式为:分子式:C 9H 13NO 2·HCl分子量:【性状】本品为无色的澄明液体.【药理毒理】本品为α肾上腺素受体兴奋药。
本品为直接作用于受体的拟交感胺类药,但同时也间接通过增进去甲肾上腺素自贮存部位释放而生效。
作用于α受体(尤其皮肤、粘膜、内脏等处),引发血管收缩,外周阻力增加,使收缩压及舒张压均升高。
随血压升高可激发迷走神经反射,使心率减慢,由此可医治室上性心动过速。
本品收缩血管的作用比肾上腺激素或麻黄碱为长,在医治剂量,很少引发中枢神经系统兴奋作用;本品可使肾、内脏、皮肤及肢体血流减少,但冠状动脉血流增加。
作为血管收缩剂加入局麻药液可减慢后者的吸收,从而局限局麻的范围并延长其时效。
【药代动力学】在胃肠道和肝脏内被单胺氧化酶降解,不宜口服。
皮下注射,升压作用10-15分钟起效,持续50-60分钟;肌注一样也是10-15分钟起效,持续30-120分钟;静注当即起效,持续15-20分钟。
【适应症】, HClCH 3用于医治休克及麻醉时维持血压。
也用于医治室上性心动过速。
【用法用量】(1)血管收缩,局麻药液中每20ml可加本品1mg,达到1:20000浓度;蛛网膜下腔阻滞时,每2~3ml达到1:1000浓度。
(2)升高血压,轻或中度低血压,肌内注射2~5mg,再次给药距离不短于10~15分钟,静脉注射一次,按需每隔10~15分钟给药一次。
(3)阵发性室上性心动过速,初量静脉注射,20~30秒钟注入,以后用量递增,每次加药量不超过~,一次量以1mg为限。

盐酸赖氨酸注射液
英文名:Lysine Hydrochloride Injection
汉语拼音:Yan Suan Lai An Suan Zhu She Ye
【成份】
化学名称:L-2,6-二氨基乙酸盐酸盐,分子式:C6H14N2O2·HCl,分子量:182.65,学结构式:
【性状】
本品为无色或微黄色澄明液体。
【适应症】
本品为用于治疗颅脑外伤、慢性脑组织缺血、缺氧性疾病的脑保护剂。
【规格】
10ml:3g
【用法用量】
成人每日一次,每次10ml(一支),用生理盐水或5%葡萄糖注射液250ml稀释后,缓慢静脉滴注,20次为一个疗程,或遵医嘱。
【不良反应】
少数患者出现轻度胃肠不适。
【禁忌】
尚不明确。
【注意事项】
急性缺血性脑血管病慎用。
【孕妇及哺乳期妇女用药】
尚不明确。
【儿童用药】
尚不明确。
【老年患者用药】
尚不明确。
【药物过量】
尚不明确。
【药理毒理】
药理作用:L-赖氨酸是人体8种必需氨基酸之一,能促进人体发育、增强免疫功能,并有提高中枢神经组织功能的作用。
毒理研究:尚不明确。
【药代动力学】
尚不明确。
【药物相互作用】
尚不明确。
【贮藏】
遮光,密闭,置阴凉处(不超过20℃)保存。

含特殊药品复方制剂管理含特殊药品复方制剂包括含麻黄碱类复方制剂、复方地芬诺酯片和复方甘草片、复方可待因口服溶液。
其中食药总局、公安部、卫计委联合发布2015第10号公告自2015年5月1日起,将含可待因口服溶液制剂列入第二类精神药品管理。
经营该类药品不需要单独审批,但在管理上有严格的要求。
因为这些药品可直接做毒品被滥用或用于提取制造毒品,危害公众健康安全。
含麻黄碱类复方制剂中的麻黄碱类是指《易制毒化学品管理条例》(国务院令445号)中,附表《易制毒化学品的分类和品种目录》第一类的第12项,包括麻黄素、伪麻黄素、消旋麻黄素、去甲麻黄素、甲基麻黄素、麻黄浸膏、麻黄浸膏粉等麻黄素类物质,不包括含麻黄的中成药)。
复方地芬诺酯片(甲类OTC,每片含盐酸地芬诺酯 2.5mg、硫酸阿托品0.025mg。
主要用于治疗急、慢性功能性腹泻及慢性肠炎等)。
复方甘草片(主要成份甘草流浸膏粉、阿片粉、樟脑、八角茴香油等。
为“老牌”的祛痰止咳药,由于有良好的祛痰镇咳作用及价廉的特点,在止咳药中占有一定的位置。
其中的管制成分是阿片粉。
)《关于切实加强部分含特殊药品复方制剂销售管理的通知》(国食药监安[2009]503号)中规定:1.具有《药品经营许可证》的企业均可经营含特殊药品复方制剂。
药品生产企业和药品批发企业可以将含特殊药品复方制剂销售给药品批发企业、药品零售企业和医疗机构。
药品零售企业销售含特殊药品复方制剂时,处方药应当严格执行处方药与非处方药分类管理有关规定,非处方药一次销售不得超过5个最小包装(2012年改为2个最小包装,而且登记购买人身份证号)。
药品生产、批发企业经营含特殊药品复方制剂时,应当按照药品GMP、药品GSP的要求建立客户档案,核实并留存购销方资质证明复印件、采购人员(销售人员)法人委托书和身份证明复印件、核实记录等;指定专人负责采购(销售)、出(入)库验收、签订买卖合同等。
销售含特殊药品复方制剂时,如发现购买方资质可疑的,应立即报请所在地设区的市级药品监管部门协助核实;发现采购人员身份可疑的,应立即报请所在地县级以上(含县级)公安机关协助核实。

盐酸纳布啡注射液核准日期:2013年11月27日修改日期:2014年04月28日【药品名称】通用名称:盐酸纳布啡注射液? ?? ?? ?? ?? ???商品名:瑞静?英文名:Nalbuphine Hydrochloride Injection【成份】本品主要成份为盐酸纳布啡。
化学名称:(-)-17-(环丁烷甲基)-4,5α-环氧吗啡-3,6α,14-羟基盐酸盐倍半水合物。
化学结构式为:分子式:C 21H 27NO 4 ·HCl·11/2H 2O分子量:420.93本品的辅料:枸橼酸,枸橼酸钠,氯化钠。
【性状】本品为无色的澄明液体。
【适应症】盐酸纳布啡作为复合麻醉时诱导麻醉的辅助用药。
【规格】2ml:20mg【用量用法】诱导麻醉时,盐酸纳布啡的用量为0.2mg/kg,应在10---15分钟内静脉输注完。
使用盐酸纳布啡注射液过程中,若出现呼吸抑制现象,可用阿片受体拮抗剂纳洛酮逆转。
【不良反应】据国外文献报道,临床用纳布啡治疗中,最常见的不良反应为镇静,临床1066例接受该药治疗的患者381例出现了镇静(发生率为36%)。
不常见的不良反应包括:多汗99例(9%),恶心/呕吐68例(6%)、眩晕58例(5%)、口干44例(4%)和头痛27例(3%)。
此外还可发生一些罕见的不良反应(报道的发生率为1%或更低)中枢神经系统效应:神经质、抑郁、坐立不安、烦躁尖叫、欣快、敌意、多梦、精神错乱、晕厥、幻觉、焦虑、悲观、麻木、麻刺感,心理反应,如非真实感、人格解体、妄想、焦虑和幻觉的发生率较使用喷他佐辛时低。
心血管系统:高血压、低血压、心动过缓、心动过速;消化系统:胃肠绞痛、消化不良、口苦;呼吸系统:呼吸抑制、呼吸困难、哮喘;皮肤:瘙痒、干燥、荨麻疹;其他症状:吐字不清、尿急、视物模糊、面部潮红;过敏反应:在使用纳布啡过程中可出现过敏反应。
严重过敏反应也有报道,若出现了过敏反应应立即采取药物支持治疗。



一、目的加强我站含特殊药品复方制剂的管理,有效遏制含特殊成份药品复方制剂从药用渠道流失和滥用,特制定本规程。
二、依据《中华人民共和国药品管理法》及其实施条例;《药品经营质量管理规范》;《药品经营质量管理规范现场检查指导原则》;《药品流通监督管理办法》;《关于规范药品购销活动中票据管理有关问题的通知》(国食药监安[2009]283号);《关于切实加强部分含特殊药品复方制剂销售管理的通知》(国食药监安〔2009〕503号);《关于进一步加强含可待因复方口服溶液、复方甘草片和复方地芬诺酯片购销管理的通知》(食药监办药化监〔2013〕33号);《食品药品监管总局办公厅关于进一步加强含麻醉药品和曲马多口服复方制剂购销管理的通知》(食药监办药化监〔2014〕111号);《关于加强含可待因复方口服液体制剂管理的通知》(食药监药化监〔2015〕46号);《关于将含可待因复方口服液体制剂列入第二类精神药品管理的公告》(2015年第10号);《含特殊药品复方制剂管理制度》等。
三、适用范围本站含特殊药品复方制剂进销存各过程,包括购进、验收、储存养护检查、销售、出库复核、运输、退货、报损及安全等环节的操作流程。
含特殊药品复方制剂包括含麻黄碱类复方制剂(不包括含麻黄的中成药)、含麻醉药品和曲马多口服复方制剂、复方地芬诺酯片和复方甘草片。
对该类药品的管理,除应遵守国家的法律、法规、规章和本站质量管理制度中对一般药品管理的规定外,还应遵守本操作规程的各项要求。
依据《关于将含可待因复方口服液体制剂列入第二类精神药品管理的公告》(2015年第10号),含可待因复方口服液体制剂(包括口服溶液剂、糖浆剂)列入第二类精神药品管理,不属于含特殊药品复方制剂。
四、责任质量管理部、综合内务部、销售部对本操作规程实施负责。
五、内容(1)我站指定综合内务部采购管理组具体负责该类药品的采购工作。
综合内务部采购管理组会同质量管理部审核供货单位的法定资格和质量信誉,并建立首营企业(供货单位)档案。

盐酸奈福泮氯化钠注射液使用说明书请仔细阅读说明书并在医师指导下使用盐酸奈福泮氯化钠注射液使用说明书【药品名称】通用名称:盐酸奈福泮氯化钠注射液英文名称:Nefopam Hydrochloride and Sodium chloride Injection汉语拼音:Yansuan Naifupan Lühuana Zhusheye【成份】本品主要成份为:盐酸奈福泮。
【性状】本品为无色的澄明液体。
【适应症】用于术后止痛、癌症痛、急性外伤痛。
亦用于急性胃炎、胆道蛔虫症、输尿管结石等内脏平滑肌绞痛。
局部麻醉、针麻等麻醉辅助用药。
【规格】100ml:20mg(盐酸奈福泮)-900mg(氯化钠)【用法用量】缓慢静脉滴注,常用量一次20mg,必要时每3~4小时1次,或遵医嘱。
滴注时患者应躺下,滴注完后15分钟方可起身。
【不良反应】有心绞痛、心动过速、癫痫发作、神经刺激症状、呼吸抑制、尿潴溜、肝功能异常、嗑睡、恶心、出汗、头晕、头痛等,但一般持续时间不长。
偶见口干、眩晕、皮疹。
【禁忌】严重心血管疾病,心肌梗死或惊厥者禁用;服用单胺氧化酶抑制剂者禁用;对本品中任何成份过敏者禁用。
【注意事项】(1)有中风病史、青光眼、尿潴留和严重肝、肾功能不全者慎用。
(2)服用三环类抗抑郁药物者慎用。
(3)因本品可引起嗜睡,所以,驾驶者和机械操作者慎用。
【孕妇及哺乳期妇女用药】对孕妇的影响尚不明确;由于乳汁中的药物浓度与血浆中的浓度相当,故哺乳期妇女使用应遵医嘱。
【儿童用药】尚缺乏本品儿童用药的有效性和安全性资料。
【老年用药】尚缺乏本品老年患者用药的有效性和安全性资料。
【药物相互作用】(1)本品不宜与抗惊厥药合用。
(2)本品不得与单胺氧化酶抑制剂合用。
(3)本品与可待因、喷他佐辛、右丙氧酚合用时,后者的副作用和成瘾性增强。
【药物过量】药物过量可引起兴奋,宜用地西泮解救,并用常规支持疗法。
【药理毒理】奈福泮为一种新型的非麻醉性镇痛药,兼有轻度的解热和肌松作用。
盐酸麻黄碱注射液说明书
【药品名称】
通用名:盐酸麻黄碱注射液
英文名:Ephedrine Hydrochloride Injection
汉语拼音:Yansuan Mahuangjian Zhusheye
本品主要成分及其化学名称为:本品主要成分为盐酸麻黄碱,化学名称为(1R,2S)-2-甲氨基-苯
丙烷-1-醇盐酸盐
分子式:C10H15NO.HCl 分子量:201.70
【性状】本品为无色的澄明液体
【药理作用】本品可直接激动肾上腺素受体,也可通过促使肾上腺素能神经末梢释放去甲肾
上腺素而间接激动肾上腺素受体,对α和β受体均有激动作用.可舒张支气管并收缩局部血管,
其作用时间较长;加强心肌收缩力,增加心输出量,使静脉回心血量充分;有较肾上腺素更强
的兴奋中枢神经作用
【药代动力学】肌注或皮下注射很快被吸收,可通过血脑屏障进入脑脊液.肌注10~20分钟起
效,持续作用肌注或皮下注射25~50mg小时.T1/2当尿pH 为5时约3小时,尿pH值为6.3
时约6小时.吸收后仅有少量经脱胺氧化,大部分以原形自尿排出
【适应症】用于蛛网膜下腔麻醉或硬膜外麻醉引起的低血压症及慢性低血压症
【用法用量】
1.常用量 皮下或肌内注射一次15~30mg(05-1支),一日3次
2.极量 皮下或肌内注射一次60 mg(2支),一日150 mg
【不良反应】
①对前列腺肥大者可引起排尿困难;
②大剂量或长期使用可引起精神兴奋震颤、焦虑、失眠、心痛、心悸、心动过速等
【禁忌症】甲状腺机能亢进、高血压、动脉硬化、心绞痛等病人禁用
【注意事项】
⑴交叉过敏反应 对其他拟交感胺类药,如肾上腺素、异丙肾上腺素等过敏者,对本品也过敏
⑵如有头痛、焦虑不安、心动过速、眩晕、多汗等症状,应注意停药或调整剂量
⑶短期内反复用药,作用可逐渐减弱(快速耐受现象),停药数小时后可以恢复.每日用药如不超
过3次,则耐受现象不明显
【孕妇及哺乳期妇女用药】
⑴剖腹产麻醉过程中用本品维持血压,可加速胎儿心跳,当母体血压超过
17.3/10.7kPa(130/80mmHg)时不宜用
⑵本品可分泌入乳汁,哺乳期妇女禁用
【儿童用药】
【老年患者用药】
【药物相互作用】
⑴与肾上腺皮质激素合用,本品可增加它们的代谢清除率,须调整皮质激素的剂量
⑵尿碱化剂,如制酸药、钙或镁的碳酸盐、枸橼酸盐、碳酸氢钠等,影响本品在尿中的排泄,
增加本品的半衰期,延长作用时间,特别是如尿保持碱性几日或更长,患者大多致麻黄碱中毒,
本品用量应调整
⑶与α受体阻滞药如酚妥拉明、哌唑嗪、妥拉唑林以及酚噻嗪类药合用时,可对抗本品的加
压作用
⑷与全麻药如氯仿、氟烷、异氟烷等同用,可使心肌对拟交感胺类药反应更敏感,有发生室性
心律失常危险,必须同用时,本品用量应减小
⑸与三环类抗抑郁药如马普替林同用时,降低本品的加压作用
⑹与洋地黄苷类合用,可致心律失常
⑺与麦角新碱、麦角胺或缩宫素同用,可加剧血管收缩,导致严重高血压或外围组织缺血
⑻与多沙普仑同用,两者的加压作用均可增强
【药物过量】
【规格】1ml:30mg
【贮藏】遮光,密闭保存