颅内外动脉狭窄的测量(最详细)
- 格式:ppt
- 大小:8.00 MB
- 文档页数:31

颈动脉狭窄及药物治疗一、疾病简介颈动脉狭窄(carotid atery stenosis,CAS)是一类由于动脉粥样硬化等原因引起颅外颈动脉系统狭窄或闭塞的疾病。
颈动脉狭窄是导致缺血性脑卒中的重要原因之一。
由于颈动脉狭窄导致的卒中约占所有缺血性卒中的8%~11%。
颅外颈动脉狭窄的患者年卒中发生率约为13.4/10万人。
药物治疗及外科干预的目的是减少卒中的发生率。
(一)病因和发病机制颈动脉狭窄的病因主要是动脉粥样硬化,约占90%,其他病因还包括大动脉炎、纤维肌性发育不良、外伤、颈动脉迁曲、先天性动脉闭锁、肿瘤、夹层、动脉炎、放疗后纤维化等。
受到血流动力学的影响,动脉粥样硬化性颈动脉狭窄主要好发于颈动脉分叉部位。
颈动脉狭窄或闭塞可能导致缺血性脑卒中的原因主要有两方面,一是颈动脉粥样斑块脱落或斑块破裂形成栓塞或血栓形成,二是严重的狭窄或闭塞造成的直接脑灌注减少。
因为颅内外存在广泛的代偿机制,因此由低灌注引起的缺血性脑卒中较为少见。
颈动脉狭窄导致缺血性脑卒中的风险大小与颈动脉狭窄的程度和斑块的性质有关。
通常认为易损斑块(vulnerable plaque)较稳定斑块更容易导致缺血性脑卒中的发生。
(二)临床表现颈动脉狭窄可以是无症状的,患者只有在做体格检查时才被发现。
也有部分颈动脉狭窄是症状性的,主要症状包括局灶性脑缺血表现、全脑缺血、腔隙性脑梗死或者认知功能障碍。
局灶性脑缺血表现主要包括短暂脑缺血发作(transient ischemic attacks,TIA)和脑卒中。
患者可以出现单眼失明或黑蒙、单侧肢体或偏侧肢体无力、麻木、构音障碍、语言障碍、偏盲、霍纳综合征等表现。
TIA被认为是一次小的缺血事件,持续时间从几分钟到几小时,最长不超过24小时。
TIA的患者在后续5年发生脑卒中的风险约为30%。
脑卒中患者由于大脑局灶梗死,其症状持续时间超过24小时,症状的严重程度与脑梗死的面积相关。
NIHSS评分常用于评估脑卒中患者症状严重程度和预后情况。

头部核磁和头部多普勒1.引言1.1 概述头部核磁共振成像(MRI)和头部多普勒超声技术作为现代医学诊断中的两项重要技术,被广泛应用于头部疾病的检测和评估。
头部核磁共振成像以磁共振原理为基础,通过对头部组织的信号进行收集和分析,可以生成高质量的图像,提供详尽而准确的解剖学信息。
而头部多普勒则是利用超声波传播的速度、方向和频率变化来观察和评估头部血管的血流情况,从而帮助医生诊断血管相关的疾病。
头部核磁共振成像技术的发展,使得医生在诊断脑部肿瘤、中风等疾病时有了更加准确和可靠的手段。
通过利用核磁共振成像技术,医生可以清晰地观察到脑组织结构、解剖学特征和异常信号的变化,从而可以更好地进行病灶的定位和定性。
此外,头部核磁共振成像还可以提供脑功能成像,通过检测不同脑区的活动水平,帮助医生了解神经系统的功能状态,进一步诊断和治疗神经系统相关的临床问题。
头部多普勒超声技术则主要用于评估头部的血管功能和血流情况。
该技术利用超声波对头部血流进行实时监测和分析,可以评估血管的血流速度、血流方向、血流量等参数,从而帮助医生诊断和治疗脑血管相关的疾病。
头部多普勒超声广泛应用于病理性疾病的鉴别和脑血管病变的评估,如脑卒中、脑梗塞、脑血管瘤等。
其非侵入性、实时性和可重复性等特点,使其成为临床医生首选的头部血流动力学评估工具。
综上所述,头部核磁共振成像和头部多普勒超声是两种不同的技术手段,但在头部疾病的检测和评估中起着至关重要的作用。
它们的应用领域广泛,并且在临床实践中已经取得了显著的成果。
然而,它们各自也存在一定的局限性和特点,需要进一步完善和发展。
因此,在未来的发展中,需要进一步深入研究和探索,以提高其在头部疾病诊断和治疗中的应用价值。
1.2 文章结构文章结构部分的内容:本文主要分为引言、正文和结论三个部分。
1. 引言:引言部分对头部核磁和头部多普勒进行简要介绍,概述其应用和作用,并说明文章的目的。
2. 正文:正文部分主要包括头部核磁和头部多普勒的详细介绍。


颅内MR血管壁成像技术与应用中国专家共识Ⅰ研究证据表明,颅内动脉狭窄是中国人群缺血性卒中的主要原因,约占46.6%[1]。
导致颅内动脉狭窄的病因主要包括动脉粥样硬化、夹层、血管炎、烟雾病和可逆性脑血管收缩综合征(reversible cerebral vasoconstriction syndrome,RCVS)等[2]。
单纯利用传统的CTA、MRA等针对血管的成像手段,无法准确判断血管壁本身的情况及其病理学特征的相关信息。
此外,对于动脉粥样硬化性病变,斑块的大小、形态、信号强度和强化特征均与易损性相关,而这些特征亦无法通过管腔成像获得。
然而,由于不同类型的血管壁病变其临床治疗策略和预后均存在一定的差异,因此,在治疗前明确颅内动脉狭窄的病因具有重要临床意义。
此外,颅内动脉易损斑块具有更高的脑血管事件发病风险,评估颅内斑块的易损性有助于预测未来发生脑血管事件的风险。
MR血管壁成像最初仅被应用于颈动脉斑块的评估。
该技术能够准确定性和定量评价动脉管壁的形态和信号特征,是诊断颈动脉和颅内动脉管壁病变的最佳无创性方法。
然而受到空间分辨率的限制,应用MR血管壁成像评估颅内动脉管壁病变仍然存在一定的挑战。
随着MR成像技术的进展,颅内动脉血管壁成像已由二维(two dimension,2D)成像进入到了三维(three dimension,3D)成像的新阶段[3]。
由于3D成像具有更高的各向同性分辨率、更快的成像速度和更大的覆盖范围等优势,其在颅内动脉管壁病变的诊断方面发挥着越来越重要的作用。
然而,由于颅内动脉MR血管壁成像的质量和效果受到磁场强度、接收线圈、成像维度、成像序列、空间分辨率等软硬件条件和成像参数的影响,不同成像中心或医院之间的MR软硬件配置和成像参数均存在一定的差异,缺乏规范化的成像方案,难以实现对图像的标准化判读分析。
我国颅内动脉高分辨血管壁成像起步较早[4],但目前仍缺乏规范化成像技术及临床应用方案。



2024未破裂颅内动脉瘤临床管理指南(全文)摘要未破裂颅内动脉瘤(UIA)在我国35~75岁成人中的患病率约7%。
随着人口老龄化趋势,UIA检出率增加。
大多数UIA是偶然发现的,通常无症状,选择手术治疗还是保守治疗一直存在争议。
尽管UIA的年破裂风险低,但一旦发生破裂,其致死率和致残率高。
本临床管理指南基于循证证据,围绕UIA的人群筛查、临床影像诊断、生长破裂风险评估、治疗策略及选择、术后随访和特殊人群UIA管理建议等方面,共形成44条推荐意见,旨在为临床医师、其他相关专业人员提供实用的临床指导建议。
颅内动脉瘤,一种动脉壁异常膨出所形成的突起,普遍存在于全球成年人群中。
据统计,全球范围内,在50岁左右的人群中未破裂颅内动脉瘤(unruptured intracranial aneurysm,UIA)患病率约3%。
颅内动脉瘤的破裂是导致自发性蛛网膜下腔出血(SAH)的主要原因,其全球发病率约6.1/100 000人年,不同地区差异显著,特别是在日本和芬兰,该病症尤为常见。
尽管不同地区的死亡率有所下降,但大多数患者仍遗留有明显的神经功能障碍,严重影响了患者的生活质量。
随着影像学技术的进步和人口老龄化趋势,UIA的检出率逐渐提高。
在中国,35~75岁成人中的UIA患病率约7%。
大多数UIA是偶然发现的,这些动脉瘤通常无症状,绝大多数不会发生破裂出血。
由于外科夹闭手术和血管内介入手术治疗均存在潜在风险,因此,对于偶然发现的UIA,选择积极手术治疗还是保守治疗一直存在争议。
尽管UIA的年破裂率低,但一旦发生破裂,可能导致致命的SAH,不仅病死率高,还会在幸存者中留下严重的神经功能障碍,给患者家庭和社会造成沉重的负担。
因此,关于UIA的筛查、破裂风险评估及其处理策略是临床管理的重要组成部分。
二、UIA的流行病学与筛查推荐意见1:对于常染色体显性多囊肾病(autosomal dominant polycystic kidney disease,ADPKD)患者,特别是在有动脉瘤家族史的情况下,建议定期进行颅内动脉瘤的筛查。

经颅多普勒超声操作流程不同医疗机构之间的TCD自从经颅多普勒超声(TCD)发明以来,这项技术在临床的使用不断扩展。
但检查程序、需要检测的血管数量、常规使用的深度范围以及报告形式各有不同。
鉴于血管检查的重要性,有必要制定标准化的检查程序和诊断标准。
1 完整的诊断性TCD检查技术TCD是一种无创伤性的检查手段,Rune Aaslid报导了利用单通道频谱TCD评价脑血流动力学的方法,操作过程中使用了颞窗、眼窗、枕窗及下颌下窗(图1A、B)。
完整的TCD检查不仅要评价双侧脑血管,还要利用上述4窗分别探查前循环和后循环的血流情况。
颞窗通常是用来探查大脑中动脉(MCA)、大脑前动脉(ACA)、大脑后动脉(PCA)、颈内动脉(ICA)终末段或颈内动脉C1段的血流信号。
眼窗用于眼动脉(OA)和颈内动脉虹吸部检查。
枕窗则通过枕骨大孔来观察椎动脉(VA)远端和基底动脉(BA)。
脑血流动力学应该被视为一个内部相互依赖的系统。
尽管每段血管都有自己的特定深度范围,但是应该意识到它们的形态学表现、血流速度以及搏动情况会因解剖变异不同,因Willis环或其它部位的血管出现疾患而受到影响发生变化。
无论是脑缺血还是存在卒中风险,以及在神经重症监护病房或有痴呆等慢性病的患者,在施行完整的诊断性TCD时,均应检查双侧的脑动脉,包括:大脑中动脉M2段(深度30~40 mm),M1段(40~65 mm),大脑前动脉A1段(60~75 mm),颈内动脉C1段(60~70 mm),大脑后动脉P1~P2段(55~75 mm),前交通动脉(AComA)(70~80 mm),后交通动脉(PComA)(58~65 mm),眼动脉(40~50 mm),颈内动脉虹吸部(55~65 mm),椎动脉(40~75 mm),基底动脉近段(75~80 mm)、中段(80~90 mm)、远段(90~110 mm)。
尽管没有额外要求一定要对血管分支进行检查,例如大脑中动脉的M2段,但只要诊断需要就应该实施完整的TCD检查。


中国颈动脉狭窄介入诊疗指导规范(最全版)脑血管病是我国致死致残率最高的疾病,其中颈动脉狭窄是缺血性脑卒中的常见发病原因。
已有多项随机试验证实颈动脉内膜剥脱术(carotid endarterectomy,CEA)能够有效降低颈动脉狭窄患者的卒中风险。
近年来,随着介入治疗器械和技术的进步,颈动脉支架成形术(carotid artery stenting,CAS)正在成为可能替代CEA的一种微创、安全和有效的颈动脉狭窄血流重建手段。
本规范依据国内外重要CAS指南内容和最新循证医学的证据编写,目的是为脑卒中筛査和防控基地医院有美医师提供临床参考。
一、颈动脉粥样硬化性疾病的自然病史北美症状性颈动脉狭窄内膜剥脱术试验(North American Symptomatic Carotid Endarterectomy Trial,NAS CET)对症状性颈动脉狭窄程度与卒中风险的关系有清晰的描述。
在18个月的内科药物治疗期间狭窄程度为70%-79%的患者卒中风险为19%,狭窄程度为80%-89%的患者卒中风险为33%,狭窄程度为90%-99%的患者卒中风险为33%。
对于近全闭塞的患者风险下降。
但对于无症状患者卒中风险与狭窄严重程度间的关系在其它研究中尚不明确。
早期的研究显示≥75%无症状狭窄患者累积的年卒中风险超过5%,无症林颈动脉狭窄外科试验(symptomatic Carotid Surgery Trial,ACST)显示狭窄程度≥7%药物治疗的患者中5年同侧卒中或死亡率仅为4.7%。
越来越多的研究显示在积极的药物治疗下无症状中重度颈动脉狭窄患者神经系统事件发生率相对较低。
二、颈动脉狭窄的病因及病理生理学1.颈动脉狭窄病因学颈动脉狭窄的主要病因有动脉粥样硬化、大动脉炎及纤维肌肉结构不良等,其它病因如外伤、动脉扭转、先天性动脉闭锁、肿瘤、动脉或动脉周围炎、放疗后纤维化等较少见。
在欧洲的一些国家和美国,约90%的颈动脉狭窄是由动脉粥样硬化所致;在我国中青年患者中,大动脉炎也是比较常见的病因。
脑功能监测脑功能监测(cerebral function monitor)是指采用脑功能研究工具对患者大脑功能的病理生理变化进行监测,可以指导临床治疗,以求最大限度减少全身或脑部病变带来的脑功能损害,促进脑功能恢复。
目前常用的监测项目包括颅内压监测、脑电监测、脑血流监测和脑组织氧合监测。
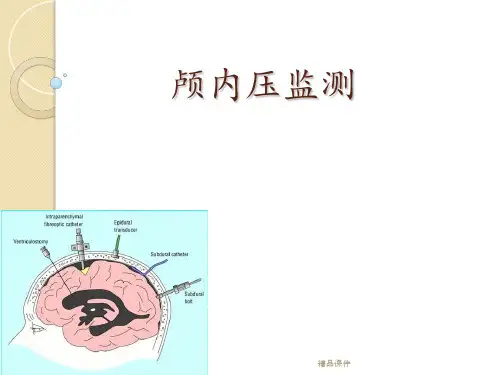
一、颅内压监测颅腔的内容物包括脑组织、脑脊液和血液使颅内保持一定的压力,称为颅内压。
通常机体可以通过调节颅内血容量和脑脊液含量使颅内压在一定范围内波动。
颅内占位或继发性脑水肿等病变超出颅腔的代偿能力,可导致颅内压升高,甚至脑疝。
因此,需要监测颅内压以指导临床处理。
(一)适应证1.创伤性脑损伤急性颅脑创伤后3~5天病情变化迅速,且仅依据临床征象不能反映颅内压增高水平,颅内压监测可以准确及时地发现颅内压变化。
2.急性脑血管病变对于蛛网膜下腔和脑室出血,在监测颅内压的同时还可以引流血性的脑脊液,减轻继发性脑损害。
3.缺血缺氧性脑病心搏骤停、窒息、中毒等各种原因引起全脑的缺血、缺氧,可发生脑水肿、颅内压增高。
(二)方法颅内压监测分为有创监测和无创监测两类。
1.有创监测(1)脑室内测压:通常选择冠状缝前1cm、中线旁开2.5cm处颅骨钻孔,穿刺侧脑室置入测压管,另一端连接压力传感器进行持续测压。
该方法简单、准确,可取获脑脊液样本或释放脑脊液降颅压,也可注入药物治疗或注入液体,测量脑室顺应性。
但此法偶有穿刺困难,可能损伤颅内静脉窦,存在感染风险,一般置管不超过1周。
(2)硬脑膜下测压:颅骨钻孔后打开硬脑膜,置入专用的中空螺栓至蛛网膜表面,并与之贴紧;螺栓内注入液体,连接传感器。
此法不穿透脑组织、不进入侧脑室,穿刺简单,避开静脉窦,可多处选点测压。
但需打开硬脑膜,有感染的机会,且准确性受螺栓与脑表面紧贴程度影响,干扰因素多,现临床上已经较少应用。
(3)硬膜外测压:将传感器置于颅骨与硬膜之间,所测压力较脑室内测压高2~3mmHg。
脑血流监测目前监测脑组织血流的方法很多,临床研究中比较常用的有氢清除法、放射核素法、单光子发射计算机断层法(SPECT)和正电子发射扫描(PET)等,但以上方法较复杂,主要应用于诊断而难以用于术中监测。
在手术中和手术后使用的脑血流监测方法主要有激光多普勒血流测定法、热弥散法、经颅多普勒法等。
一、激光多普勒血流测定法激光多普勒血流测定法(laser Doppler flowmeter,LDF)是一种连续、实时、微创和敏感的微循环血流监测技术,适用于神经外科术中rCBF的监测。
1.工作原理LDF的工作原理是利用激光多普勒效应。
激光通过探头照射到脑组织内的快速运动的红细胞表面,使其波长发生改变,产生多普勒位移效应(Doppler shift)。
波长改变的程度及幅度与红细胞的数量和运动速度相关。
通过记录波长改变的幅度和强度,从而可以推测局部脑组织血流(rCBF)。
LDF的测量范围较小,在探头周围1mm3,适合检测大脑皮层的血流量,尤其使用于比较血流的相对变化。
PU值为LDF 的基本测量指标,即流动的红细胞产生多普勒位移值,是一个表示测量深度内rCBF大小的相对单位,PU值的变化反映了rCBF的改变。
2.临床应用(1)监测脑过度灌注:在脑动静脉畸形(AVM)切除前后用LDF连续监测畸形血管团周边脑组织rCBF的动态变化,可及时发现脑过度灌注,指导临床及时处理。
(2)监测局部脑灌注不足:脑动脉瘤手术中有时需暂时阻断颈总动脉或载瘤动脉,此时以LDF连续监测被阻断动脉供血区的rCBF,能准确地反映该区域脑血流的下降程度,则有助于决定动脉阻断时间,减少脑组织不可逆的缺血性损伤的可能。
动脉瘤夹闭术中LDF连续监测邻近脑组织rCBF的实时变化,以免造成夹闭血管狭窄以致出现供血区缺血,减少手术并发症的发生。
(3)观察脑血流反应:LDF持续监测重型颅脑损伤脑皮质rCBF,可了解皮层血液灌注及脑血管自动调节功能,有助于指导治疗和判断预后。
脑血管储备检测的方法及意义脑血管储备检测的方法及意义作者:宋清扬文章号:W035019人脑血管在各种因素的作用下,会产生不同程度的狭窄,直至闭塞。
最常见的病变原因是动脉粥样硬化,其次还有动脉炎,外伤,Moyamoya病,放疗所致的动脉损伤性狭窄及与肿瘤有关的动脉狭窄等。
而狭窄或闭塞之后,是否将会发生远端供血区域的功能改变和梗死,一个重要的因素是脑的适应能力,发挥适应能力的过程是代偿的过程,而潜在的代偿能力则被称为脑血管的储备能力。
1 脑血管储备的概念脑血管储备(cerebrovascular reserve)狭义主要指脑循环储备力(cerebral circulation reserve,CCR)或称之为脑血管反应性(cerebrovascular reactivity,CVR)[1]。
广义上脑血管储备为机体的一种内源性抗缺血能力,是指在生理或病理状态下,脑血管通过小动脉和毛细血管的代偿性扩张或收缩(Bayliss效应)、脑血流量的调节、脑血管侧支循环开放等维持稳定的脑血流的能力。
脑储备能力发挥作用历经4个途径,即脑结构储备、脑血流储备、脑功能储备和脑化学储备[2] 。
2 脑血管储备的检测方法已经有大量研究发现,脑血管储备功能在缺血性卒中后脑功能的恢复过程中起着重要作用,而如何激发CVR是人们关心的热点。
目前,临床上多采用影像学技术结合脑血流负荷试验来评价脑血管储备能力。
虽然方法多,血流负荷试验的可靠性也已得到证实,但尚缺乏一种公认有效且便捷的方法,尚有待进一步研究和探索。
2.1 仪器检查临床上有多种技术可以用来评价脑血管储备能力。
常用的技术包括:正电子发射计算机体层摄影术(PET)、SPECT、Xe-CT、CT灌注成像(CTP)和磁共振成像(MRI)、TCD、激光多普勒(laser Doppler,LD)、经颅超声谐波灌注成像(harmonic perfusion imaging,HPI)和近红外线频谱分析(near infrared spectroscopy,NIRS)等。
椎动脉狭窄67例彩色多普勒超声影像分析目的探讨椎动脉狭窄的彩色多普勒超声影像,为临床诊断提供依据。
方法选择2011年2月~2012年3月本院经彩色多普勒超声检查确诊为椎动脉狭窄的67例患者,对其二维超声、彩色多普勒血流显像(CDFI)、频谱多普勒(SD)图像进行分析。
结果本组67例患者中有134条血管显示效果均较为理想,其中单侧椎动脉狭窄27例,双侧椎动脉狭窄40例,共107条受累血管;狭窄程度:1级15条,2级36条,3级41条,4级15条。
除完全闭塞者外,本组测得的椎动脉血管管径为0.5~2.7 mm,平均(1.87±0.38)mm。
结论彩色多普勒超声可以测量血管内径,显示颅外段椎动脉走行、管壁回声、血流方向及分布,直观而又准确地确定血管狭窄情况及程度,可作为椎动脉狭窄的首选影像学检查方法在临床推广。
标签:椎动脉狭窄;彩色多普勒超声;影像特点;分析椎动脉由锁骨下第一动脉后上方发出,经C6~C1横突孔穿出,穿过枕骨大孔进入颅内,左右两条椎动脉于脑桥下缘汇合成一条粗大的基底动脉。
椎动脉直径约3~5 mm,椎动脉狭窄导致的脑供血不足是短暂性脑缺血发作(TIA),以及相当一部分以眩晕为主诉就诊患者的主要致病原因。
据报道,一组来自新英格兰医学中心后循环登记(New England Medical Center posterior circulation registry,NEMCPCR)的数据显示,407例症状性后循环脑卒中和(或)TIA患者中,发现椎动脉起始段狭窄> 50%者有80例(20%)[1]。
目前临床确定可导致椎动脉狭窄的原因有:动脉粥样硬化以及血管炎症使椎动脉血管管腔狭窄、血栓形成;颈椎变形或增生导致颈椎横突孔狭窄,压迫椎动脉;先天性发育异常。
2011年2月~2012年3月,本院经彩色多普勒超声检查确诊为椎动脉狭窄患者67例,现就其超声影像特征分析报道如下:1 资料与方法1.1 一般资料选择2011年2月~2012年3月本院经彩色多普勒超声检查确诊为椎动脉狭窄的患者67例,其中,男48例,女19例;年龄30~73岁,平均(48.2±6.8)岁。