试验7:正溴丁烷的制备
- 格式:ppt
- 大小:2.16 MB
- 文档页数:23


实验名称:正溴丁烷的制备实验日期:2023年11月X日实验者:XXX一、实验目的1. 学习由醇和氢卤酸制备卤代烷的原理和方法。
2. 掌握回流操作及有害气体的吸收操作。
3. 掌握萃取、洗涤的原理及操作方法。
二、实验原理正溴丁烷是由正丁醇与氢溴酸反应制备的卤代烷。
在实验室中,伯卤代烷可由相应的醇与氢卤酸发生亲核取代反应来制备,溴代烷的制备一般需要硫酸作催化剂。
本实验中采用过量硫酸与溴化钠反应生成溴化氢,进而与正丁醇作用生成正溴丁烷。
反应方程式如下:C4H9OH + HBr → C4H9Br + H2O三、实验仪器与试剂1. 仪器:圆底烧瓶、回流装置、蒸馏装置、分液漏斗、冷凝管、沸石、烧杯、锥形瓶、量筒、滴定管、酒精灯、电热套等。
2. 试剂:正丁醇、溴化钠、浓硫酸、饱和碳酸氢钠溶液、无水氯化钙、水等。
四、实验步骤1. 投料:在圆底烧瓶中加入5ml水,再慢慢加入7ml浓硫酸,混合均匀并冷至室温后,再依次加入4.7ml正丁醇和6.5g溴化钠,充分振荡后加入几粒沸石。
2. 安装回流装置:将回流装置安装好,确保气体吸收部分连接正确。
3. 加热回流:以电热套为热源,加热回流,保持沸腾而又平稳回流,不时摇动烧瓶促使反应完成。
反应约30min。
4. 分离粗产物:待反应液冷却后,改回流装置为蒸馏装置,蒸出粗产物。
注意判断粗产物是否蒸完。
5. 洗涤粗产物:将馏出液移至分液漏斗中,加入10ml的水洗涤(产物在下层),静置分层后,将产物转入另一干燥的分液漏斗中,用5ml的浓硫酸洗涤(除去粗产物中的少量未反应的正丁醇及副产物正丁醚、1-丁烯、2-丁烯。
尽量分去硫酸层(下层)。
6. 萃取:有机相依次用10ml的水(除硫酸)、饱和碳酸氢钠溶液(中和未除尽的硫酸)和水(除残留的碱)洗涤后,转入干燥的锥形瓶中。
7. 干燥:向锥形瓶中加入适量的无水氯化钙,充分振荡,待晶体析出后,过滤、洗涤、干燥,得到正溴丁烷。
8. 蒸馏精制:将干燥后的正溴丁烷进行蒸馏,收集沸点范围内的馏分,即为精制的正溴丁烷。


一、实验目的1. 学习正丁醇与氢溴酸在浓硫酸催化下进行亲核取代反应的原理。
2. 掌握回流反应与气体吸收装置的安装与使用。
3. 通过实验,了解正溴丁烷的制备过程,并学习其提纯和纯化方法。
二、实验原理正溴丁烷的合成是通过正丁醇与氢溴酸在浓硫酸催化下进行亲核取代反应实现的。
反应过程中,正丁醇的羟基(-OH)被溴原子(-Br)取代,生成正溴丁烷和水。
反应方程式如下:\[ \text{CH}_3\text{CH}_2\text{CH}_2\text{CH}_2\text{OH} + \text{HBr} \rightarrow \text{CH}_3\text{CH}_2\text{CH}_2\text{CH}_2\text{Br} +\text{H}_2\text{O} \]浓硫酸在反应中起催化作用,同时吸收反应生成的水,促进反应向生成正溴丁烷的方向进行。
三、实验材料与仪器材料:- 正丁醇- 溴化钠- 浓硫酸- 饱和碳酸氢钠溶液- 无水氯化钙- 乙醇- 水浴锅- 圆底烧瓶- 冷凝管- 蒸馏装置- 分液漏斗- 滤纸- 干燥器仪器:- 烧杯- 量筒- 滴定管- 酒精灯- 搅拌棒四、实验步骤1. 准备反应物:将4.7 mL正丁醇和6.5 g无水溴化钠加入圆底烧瓶中,然后加入7 mL浓硫酸。
2. 安装回流装置:将圆底烧瓶与冷凝管连接,并在冷凝管上安装气体吸收装置,防止碱液被倒吸。
3. 加热回流:将反应混合物加热至回流,保持沸腾而又平稳回流,不时摇动烧瓶促使反应完成。
反应约30分钟。
4. 分离粗产物:待反应液冷却后,改回流装置为蒸馏装置,蒸出粗产物。
注意判断粗产物是否蒸完。
5. 洗涤粗产物:- 水洗:将蒸出的粗产物加入等体积的水中洗涤,取下层液体。
- 浓硫酸洗涤:用等体积的浓硫酸洗涤,去除残留的碱液。
6. 干燥:将洗涤后的正溴丁烷加入干燥器中干燥。
7. 纯化:通过蒸馏对干燥后的正溴丁烷进行纯化。
五、实验现象1. 反应过程中,溶液颜色由无色变为淡黄色。

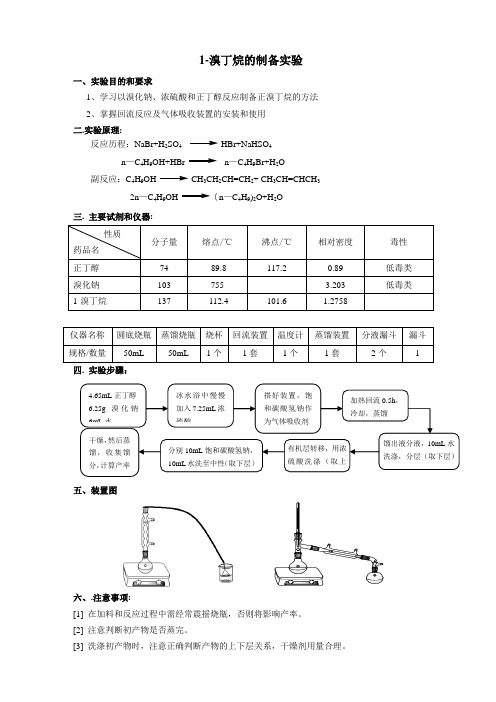
1-溴丁烷的制备实验一、实验目的和要求1、学习以溴化钠、浓硫酸和正丁醇反应制备正溴丁烷的方法2、掌握回流反应及气体吸收装置的安装和使用 二.实验原理:反应历程:NaBr+H 2SO 4HBr+NaHSO 4 n —C 4H 9OH+HBrn —C 4H 9Br+H 2O副反应:C 4H 9OHCH 3CH 2CH=CH 2+ CH 3CH=CHCH 32n —C 4H 9OH( n —C 4H 9)2O+H 2O三. 主要试剂和仪器: 性质 药品名 分子量 熔点/℃ 沸点/℃ 相对密度 毒性 正丁醇 74 -89.8 117.2 0.89 低毒类 溴化钠 103 755 3.203 低毒类 1-溴丁烷 137-112.4101.61.2758仪器名称 圆底烧瓶 蒸馏烧瓶 烧杯 回流装置 温度计 蒸馏装置 分液漏斗 漏斗 规格/数量50mL50mL1个1套1个1套2个1四. 实验步骤:五、装置图六、.注意事项:[1] 在加料和反应过程中需经常震摇烧瓶,否则将影响产率。
[2] 注意判断初产物是否蒸完。
[3] 洗涤初产物时,注意正确判断产物的上下层关系,干燥剂用量合理。
4.65mL 正丁醇 6.25g 溴化钠6mL 水 冰水浴中慢慢加入7.25mL 浓硫酸搭好装置,饱和碳酸氢钠作为气体吸收剂加热回流0.5h ,冷却,蒸馏馏出液分液,10mL 水洗涤,分层(取下层)有机层转移,用浓硫酸洗涤(取上分别10mL 饱和碳酸氢钠,10mL 水洗至中性(取下层)干燥,然后蒸馏,收集馏分,计算产率。
实验七正溴丁烷的制备 WTD standardization office【WTD 5AB- WTDK 08- WTD 2C】正溴丁烷的制备【实验目的】1.了解以正丁醇、溴化钠和浓硫酸为原料制备正溴丁烷的基本原理和方法。
2.掌握带有害气体吸收装置的加热回流操作。
3.进一步熟悉巩固洗涤、干燥和蒸馏操作。
【实验原理】【实验的准备】仪器:圆底烧瓶(50 ml、100 ml 各1个);冷凝管(直形、球形各1支);温度计套管(1个);短径漏斗(1个);烧杯(800 ml 1个);蒸馏头(1个);接引管(1个);水银温度计(150℃ 1支);锥形瓶(2个);分液漏斗(1个)。
药品:正丁醇 5 g ml mol);溴化钠(无水) g mol);浓硫酸(d= 10 ml mol);10 % 碳酸钠溶液、无水氯化钙。
【物理常数】【仪器安装要点】1.按教材p28图-(3)安装仪器。
2.有害气体吸收装置的漏斗要靠近水面,但不能浸入水中,以免水倒吸。
纯化过程:【操作要点】1.加料:(1)溴化钠不要粘附在液面以上的烧瓶壁上。
(2)从冷凝管上口加入已充分稀释、冷却的硫酸时,每加一次都要充分振荡,混合均匀。
否则,因放出大量的热而使反应物氧化,颜色变深。
2.加热回流:开始加热不要过猛,否则回流时反应液的颜色很快变成橙色或橙红色。
应小火加热至沸,并始终保持微沸状态。
反应时间约30 min 左右,反应时间太短,反应液中残留的正丁醇较多(即反应不完全);但反应时间过长,也不会因时间增长而增加产率。
本实验在操作正常的情况下,反应液中油层呈淡黄色,冷凝管顶端亦无溴化氢逸出。
3.粗蒸馏终点的判断:(1)看蒸馏烧瓶中正溴丁烷层(即油层)是否完全消失,若完全消失,说明蒸馏已达终点。
(2)看冷凝管的管壁是否透明,若透明则表明蒸馏已达终点。
(3)用盛有清水的试管检查馏出液,看是否有油珠下沉,若没有,表明蒸馏已达终点。
4.用浓硫酸洗涤粗产物时,一定先将油层与水层彻底分开,否则浓硫酸会被稀释而降低洗涤效果。
实验七 正溴丁烷的制备Experiment 7 Preparation of n-bromobutane计划学时:6学时 [实验目的]1、学习以溴化钠、浓硫酸和正丁醇反应制备正溴丁烷的原理与方法。
2、掌握回流反应及气体吸收装置的安装和使用。
[实验重点] 卤代烃的制备方法[实验难点] 正溴丁烷粗产物的提纯:即分步多次洗涤和简单蒸馏。
[教学内容]一、实验原理卤代烷制备中的一个重要方法是由醇和氢卤酸发生亲核取代(nucleophilic substitution reaction)来制备。
反应一般在酸性介质中进行。
实验室制备正溴丁烷是用正丁醇与氢溴酸反应制备,由于氢溴酸是一种极易挥发的无机酸,因此在制备时采用溴化钠与硫酸作用产生氢溴酸直接参与反应。
在该反应过程中,常常伴随消除反应和重排反应的发生。
该反应方程式为:(插入讲解反应机理)NaBr H 2SO 4++n-C 4H 9OH +n-C 4H 9Br +H 2OHBr NaHSO 4+H 2SO 4n-C 4H 8+H 2O H 2O C 4H 9OC 4H 9+2HBr H 2SO 4Br 2++SO 22H 2O n-C 4H 9OH 2n-C 4H 9OH 主反应:副反应: 二、实验仪器及药品仪器:100 mL 的圆底烧瓶、球形冷凝管、长颈玻璃漏斗、烧杯等所需药品:7.4 g (9.2 mL ,0.10 mol )正丁醇 (M = 74.12),13 g (约0.13 mol )无水溴化钠(M = 102.89),浓硫酸,饱和碳酸氢钠溶液,无水氯化钙 三、实验步骤1、投料在圆底烧瓶中加入10 mL 水,再慢慢加入14 mL 浓硫酸,混合均匀并冷至室温后,再依次加入9.2 mL 正丁醇和13 g 溴化钠,充分振荡后加入几粒沸石。
(硫酸在反应中与溴化钠作用生成氢溴酸,氢溴酸与正丁醇作用发生取代反应生成正溴丁烷。
硫酸用量和浓度过大,会加大副反应进行;若硫酸用量和浓度过小,不利于主反应的发生,即氢溴酸和正溴丁烷的生成)投料注意事项:(1)加料顺序不能颠倒。
实验七_正溴丁烷的制备资料讲解
正溴丁烷是一种有机化合物,化学式为C4H9Br。
它是一种无色液体,有较大的极性和不良挥发性。
正溴丁烷可以在有机合成中作为原料或反应中间体使用,可用于制备酯类、醇、酸等化合物。
本实验主要介绍正溴丁烷的制备过程。
1.实验原理
正溴丁烷的制备可以通过亲电取代反应实现。
在反应中,n-丁基溴和氢溴酸在硫酸的催化下进行取代反应,生成正溴丁烷。
反应方程式如下:
CH3CH2CH2CH2Br + HBr → CH3CH2CH2CH2Br + H2O
n-丁基溴+ HBr → 正溴丁烷 + H2O
2.实验步骤
2.1 实验操作
取一定质量的n-丁基溴加入干燥的圆底烧瓶中,加入硫酸,混合均匀后放在恒温水浴上加热搅拌。
同时,在气液分配装置中加入少量氢溴酸,调节反应液的温度和反应速度。
2.2 实验注意事项
(1)实验中药品应用双手操作,必要的实验器材必须佩戴手套,保护手部。
(2)实验中需要使用硫酸,需要拿到实验室老师的许可,操作前认真阅读化学品安全说明书。
(3)在反应液储存容器中储存反应液,反应液不得随便倾倒,避免污染环境。
3.实验结果及分析
正溴丁烷是一种无色液体,有刺激性气味、密度为1.2730 g/cm3,在水中微溶,易溶于有机溶剂。
实验成功合成正溴丁烷,产率也与预期相符合。
4.实验结论
通过本实验合成了正溴丁烷,合成过程通过氢溴酸和n-丁基溴的亲电取代反应进行,实验结果符合预期,反应产物品质良好。
实验七正溴丁烷的制备黄治炎zyhuang@办公室:致知楼1759实验室:致知楼1527-1528实验内容•1. 实验目的•4. 实验步骤•2. 实验原理•5. 思考题•3. 药品和仪器1、学习由醇制备溴代烃的原理(S N2)及方法。
2、练习回流及有害气体吸收装置的安装与操作。
3、进一步练习液体产品的纯化方法洗涤、干燥、蒸馏等操作。
:取代反应:S N2取代反应可能存在的副反应可能存在的副反应::3、药品和仪器•药品:正丁醇、无水溴化钠、浓硫酸、饱和碳酸氢钠溶液、无水氯化钙。
•主要仪器:100ml圆底烧瓶、球形冷凝管、蒸馏装置、搅拌套管、普通漏斗等4、实验步骤1)正溴丁烷的正溴丁烷的制备制备1)在100 mL 两口圆底烧瓶中加入10mL 水、搅拌子,搅拌下慢慢加入14.5mL 浓硫酸,混合均匀并冷至室温后,再加入9.5mL 正丁醇,搅拌均匀后分三次加入12.5 g 研细的溴化钠;2)小火加热,保持微沸,回流30分钟,待反应液冷却后,改回流装置为蒸馏装置,蒸出粗产物。
2)蒸馏反应液蒸馏反应液,,得粗品蒸馏终点判断标准蒸馏终点判断标准::1)烧瓶内油层消失;2)馏出液与水混合无油珠,温度计读数接近100 ℃;3)馏出液澄清粗品构成分析水干燥粗品分液除水干燥3)粗品分液除向馏出液加入10ml水洗涤(取下层)。
完全分离水层后,再用3 ml 浓硫酸洗涤有机层。
尽量除去硫酸层(产物在上层)。
其后,有机相依次用10 ml水(要下层)、饱和碳酸氢钠溶液(要下层)和水(要下层)洗涤后,转入干燥的锥形瓶中,加入无水氯化钙干燥,间歇摇动锥形瓶,至液体清亮为止。
4)干燥粗品干燥粗品、、蒸馏蒸馏纯化纯化整个蒸馏装置需要干燥整个蒸馏装置需要干燥;;收集99~102℃馏分;接收瓶需要提前称重接收瓶需要提前称重。
要求要求::1.每位同学单独完成一次蒸馏操作;2.每位同学回顾本实验中可能存在的化学反应,并写在实验报告上;3.认真记录所收集到正溴丁烷的重量,计算回收产率;注意事项•1.加浓硫酸时要少量多次,边加边冷却,彻底冷却后加溴化钠。