苏教版 硫酸的制备和性质汇总
- 格式:ppt
- 大小:3.21 MB
- 文档页数:46



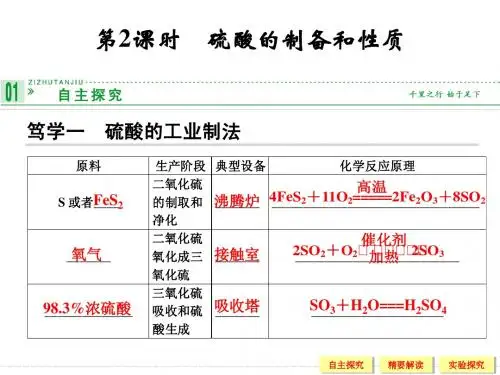




硫酸的制备与性质【教学目标】学生了解硫酸工业制备的原理和方法,掌握硫酸的有关性质 【教学重点】硫酸的化学性质 【教学难点】浓硫酸的特性 【教学过程】一、硫酸的工业制备1、古老的制备硫酸的方法:加热胆矾或绿矾强热2FeSO 4 Fe 2O 3+SO 2↑+SO 3↑2、接触法制硫酸 (1)三个步骤:(2)三个反应:4FeS 2+11O 2=2Fe 2O 3+8SO 2↑2SO 2+ O 2 2SO 3SO 3+H 2O=H 2SO 4(3)三个设备:沸腾炉、接触室、吸收塔 二、硫酸 (一)稀硫酸二元强酸,具有酸的通性。
H 2SO 4=2H ++SO 42-〖练习〗写出:铁、氢氧化钡、碳酸氢钠、氧化铝分别与稀硫酸的反应。
(二)浓硫酸物理性质:为无色粘稠状的液体,能溶于水放热。
(注意浓硫酸的稀释?) 〖实验〗1、胆矾与浓硫酸:蓝色晶体变白。
2、蔗糖与浓硫酸:蔗糖变黑、膨胀、产生刺激性气味的气体、发热。
3、铜与浓硫酸:产物溶于水变蓝、生成能使品红溶液褪色的气体。
特性:吸水性、脱水性、强氧化性。
1、难挥发性:可制取一些挥发性酸,如:HCl HNO 3 Na NO 3+H 2SO 4(浓)= NaHSO 4+ H NO 3↑2、吸水性:可作干燥剂,可干燥氧气、氢气、氯气、氯化氢等。
(不可用于氨气)3、脱水性:按水的组成比夺取有机物中的氢、氧元素形成水分子。
如:蔗糖、木材、纸张等。
(这种作用又称为炭化作用) C 12H 22O 11 12C+11H 2O4、强氧化性:①钝化作用:铁和铝在浓硫酸的作用下在表面生成一层致密的氧化保护膜。
(浓硝酸也有这种性质)可用铁或铝槽运输浓硫酸。
〖思考〗贮存浓硫酸的铁制容器不能敞口放置? ②与不活泼的金属反应Cu+2H 2SO 4(浓) CuSO 4+SO 2↑+H 2O 实验室可制取少量的二氧化硫∆催化剂∆对比:Fe+H 2SO 4= Fe SO 4 +H 2↑〖说明〗1、酸的氧化性:酸中的氢元素表现出来的性质,产生一般为氢气。


