HIV的致病机制
- 格式:ppt
- 大小:1.97 MB
- 文档页数:20



HIV的致病机制(一)HIV的基因及基因产物的主要功能HIV于1983年首次分离出,但它是生物理学医学研究得最广泛的一个病毒。
所分离出的大量HIV已进行了克隆和序列分析。
HIV的基因及其表达产物已得到鉴定(表17-3),表17-3 HIV基因、蛋白质产物及戎功能基因名称蛋白质产物大小(KD)功能Gag P25(p24)p17 衣壳结构蛋白质基质蛋白质Pol(多聚酶)P55,p63 逆转录酶(RT),Rnase,HpR(蛋白酶)P15 病毒蛋白转录后加工IN(整合酶) P11 HIV,cDNA整合env g120,gp41(gp36) HIV,cDNA整合包膜表面蛋白质包膜表面蛋白质Tat P14 结合到病毒LTR序列并激活病毒所有基因的转录Rev P19 调节病毒mRNA的表达,为gag和env基因表达后的转录所需nef P27 抑制HIV转录和延缓HIV复制vif P23 增加HIV的感染力和细胞-细胞间传播有助病毒复制vpr P18 有助病毒复制;激活转录vpu P15 有助HIV的释放;可能为新病毒子的包装所需(?)vpx P15 对HIV的感染力有利Tev P26 是Tat的Rev的激活剂(二)HIV感染的过程1.急性HIV综合征初次感染HIV后3~6周50%~70%病人有急性单核细胞增多症样综合症,高度病毒血症,HIV广泛播散。
1周~3月内出现抗HIV体液和细胞免疫应答,但HIV仍在淋巴结中持续表达。
2.潜伏期(1)细胞潜伏期:HIV基因组以非整合状态停留在某些非活化细胞中数天但无病毒复制的现象,这种静息感染与经典的病毒潜伏不同,它是全部毒基因组在细胞中的但表达被抑制。
细胞潜伏在临床上的反映是感染了HIV但抗HIV抗体和病毒血症均阴性。
细胞潜伏的机制仍不明,也不知为何有些HIV株较易进入潜伏状态,可能机制:①HIV DNA的甲基化;②Tat、Rev、Vpu和Vpr表达不足或缺乏;③Nef蛋白质的表达;④抑制了一些能与某些蛋白质相互作用的细胞内因子;⑤CD8+细胞因子抑制HIV的表达。

AIDS致病机制再认识[关键系] AIDS;致病;认识艾滋病亦称为“获得性免疫缺陷综合征”,是以CD4+T淋巴细胞减少引起免疫缺陷的临床综合征。
CD4细胞计数持续降低是艾滋病特有的免疫学改变。
1 CD4及受体HIV致病性的突出特征是表达分化群(cluster differentiation)CD4的CD4+T淋巴细胞进行性耗竭,表明HIV对该细胞群具有特殊的亲嗜性,支持这一推论的体外实验依据包括:纯化的CD4细胞是HIV优先复制的靶细胞,HIV感染介导的合胞体形成与细胞丢失均可被抗CD4单克隆抗体所阻断,HIV外膜糖蛋白可与CD4结合,对HIV不敏感的细胞在转染CD4基因后可被HIV感染,可溶性CD4分子能竞争性阻断HIV感染[1]。
CD4基因的表达使细胞对HIV易感。
所有结果都表明CD4糖蛋白是HIV的受体,表达CD4抗原细胞是HIV的敏感细胞。
对HIV感染敏感细胞都带OKT4/leu3a表型受体,即针对CD4的单克隆抗体及CD4抗原识别系统。
CD4分子为T细胞分化抗原分布在多种细胞膜上。
2 敏感细胞病毒因缺乏代谢及蛋白质合成系统,专营细胞内寄生。
病毒必须侵入宿主易感细胞,借助宿主的原料、酶和细胞器来复制子代病毒。
病毒增殖必须首先与易感细胞受体结合介导核酸进入。
HIVGP120选择识别感染带CD4分子细胞,与CD4受体结合在辅助受体协助下促成其细胞感染完成复制周期。
对HIV感染敏感的人CD4细胞群涉及造血系统、脑、皮肤、肠道及其他。
造血系统有:CD4+T细胞、单核细胞和组织巨噬细胞、少量B细胞、滤泡树突状细胞、骨髓CD34+造血干细胞、胸腺上皮细胞。
脑部有:星形细胞、毛细血管内皮细胞、小胶质细胞、树突状细胞、脉络膜丛、神经节细胞、神经元等。
皮肤有:郞格汉斯细胞、成纤维细胞。
肠道有:柱状和杯状细胞、肠道相关淋巴组织、肠嗜铬细胞。
其他部位有:肾管状细胞、关节滑膜、肝波状内皮细胞、肺成纤维细胞、前列腺、睾丸、滋养层细胞、橫纹肌肉瘤细胞、胎儿肾上腺细胞、肝癌细胞等。

文章编号:1007-8738(2007)09-0886-03H I V 致病机制的研究进展李莉平综述 康佳丽*,夏 薇审阅(广州市第一人民医院妇产科,广东广州510180)收稿日期:2006-10-16; 接受日期:2006-11-16基金项目:国家自然科学基金面上资助项目(30500466)作者简介:李莉平(1976-),女,湖北监利人,主治医师,博士Te:l 020-********;E-m ai:l seli n al ee @to m.co m*Correspond i ng au t hor ,E-m ai:l k angjiali 1961@21cn .com[关键词]H I V;致病机制;凋亡;免疫逃逸[中图分类号]R512.91 [文献标识码]A获得性免疫缺陷综合征(acqu ired i m munodefi c iency syn -dro m e ,A I D S)是由人免疫缺陷病毒(hu m an i m munodefi c iency v irus ,H I V )感染所致的以循环CD 4+T 细胞显著下降、机会感染及恶性疾病为特征的继发性免疫缺陷综合征。
据估计,截止2004年底,全球有3940万人感染H I V,仅2004年,超过310万人死于A IDS ,其中包括50万小于15岁的儿童[1]。
A I D S 的发病机制尚未完全阐明,但病毒和宿主因素相互作用的复杂过程是其主要原因。
A I D S 的最主要的特征之一是CD 4+T 细胞的逐渐丢失。
H I V 诱导的免疫活化和细胞死亡在CD 4+T 细胞的减少中具有重要作用[2]。
H I V 还通过快速的突变、寡聚体形成、高度糖基化、构象改变等逃逸宿主免疫攻击。
此外,病毒蓄积库的存在也是导致H I V 持续感染的重要原因。
1 凋亡在H I V 致病机制中的作用凋亡是程序化的细胞死亡,对维持恒定的淋巴细胞群数量具有重要作用[3]。

HIV病毒结构、复制、致病机理及研究进展2013级生物技术基地一班刘雨桐摘要:本文简要介绍了HIV病毒的形态结构基因组及其编码的蛋白,重点论述了HIV的复制和基因表达调控,并扼要阐述了HIV的致病机理以及艾滋病的研究治疗进展。
关键词:HIV;形态结构;复制;基因表达调控;致病机理;研究进展引言:人类免疫缺陷病毒(HIV),俗称艾滋病(AIDS)病毒,诱发人类获得性免疫缺陷综合症。
HIV病毒属反转录病毒的一种。
已发现人类免疫缺陷病毒主要有两种,即HIV-Ⅰ和HIV-Ⅱ。
有关HIV的研究主要是针对HIV-Ⅰ进行的。
一.HIV病毒结构①组织结构通过电子显微镜观察,HIV-1和HIV-2都具有慢病毒(1entivirus)种属的特征。
病毒粒子直径1 00~200nm,主要由Env蛋白、Gag蛋白和Pol蛋白构成。
HIV外层为脂质包膜,包膜蛋白由env基因编码的外膜蛋白gpl20(external protein,SU)和跨膜蛋白gp41(transmembrane protein,TM)组成,gpl20通过非共价键与gp41相连,gp41是穿过Env脂质双层的跨膜蛋白。
Gag蛋白包括3个结构性蛋白:基质蛋白(MA p17)、衣壳蛋白(CA p24)和核壳蛋白(NC p15)。
酰胺化(myristoylated)的基质蛋白MA附着于病毒包膜的内部,对病毒的完整性至关重要,也是Env蛋白包装到成熟病毒颗粒中所必需的;中层为由衣壳蛋白CA组成的圆锥形核心;核心内部为病毒基因组RNA分子、逆转录酶(p6 4)、整合酶(p3 2)、蛋白酶(pl 0)及与RNA结合的核壳(nucleocapsid)蛋白p9和p6。
HIV病毒核心内的RNA 是两个拷贝的单股正链RNA(ssRNA),两个单体在5’端借氢键结合成二聚体,每个RNA基因组的长度约为9.8kb。
在5'端有一帽结构(m7 G5 PPP5'GmpNp),3'端有poly A尾。



健康答人如何解读艾滋病病毒抗体检测结果姜丽花 (四川省广元市第三人民医院检验科,四川广元 628000)1艾滋病的定义艾滋病又被称为获得性免疫缺陷综合征,是一种由人类免疫缺陷病毒(HIV)侵入T细胞引起的慢性传染病,是当今社会严重危害人类健康的一种疾病,也是众多人谈之色变的疾病之一。
目前,医学界尚无对付艾滋病的特效疗法或疫苗,所以它又被称为医学领域的重大难题之一。
这种疾病不仅危害性极大,而且极具传染性。
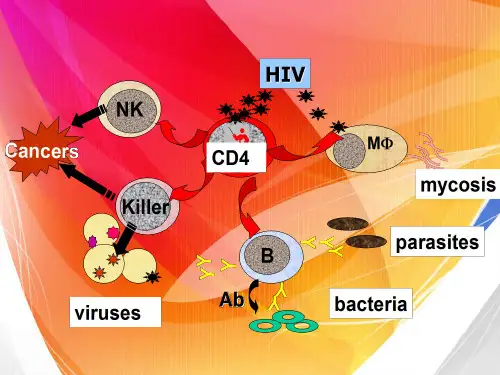
2艾滋病的致病机制HIV是一种对人体免疫系统具有一定攻击性的病毒,它可以大量破坏人体免疫细胞,特别是对具有特异性免疫功能的淋巴细胞进行攻击和破坏,致使人体内免疫系统紊乱,产生破坏人体免疫防线的负面影响,从而导致免疫功能丧失。
当人体免疫系统受到破坏后,免疫功能下降,许多病毒、细菌趁虚而入,带来的负面影响是十分明显的。
这时患者易感染各种疾病,如各种恶性肿瘤以及其他恶性疾病,发病率高。
最重要的一点是,人体免疫系统已经遭到破坏,对疾病的防范能力以及自愈能力也受到一定程度的影响,所以患者病死率较高。
一般而言,HIV在人体内的潜伏期很长,有的HIV感染者要经过数年,甚至长达10年或更长的潜伏期后才会出现艾滋病症状。
在潜伏期内,HIV对人体并没有危害,感染者可以正常工作,学习以及生活,也和普通人一样,是健康、正常的。
但当HIV感染者处在急性感染期时,其血液中就会携带大量的病毒,极具传染性。
3传播途径对艾滋病的定义进行解读时,提到过艾滋病是一种世界范围内的高度传染性疾病,具有较强的传染性和危害性。
一般而言,性传播是HIV传播的主要途径。
当然,HIV还有其他传播途径,如血液传播、母婴垂直传播等。
4艾滋病的预防艾滋病虽传染性强,但也是可以预防的。
HIV存在于患者的体液中,只要不接触患者的体液(包括唾液、血液、精液等)就不存在被传染的风险,如普通的拥抱和握手等行为都是可以的。
当然,在日常生活中,也要注意个人卫生,减少被感染的风险。
AIDS(艾滋)的致病机理一、 HIV感染对CD4T淋巴细胞的影响HIV病毒为逆转录病毒,所以遗传信息存在于两个相同的RNA单链模板中。
该病毒能结合人类具有CD4+受体的细胞,特别是和 CD4T 辅助淋巴细胞相结合,还能与神经细胞表面的半乳糖神经酰胺结合,逆转录酶可将病毒RNA逆转录为DNA,然后DNA再与人类基因相整合。
病毒DNA序列被感染细胞及其子代细胞终身携带。
HIV进入人体后能选择性地侵犯有CD4受体的淋巴细胞,以CD4T 淋巴细胞为主。
当HIV的包膜蛋白gp120与CD4T淋巴细胞表面的CD4受体结合后,在gp41透膜蛋白的协助下,HIV的膜与细胞膜相融合,病毒进入细胞内。
当病毒进入细胞内后迅速脱去外壳,为进一步复制作好准备。
最近研究表明,HIV进入细胞内除CD4受体外,还需要细胞表面的蛋白酶同gp120的V3环发生相互作用才能完成。
HIV病毒在宿主细胞复制开始,首先二条RNA在病毒逆转录酶的作用下逆转为DNA,再以DNA为模板,在DNA多聚酶的作用下复制DNA,这些DNA部分存留在细胞浆内。
进行低水平复制。
部分与宿主细胞核的染色质的DNA整合在一起,成为前病毒,使感染进入潜伏期,经过2-10年的潜伏性感染阶段,当受染细胞被激活,前病毒DNA在转录酶作用下转录成RNA,RNA再翻译成蛋白质。
经过装配后形成大量的新病毒颗粒,这些病毒颗粒释放出来后,继续攻击其他CD4T淋巴细胞。
大量的CD4+T淋巴细胞被HIV攻击后,细胞功能被损害和大量破坏是AIDS患者免疫功能缺陷的原因。
HIV感染CD4+T淋巴细胞后,首先引起细胞功能的障碍。
表现有对可溶性抗原如破伤风毒素的识别和反应存在缺陷,虽然对有丝分裂原植物血凝素(PHA)的反应仍然正常。
细胞因子产生减少,IL-2R 表达减少和对B淋巴细胞提供辅助能力降低等。
当HIV病毒在宿主细胞内大量繁殖,导致细胞的溶解和破裂。
HIV在细胞内复制后,以芽生方式释出时可引起细胞膜的损伤。
艾滋病的发病机制从1981年美国报告首例艾滋病(AIDS)病例后,AIDS已成为人类面临的最灾难性的疾病。
至今全球已有超过6000万人感染了人类免疫缺陷病毒(HIV),至少已有2500万人死于AIDS[1]。
在全世界范围内,AIDS在死因谱中排在第四位。
我国的第一例AIDS患者是在1985年6月发现的,截至2008年12月,全国累计报告HIV/AIDS 740,000例,其中105,000例已经是艾滋病病人。
艾滋病已经成为威胁人类健康的热点问题。
人类免疫缺陷病毒(HIV)感染人体后,造成T4细胞数量进行性减少,损害细胞免疫功能,最终导致各种机会性感染和肿瘤,即艾滋病。
然而,目前越来越多的证据显示HIV感染的致病过程不是缓慢的,而是始动于感染后的最初数周至数月。
原发感染期大量的病毒复制导致两个关键性的后果:1)淋巴外组织的CD4+效应记忆T细胞(T EM)严重缺失;2)建立了一种持续的机能亢进状态,记忆T细胞增殖显著升高,但是细胞的平均寿命显著缩短。
前者可以在感染初期削弱免疫系统,迫使这些细胞快速再生以避免免疫崩溃;后者延缓了免疫崩溃,再生CD4+T EM 细胞以阻止免疫衰竭,但同时也不断给病毒提供了感染所需的新的靶细胞,并且导致细胞再生能力受损,最终打破机体稳态[2]。
A.急性感染阶段的靶细胞T淋巴细胞分为未受过抗原刺激的初始细胞和经历抗原刺激的记忆细胞。
记忆细胞是功能和表型异质的细胞群,可以分为中枢记忆性细胞(T CM)和效应记忆性细胞(T EM)。
T EM细胞的再生能力远远低于初始T细胞和中枢记忆T细胞,也就是说这些细胞受到刺激和再刺激后产生的细胞总数量很少且快速衰竭[3]。
黏膜效应部位主要的CD4+T细胞是效应记忆T细胞,这些细胞表达趋化因子受体CCR5。
由于CCR5是猴免疫缺陷病毒(SIV)和HIV感染靶细胞需要的辅助受体,所以CCR5+ CD4+T细胞是急性感染阶段病毒感染的靶细胞。
HIV对CD4+细胞的特殊亲嗜性是由其包膜糖蛋白gp120与CD4分子决定的,即CD4分子是gp120的特异性亲和受体。