微生物室抗酸染液质控记录表
- 格式:docx
- 大小:41.00 KB
- 文档页数:1


竭诚为您提供优质文档/双击可除抗酸染色法实验报告篇一:抗酸染色法抗酸染色法目录1简介2抗酸染色的原理3抗酸染色一般步骤?1)初染?2)脱色?3)复染4抗酸染色的染液配制简介编辑抗酸染色法acid-faststainingmethod1882年由埃利希(F.ehrlich)首创并经F.齐尔(Ziehl)改进而创造出的细菌染色法。
其中最具代表性的为对结核菌的齐尔-尼尔森(Ziehl-neelsen)染色法和齐尔-加贝特(Ziehl-gabbet)染色法。
用石炭酸复红染色后,用盐酸乙醇分色,再用美蓝进行对比染色,即不再脱色而呈现石炭酸复红的红色。
抗酸染色的原理编辑分枝杆菌的细胞壁内含有大量的脂质,包围在肽聚糖的外面,所以分枝杆菌一般不易着色,要经过加热和延长染色时间来促使其着色。
但分枝杆菌中的分枝菌酸与染料结合后,就很难被酸性脱色剂脱色,故名抗酸染色。
齐-尼氏抗酸染色法是在加热条件下使分枝菌酸与石炭酸复红牢固结合成复合物,用盐酸酒精处理也不脱色。
当再加碱性美兰复染后,分枝杆菌仍然为红色,而其他细菌及背景中的物质为蓝色。
抗酸染色一般步骤编辑1)初染用玻片夹夹持涂片标本,滴加石炭酸复红2-3滴,在火焰高处徐徐加热,切勿沸腾,出现蒸汽即暂时离开,若染液蒸发减少,应再加染液,以免干涸,加热3-5分钟,待标本冷却后用水冲洗。
2)脱色3%盐酸酒精脱色30秒~1分钟;用水冲洗。
3)复染用碱性美兰溶液复染1分钟,水洗,用吸水纸吸干后用油镜观察。
抗酸染色的染液配制编辑1、石炭酸复红碱性复红酒精饱和溶液10mL5%石炭酸90mL2、3%盐酸酒精浓盐酸3mL95%酒精97mL3、吕氏美兰液美兰酒精饱和液30mL氢氧化钾(1:10000)100mL篇二:实验二十四抗酸染色-jpkchnadlcn课程名称:微生物学检验技术授课专业:医学检验学时:2学时实验十七结核杆菌检验(m.TuberculosisTest)一、实验目的⒈掌握结核杆菌的菌落特征,镜下形态、染色特性⒉掌握抗酸染色的原理、操作步骤,结果报告二、实验器材与试剂⒈菌种:bcg⒉试剂:抗酸染液⒊其他:三脚架、铁片、木夹子等三、实验内容㈠微生物学诊断⒈标本采取根据病灶器官取材,包括痰,尿,脑脊液,粪便等。
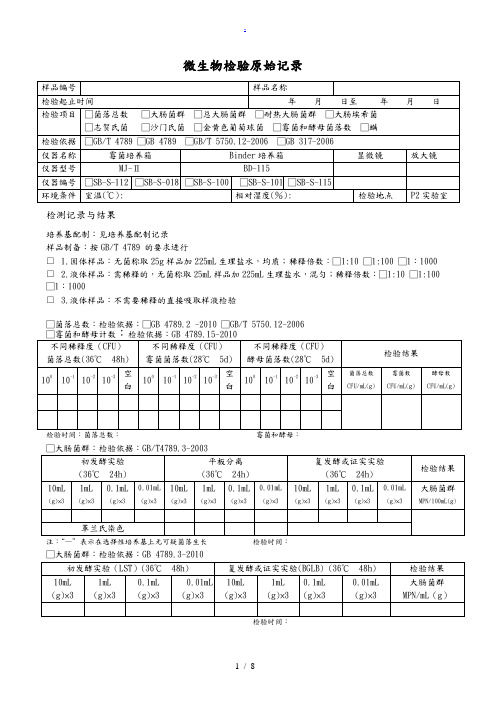
微生物检验原始记录
检测记录与结果
培养基配制:见培养基配制记录
样品制备:按GB/T 4789 的要求进行
□ 1.固体样品:无菌称取25g样品加225mL生理盐水,均质;稀释倍数:□1:10 □1:100 □1:1000 □ 2.液体样品:需稀释的,无菌称取25mL样品加225mL生理盐水,混匀;稀释倍数:□1:10 □1:100 □1:1000
□ 3.液体样品:不需要稀释的直接吸取样液检验
□菌落总数:检验依据:□GB 4789.2 -2010 □GB/T 5750.12-2006
检验时间:菌落总数:霉菌和酵母:
□大肠菌群:检验依据:GB/T4789.3-2003
注:“—”表示在选择性培养基上无可疑菌落生长检验时间:
检验时间:
□总大肠菌群:检验依据:GB/T 5750.12-2006
注:“—”表示在选择性培养基上无可疑菌落生长检验时间:
□耐热大肠菌群:检验依据:GB/T 5750.12-2006
注:“—”表示在选择性培养基上无可疑菌落生长检验时间:
□大肠埃希氏菌:检验依据:GB/T 5750.12-2006
检验时间:
□致病菌□沙门氏菌□志贺氏菌□金黄色葡萄球菌
检验依据 GB 317.4-.10-2006
检测人:复核人:
微生物限度检验记录(复合膜)
检验人:复核人:
微生物限度检验记录(辅料)
检验人:复核人:
微生物限度检验记录(铝箔、PVC硬片)
微生物限度检验记录(半成品、成品)
检验人:复核人:
微生物限度检验记录(辅料)
检验人:复核人:。



微生物检验原始记录
培养基配制:见培养基配制记录
样品制备:按GB/T 4789 的要求进行
□ 1.固体样品:无菌称取25g样品加225mL生理盐水,均质;稀释倍数:□1:10 □1:100 □1:1000 □ 2.液体样品:需稀释的,无菌称取25mL样品加225mL生理盐水,混匀;稀释倍数:□1:10 □1:100 □1:1000
□ 3.液体样品:不需要稀释的直接吸取样液检验
□菌落总数:检验依据:□GB 4789.2 -2010 □GB/T 5750.12-2006
检验时间:菌落总数:霉菌和酵母:
□大肠菌群:检验依据:GB/T4789.3-2003
注:“—”表示在选择性培养基上无可疑菌落生长检验时间:
检验时间:
□总大肠菌群:检验依据:GB/T 5750.12-2006
注:“—”表示在选择性培养基上无可疑菌落生长检验时间:
注:“—”表示在选择性培养基上无可疑菌落生长检验时间:
检验时间
□致病菌□沙门氏菌□志贺氏菌□金黄色葡萄球菌
□螨:检验依据 GB 317.4-.10-2006
检测人:复核人:
微生物限度检验记录(复合膜)
检验人:复核人:
微生物限度检验记录(辅料)
检验人:复核人:
微生物限度检验记录(铝箔、PVC硬片)
检验人:复核人:
微生物限度检验记录(半成品、成品)
检验人:复核人:
微生物限度检验记录(辅料)
检验人:复核人:。
微生物室室内质量控制操作程序1 目的指导微生物室工作人员进行室内质量控制,规范所有检测项目的室内质控操作程序,保证检测结果准确可靠,决定常规报告能否正确发出。
2 适用范围适用于微生物室所有检测项目的室内质量控制。
3 职责3.1 微生物室技术人员应分别负责微生物室检测标本前、中、后的各项室内质量控制工作,若有失控,应进行相应的分析和失控后处理,并及时填写失控分析报告。
同时,做好微生物室试剂、培养基、仪器、接种环和标准菌株等的质控工作。
3.2 质量监督员负责对微生物室所有检测项目的室内质控进行指导、监督和分析,并定期汇总、回顾室内质控结果,制订和修改质控计划。
3.3 微生物室组长负责协调、监督和检查质量监督员的工作,定期召开组内质量控制会议,总结小组室内质控情况。
4 室内质控工作程序4.1 培养基的质控程序4.1.1 配制培养基时,所用原料如各类培养基干粉应在瓶身注明收到日期,开启时应注明开启时间,且严格遵守厂家规定的贮存条件和有效使用期限。
配制完后填写《微生物室自制培养基(试剂)配制及质控记录表》。
4.1.2 商品化成品培养基要记录购入日期、失效日期,且每批培养基均需由厂家提供质量评估报告并存档,培养基按照厂家说明书规定的条件贮存并在有效期内使用。
商品培养基应用相应的质控办法和相应菌株进行质量监测并填写《商品化培养基质控结果记录》。
4.1.3 质控频率:每次配制培养基后;每批次或每货次培养基使用前。
4.1.4 质控方法:4.1.4.1 培养基外观检查:要求培养基外观良好,光滑、水分适宜,无污染,有适当的颜色和厚度、试管培养基湿度适宜。
4.1.4.2 无菌试验:每批随机抽样5%,35℃培养24 小时,抽样中每个培养基出现2 个以上菌落,视为本批培养基不合格;无菌生长视为合格。
4.1.4.3 合格试验:包括生长试验和生长抑制试验。
用标准菌株或经准确鉴定的临床分离株,检测培养基的生长情况或生长抑制情况。
革兰染色和抗酸染色涂片镜检的质控
1.革兰染色用转种24小时的ATCC25923(金黄色葡萄球菌)和ATCC25923(大肠埃希菌)制备菌悬液,作为革兰染色的质量控制,每天质控和标本同步进行。
2.抗酸染色用标准的结核抗酸杆菌制备成菌悬液,经高压灭菌后冰箱保存,作为抗酸染色的质量控制,每次质控和标本同步进行。
染色液阳性对照菌阴性对照菌监控频率
革兰染色金黄色葡萄球菌大肠埃希菌每天
抗酸染色结核抗酸杆菌每次
3.涂片镜检的质控
本室组4人定于每周2镜检革兰染色和抗酸染色的质控菌株,看镜检结果的符合率,符合率达100%。
及随机抽查10张痰标本涂片的革兰染色和抗酸染色,4人镜检后,经集体讨论:每一张涂片得最终结果。
并与个人的镜检结果进行对比,4人革兰染色结果的符合率应达90%以上,抗酸染色结果的符合率达100%。