第四章第四节 氨硫酸硝酸
- 格式:ppt
- 大小:3.87 MB
- 文档页数:81



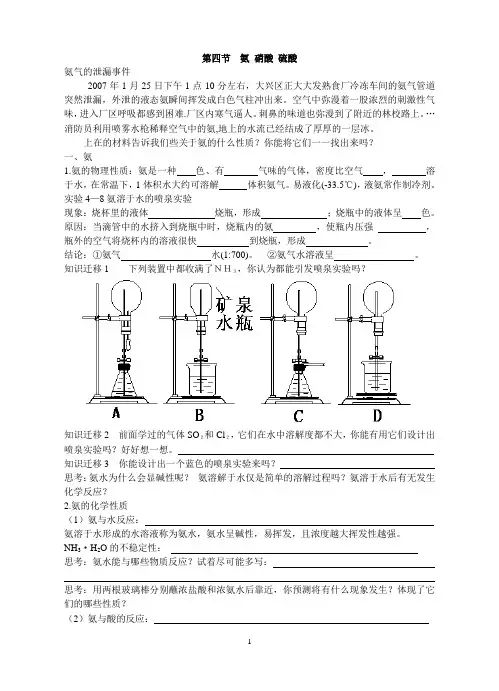
第四节氨硝酸硫酸氨气的泄漏事件2007年1月25日下午1点10分左右,大兴区正大大发熟食厂冷冻车间的氨气管道突然泄漏,外泄的液态氨瞬间挥发成白色气柱冲出来。
空气中弥漫着一股浓烈的刺激性气味,进入厂区呼吸都感到困难.厂区内寒气逼人。
刺鼻的味道也弥漫到了附近的林校路上。
…消防员利用喷雾水枪稀释空气中的氨,地上的水流已经结成了厚厚的一层冰。
上在的材料告诉我们些关于氨的什么性质?你能将它们一一找出来吗?一、氨1.氨的物理性质:氨是一种色、有气味的气体,密度比空气,溶于水,在常温下,1体积水大约可溶解体积氨气。
易液化(-33.5℃),液氨常作制冷剂。
实验4—8氨溶于水的喷泉实验现象:烧杯里的液体烧瓶,形成;烧瓶中的液体呈色。
原因:当滴管中的水挤入到烧瓶中时,烧瓶内的氨,使瓶内压强,瓶外的空气将烧杯内的溶液很快到烧瓶,形成。
结论:①氨气水(1:700)。
②氨气水溶液呈。
知识迁移1 下列装置中都收满了NH3,你认为都能引发喷泉实验吗?知识迁移2 前面学过的气体SO2和Cl2,它们在水中溶解度都不大,你能有用它们设计出喷泉实验吗?好好想一想。
知识迁移3 你能设计出一个蓝色的喷泉实验来吗?思考:氨水为什么会显碱性呢?氨溶解于水仅是简单的溶解过程吗?氨溶于水后有无发生化学反应?2.氨的化学性质(1)氨与水反应:氨溶于水形成的水溶液称为氨水,氨水呈碱性,易挥发,且浓度越大挥发性越强。
NH3·H2O的不稳定性:思考:氨水能与哪些物质反应?试着尽可能多写:思考:用两根玻璃棒分别蘸浓盐酸和浓氨水后靠近,你预测将有什么现象发生?体现了它们的哪些性质?(2)氨与酸的反应:氨与酸反应生成铵盐。
铵盐又叫铵态氮肥。
思考:有一位农民看到自己买的一袋碳酸氢铵化肥受了潮,就在太阳底下晒,等他下午去取时,发现少了许多,是谁偷了他的氮肥?铵盐可以做氮肥体现了铵盐的什么物理性质?铵盐的性质①铵盐都易溶于水②铵盐受热易分解NH4HCO3受热:NH4Cl受热:③铵盐与碱反应(NH4)2SO4 + NaOH:实质:(离子方程式)NH4HCO3 + NaOH:实质:(离子方程式)一切铵盐的共同性质,实验室可利用这个性质来检验NH4+的存在。




第四章非金属及其化合物第4节氨硝酸硫酸课程标准:了解NH3与水、酸的反应,了解氨水的成份及氨水的不稳定性,了解铵盐的通性省教学要求:了解NH3的性质和用途掌握NH3的实验室制法了解铵盐的性质,掌握NH4+的检验教学目标:知识与技能:了解氨的物理性质,掌握氨的化学性质;了解铵盐的性质。
过程与方法:通过学生分组讨论、实验探究,培养学生分析问题、解决问题的能力、实验操作的能力。
情感态度与价值观:使学生体会化学对环保的重要意义,培养学生关注社会的意识和责任感;通过对问题的讨论、实验的探究,培养学生积极思考、勇于探究的精神。
教学重点:NH3的化学性质、实验室制法、NH4+的检验教学难点:喷泉实验的原理及相关类似的实验的设计教学流程:Ⅰ、课前检测:一、复习检测:1、把SO2气体通入品红溶液中,现象为,加热溶液煮沸后,现象为2、将Cl2通入紫色石蕊试液中,现象为将SO2通入紫色石蕊试液中,现象为二、预习检测:关于氨的下列叙述中,错误的是()A.氨易液化,因此可用来作制冷剂B.氨易溶解于水,因此可用来作喷泉实验C.氨极易溶解于水,因此氨水比较稳定(不容易分解)D.氨溶解于水显弱碱性,因此可使酚酞试剂变为红色Ⅱ、课堂新授:【展示】一瓶氨气,引导学生观察氨气的色、味、态、密度(与空气比较)。
阅读教材P.97-98。
小结氨的物理性质【演示实验】实验4-8,观察实验现象,思考下列问题并小组交流实验装置分析:1、为什么烧瓶内会产生喷泉?2、为什么要用干燥的烧瓶?3、胶头滴管的作用是什么?实验现象分析:1、实验体现氨气的什么性质?2、烧瓶中的溶液为什么会变红?3、如果变红的原因是生成OH -,那么OH -来源于什么物质?【归纳】1、氨的物理性质:无色、刺激性气味的气体,易溶于水(1︰700)。
2、化学性质:(1)与水的反应:NH 3+H 2O NH 3.H 2O NH 4++OH -【思考】1、水中的粒子有哪些?液氨与氨水是否是一种物质?2、如何检验氨气?3、把一瓶浓氨水露置在空气中,有何现象?【过渡】氨气溶与水所得溶液显碱性,氨气是一种碱性气体,那么它遇到酸会不会反应呢?【演示实验】氨气与氯化氢的反应观察现象写出化学反应方程式:NH 3+HCl =NH 4Cl (白烟)【拓展】1、写出氨气与硫酸、硝酸反应的化学方程式:2、下列不可用浓硫酸干燥的气体有( )A 、氨气B 、氯气C 、氧气D 、一氧化氮3、试分析如何检验氨气?【过渡】氨气与酸反应生成的盐叫铵盐。



第四章第四节氨硝酸硫酸一、氨1、氮的固定:概念:的方法叫氮的固定。
2、氛的物理性质:色气味气体,密度空气,溶于水,常温下,1体积水大约可溶解体积氨气。
氨的水溶液叫做。
氨液化(液态的氨称为)液化时热。
3、氛的化学性质(1)与水反应:氨溶于水后大部分与水反应,化学方程式为:氛水不稳定性:O 氨水有性,故氨气可以使酚猷溶液变色或使湿润的红色石蕊试纸变色。
(可用于氨气的检验。
)(2)与酸反应生成铉盐,请完成下列方程式:NH3+1IC1=(课本P98 “图4-28〃操作可用于氛气的检验)NH3+H2S0J=(可用于吸收氨气)NH3+C02÷H20=(生成破铉)(3)NH3的还原性。
NFh中N是一3价,处于最低价态,具有还原性,可被氧化剂(如0/氧化,写出氨被。
2氧化的化学方程式:C4、铉盐的性质:(1)农业上常见的化肥,如、、等都是铉盐。
铉盐都溶于水。
(2)铉盐的不稳定性:铉盐受热易分解例如:NH出CO : , 4 _________________________________________________________NHiC 1 些二_______________________________________(3)铉盐与碱的反应:铉盐与碱的反应放出氨气NH. lN03+Na0H= _________________________________(NH., ) 2S0, i + NaoH二____________________二、氨的实验室制法1、__________________________________________ 反应原理2、装置:〃+”加热装置;发生装置与制相似。
3、收集法;收集的试管口塞上棉团,作用是4、干燥:O不可以用、做干燥剂。
5、检验:(1)用湿润的试纸放在试管口可以看到试纸变;(2) ____________________________________________________6、尾气吸收:导管口放一团用一或浸湿的棉花球),棉花作用:温馨提示:在实验室有时也用①加热浓氨水的方法得到氨气:②把浓氨水滴入固体氢氧化钠中制得氨气:7、实验室能不能用加热氯化铉反应制备氨气?为什么?(3) NHU的检验:如何证明某物质中含有NH「(铉盐)?%1.浓硫酸(一)物理性质:色状液体,挥发,密度比水O(二)浓硫酸的特性1.脱水性:用玻璃棒蘸取浓硫酸滴到滤纸上,现象,体现浓硫酸的性。