过程装备腐蚀与防护
- 格式:wps
- 大小:62.34 KB
- 文档页数:10


第一章腐蚀电化学基础一、概念及简答1.双电层金属浸入电解质溶液内,其表面的原子与溶液中的极性水分子、电解质离子、氧等相互作用,使界面的金属和溶液侧分别形成带有异性电荷的结构——双电层。
2.电极电位电极反应使电极和溶液界面上建立的双电层电位跃。
3.极化、极化曲线及极化图电池工作过程中,由于电流流动而引起电极电位偏离初始值的现象。
用来表示极化电位与极化电流或极化电流密度之间关系的曲线。
将构成腐蚀电池的阴极和阳极极化曲线绘在同一E-I坐标上得到的图线,简称极化图。
4.超电压腐蚀电池工作时,由于极化作用使阴极电位下降,阳极电位升高。
这个值与各极的平衡电位差值的绝对值称为超电压或过电位。
以η表示。
5.钝化金属表面从活性溶解状态变成非常耐蚀的状态的突变现象称为钝化。
6.去极化反应:发生在阴极上的吸收电子的还原反应。
析氢腐蚀其发生的条件析氢腐蚀定义:指溶液中的氢离子作为去极剂,在阴极上进行阴极反应,使金属持续溶解而被腐蚀。
条件:腐蚀电池中的阳极电位必须低于阴极的析氢电极电位。
7. 耗氧腐蚀其发生的条件腐蚀电池上的阴极反应由溶液内氧分子参与完成,称为吸氧或耗氧反应。
耗氧腐蚀的条件为:腐蚀电池中的阳极初始电位EºM必须低于该溶液中氧的平衡电位Ee,O28.金属腐蚀的热力学条件金属溶解的氧化反应若进行,则金属的实际电位必更正于金属的平衡电极电位。
E>Ee,M 去极化反应若进行,则有金属电极电位必更负于去极剂的氧化还原反应电位。
E<Ee,k 上述条件需同时满足。
9.腐蚀速度的工程表示方法重量法和深度法10.耐蚀性评定及其适用范围第二章局部腐蚀一、概念及简答1、应力腐蚀:在固定拉应力和特定介质的共同作用下所引起的破裂。
应力腐蚀产生的条件(特定材料+)固定拉应力+ 特定腐蚀性介质2、腐蚀疲劳:金属材料在循环应力或脉动应力和腐蚀介质的联合作用下,所引起的腐蚀。
(注意与疲劳断裂的区别)条件:变应力+腐蚀性介质3、磨损腐蚀:腐蚀性流体与金属以较高速度做相对运动而引起金属的腐蚀损坏,简称磨蚀。

关于过程装备与控制工程专业过程装备腐蚀与防护课程教学方法的探讨近年来随着石油化工、能源化工等各类工业的崛起和迅速发展,对过程装备与控制工作专业人才的需求越来越多。
在各类工业中生产的装备都无法避免腐蚀。
因此,过程装备腐蚀与防护是一门实用性与知识性很强的专业选修课,涉及物理、化学、冶金学、表面科学、力学、机械学和生物学等多学科知识。
这门课程的学习主要面向大四学生。
首先是因为学生经过前三年基础课的学习沉淀,有扎实的理论知识,经过这门课的学习可以将这些枯燥的单学科的理论知识进一步吸收学习和转化。
其次是因为学生面临毕业实习找工作,这门课的知识又非常“接地气”,可以让学生提前熟悉各类企业的装备和生产流程。
因此,这是一门非常有意义的专业选修课。
而如何提高过程装备与控制工程专业的过程装备腐蚀与防护课程的教学质量,加强课程理论知识与实际工业系统性衔接和传承,是一门值得我们承教者需要探索和研究的新课题。
针对上述问题,笔者根据自己在教学中的经验和思考,提出如下个人见解。
一、过程装备与控制工程专业过程装备腐蚀与防护课程现状与存在问题由于课程总学时数的限制,过程装备与控制工程专业学生有关装备腐蚀与防护课程涉及的物理化学方面的基础知识较为薄弱;且以往教学中基础理论学时相对较多,传统“填鸭式”教学使学生在听课过程中觉得比较枯燥乏味;另外实践课程相对较少,学生的实际应用能力较差,这些问题都影响着学生对专业知识的学习和掌握。
因此如何在过程装备腐蚀与防护课程教学过程中强化学习方法的传授、提高学生学习的主动性和重视实践能力的培养,与高素质、创新型过程装备与控制工程专业人才培养目标的要求相符合,已经成为该门课程教学深入探讨的关键。
二、过程装备腐蚀与防护课程案例教学方法的实现1.优化课程教学内容由于绪论是整个教材的前言和正文内容的提纲挈领,因此绪论排布要合理,有侧重性。
由于课时限制,大多数老师讲解的时候都是将绪论简言概之,加之学生对物理化学等方面知识的欠缺,使学生盲目而机械地学习这门课程,效果当然很不理想。

腐蚀的控制措施:一是不就行控制,即腐蚀发生后再消除它;二是预防性控制,即事先采取防止腐蚀的措施腐蚀的定义:金属与其周围介质发生化学或电化学作用而产生的破坏腐蚀的广义概念:材料(包括金属与非金属)由于环境作用引起的破坏或变质叫腐蚀去极剂:能够吸收电子的物质非平衡电极电位:电极上同时存在两种或两种以上不同物质参与的电化学反应,正逆过程的物质始终不可能达到平衡状态,这种电极电位称为非平衡电极电位参比电极:用一个点位很稳定的电极作参照基准来测量任一电极的电极电位的相对值,这种参照基准电极称为参比电极常用的参比电极:饱和甘汞电极、氯化银电极、硫酸铜电极、金属单质常见的宏观腐蚀电池及其阴阳极:异种金属电池(还原性较强的为阳极,较弱的的为阴极)、温差电池(一般温度较高的部位为阳极,温度较低的部位为阴极)、浓差电池构成微电池(电化学不均一性)的主要原因:1.化学成分不均一2.组织结构不均一3.物理状态不均一4.表面膜不完整过程自发进行的条件:反应过程能量(自由能)降低,即G为负值,则此反应就有可以无需外加能量而自发进行金属自发腐蚀热力学条件:金属自发地产生电化学腐蚀的条件必须是溶液中含有能从金属上夺走电子的去极剂,并且去极剂的氧化还原电位要比金属溶解反应的平衡电位要正极化现象:电池工作过程中由于电流流动而引起电极电位偏离初始值的现象极化现象的产生原因:产生极化现象的根本原因是阳极或阴极的电极反应与电子迁移(从阳极流出或流入电极)速度存在差异极化现象的类型:电化学极化、浓差极化、膜阻(电阻)极化超电压:腐蚀电池工作时,由于极化作用使阴极电位降低或阳极电位升高,其偏离平衡电位的差值,称为超电压或过电位极化曲线的含义:极化率低的曲线趋于平坦,它表示电极电位随极化电流的变化很小,也就是说电极材料的极化性能弱,电极过程容易进行。
反之,极化率高,极化曲线越陡,表明极化性能强,电极过程进行的阻力大腐蚀速度的影响因素:1.金属本身2.处理工艺3.介质环境4.其他环境从金属本身分析影响腐蚀速度有哪些?金属本身包括金属的电极电位、超电压、钝性、组成(尤其合金元素)、组织结构、表面状态、腐蚀产物性质等以上几个因素如何影响从介质环境分析影响腐蚀速度有哪些?介质环境包括介质组成、浓度、PH值、温度、压力、流速等。


过程装备腐蚀与防护1.自动调节系统主要由调节器,调节阀,调节对象和变送器四大部分组成。
2.自动调节系统按调节器具有的调节规律来分通常有比例,比例积分,比例微分,比例积分微分等调节系统3.自动控制系统一般由被控对象,测量元件和变送器,自动控制器,执行器组成4.自动控制系统按给定值不同可分为定值控制系统,程序控制系统和随动控制系统。
按结构分类开环控制系统和闭环控制系统5、根据使用的能源不同,调节阀可分为气动调节阀、电动调节阀和液动调节阀三大类。
8、在工业生产中常见的比值控制系统可分为单闭环比值控制、双闭环比值控制和变比值控制三种。
10、随着控制通道的增益K0的增加,控制作用增强,克服干扰的能力最大,系统的余差减小,最大偏差减小。
13、控制系统对检测变送环节的基本要求是准确、迅速和可靠。
14、控制阀的选择包括结构材质的选择、口径的选择、流量特性的选择和正反作用的选择。
5控制系统的品质指标有:最大偏差,衰减比,余差,过渡时间,震荡周期或频率6与热电偶配套的显示仪表主要有毫伏计和电位差计7双杠杆差压变送器是根据力矩平衡原理工作的他可以用来检测被测压力,压差,绝对压力8仪表的技术指标主要有精度,变差,灵敏度与灵敏限,分辨力,线性度和反应时间11常用的基本控制规律是双位控制,比例控制,积分控制,微分控制。
其中积分控制能消除余差。
20控制器的比例度增大,积分时间减小,时控制器的比例作用越小,积分作用增强6仪表测量中的五大参数是温度,压力,物位,流量,在线分析9管道内的流体速度在一般情况下沿管道中心处的流速最大,管壁处的流速等于零32节流式测量装置有孔板,喷嘴和文丘里管三种形式,都是利用流体流经节流装置时产生的压力差而实现流量测量它与流速成平方关系化工自动化:自动检测,自动保护,自动操纵,自动控制。
自动控制系统基本组成:人工控制,自动控制系统(测量元件与变送器,控制器,执行器,被控对象)。
检测仪表的基本性能指标:精度和精度等级,变差,灵敏度、不灵敏区。
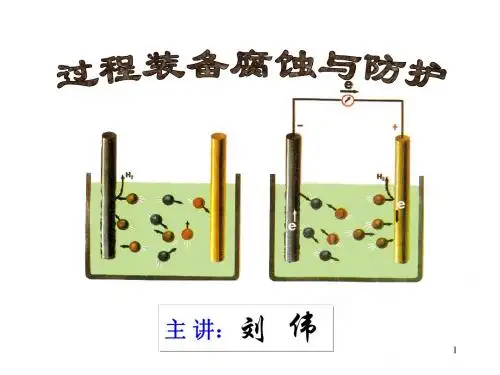
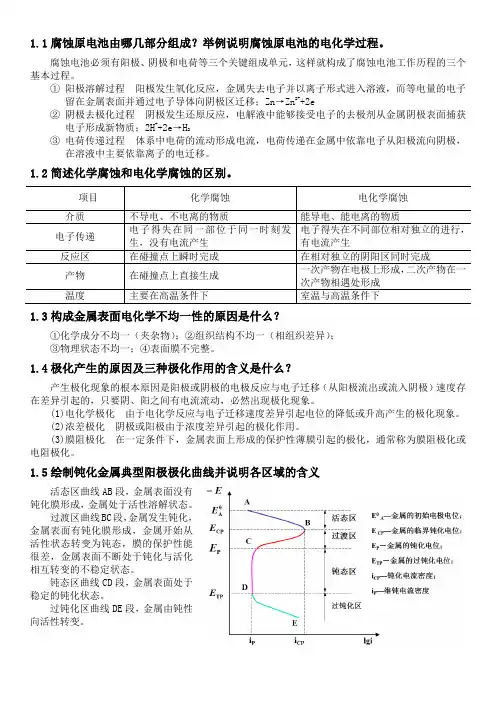


一、腐蚀的危害性与控制腐蚀的重要意义腐蚀现象几乎涉及国民经济的一切领域。
腐蚀不仅造成经济上的巨大损失,并且往往阻碍新技术、新工艺的发展。
因此,研究材料的腐蚀规律,弄清腐蚀发生的原因及采取有效的防止腐蚀的措施。
对于延长设备寿命、降低成本、提高劳动生产率无疑具有十分重要的意义。
二、设计者掌握腐蚀基本知识的必要性腐蚀控制通常有两种措施,一是补救性控制,即腐蚀发生后再消除它;二是预防性控制,即事先采取防止腐蚀的措施,避免或延缓腐蚀,尽量减少可能引起的其他有害影响。
三、腐蚀的定义与分类腐蚀是在金属材料和环境介质在相界面上反应作用的结果,因而金属腐蚀可以定义为“金属与其周围介质发生化学或电化学作用而产生的破坏”。
腐蚀有不同的分类方法。
按照腐蚀机理可以将金属腐蚀分为化学腐蚀与电化学腐蚀两大类。
1) 化学腐蚀是指金属与非电解质直接发生化学作用而引起的破坏。
2) 电化学腐蚀是金属与电解质溶液发生电化学作用而引起的破坏。
按照金属破坏的特征,可分为全面腐蚀和局部腐蚀两类。
(1) 全面腐蚀是指腐蚀作用发生在整个金属表面,它可能是均匀的,也可能是不均匀。
(2) 局部腐蚀是指腐蚀集中在金属的局部区域,而其他部分几乎没有腐蚀或腐蚀很轻微。
局部腐蚀有以下几种:a.应力腐蚀破裂在拉应力和腐蚀介质联合作用下,以显著的速率发生和扩展的一种开裂破坏。
b.腐蚀疲劳金属在腐蚀介质和交变应力或脉动应力作用下产生的腐蚀。
c.磨损腐蚀金属在高数流动的或含固体颗粒的腐蚀介质中,以及摩擦副在腐蚀性质中发生的腐蚀损坏。
d.小孔腐蚀腐蚀破坏主要集中在某些活性点上,蚀孔的直径等于或小于蚀孔的深度,严重时可导致设备穿孔。
e.晶间腐蚀腐蚀沿晶间进行,使晶粒间失去结合力,金属机械强度急剧降低。
破坏前金属外观往往无明显变化。
f.缝隙腐蚀发生在铆接、螺纹接头、密封垫片等缝隙处的幅度hi。
g.电偶腐蚀在电解质溶液中,异种金属接触时,电位较正的金属促使电位铰负的金属加速腐蚀的类型。

为什么说“材料的腐蚀是自发产生的”自然界中物质最稳定的存在状态是以金属化合物的形态存在..如:Fe 2O 3、FeS 、Al 2O 3等等..由于它们的强度、硬度、刚度等性能不能满足工业结构材料的要求;用冶金方法外加能量将它们还原成金属元素及其合金;它们比其化合物具有更高的自由能;根据热力学第二定律;金属元素必然自发地转回到热力学上更稳定的化合物状态..这就是金属的腐蚀过程..有机非金属材料是由有机小分子材料经聚合成为大分子材料而具有一定的强度、刚度和硬度;具备满足工业结构材料性能的..在聚合过程中加入的能量;使其比小分子具有更高的自由能..在介质中材料发生一些化学或物理作用;使其从高能的聚合态向低能而稳定的小分子状态转变;使材料的原子或分子间的结合键破坏..也是服从热力学第二定律的.. 无机非金属材料有天然的和人工的..两者均是由在自然界较稳定的化合物状态的分子或元素;在天然或人工外部作用下;结合成具有一定形状、强度、刚度和硬度的材料..这些材料在形成过程中受到的外部作用;使其内能增加;具有比它们的化合物状态的分子或元素高的能态;同样由热力学第二定律;它们在腐蚀性介质环境下;发生化学或物理作用;使材料的原子或分子间的结合键断裂破坏..也服从热力学第二定律..材料腐蚀危害性 a.涉及范围广泛:因腐蚀是自发产生的;腐蚀现象就涉及到所有使用材料的一切领域;b.造成的经济损失巨大;间接损失:由于腐蚀引起停产、更新设备、产品和原料流失、能源浪费..一般间接损失比直接损失大很多..污染环境、造成中毒、火灾、爆炸等重大事故..c.阻碍新技术、新工艺的发展..直接损失:由于腐蚀造成的材料自身的损失;使材料变成废物..间接损失:由于腐蚀引起停产、更新设备、产品和原料流失、能源浪费..一般间接损失比直接损失大很多..污染环境、造成中毒、火灾、爆炸等重大事故..控制腐蚀重要意义 研究材料的腐蚀规律;弄清腐蚀发生的原因及采取有效的防腐蚀措施;可以延长设备寿命、降低成本、提高劳动生产率.. 什么叫腐蚀 材料由于环境作用引起的破坏或变质..化学腐蚀 金属与非电解质直接发生化学作用引起的破坏..电化学腐蚀 金属与电解质溶液发生电化学作用引起的破坏..腐蚀按腐蚀机理 化学腐蚀和电化学腐蚀两类腐蚀按破坏特征 全面腐蚀和局部腐蚀两类局部腐蚀 应力腐蚀破裂、腐蚀疲劳、磨损腐蚀、小孔腐蚀、晶间腐蚀、缝隙腐蚀、电偶腐蚀、氢脆、选择性腐蚀、空泡腐蚀、丝状腐蚀腐蚀按腐蚀环境 大气腐蚀、土壤腐蚀、电解质溶液腐蚀、熔融盐中的腐蚀、高温氧化腐蚀和氢腐蚀作为过程装备设计人员;学习腐蚀知识有哪些必要性 a.合理选材:满足工艺和机械性能、防腐蚀要求;b.合理的结构设计:在结构设计时;要考虑工艺要求、强度要求;同时考虑腐蚀问题;c.制定正确的机械制造工艺和热处理方法;d.采用经济实用的防腐蚀技术..金属腐蚀过程;可能按照哪些历程进行 各具有什么特点 金属腐蚀过程 可按化学和电化学两种历程进行..化学历程 氧化剂直接与金属表面的原子相碰;化合物形成腐蚀产物;该过程无电流产生..电化学历程 金属腐蚀的氧化还原反应的两个过程同时进行又相对独立;该过程有电流产生..电化学腐蚀的条件 阳极氧化、阴极还原、电解质存在..金属在含有其自身离子的盐溶液中;界面上形成双电层;使金属表面带有:①一定是正电;②一定是负电;③可能是正电;也可能是负电..三者哪个正确;为什么 说明双电层的特点答:②正确..在含有其自身离子的盐溶液中;盐溶液的极性水分子与金属离子之间的水化力大于金属离子与电子之间的结合力;形成的双电层;在金属表面上带负电;在金属和溶液界面溶液侧带正电.. 双电层的特点:①双电层的两层“极板”可能分处于不同的相中;如第一类双电层;也可能分处于同一相中;如第二类和第三类双电层..②双电层的内层有过剩的电子或阳离子;当系统形成回路时;电子可沿导线流入或流出电极..③双电层间存在很大的电位跃..举例说明什么是平衡电极电位和非平衡电极电位;标准电极电位是哪一种电位 非平衡电极电位能否用能斯特公式进行计算 为什么 铜电极放入硫酸铜溶液中;当溶液中铜离子的浓度达到使铜电极的溶解与铜离子在铜电极上析出的速率相等时;这时电极反应的正逆两过程的电荷和物质都达到了动态平衡;此时铜电极的电位就是铜的平衡电极电位..如果把铁电极放入硫酸铜溶液中;铁电极溶解使溶液中铁离子浓度逐渐增加;到达一定程度后;溶液中的铁离子也会在铁电极上析出;但铜离子也析出;总不能使溶解出的金属离子在电量和质量上同时达到动态平衡;铁电极的电位成为非平衡电极电位..标准电极电位是标准状态下的平衡电极电位..非平衡电极电位不能用能斯特方程计算..因为能斯特方程是建立在平衡状态条件下计算电极电位的方程..写出下列电极反应的电极电位表达式.. 解:①查表1-5标准氧化还原电位;电极电位表达式①的标准氧化还原电位为0②查表1-5标准氧化还原电位;电极电位表达式②的标准氧化还原电位为+0.771V③查表1-5标准氧化还原电位;电极电位表达式③的标准氧化还原电位为+0.401说明什么叫氧化还原电极 什么叫氧化还原电位答:各种去极化反应在阴极进行时;阴极的电极材料本身不发生任何变化;只是当反应物在其表面氧化或还原时起输送或带走电子的作用;且氧化或还原的产物留在溶液中而不在电极上析出;这种电极称为氧化还原电极当去极化反应达到动态平衡时;其相应的平衡电位称为氧化平衡电位写出金属电化学腐蚀的热力学条件.. 答:0.K M e E E E <<何谓腐蚀电池 腐蚀电池有哪些类型 如图请标明腐蚀电池的各个组成部分..和原电池的工作原理一样;所不同的是腐蚀系统中电子回路短接;电流不对外作功;实际上是一个短路原电池..有宏观腐蚀电池和微观腐蚀电池两种类型..由铜和铁在稀H 2SO 4溶液中组成电池;指出正、负极和阴、阳极;并写出两电极反应的方程式;说明发生腐蚀的是哪个电极..答:铜是负极和阳极;铁是正极和阴极..e Fe Fe e Cu Cu 2;222+⇔+⇔++;铁电极发生腐蚀..极化现象 阳极极化和阴极极化 答:腐蚀电池工作时;由于电流流动而引起电极电位偏离初始值的现象;称为极化现象..通阳极电流后;阳极电位向正方向偏离称为阳极极化..通阴极电流后;阴极电位向负方向偏离称为阴极极化..电化学极化 浓差极化和膜阻极化 答:阴极上由于去极剂与电子结合的反应速度迟缓;来不及全部消耗来自阳极流来的电子;造成阴极电子增高;便阴极电位向负方向变化;阳极上金属失去电子成为水化离子的反应速度落后于电子流出阳极的速度;造成阳极电位向正方向偏离;叫做电化学极化..溶液中的去极剂到达阴极上与电子结合的速度比去极剂扩散到阴极上的速度高很多;造成阴极电位向负方向偏离..去极剂的扩散速度决定它在溶液中的浓度差;从而由它造成的极化叫浓差极化..金属表面形成的保护膜;具有较大的电阻;造成阳极溶解过程受阻;产生阳极电位向正方向的偏离;称为膜阻极化..解释P a 、P k 的物理意义..答:P a 是阳极极化曲线的极化率;P K 是阴极极化曲线的极化率;它们分别表示阳极过程和阴极过程的阻力大小..它们的数值大说明电极过程阻力大..腐蚀极化图;Evans 图 把构成腐蚀电池的阴极和阳极极化曲线绘在同一个电位E —I 电流强度坐标上;得到的图线称为腐蚀极化图.. 腐蚀极化图略去电位随电流的详细过程;将极化曲线简化成直线;这种简化了的极化图称为Evans 图..混合电位 腐蚀电位答:由于金属表面的电化学不均一性;存在很多微阳极和微阴极;在电解质溶液中在金属表面上同时进行着两个以上的共轭电极反应..因阴极与阳极间从金属内部自然导通;金属上总的阳极反应电流必然等于总的阴极电流;恰好抵消..当达到稳定状态时;阴极和阳极彼此相互极化到同一电位;这一电位就是腐蚀电位;又称自腐蚀电位..腐蚀电位既非金属上阳极的平衡电位;也不是阴极的平衡电位;而是处在二者之间;又称为混合电位..1. 请解释下式中各参数的物理意义..C PP P R E E a aa k a o =++=⨯∆∆100% C a -阳极控制程度; -阳极极化率;P K -阴极极化率;R-腐蚀系统电阻;ΔEa=I P a ;阳极极化引起的电位差;ΔE 0-阳极和阴极平衡电极电位之差下列电极过程为何种控制 为什么 答:a 为阳极控制过程;因为阳极极化率>阴极极化率;b 为阴极控制过程;因为阴极极化率>阳极极化率;c 为混合控制;阳极极化率与阴极极化率接近相等;d 是电阻控制;系统电阻在腐蚀控制中占主导地位根据下图你能得出何结论 此时;改变阳极极化曲线对其腐蚀有无影响 答:当阳极极化曲线在A 点以上变化时;对腐蚀速度无影响;低于A 点后;随阳极极化曲线变化;对腐蚀速度的变化有较大影响..如图说明为什么标准氢电极参比电极采用金属铂制成..答:是因为金属铂的超电压在较大电流密度下相对其他金属的小;偏离平衡电位的数值就小;作为标准氢电极采用的金属;测定的电极电位误差就小..说明影响析氢腐蚀的因素和特点.. 答:影响析氢腐蚀的因素有: a.电极表面状态 粗糙表面析氢超电压低;光滑表面析氢超电压高..原因是粗糙表面积大;阴极面积大..b.PH 值 酸性溶液中PH 值上升;析氢超电压升高;碱性溶液中PH 值下降;析氢超电压升高..c.温度 温度升高析氢超电压下降;约温度每增加1℃;析氢超电压减小2mV..d.溶液中的添加剂的性质不同;引起析氢超电压的变化不同.. 析氢腐蚀的特点:①阴极材料的性质对腐蚀速度影响很大..②溶液的流动状态对腐蚀速度影响不大..③阴极面积增加;腐蚀速度加快..④氢离子浓度增高PH下降、温度升高均会促使析氢腐蚀加剧..求25℃1atm时氢在中性溶液中的平衡电极电位.. 题给条件是标准状态;在标准状态下;氢的平衡电极电位规定为0..影响耗氧腐蚀的因素有哪些如何影响答:影响耗氧腐蚀的因素有:金属的本性、溶液的含氧量、阴极面积大小、溶液的流动状态..阳极金属的电位和极化性能不同;它的极化曲线与耗氧腐蚀的阴极极化曲线相交的位置不同;腐蚀速度不同;溶液的含氧量不同;耗氧腐蚀阴极极化曲线不同;氧含量大时;对应同样的阳极极化曲线;腐蚀电流大;对于宏观腐蚀电池阴极面积大;腐蚀速率大;对于微观腐蚀电池;阴极面积大小对腐蚀电流大小的影响很小;几乎无影响;溶液流动状态不同;造成溶液中的氧量补充到阴极的数量不同;一般流速大时腐蚀速率高..对一般电化学腐蚀;微阴极的数目对腐蚀有很大影响;为什么若阴极过程为耗氧反应;是否受微阴极多少的影响为什么答:因为一般电化学腐蚀;微阴极数目大时;还原反应进行的多;阳极就必须提供相应量的电子;腐蚀速度就大..到达微阴极的去极剂是溶解在电解质溶液中靠浓度差传递的;阴极面积越大;与去极剂相遇的机会就高..若为耗氧反应;氧从气液界面进入溶液向金属界面传递;传递途径类似一个圆锥体;一定数量的微阴极就已经利用了全部输送氧的扩散通道;微阴极增加;并不能增加扩散到微阴极上的总量..何为金属的钝化指出钝化时典型阳极极化曲线上各区域的名称活态区;过渡区、钝态区、过钝化区及各符号的物理意义..画图说明答:金属从活性溶解状态变成非常耐蚀的状态;这种表面状态的突变过程称为“钝化”铁制容器能否用来盛稀硝酸和浓硝酸为什么答:不能..因为铁虽可在硝酸浓度>40%后;被钝化;但钝化层会随温度升高;硝酸浓度的变化出现溶解;失去钝化作用..成相膜理论和吸附理论的要点是什么答:成相膜理论认为:钝化是由于金属溶解时;在金属表面生成了致密的、覆盖性良好的固体产物保护膜;这层保护膜作为一个独立的相而存在;它或者使金属与电解质溶液完全隔开;或者强烈地阻滞了阳极过程的进行;结果使金属的溶解速度大大降低;亦即使金属转变为钝态..吸附理论认为:金属钝化并不需要固态产物膜;而只要在金属表面或部分表面上生成氧或含氧粒子的吸附层就足够使金属钝化了..当这些粒子在金属表面上吸附以后;就改变了金属—溶液的界面的结构;并使阳极反应的活化能显着升高;因而金属表面本身的反应能力降低了;亦即呈现钝态..何谓金属的应力腐蚀破裂金属的应力腐蚀破裂有何特征金属的应力腐蚀破裂是金属结构在拉应力和腐蚀环境共同作用下引起的破裂.. ①在拉应力作用下;发生应力腐蚀破裂的金属材料对应的腐蚀环境是特定的—包括腐蚀介质性质、浓度、温度..②SCC断裂速度约0.01~3mm/h;比不存在拉应力时的局部腐蚀速率大很多倍;比无腐蚀环境时的纯力学断裂速度低很多;但承受的应力水平也低很多..③断口形貌;宏观上属于脆性断裂;微观上在断裂面上仍有流变痕迹..应力腐蚀破裂的机理电化学阳极溶解理论的论点:认为合金中存在一条阳极溶解的“活性途径”;腐蚀沿这些途径优先进行;阳极侵蚀处就形成狭小的裂纹或蚀坑..小阳极的裂纹内部与大阴极的金属表面构成腐蚀电池;由于活性阴离子如Cl—进入形成闭塞电池的裂纹或蚀坑内部;使浓缩的电解质溶液水解而被酸化;促使裂纹尖端的阳极快速溶解;在应力作用下使裂纹不断扩展;直至破裂..防止金属应力腐蚀破裂的途径有哪些答:有①降低设计应力;使最大有效应力或应力强度降低到临界值以下..②合理设计与加工减少局部应力集中..③采用合理的热处理方法消除残余应力..④合理选材;去除介质中的有害成分;添加缓蚀剂;阴极保护..金属的腐蚀疲劳是什么金属构件在交变负荷和腐蚀环境的联合作用下;经过一定周期后发生的断裂破坏;称为腐蚀疲劳..特点:①腐蚀疲劳的产生条件;没有特定的腐蚀介质的限定;只要有交变载荷存在;任何腐蚀环境中都可能发生..②腐蚀疲劳裂纹多为穿晶型;裂纹分支较少..③不存在疲劳极限;同样循环次数;承受的应力幅度值大量降低..④疲劳裂纹的断面大部分被腐蚀产物所覆盖;小部分呈粗糙的碎裂状..防止金属腐蚀疲劳的方法:①降低局部应力集中..②金属表面电镀..③介质中加缓蚀剂..④金属表面氮化和喷丸处理..⑤阴极保护..金属的SCC与腐蚀疲劳有何区别答:SCC承受的是拉应力;当拉应力低于某一定应力水平时不发生..腐蚀疲劳承受的是交变载荷;并不存在疲劳极限;也就是应力水平无下限..腐蚀疲劳的产生条件与应力腐蚀比较;它没有特定的腐蚀介质的限定;也就是说;在任何腐蚀环境中都可能发生..从撕裂特征来看;应力腐蚀裂纹既可为穿晶型;也可能为晶间型;且裂纹分枝多;呈树根状..而腐蚀疲劳裂纹多为穿晶型;裂纹分支较少..它所产生的裂纹数量往往比纯力学疲劳的多得多..从破坏的断面来看;纯力学疲劳破坏的断面大部分是光滑的;小部分是粗糙面;呈现一些结晶形状..腐蚀疲劳破裂的断面大部分被腐蚀产物所覆盖;小部分呈粗糙的碎裂状..磨损腐蚀腐蚀性流体与金属构件以较高的速度作相对运动而引起金属的腐蚀损坏;称为磨损腐蚀..形式有:湍流腐蚀、空泡腐蚀、微振腐蚀..湍流腐蚀的机理:流体速度达到湍流状态;击穿紧贴金属表面几乎静态的边界液膜;加速去极剂供应和阴、阳极腐蚀产物迁移;产生附加切应力;带动颗粒磨损..这些都加速了腐蚀速度..空泡腐蚀的机理:腐蚀介质与金属构件作高速相对运动;使流体的动能增加;而静压能降低..当流速足够高时;流体的静压力将低于流体的蒸汽压;使流体蒸发形成汽泡..在低压区产生的汽泡在高压区被压缩崩溃;气泡崩溃所产生的冲击波将对金属表面起强烈的锤击作用;使金属表面膜被破坏;甚至可使膜下金属的晶粒产生龟裂和剥落..这样重复的锤击作用;使金属造成小阳极大阴极而遭受腐蚀..微振腐蚀机理:由于流体高速流动;产生卡曼涡街;造成金属构件的振动;从而使边界层减薄或破碎;加速了阴、阳极腐蚀产物的迁移和去极剂的供应;从而加速了腐蚀速度..小孔腐蚀腐蚀破坏主要集中在某些活性点上;蚀孔的直径等于或小于蚀孔的深度的腐蚀现象..机理:易钝化金属在含有活性阴离子的溶液中;在钝化膜破损处;金属光滑表面上有夹杂的硫化物处、晶间有碳化物沉积处等很小的局部缺陷处;由于钝化膜的高电阻;造成小阳极大阴极的腐蚀电池;而形成蚀核..有些蚀核不再长大;有些蚀核继续长大;长成蚀孔..形成蚀孔后;孔内表面金属处于活态;电位较负..蚀孔外的金属表面处于钝态;电位较正;孔内外构成一个活态~钝态微电池..钝态表面被保护;孔内金属加速腐蚀..随腐蚀过程进行;孔深加深;孔外的氧不易扩散入孔内;孔内溶解的金属离子也不易往外扩散;孔内带正电的金属离子浓度增加;为保持溶液的电中性;带负电的氯化物水解;生成盐酸;使孔内介质的酸度增高;加速阳极溶解;从而形成具有“自催化酸化作用”的闭塞电池..从而使蚀孔沿重力方向迅速深化;以至把金属断面蚀穿..防止方法:①降低金属材料中的有害杂质..②在金属材料中加抗孔蚀合金元素..③降低溶液中氯离子浓度..④改善热处理制度;结构设计上消除死区..⑤阴极保护..什么叫缝隙腐蚀金属与金属或金属与非金属之间存在很小的缝隙时;缝内介质不易流动而形成滞留状态;促使缝隙内的金属加速腐蚀;称为缝隙腐蚀..原因有:开始在缝隙口处是氧去极化作用;继而是氧扩散的浓差极化控制;最后形成闭塞电池的自催化腐蚀过程..简述小孔腐蚀与缝隙腐蚀的区别.. 答:区别为腐蚀的起因不同;一旦腐蚀发展两者一样都属于闭塞电池的自催化腐蚀过程..小孔腐蚀的起因为:在易钝化的金属表面钝化层有破损处形成蚀孔活性中心;有些活性中心发展成为蚀孔..缝隙腐蚀的起因为:初期缝隙内外发生氧去极化的均匀腐蚀..随后构成宏观的氧浓差电池;缺氧的缝内成为阳极;缝外为阴极;逐步发展为闭塞电池..电偶腐蚀异种金属彼此接触或通过其他导体连通;处于同一种介质中;会造成接触部位的局部腐蚀..其中电位较低的金属;溶解速度大;电位较高的金属;溶解速度反而减小;这种腐蚀称为电偶腐蚀;或称接触腐蚀、双金属腐蚀..机理:一种阳极电位较负的金属和一种阳极电位较正的金属偶接;电位较低的金属成为偶接电池的阳极;电位较高的金属成为偶接电池的阴极..从而使电位较低的金属在偶接电池的腐蚀电流强度比单独存在时;更大;电位较高的金属在偶接电池的腐蚀电流强度比单独存在时更小..电位较低的金属腐蚀速度增加;电位较高的金属腐蚀速度减小..防止电偶腐蚀可采用哪些方法①选择相容性材料;选择电偶序表中;相邻的金属偶接;减小偶接电位差..②合理的结构设计a.尽量避免小阳极大阴极结构;b.将不同金属的部件彼此绝缘;c.插入第三种金属;降低两种金属间的电位差;d.将阳极性部件设计为易于更换的或适当增厚以延长寿命..焊接表面缺陷主要有哪几种它们引起什么腐蚀类型有焊瘤、咬边、飞溅及电弧熔坑..焊瘤或咬边常形成可见的狭缝;而飞溅往往在母材板和金属颗粒的接触区形成缝隙;从而引起缝隙腐蚀..熔坑是孔蚀的发源地..写出焊接残余应力的分布情况.. 答:当已凝固的焊缝金属在冷却的时候;由于垂直焊缝方向上各处的温度差别很大;结果高温区金属的收缩会受到低温区金属的限制;而使这两部分金属中都引起内应力;高温区金属内部产生残余拉应力;低温区金属内部产生残余压应力..焊缝晶间腐蚀的特征..焊缝晶间腐蚀的特征为;在表面还看不出破坏时;晶粒间已几乎完全丧失了结合强度;并失去金属声音;严重时只要轻轻敲打即可破碎;甚至成粉状..特别是不锈钢材料;有时即使晶间腐蚀已发展到相当严重的程度;其表观仍保持着光亮无异的原态..晶间腐蚀的机理..奥氏体不锈钢在450~850℃长时间加热;例如焊接时;焊缝两侧2~3㎜处将被加热到这个温度范围的所谓晶间腐蚀敏化区;此时晶间的铬和碳化合成为Cr、Ni、Fe4C、Cr、Fe、Ni7C3或Cr23C6;从固溶体中沉淀出来;生成的碳化物;每1%C 约需10%~20% Cr;导致晶间铬含量降低..这时由于晶内与晶间的元素存在浓度梯度;晶内的碳及铬将同时向晶间扩散;但在450~850℃;Cr 比C 的扩散速度慢原子半径Cr=1.28;C=0.771;因此进一步形成的碳化铬所需的Cr 仍主要来自晶粒边缘;致使靠近碳化铬的薄层固溶体中严重缺Cr;使Cr 量降到钝化所必需的最低含量11%以下..这样;当与腐蚀介质接触时;晶间贫铬区相对于碳化物和固溶体其他部分将形成小阳极对大阴极的微电池;而发生严重的晶间腐防止晶间腐蚀有哪些方法答:有固溶处理、稳定化退火、超低碳法、合金化法和焊接材料中掺入铁素体形成元素使焊缝呈奥氏体-铁素体双相组织..金属F e 在P O2=1atm 的环境中腐蚀达到平衡后;把其放入P=1atm 的空气环境中;平衡将有何变化 为什么答:出现铁的氧化物分解..因为在1个大气压的空气中;氧的分压只有0.21个大气压;而氧化是在氧压力为1个大气压下达到平衡的;它高于空气中氧的分压;因此分解..如下图;造成氧化膜生长的位置不同的原因 a 图的膜生长位置在MO/O 2界面;是因为氧化膜中金属离子过剩;过剩的金属离子可能处于晶格的间隙位置上;膜内晶格缺陷便是间隙金属离子和自由电子;间隙金属离子和电子通过膜中的间隙向外扩散;在MO/O 2界面与O 2反应生成MO..当氧化膜中金属离子不足时;则膜内晶格缺陷是金属离子空位和电子空位;在氧化期间;金属离子和电子通过金属离子空位和电子空位向外扩散;并在MO/O 2界面与O 2反应生成MO..b 图膜中过剩的金属离子处于正常晶格位置;膜内晶格缺陷则是阴离子如O 2-和自由电子;氧化期间;电子向外运动;O 2-通过O 2-空位向内扩散;并在M/MO 界面与M 2+反应生成MO..c 图膜中的晶格缺陷同时包含以上两种情况下的晶格缺陷;因此膜生成双向扩散同时存在;膜在中间位置生长.. 什么叫N 型半导体氧化物和P 型半导体氧化物 N 型半导体氧化物是:主要通过带负电荷的自由电子而导电的氧化物..P 型半导体氧化物是:主要通过电子空位的运动而导电的氧化物..金属表面膜完整的必要条件是什么 庇林-贝德沃斯比r>1.. 完整的表面膜不一定具有保护性..保护膜的条件:①膜必须是完整的;②膜具有足够的强度和塑性..并且与基体金属结合力强;膨胀系数相近;③膜内晶格缺陷浓度较低;④氧化膜在高温介质中是稳定的;表现为高的熔点和高的生成热..在氧化物中加入少量高价离子或低价离子N 型、P 型半导体氧化物有何影响答:对于金属离子过剩型的氧化膜N 型半导体;加入少量较高原子价的金属离子;可以减少间隙金属离子浓度;使金属氧化速度降低..对于金属离子不足型的氧化膜P 型半导体;加入少量较低原子价的金属离子;可以减少金属离子空位度;提高金属的抗氧化能铁有三种腐蚀产物FeO 、Fe 2O 3、Fe 3O 4;如图;为什么最内层是FeO;最外层是Fe 2O 3 答:因为FeO 是P 型半导体;具有高浓度的Fe 2+空位;晶格缺陷是金属离子空位;使得Fe 2+快速向外扩散;在FeO/界面与O 2-结合成FeO..Fe 2O 3是具有阴离子O 2-空位的N 型半导体;O 2-通过空位向内扩散;在Fe 2O 3/ Fe 3O 4界面与结Fe 2+合成Fe 2O 3..Fe 3O 4中P 型半导体占优势;它的导电率比FeO 要低得多..Fe 3O 4膜的成长是由于离子电导的80%是Fe 2+向外扩散;20%是O 2-向内扩散..提高钢的抗氧化性的主要途径 :合金化..-铁碳合金发生氢腐蚀的机理和条件.. 机理:氢脆阶段;钢材与氢气接触后;氢被吸附在钢表面上;然后分解为氢原子并沿晶粒边界向钢材内部扩散..尤其当钢材受力变形时;会剧烈地加速氢原子的扩散;高速扩散的氢原子在滑移面上转变成为分子状态;而分子氢不具有扩散能力;在晶间积聚产生内压力;使钢材进一步变形受到限制而呈现脆性..氢侵蚀阶段;当温度和压力较高;或者钢材与氢气接触的时间很长;则钢材将由氢脆阶段发展为氢侵蚀阶段;溶解在钢中的氢将与钢中渗碳体发生脱碳反应生成甲烷;随着反应的不断进行;钢中的渗碳体不断脱碳变成铁素体;并不断生成甲烷;而甲烷在钢内扩散困难;积聚在晶界原有的微观空隙内;随着反应的不断进行而愈聚愈多;产生很大的内压力;形成局部高压;造成应力集中;使细微开口、扩大、传播;引起钢材中出现大量细小的晶界裂纹和气泡;使钢的强度和韧性大为降低;甚至开裂;导致设备破坏..钢内裂纹的产生;除了上述甲烷积聚形成局部高压、钢材脱碳强度降低以外;还由于渗碳体转变为铁素体后;体积缩小了0.7%;因而使钢材内部产生裂纹.. 条件:在一定的氢气压力下;渗碳体与氢气发生反应有一最低温度;称为氢腐蚀的起始温度;它是衡量钢材抗氢腐蚀的性能指标..低于这个温度时氢腐蚀反应速度极慢;可以认为对钢材无害..对应相应材料曲线;根据工作温度和氢气分压;查Nelson 线图;当纵坐标的工作温度和横坐标的氢气分压的交点在对应材料曲线的上方为发生腐蚀;在曲线下方为不发生腐蚀..方法:①在钢中加入强碳化物形成元素;它们把钢中的碳优先结合成稳定的碳化物;提高钢的抗氢腐蚀性能;②采用微碳纯铁含碳量<0.015%也具有很好的抗氢腐蚀性。
过程装备腐蚀与防护心得体会(5篇材料)第一篇:过程装备腐蚀与防护心得体会学习《过程装备腐蚀与防护》心得腐蚀现象几乎涉及国民经济的一切领域。
例如,各种机器、设备、桥梁在大气中因腐蚀而生锈;舰船、沿海的港口设施遭受海水和海洋微生物的腐蚀;埋在地下的输油、输气管线和地下电缆因土壤和细菌的腐蚀而发生穿孔;钢材在轧制过程因高温下与空气中的氧作用而产生大量的氧化皮;人工器官材料在血液、体液中的腐蚀;与各种酸、碱、盐等强腐蚀性介质接触的化工机器与设备,腐蚀问题尤为突出,特别是处于高温、高压、高流速工况下的机械设备,往往会引起材料迅速的腐蚀损坏。
目前工业用的材料,无论是金属材料或非金属材料,几乎没有一种材料是绝对不腐蚀的腐蚀造成的危害是十分惊人的。
据估计全世界每年因腐蚀报废的钢铁约占年产量的30%,每年生产的钢铁约10%完全成为废物。
实际上,由于腐蚀引起工厂的停产、更新设备、产品和原料流失、能源的浪费等间接损失远比损耗的金属材料的价值大很多。
各工业国家每年因腐蚀造成的经济损失约占国民生产总值的1%~4%。
腐蚀不仅造成经济上的巨大损失,并且往往阻碍新技术、新工艺的发展。
例如,硝酸工业在不锈钢问世以后才得以实现大规模的生产;合成尿素新工艺在上世纪初就已完成中间试验,但直到20世纪50年代由于解决了熔融尿素对钢材的腐蚀问题才实现了工业化生产。
通过学习我们可以从最开始的设计阶段就考虑腐蚀对工程的影响,用正确的方法控制腐蚀,这样既能节省资源,又能延长设备的使用寿命,提高了我们的效率。
对我们来说,我们更要踏实的学习知识,如果缺乏对于温度的、压力、浓度等的影响腐蚀规律的分析判断能力,那么按照手册相近选定的材料,往往会造成设备的过早破坏。
结构复杂的机器、设备,出于某种特定功能的需要,常常选用不同材料的组合结构,如果不注意材料之间的电化学特征的相容性,或两种材料的结构相对尺寸比例不恰当,热处理度不合理,都会加速设备的腐蚀。
所以腐蚀贯穿整个设计过程,所以我们要掌握腐蚀的一些基本知识是十分必要的。
过程装备腐蚀与防护课程设计
一、课程概述
本课程旨在介绍过程装备的腐蚀问题及其防护措施,内容主要包括以下几个方面:
•过程装备的腐蚀分类和机理
•各种材料的耐腐蚀性能及应用
•腐蚀监测和评估方法
•腐蚀防护技术和措施
•腐蚀事故案例分析和预防措施
本课程适合化工、冶金、能源等相关专业本科及研究生学生、工程师等参与学习。
二、课程大纲
章节主要内容学时
第一章过程装备腐蚀的分类及机理 2
第二章材料的耐腐蚀性及应用 4
第三章腐蚀监测与评估 2
第四章腐蚀防护技术和措施 4
第五章腐蚀事故案例分析及预防措施 2
第一章:过程装备腐蚀的分类及机理
学习目标: - 了解过程装备腐蚀的分类和机理 - 理解腐蚀对装备的危害
1。
《腐蚀与防护》课程简介
课程性质:选修课课程类型:专业课
总学时:32学分:2
开课教研室:过程装备与控制适用专业:过程装备与控制工程
课程简介:
《过程装备腐蚀与防护》为过程装备与控制工程专业的一门专业选修课程,同时。
它又是一门应用性很强的技术科学。
通过这门课程的学习,使学生在从事过程装备的设计、制造、安装与维修工作中,能从腐蚀与防护的角度,正确的选择材料,进行合理的结构设和采取必要的防护措施。
本门课程的主要内容包括金属腐蚀基本原理,影响腐蚀的结构因素,金属在典型介质中的腐蚀特点,耐蚀材料金属和非金属材料的耐蚀机理以及防护方法等。
通过本门课程的学习,要求学生能合理地运用所学到的有关腐蚀与护护的知识,解决实际中的问题。
对金属腐蚀理论、基本概念及重要的作用机理要有较清楚的理解,对一般的腐蚀现象能进行初步的分析。
初步掌握化工机械制造中的主要金属材料和非金属材料的耐腐蚀性能、主要的物理、机械性能及应用范围。
在防止腐蚀方面,要求学生了解基本原理、主要应用场合及条件。
本门课程是特点是理论知识比较抽象,因此,在学习的过程中,应该结合实际工程中化工设备和机械的腐蚀实例,才能更好地掌握这门课程。
选用教材:陈匡民,《过程装备腐蚀与防护》.北京:化学工业出版社,2002.6。
《过程装备腐蚀与防护》(论文)题目关于氯碱生产装置腐蚀与防护的浅析系(院)城市与环境系专业安全工程班级2010级1班学生姓名王学志学号1014140311指导教师李超二〇一三年六月二十六日关于氯碱生产装置腐蚀与防护的浅析摘要工业上用电解饱和氯化钠溶液的方法制取氢氧化钠、氯气和氢气,并以它们为原料生产一系列化工产品,成为氯碱工业。
氯碱的生产按流程分为盐水、电解、氯处理和碱浓缩四大工艺系统。
氯碱装置中的氯气、盐酸、烧碱等具有强腐蚀性,以及电解槽、盐水预热器等装置的腐蚀都比较常见。
腐蚀一直是制约氯碱工业安全生产运行的一个难题,因此如何正确选材和防止腐蚀是氯碱装置安全稳定运行的关键。
本文分析了氯碱装置中介质的腐蚀、常用材料的耐腐蚀特性以及生产流程中典型装置的腐蚀特性及防腐措施。
关键字:氯碱生产装置;腐蚀;防护AbstractIndustrial electricity XieBao and preparing method of the sodium chloride solution sodium hydroxide, chlorine and hydrogen, and using them as a raw material to produce a series of chemical products, become a chlor-alkali industry. Chlor-alkali production according to the process can be divided into salt water, electrolysis, chlorine and alkali enrichment four process system. Chlor-alkali plant of chlorine gas, hydrochloric acid, caustic soda etc. Have strong corrosion resistance, corrosion and electrolytic cell, brine preheater and other devices are common. Chlor-alkali industry is restricted by the corrosion production safety running of a problem, so how to correctly select material and prevent corrosion is the key to the chlor-alkali equipment safe and stable operation. Chlor-alkali plant agents are analyzed in this paper the corrosion and corrosion resistant characteristics of commonly used materials and production process of typical devices corrosion characteristics and corrosion protection measures.Key words:Chlor-alkali production device;corrosion;protective目录前言 (1)1.氯碱生产装置 (1)2.介质的腐蚀特性 (2)2.1氯气 (2)2.2盐酸 (2)2.3氢氧化钠 (2)2.4氯化钠溶液 (3)2.5杂散电流 (3)2.6硫酸 (3)2.7其他方面 (3)3、控制介质防护措施 (3)3.1氯气 (3)3.2盐酸 (4)3.3氢氧化钠 (4)4.典型装置的防护 (5)4.1电解槽的防护 (5)4.2盐水预热器的杂散电流服饰防护 (5)4.3其他装置 (6)5.结论与展望 (6)参考文献 (7)前言腐蚀是材料在环境的作用下引起的破坏或变质。
金属和合金的腐蚀主要是化学电化学作用引起的破坏,有时还同时包含机械、物理或生物作用。
对于非金属材料来说, 腐蚀一般是由于直接的化学作用或物理作用(如氧化、溶解、溶胀等)引起的。
腐蚀的危害是巨大的, 使生产设施过早地报废,引起生产停顿、产品或生产流体的流失、环境污染、着火爆炸, 甚至危及人员和设备安全。
氯碱装置中的烧碱、氯气、盐酸、盐等具有强腐蚀性, 因此如何正确选材和防止腐蚀是氯碱装置安全稳定运行的关键。
目前, 氯碱行业有隔膜及离子膜烧碱装置、乙炔及乙烯法(聚)氯乙烯装置、氯醇化法环氧丙烷装置等, 所用结构材料以碳钢、铸铁、不锈钢、钛( 合金)、镍( 合金) 等金属材料为主, 耐蚀非金属材料如聚氯乙烯(PVC)、聚四氟乙烯(PTFE)、聚偏二氟乙烯(PVDF)、全氟烷氧乙烯与四氟乙烯的共聚物(PFA)、玻璃钢(FRP)、不透性石墨等材料也得到了广泛的应用。
1.氯碱生产装置氯碱的生产按流程分为盐水、电解、氯处理和碱浓缩四大工艺系统。
盐水系统主要是以原盐氯化钠为原料,经过原盐溶解、精制与澄清、盐水过滤、pH调节等工序制成精制食盐溶液供离子膜电解槽进行电解。
该系统中的腐蚀介质为氯化钠溶液。
电解系统主要是电解精制的食盐水,产品是氯气、氢气和氢氧化钠稀溶液。
该系统中的腐蚀介质主要是盐酸和次氯酸、氢氧化钠溶液及杂散电流。
氯处理系统主要是采用硫酸作为干燥剂,将湿氯脱水成为干氯,该系统中的腐蚀介质主要是湿氯和硫酸。
碱浓缩系统主要是将低浓度的电解液浓缩为高浓度的电解液,同时去除电解液中未电解的氯化钠及杂质硫酸钠等,获得高质量的烧碱溶液或固碱。
该系统主要包括蒸发、精制、固碱这三大操作单元,腐蚀介质主要是高浓度烧碱溶液。
2.介质的腐蚀特性2.1氯气这里氯气包括干氯和湿氯。
氯气是氯碱生产中的主要原料之一,它会对生产装置造成严重腐蚀,因此,防止它的腐蚀是至关重要的。
氯的化学性质非常活泼,常温干燥的氯对大多数金属的腐蚀都很轻,但当温度升高时腐蚀加剧。
这是由于干氯与金属作用生成的金属氯化物具有较高的蒸气压或较易融化的缘故。
湿氯气(水的体积分数大于100ppm) 中的氯与水反应生成强腐蚀性的盐酸和强氧化性的次氯酸,许多金属如碳钢、铝、铜、镍、不锈钢等均可被腐蚀,只有某些金属或非金属材料在一定条件下能抵抗湿氯气的腐蚀。
因此,氯碱生产中电解生成的湿氯气必须经过氯气冷却、水雾捕集器、填料干燥塔、泡罩干燥塔、酸雾捕集器等工序处理。
2.2盐酸在氯碱装置中,含有水分的湿氯会有相当部分转化为盐酸。
盐酸是一种典型的非氧化性酸,金属在盐酸中的腐蚀特点是:金属腐蚀的速度随盐酸浓度和温度的增加而上升。
对于碳钢而言,随着盐酸浓度的增加,其腐蚀速度按指数关系增大,这主要是因为由于氢离子浓度的增加,氢的平衡电位往正的方向移动,在超电压不变时,因腐蚀的动力增加了,故腐蚀加剧。
2.3氢氧化钠大多数金属在碱溶液中的腐蚀是氧去极化腐蚀。
常温时,金属在碱中是十分稳定的。
当pH很低时,由于氢的析出放电和析出的效率增加了,同时腐蚀产物也变得可溶了,因而腐蚀加剧。
但当pH值为4——9之间时,由于处在氧的扩散控制阶段,而氧的溶解度及其扩散速度与pH值关系不大,所以这是铁的腐蚀速度与pH值无关。
当pH值为9——14时,铁的腐蚀速度大为降低,这主要是由于腐蚀产物在碱中的溶解度很小,并能牢固地覆盖在金属的表面,从而阻滞阳极的溶解,也影响了氧的去极化作用。
当碱的浓度高于pH值14时,铁将会重新发生腐蚀,这是由于氢氧化铁膜主编为可溶性的铁酸钠所致。
2.4氯化钠溶液金属在氯化钠盐水系统中的腐蚀实质是氧去极化腐蚀。
在含氧的盐水溶液中,由于氧去极化的阴极反应是铁作为阳极发生腐蚀不断溶解。
金属在氯化钠盐水中,常常由于金属的不均匀性或者介质的不均匀性而形成腐蚀电池导致金属的腐蚀。
2.5杂散电流电解槽在工作的时候,电流应从阳极流回阴极,但可能会有部分电流从电解槽内泄漏出来,流出电解系统之外,最终又返回电解系统,形成漏电回路。
这种泄漏出来的电路成为杂散电流。
在氯碱工业中,它的存在可能使盐水管路、电解液管路、盐水预热期、电解槽等设备发生腐蚀。
2.6硫酸在氯碱装置中,氯处理系统通常是用浓硫酸作为干燥剂处理湿氯,使其干燥。
硫酸本身具有一定的腐蚀性。
2.7其他方面由于氯碱生产装置运行于高温环境,因此高温会对设备产生腐蚀。
另外,设备周围空气如若湿度过大或是含有某些盐类蒸汽,也会造成设备的大气腐蚀。
3、控制介质防护措施综上所述,并结合以往一些案例,在影响氯碱生产装置腐蚀的程度中,起决定性作用的主要有氯气、盐酸、氢氧化钠。
下面主要针对这三个方面,结合上面讨论的腐蚀性能提出防护措施。
3.1氯气通过查阅资料可知,下列材质可作为氯防护。
(1)碳钢应用在小于 90℃干燥的氯气中是比较稳定的,但在湿的氯气环境中则被腐蚀,因此,碳钢材质的透平压缩机、输送管线、设备可用于经冷却、干燥及水的体积分数小于 100ppm的氯气环境中,但要必须控制氯气温度小于 90℃。
当氯气压缩机出口温度大于 90℃,压缩机及后冷却器材质应采用不锈钢 316L。
(2)钛本身为活性金属,但在常温下能生成保护性很强的氧化膜,因而具有非常优良的耐蚀性能。
能耐各种氯化物和次氯酸盐、湿氯、氧化性酸(包括发烟硝酸)、有机酸、碱等的腐蚀。
不耐还原性酸(如硫酸、盐酸)的腐蚀。
常温下钛能耐小于 10%盐酸,当 50℃时能耐 3%盐酸。
加入少量贵金属(0.15%钯、铂等)可提高钛在还原酸中的耐蚀性。
但在生产过程中要特别关注干燥氯气中钛会腐蚀燃烧,干氯气如果进入钛制管线会引起着火燃烧的安全事故。
(3)橡胶的在生产中用途很广,主要用作各种橡胶制品,因其具有良好的耐腐蚀及防渗性能,所以被广泛地用于金属设备的防腐衬里。
橡胶分为天然橡胶和合成橡胶两大类,天然橡胶的化学性能较好,可耐一般非氧化性强酸、有机酸、碱溶液和盐溶液腐蚀,但在强氧化酸和芳香族化合物中不稳定。
在氯碱生产中橡胶对于湿氯和氯水有着较好的耐腐性,但在干燥的氯气中会腐蚀成粉末。
隔膜电解装置中盐水工序的设备、管路多采用衬橡胶,使用寿命较长。
3.2盐酸通过查阅资料可知,下列材质可作为氯防护。
不透性石墨对绝大多数腐蚀环境都有优良的耐蚀性,包括沸点盐酸、稀硫酸、氢氟酸、磷酸、碱液、有机溶剂等。
只有强氧化性介质如硝酸、浓硫酸、溴和氟能破坏它。
不透性石墨的品种因所浸渍树脂不同,耐蚀性也有差异。
石墨在还原性气氛中可耐 2000~3000℃,在氧化气氛中 400℃开始氧化。
耐温性因不透性石墨随浸渍剂而异,据了解进口石墨设备使用寿命一般在 15~20 年以上。