第七章 原子结构与元素周期律
- 格式:ppt
- 大小:264.00 KB
- 文档页数:20




《原子结构与元素周期表》说课稿尊敬的各位评委老师:大家好!今天我说课的题目是《原子结构与元素周期表》。
下面我将从教材分析、学情分析、教学目标、教学重难点、教学方法、教学过程以及教学反思这几个方面来展开我的说课。
一、教材分析《原子结构与元素周期表》是高中化学必修课程中非常重要的内容,它不仅是化学学科的基础,也是后续学习元素化合物、化学反应原理等知识的重要基石。
在教材的编排上,这部分内容先介绍了原子的结构,包括原子的组成、核外电子的排布等,然后在此基础上引入元素周期表,阐述了元素周期表的结构、周期和族的划分以及元素周期律等内容。
通过这部分内容的学习,学生能够从微观结构的角度理解元素的性质和元素之间的关系,建立起结构决定性质的化学思维。
二、学情分析对于高中学生来说,他们在初中已经初步了解了原子的构成以及元素周期表的简单知识,但对于原子结构的微观层面以及元素周期表的内在规律理解还不够深入。
这个阶段的学生具备一定的逻辑思维能力和抽象思维能力,但在理解较为抽象的概念和原理时可能会遇到困难。
因此,在教学中需要通过直观的模型、生动的示例以及适当的引导,帮助学生突破难点,掌握重点。
三、教学目标1、知识与技能目标(1)了解原子的结构,包括原子核、质子、中子、电子的关系,掌握核外电子的排布规律。
(2)理解元素周期表的结构,包括周期、族的划分以及元素周期表与原子结构的关系。
(3)能够运用原子结构和元素周期表的知识解释元素的性质。
2、过程与方法目标(1)通过对原子结构和元素周期表的学习,培养学生的观察能力、分析能力和归纳总结能力。
(2)通过探究活动,培养学生的科学探究精神和创新思维。
3、情感态度与价值观目标(1)让学生感受化学世界的奇妙,激发学生学习化学的兴趣。
(2)培养学生的辩证唯物主义观点,认识事物的发展是有规律可循的。
四、教学重难点1、教学重点(1)原子的结构及核外电子的排布规律。
(2)元素周期表的结构及元素周期律。

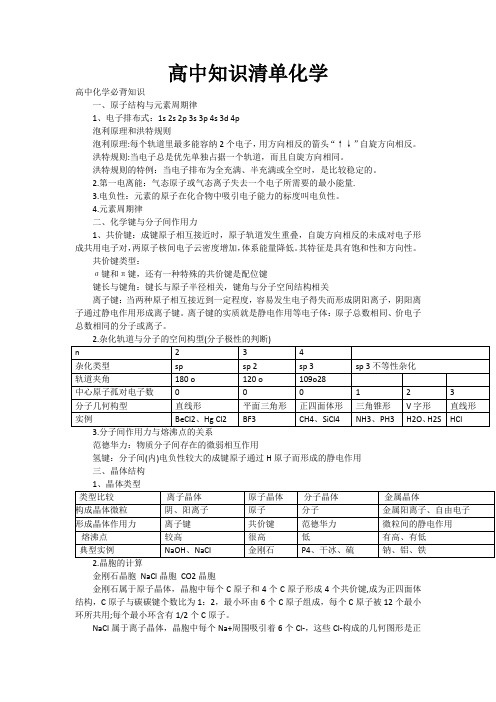
高中知识清单化学高中化学必背知识一、原子结构与元素周期律1、电子排布式:1s 2s 2p 3s 3p 4s 3d 4p泡利原理和洪特规则泡利原理:每个轨道里最多能容纳2个电子,用方向相反的箭头“↑↓”自旋方向相反。
洪特规则:当电子总是优先单独占据一个轨道,而且自旋方向相同。
洪特规则的特例:当电子排布为全充满、半充满或全空时,是比较稳定的。
2.第一电离能:气态原子或气态离子失去一个电子所需要的最小能量.3.电负性:元素的原子在化合物中吸引电子能力的标度叫电负性。
4.元素周期律二、化学键与分子间作用力1、共价键:成键原子相互接近时,原子轨道发生重叠,自旋方向相反的未成对电子形成共用电子对,两原子核间电子云密度增加,体系能量降低。
其特征是具有饱和性和方向性。
共价键类型:σ键和π键,还有一种特殊的共价键是配位键键长与键角:键长与原子半径相关,键角与分子空间结构相关离子键:当两种原子相互接近到一定程度,容易发生电子得失而形成阴阳离子,阴阳离子通过静电作用形成离子键。
离子键的实质就是静电作用等电子体:原子总数相同、价电子总数相同的分子或离子。
范德华力:物质分子间存在的微弱相互作用氢键:分子间(内)电负性较大的成键原子通过H原子而形成的静电作用三、晶体结构2.晶胞的计算金刚石晶胞NaCl晶胞CO2晶胞金刚石属于原子晶体,晶胞中每个C原子和4个C原子形成4个共价键,成为正四面体结构,C原子与碳碳键个数比为1:2,最小环由6个C原子组成,每个C原子被12个最小环所共用;每个最小环含有1/2个C原子。
NaCl属于离子晶体,晶胞中每个Na+周围吸引着6个Cl-,这些Cl-构成的几何图形是正八面体,每个Cl-周围吸引着6个Na+,Na+、Cl-个数比为1:1,每个Na+与12个Na+等距离相邻,每个氯化钠晶胞含有4个Na+和4个Cl-。
干冰属于分子晶体。
晶胞中每个CO2分子周围最近且等距离的CO2有12个。
1个晶胞中含有4个CO2金属晶体:金属Na、K、Cr、Mo(钼)、W等中金属原子堆积方式是体心立方堆积,原子的`配位数为8,一个晶胞中含有2个原子。
原子结构与元素周期律的深入理解原子结构与元素周期律是化学领域中两个基础概念,对于理解化学现象和性质具有重要的意义。
本文将从原子结构和元素周期律的角度对这两个概念进行深入理解和探讨。
一、原子结构的基本组成原子结构的基本组成由原子核和电子云两部分构成。
原子核位于原子的中心,由质子和中子组成。
质子带有正电荷,中子不带电荷。
电子云则包围着原子核,其中电子带有负电荷。
原子核中的质子数量决定了原子的原子序数,也即元素的周期表位置。
中子的数量可以变化,称为同位素。
电子的数量则与质子数量相等,保持了原子整体电荷的中性。
二、电子的能级和轨道电子云可以分为不同能级,每个能级可以容纳一定数量的电子。
在基态下,电子首先填充低能级,然后逐渐填充高能级。
根据能级理论,第一能级最低,依次为第二、第三能级等等。
每个能级又可进一步细分为不同的轨道。
最常见的是s、p、d和f轨道。
s轨道是最基础的轨道,可以容纳最多两个电子。
p轨道可以容纳最多六个电子,分为三个组合,即px、py和pz。
d轨道可以容纳最多十个电子,分为五个组合,而f轨道可以容纳最多十四个电子,分为七个组合。
三、电子的填充规则根据泡利不相容原理,即每个轨道最多只能容纳两个电子,并且电子的自旋方向相反。
在填充电子时,按照能级由低到高的顺序填充。
在同一能级下,先填充s轨道,再填充p轨道,依次类推。
四、元素周期表的构成与特点元素周期表是根据原子的原子序数和性质将元素有序地排列而成的表格。
根据周期表的特点,我们可以发现以下规律:1. 周期性规律:元素周期表中,横向排列的行称为“周期”,纵向排列的列称为“族”。
元素周期性地重复出现在周期表中。
这意味着具有相似化学性质的元素往往出现在同一族中。
例如,第一周期中的元素都是最简单的元素,而第二周期中的元素具有相似的化学性质。
2. 周期性趋势:在周期表中,原子序数逐渐增加,而元素的性质也呈现出周期性的变化。
这些性质包括原子半径、离子半径、电离能和电负性等。
化学原子结构与周期性定律化学原子结构与周期性定律是化学中的重要知识点,涉及到原子的基本组成、原子结构的排布以及元素周期表的构成。
以下是关于这一知识点的详细介绍:1.原子结构–原子核:由质子和中子组成,质子带正电,中子不带电。
–电子:围绕原子核运动的粒子,带负电。
–原子序数:原子核中质子的数量,也是元素在周期表中的序号。
–相对原子质量:原子核中质子和中子的总数,是元素的平均质量。
2.电子排布–能级:电子可能存在的不同能量状态。
–轨道:电子在原子核外空间运动的路径。
–电子层:具有相同能量的电子集合。
–电子亚层:电子层内能量相同的电子集合。
–洪特规则:电子在相同能级、相同亚层的轨道上,优先单独占据一个轨道,且自旋方向相同。
3.元素周期表–周期:周期表中的水平行,每个周期代表一个主能级的电子层。
–族(列):周期表中的垂直列,同一族元素具有相同的外层电子数。
–主族元素:周期表中1A到8A族元素,外层电子数为1到8个。
–过渡元素:周期表中3B到12B族元素,具有不完全填充的d 轨道。
–镧系元素:周期表中14B族元素,具有不完全填充的f轨道。
4.周期性定律–原子半径的周期性变化:同周期自左向右原子半径逐渐减小,同族自上向下原子半径逐渐增大。
–元素电负性的周期性变化:同周期自左向右电负性逐渐增大,同族自上向下电负性逐渐减小。
–金属性和非金属性的周期性变化:同周期自左向右金属性逐渐减弱,非金属性逐渐增强,同族自上向下金属性逐渐增强,非金属性逐渐减弱。
–化合价的周期性变化:同周期元素的最高化合价逐渐增大,同族元素的最高化合价相同。
以上是关于化学原子结构与周期性定律的知识点介绍,希望对你有所帮助。
习题及方法:1.习题:已知氢原子的核外电子数为2,写出其电子排布式。
–氢原子的核外电子数为2,根据电子排布规则,1s轨道最多容纳2个电子,因此氢原子的电子排布式为1s²。
2.习题:氧气分子的电子排布式为什么是1s²2s²2p⁴?–氧气分子O₂由两个氧原子组成,每个氧原子的电子排布式为1s²2s²2p⁴。
原子结构元素周期律原子结构和元素周期律是物质世界中最基本的概念之一、原子是构成物质的基本单位,在原子结构中包含了质子、中子和电子等多个组成要素。
元素周期律则是根据原子结构的特点和规律对元素进行分类和排列的一种方法。
下面将详细介绍原子结构和元素周期律的相关知识。
首先,我们来介绍一下原子的基本结构。
原子由原子核和围绕原子核运动的电子构成。
原子核是原子的中心部分,包含了质子和中子。
质子带有正电荷,中子没有电荷。
而电子则带有负电荷,围绕原子核中的质子和中子进行运动。
质子和中子的质量几乎相同,约为1.67x10^-27千克,而电子的质量则非常轻,约为9.11x10^-31千克。
原子的质量数等于质子数加中子数。
而原子的电荷数等于质子数减去电子数。
由于质子和电子的数目相等,所以正常情况下原子是电中性的。
但是,当原子失去或获得电子时,就会形成带电离子。
质子和中子分别位于原子核的核心部分,而电子则通过能级来描述它们在原子核周围的运动状态。
能级是指电子在原子内的一定区域内具有一定能量的状态。
能级从内到外按照顺序排列,依次称为K层、L层、M层等。
每个能级又分为不同的轨道,轨道是指电子在能级内运动的一条轨道,常用字母s、p、d、f来表示。
每个能级中的电子数是有限的,第一层K层最多容纳2个电子,第二层L层最多容纳8个电子,以此类推。
接下来我们来讨论元素周期律。
元素周期律是指把元素按照一定的规律排列的表格,以便更好地了解元素的性质和规律。
元素周期表是根据元素的原子序数(即原子核内质子的数目)将元素排列的表格。
这个表格通常显示元素的原子序数、符号和原子质量。
元素周期表中的元素按照周期和族进行排列。
周期是指元素按照原子结构的性质和规律重复出现的一行,一共有七个周期。
族是指元素按照化学性质的相似性分为的一列,一共有十八个族。
元素周期表的左边是金属元素,右边是非金属元素,左上方的位置是金属元素,右上方位置是半金属元素,左下方位置是非金属元素。