现分-第2章 光学分析法导论
- 格式:ppt
- 大小:695.50 KB
- 文档页数:28




第二章光学分析法导论一、选择题1.电磁辐射的粒子性主要表现在哪些方面()A.能量B.频率C.波长D.波数2.当辐射从一种介质传播到另一种介质时,下列哪种参量不变()A.波长B.速度C.频率D.方向3.电磁辐射的二象性是指()A.电磁辐射是由电矢量和磁矢量组成B.电磁辐射具有波动性和电磁性C.电磁辐射具有微粒性和光电效应D.电磁辐射具有波动性和粒子性4.可见光区、紫外区、红外光区、无线电波四个电磁波区域中,能量最大和最小的区域分别为()A.紫外区和无线电波区B.可见光区和无线电波区C.紫外区和红外区D.波数越大5.有机化合物成键电子的能级间隔越小,受激跃迁时吸收电磁辐射的()A.能量越大B.频率越高C.波长越长D.波数越大6.波长为的电磁辐射的能量是()A.B.C.124eV D.1240 eV7.受激物质从高能态回到低能态时,如果以光辐射形式辐射多余的能量,这种现象称为()A.光的吸收B.光的发射C.光的散射D.光的衍射8.利用光栅的()作用,可以进行色散分光。
A.散射B.衍射和干涉C.折射D.发射9.棱镜是利用其()来分光的。
A.散射作用B.衍射作用C.折射作用D.旋光作用10.光谱分析仪通常由以下()四个基本部分组成。
A.光源、样品池、检测器、计算机B.信息发生系统、色散系统、检测系统、信息处理系统C.激发源、样品池、光电二级管、显示系统D.光源、棱镜、光栅、光电池1.不同波长的光具有不同的能量,波长越长,频率、波数越(),能量越();反之,波长越短,能量越()。
2.在光谱分析中,常常采用色散元件获得()来作为分析手段。
3.物质对光的折射率随着光的频率变化而变化,这中现象称为()。
4.吸收光谱按其产生的本质分为()、()、()等。
5.由于原子没有振动和转动能级,因此原子光谱的产生主要是()所致。
6.当光与物质作用时,某些频率的光被物质选择性的吸收并使其强度减弱的现象,称为(),此时,物质中的分子或原子由()状态跃迁到()的状态。



第2章光学分析法导论光学分析法是一种常用的分析方法,广泛应用于材料科学、化学、生物、医学等领域。
在分析过程中,通过光的吸收、散射、反射等性质来获得样品的信息。
本章将介绍光学分析法的基本原理和常见的应用。
1.光学分析法原理光学分析法是利用光与物质相互作用来获得样品信息的方法。
其中最基本的原理是光的吸收、散射和发射。
当光通过物质时,会与物质的分子或原子发生相互作用,导致光的振动矢量和频率发生改变。
通过测量光的吸收、散射或发射,可以得到物质的各种信息。
2.光的吸收法光的吸收法是通过测量物质对特定波长光的吸收来确定样品中其中一种物质的含量。
该方法常用于分析有机化合物和无机物中的金属离子含量。
测量方法包括光度法、比色法、比较法等。
其中最常见的是光度法,即通过测量光的强度来确定样品中物质的含量。
在实际应用中,可以根据吸收光谱图来确定样品中各种物质的含量和种类。
3.光的发射法光的发射法是通过测量样品发光的强度来确定样品的成分和性质。
发射光谱的特点是样品发射出符合波长的光,通常用于分析无机化合物中的金属元素。
常用的方法包括原子发射光谱法和荧光光谱法。
其中原子发射光谱法是在样品被激发时,各种金属元素自发射出特定波长的光,通过测量光的强度来确定金属元素的含量。
荧光光谱法则是通过将样品激发到荧光状态,然后测量样品散射出的荧光光强度来确定样品的成分和性质。
4.光的散射法光的散射法是通过测量光的散射强度来确定样品的成分和性质。
散射光谱的特点是样品散射出具有不同波长的光,通常用于分析颗粒物质的大小、浓度和形状等。
常用的方法包括拉曼光谱法和动态光散射法。
拉曼光谱法是通过测量样品散射光中与入射光具有不同频率和振幅的拉曼散射光来确定样品的成分。
动态光散射法则是通过测量样品散射光的强度和角度分布来估算样品颗粒的大小和浓度。
5.光学分析法的应用光学分析法在各个领域都有广泛的应用。
在材料科学中,可以通过测量光的吸收、发射和散射来研究材料的光学性质、结构和相变等。



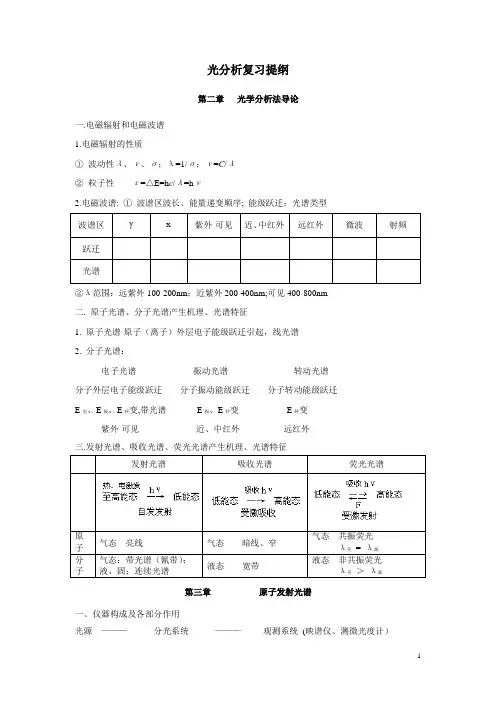
光分析复习提纲第二章光学分析法导论一.电磁辐射和电磁波谱1.电磁辐射的性质①波动性λ、ν、σ;λ=1/σ;ν=C/λ②粒子性ε=△E=h c/λ=hν2.电磁波谱: ①波谱区波长、能量递变顺序; 能级跃迁;光谱类型②λ范围:远紫外100-200nm;近紫外200-400nm;可见400-800nm二. 原子光谱、分子光谱产生机理、光谱特征1. 原子光谱-原子(离子)外层电子能级跃迁引起,线光谱2. 分子光谱:电子光谱振动光谱转动光谱分子外层电子能级跃迁分子振动能级跃迁分子转动能级跃迁E电、、E振、、E转变,带光谱E振、E转变E转变紫外-可见近、中红外远红外三.发射光谱、吸收光谱、荧光光谱产生机理、光谱特征第三章原子发射光谱一、仪器构成及各部分作用光源———分光系统———观测系统(映谱仪、测微光度计)(一)光源 1.光源的作用2.经典光源种类、特点、应用火焰、直流电弧、交流电弧、高压火花比较(p28表3-1): 从电极温度、灵敏度、电弧温度、稳定性、样品状态几方面比较 3.ICP 光源特点4. 光源选择(二)分光系统 分光元件:棱镜和光栅1.光学特性:线色散率、分辨率定义、物理意义及计算线色散率:dL/d λ mm/nm 倒线色散率:d λ/ dL nm/mm 光栅dL/d λ= k f / (d cos β)分辨率: R=λ/△λ 光栅R=NK 2. 棱镜及光栅的分光原理光栅方程式:d (sin α±sin β)=K λ 意义及计算 3. 光栅闪耀光栅 当α=β=θ时, K λβ= 2d sin βλβ= 2d sin β/K ——闪耀波长闪耀光栅适用波长范围:谱线距离、谱片摄取波长数、光谱重叠计算(三) 观测系统1. 感光板结构,黑度、曝光量定义,乳剂特性曲线 黑度S = lg 1/T 曝光量 H = kI t BC 曝光正常S = tg α(lgH-lgH i )=γlg kI t - i Hi ——惰延量 tg α=γ——反衬度定量: γ高, 紫外Ⅰ型;定性: Hi小, 紫外Ⅱ型(灵敏度高)2.光电倍增管作用二、光谱定性分析1. 原理及依据△E=hc/λ=hν2. 灵敏线、共振线、最后线、分析线定义及相互关系:最灵敏线=?第一共振线=最后线(低含量、高含量)3. 光谱定性分析方法、过程光谱定性分析方法:标准样品比较法、元素标准光谱图法(铁光谱比较法)三、光谱半定量分析:1. 谱线黑度比较法(目视强度比较法)依据:谱线强度随待测元素含量增加而增加2. 谱线呈现法依据:谱线条数和强度随待测元素含量增加而增加四、光谱定量分析三公式一曲线1. 罗马金公式:I=αC b a? b? 为什么不能直接用于定量分析?2. 内标法原理-公式及推导:lgR = lgA + b lg C A为何是常数?3. 摄谱法光谱定量分析基本关系式—三标准试样法基本公式(曝光正常)△S = S1 – S2 =γlg I1/ I2 = γlg R = γ b lg C+γlg A第四章原子吸收光谱法一、基本原理1. 波兹曼分布定理: N j / N0 = g j /g0. e -E i / kT①温度对N i和N0的影响: T↑,N i↑,N0↓;②T对N i的影响程度》对N0的影响程度③AAS和AES比较:灵敏度、准确度、选择性、适用性2. 谱线轮廓和变宽原因①朗伯定律Iν=I 0ν. e - kνL②吸收曲线Kν~ν,三参数ν0、K0、△ν10-3~10-2 nm。
第二章光学分析法导论1. 已知1电子伏特=1. 602×10-19J,试计算下列辐射波长的频率(以兆赫为单位),波数(以cm-1为单位)及每个光子的能量(以电子伏特为单位):(1)波长为900pm的单色X射线;(2)589.0nm的钠D线;(3)12.6µm的红外吸收峰;(4)波长为200cm的微波辐射。
解:已知1eV=1.602×10-19J, h=6.626×10-34J·s, c=3.0×108m·s-1①λ=900pm的X射线Hz,即3.333×1011MHzcm-1J用eV表示,则eV②589.0nm的钠D线Hz,即5.093×108MHzcm-1J用eV表示,则eV③12.6µm的红外吸收峰Hz,即2.381×107MHzcm-1J用eV表示,则eV④波长为200cm的微波辐射Hz,即1.50×102MHzcm-1J用eV表示,则eV2. 一个体系包含三个能级,如果这三个能级的统计权重相同,体系在300K温度下达到平衡时,试计算在各能级上的相对分布(N i/N).能级的相对能量如下。
(1) 0eV,0.001eV,0.02eV;(2) 0eV,0.01eV,0.2eV;(3) 0eV,0.1eV, 2eV。
解:已知T=300K, k=1.380×10-23J·K-1=8.614×10-5eV·K-1,kT=8.614×10-5×300=0.0258eV①E0=0eV, E1=0.001eV, E2=0.02eV②E0=0eV, E1=0.01eV, E2=0.2eV③E0=0eV, E1=01eV, E2=2eV3. 简述下列术语的含义电磁辐射电磁波谱发射光谱吸收光谱荧光光谱原子光谱分子光谱自发发射受激发射受激吸收电致发光光致发光化学发光热发光电磁辐射――电磁辐射是一种以巨大速度通过空间传播的光量子流,它即有波动性,又具有粒子性.电磁波谱――将电磁辐射按波长顺序排列,便得到电子波谱.电子波谱无确定的上下限,实际上它包括了波长或能量的无限范围.发射光谱――原来处于激发态的粒子回到低能级或基态时,往往会发射电磁辐射,这样产生的光谱为发射光谱.吸收光谱――物质对辐射选择性吸收而得到的原子或分子光谱称为吸收光谱.荧光光谱――在某些情形下,激发态原子或分子可能先通过无辐射跃迁过渡到较低激发态,然后再以辐射跃迁的形式过渡到基态,或者直接以辐射跃迁的形式过渡到基态。