氧、硫及其重要化合物
- 格式:pptx
- 大小:2.33 MB
- 文档页数:58
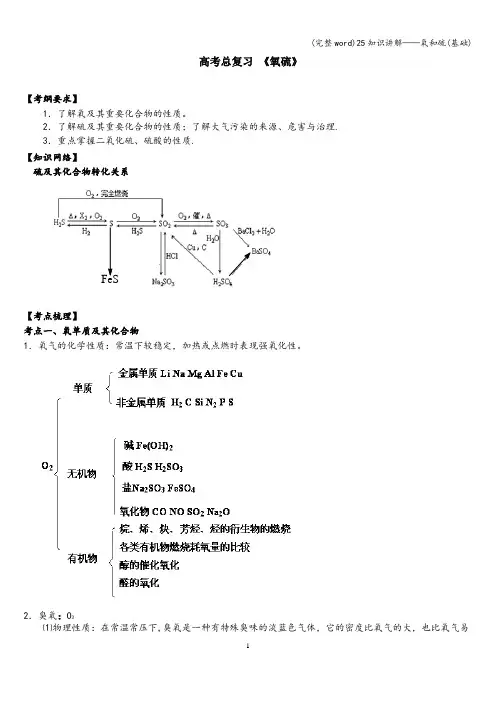
高考总复习《氧硫》【考纲要求】1.了解氧及其重要化合物的性质。
2.了解硫及其重要化合物的性质;了解大气污染的来源、危害与治理.3.重点掌握二氧化硫、硫酸的性质.【知识网络】硫及其化合物转化关系FeS【考点梳理】考点一、氧单质及其化合物1.氧气的化学性质:常温下较稳定,加热或点燃时表现强氧化性。
2.臭氧:O3⑴物理性质:在常温常压下,臭氧是一种有特殊臭味的淡蓝色气体,它的密度比氧气的大,也比氧气易溶于水.液态臭氧呈深蓝色,沸点为—112.4℃,固体臭氧呈紫黑色,熔点为—251℃。
⑵化学性质及用途:臭氧的化学性质比氧气活泼.①不稳定性:2O3=3O2;但在空气中高压放电就能产生臭氧:3O2放电2O3②强氧化性:Ag、Hg等金属在空气或氧气中不易被氧化,但可以被臭氧氧化。
也可使湿润的淀粉-KI试纸变蓝:2KI+O3+H2O=I2+O2+2KOH③用途:臭氧是一种很好的漂白剂和消毒剂.空气中的微量O3,能刺激中枢神经加快血液循环,令人产生爽快的感觉但当空气中臭氧的含量超过10—5%(体积分数)时,就会对人体、动植物以及暴露空气中的物质造成危害,臭氧可以吸收来自太阳的大部分紫外线,是人类和生物的保护伞。
近年来,臭氧层受到氟氯烃等气体的破坏,形成“臭氧空洞”,危害地球环境,各国应采取共同行动保护,氧层,维护人类和生物的生存环境。
3.过氧化氢(H2O2)(1)结构化学式:H2O2电子式:结构式: H-O-O-H(2)物理性质无色粘稠液体,它的水溶液俗称双氧水,呈弱酸性。
(3)化学性质H2O2,氧元素的化合价为中间价态(—1),即有氧化性又有还原性。
氧化性:H2O2+H2S=S↓+2H2O还原性:2KMnO4+5H2O2+3H2SO4=K2SO4+2MnSO4+5O2↑+8H2O自身氧化-还原:(实验室用此法代替KClO3分解制氧气),家庭中的“氧立得”使用时中间产物就有过氧化氢.4.H2O(1)H2O做氧化剂2Na+2H2O=2NaOH+H2↑(2)H2O做还原剂2F2+2H2O=4HF+O2(3)H2O既不做氧化剂又不做还原剂2Na2O2+2H2O=4NaOH+O2↑Cl2+H2O=HCl+HClO3NO2+H2O=2HNO3+NO(4)H2O既做氧化剂又做还原剂2H2O电解2H2+O2↑考点二、硫及其氧化物1.硫:(1)物理性质:硫为黄色晶体,不溶于水,微溶于酒精,易溶于CS2。
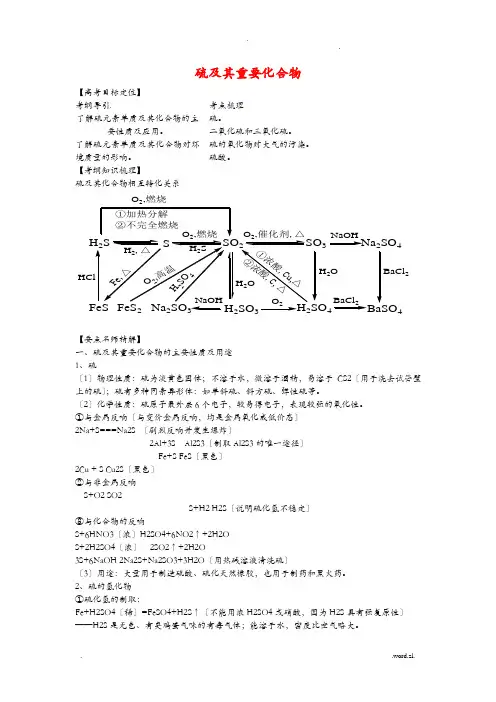
硫及其重要化合物【高考目标定位】 考纲导引考点梳理 了解硫元素单质及其化合物的主要性质及应用。
了解硫元素单质及其化合物对环境质量的影响。
硫。
二氧化硫和三氧化硫。
硫的氧化物对大气的污染。
硫酸。
【考纲知识梳理】硫及其化合物相互转化关系H 2SSSO 23Na SO 4223H 22SO 4HClH 2,△O 2,燃烧H 2SO ,燃烧①加热分解②不完全燃烧2NaOHO 2BaCl 2H 2OBaCl 2①浓酸,C u ,△②浓酸,C, △H 2OH2S O4O2,高温F e ,△【要点名师精解】一、硫及其重要化合物的主要性质及用途 1、硫〔1〕物理性质:硫为淡黄色固体;不溶于水,微溶于酒精,易溶于CS2〔用于洗去试管壁上的硫〕;硫有多种同素异形体:如单斜硫、斜方硫、弹性硫等。
〔2〕化学性质:硫原子最外层6个电子,较易得电子,表现较强的氧化性。
①与金属反响〔与变价金属反响,均是金属氧化成低价态〕 2Na+S===Na2S 〔剧烈反响并发生爆炸〕2Al+3S Al2S3〔制取Al2S3的唯一途径〕 Fe+S FeS 〔黑色〕 2Cu + S Cu2S 〔黑色〕 ②与非金属反响 S+O2 SO2S+H2 H2S 〔说明硫化氢不稳定〕 ③与化合物的反响S+6HNO3〔浓〕H2SO4+6NO2↑+2H2O S+2H2SO4〔浓〕 2SO2↑+2H2O3S+6NaOH 2Na2S+Na2SO3+3H2O 〔用热碱溶液清洗硫〕〔3〕用途:大量用于制造硫酸、硫化天然橡胶,也用于制药和黑火药。
2、硫的氢化物 ①硫化氢的制取:Fe+H2SO4〔稀〕=FeSO4+H2S ↑〔不能用浓H2SO4或硝酸,因为H2S 具有强复原性〕 ——H2S 是无色、有臭鸡蛋气味的有毒气体;能溶于水,密度比空气略大。
②硫化氢的化学性质 A .可燃性:当22/O S H n n ≥2/1时,2H2S+O2 2S+2H2O 〔H2S 过量〕当22/O S H n n ≤2/3时,2H2S+3O22SO2+2H2O 〔O2过量〕当23222<<O S H n n 时,两种反响物全部反响完,而产物既有硫又有SO2B .强复原性:常见氧化剂Cl2、Br2、Fe3+、HNO3、KMnO4等,甚至SO2均可将H2S 氧化。

氧、硫及其化合物一、氧及其化合物1.臭氧(1)与O2互为同素异形体:(2)臭氧化学性质:①极强氧化性:使润湿的淀粉KI试纸变蓝(方程式)_____________________②漂白和消毒(3)臭氧层2.H2O2(1)结构:电子式______________,结构式____________,化学键类型____________ (2)化学性质:①氧化性:I-(H+)、Fe2+(H+)、酸性条件下溶解Cu应用:杀菌消毒、漂白(讨论含酚酞的NaOH溶液)②还原性:与KMnO4(H+)反应③不稳定性:应用:实验室制氧气方法3.H2O的作用(1)氧化性:Na、Mg、Fe、C(反应条件)(2)还原性:(3)既有氧化性又有还原性:(4)既不显氧化性又不显还原性:Cl2+H2O、NO2+H2O、Na2O2+H2O等水解(盐、CaC2、卤代烃、酯、多糖)二、硫及其化合物1.硫元素的特点——多变价(-2;0;+4;+6)2.硫单质(1)物理性质(2)化学性质①弱氧化性:可氧化金属(Na、Fe、Cu、Ag、Hg等);H2②还原性:O2SO2的化学性质小结__________________________________。
SO2的实验室制备__________________________________________。
工业制法_______________________________________________。
几种漂白剂的比较:思考:SO2能使溴水、KMnO4溶液褪色与SO2使品红褪色,实质相同吗?4.三氧化硫5.硫酸(1)物理性质:浓硫酸稀释:(2)浓硫酸特性:①吸水性:干燥剂思考:浓硫酸做干燥剂可以干燥的气体_______________________________________;不能用来干燥____________________________气体。
②脱水性:属化学变化③强氧化性:钝化;Cu;C;浓硫酸与铜反应的方程式及现象:浓硫酸与碳反应的方程式:碳和浓硫酸反应产物的验证实验各试剂的作用_________________________________________________。



一、硫及其重要化合物的主要性质及用途1、硫(1)物理性质:硫为 固体; 溶于水,微溶于酒精,易溶于CS 2(用于洗去试管壁上的硫);硫有多种同素异形体:如单斜硫、斜方硫、弹性硫等。
硫在元素周期表中的位置硫原子结构示意图 硫离子结构示意图 (2)化学性质:硫原子最外层 个电子,较易 电子,表现较强的 。
①与金属反应(与变价金属反应,均把金属氧化成低价态,如Na 、Al 、Fe 、Cu ) (剧烈反应并发生爆炸)(制取Al 2S 3的唯一途径) (色)( 色)②与非金属反应(O 2、H 2)、 (说明硫化氢不稳定) ③与化合物的反应S + HNO 3(浓)= S + H 2SO 4(浓)= S + NaOH = (用热碱溶液清洗硫) (3)用途:大量用于制造硫酸、硫化天然橡胶,也用于制药和黑火药。
2、硫的氢化物①硫化氢——H 2S 是无色、有 气味的有毒气体; 溶于水,密度比空气略 。
②硫化氢的化学性质A .可燃性:当22/O S H n n ≥2/1时, (H 2S 过量) 当22/O S H n n ≤2/3时, (O 2过量) 当23222<<O SH n n 时,两种反应物全部反应完,而产物既有硫又有SO 2 B .强还原性:常见氧化剂Cl 2、Br 2、I 2、Fe 3+、HNO 3、浓H 2SO 4、KMnO 4等均可将H 2S 氧化。
C.不稳定性:300℃以上易受热分解③H2S的水溶液叫氢硫酸,是二元弱酸。
电离方程式氢硫酸在空气中放置变浑浊,方程式④实验室制法:化学方程式:FeS+2H+===Fe2++H2S↑(稀HCl 、稀H2SO4)不用浓硫酸、浓盐酸制H2S的原因浓H2SO4有强氧化性,能氧化H2S;浓盐酸有挥发性,使产生的H2S气体中混有HCl气体。
⑤不溶于水也不溶于稀酸的金属硫化物有CuS(黑)、Ag2S(黑)、PbS(黑)它们可溶于浓硝酸。
所以CuSO4、Pb(NO3)2可以与H2S反应生成沉淀:Pb(NO3)2+H2S===PbS↓+2HNO3。

高一氧硫及其化合物知识点一、氧化还原反应氧硫化物是由氧和硫的化合物组成。
在这些化合物中,氧与硫的氧化态是随着元素的化合形式而变化的。
氧的氧化态通常为-2,但在氧硫化物中,其氧化态会发生变化。
氧化还原反应是指化学反应中,物质的氧化态发生改变的过程。
当氧化剂得到电子并接受电通的时候,其氧化态会发生增加,而还原剂则会失去电子,其氧化态会减少。
二、高一氧硫的性质与应用1. 氧气氧气在化学反应中是一种重要的氧化剂。
它能与其他元素或化合物反应,使其氧化。
同时,氧气也是生物体呼吸过程中的必需物质。
2. 二氧化硫二氧化硫是一种无色气体,有刺激性气味。
它是高一氧硫化合物中常见的一种,也是被广泛应用的化合物之一。
二氧化硫的主要应用领域包括:- 工业:二氧化硫是制造硫酸的重要原料,广泛用于生产纸张、塑料、农药等产品。
- 食品:二氧化硫是一种食品添加剂,常被用于保鲜果蔬,防止其变色和腐烂。
- 环境保护:作为一种污染物,二氧化硫对环境有害。
因此,在燃煤和工业废气处理中,需要对二氧化硫进行净化处理,以减少其对大气的污染。
3. 三氧化硫三氧化硫是一种无色晶体,在空气中不稳定,会与水和氧反应。
它的主要应用是制造硫酸。
三氧化硫的制备方法包括:硫在高温下与氧反应,通过催化剂促使这个反应快速进行。
4. 亚硫酸亚硫酸是一种无色气体,呈强酸性,有刺激性气味。
它在一些化学反应中起着重要的作用。
亚硫酸的主要应用包括:- 漂白:亚硫酸是一种常用的漂白剂,广泛用于纺织品、纸张等行业。
- 消毒:亚硫酸也可以用于消毒,如清洁和消毒水。
- 食品加工:亚硫酸是一种食品添加剂,可用于保鲜、防腐和抗氧化。
5. 硫酸硫酸是一种无色液体,具有强酸性。
它是一种重要的化学品,广泛应用于各种工业中。
硫酸的主要应用领域包括:- 化肥:硫酸是制造化肥的重要原料,如硫酸铵、硫酸钾等。
- 汽车电池:硫酸被用作蓄电池中的电解液。
- 腐蚀剂:硫酸在工业中也用作腐蚀剂,用于清洗金属表面。


非金属元素及其化合物最常见的非金属元素包括氧、碳、氮、硫、磷、氯、氢和硅等。
以下分别介绍一些常见的非金属元素及其化合物。
氧(O)是地球上最丰富的元素之一,占地壳质量的49.2%。
在化合物中,氧通常以氧分子(O2)的形式存在,是支持生命的必需气体。
氧气是我们呼吸过程中吸入的气体,同时还参与燃烧反应。
氧与许多元素的化合物被称为氧化物。
碳(C)是生命中最重要的元素之一、它是有机化合物的基础,包括脂肪、蛋白质和碳水化合物等。
除了形成分子间键,碳还能形成与其他元素共价的键,形成无限多的化合物。
例如,二氧化碳(CO2)是一种重要的气体,它参与光合作用和呼吸过程。
氮(N)是氨基酸和核酸等生物分子的关键组成部分。
氮既形成氨分子(NH3)也形成亚硝酸(NO2)和亚硝酸盐等含氮化合物。
氮气(N2)是大气中的主要成分之一,氮气通过闪电、固氮细菌和工业生产过程等途径转化成可用的氮化合物。
硫(S)是一种黄色固体,在天然界中以硫矿石的形式存在。
硫通常以硫化物形式存在,如硫化氢(H2S)和二硫化碳(CS2)。
硫还参与形成许多其他化合物,如硫酸和亚硫酸。
磷(P)是DNA、RNA和ATP等核酸分子的重要组成部分。
磷与氧形成的磷酸盐在能量传递和储存的过程中起着重要作用。
在自然界中,磷主要以磷酸盐的形式存在,并广泛应用于农业肥料。
氯(Cl)是一种非金属卤素,在自然界中以氯化物的形式广泛存在。
氯被广泛应用于水处理、消毒和生产塑料等工业过程中。
氯还是盐酸(HCl)的组成部分。
氢(H)是宇宙中最丰富的元素,几乎在所有化合物中都有出现。
氢气(H2)是一种清洁的能源,并被广泛应用于燃料电池技术。
硅(Si)是地壳中的第二大成分,占地壳质量的27.7%。
硅是生命体中最常见的非金属元素之一,也是硅酸盐矿物的重要成分。
硅在电子行业中广泛应用于制造半导体材料。

硫及其重要化合物的性质和应用一、知识梳理1.硫(1)游离态:硫单质俗名硫黄,主要存在于火山口附近或地壳的岩层里。
(2)化合态:主要以金属硫化物和硫酸盐的形式存在,如硫铁矿(FeS 2)、黄铜矿(CuFeS 2)、石膏(CaSO 4·2H 2O)和芒硝(Na 2SO 4·10H 2O)等。
(3)物理性质:硫为淡黄色固体;不溶于水,微溶于酒精,易溶于CS 2(用于洗去试管壁上的硫);硫有多种同素异形体:如单斜硫、斜方硫、弹性硫等。
(4)化学性质:硫原子最外层6个电子,较易得电子,表现较强的氧化性。
①与金属反应(与变价金属反应,均是金属被氧化成低价态)2Na+SNa 2S (剧烈反应并发生爆炸) 2Al+3S Al 2S 3(制取Al 2S 3的唯一途径)Fe+S FeS (黑色) 2Cu + S Cu 2S (黑色) ②与非金属反应S+O 2 点燃SO 2 S+H 2 H 2S (说明硫化氢不稳定)③与化合物的反应S+6HNO 3(浓)H 2SO 4+6NO 2↑+2H 2O S+2H 2SO 4(浓)2SO 2↑+2H 2O 3S+6NaOH2Na 2S+Na 2SO 3+3H 2O (用热碱溶液清洗硫)(5)用途:大量用于制造硫酸、硫化天然橡胶,也用于制药和黑火药。
2、硫的氢化物 (1)硫化氢的制取Fe+H 2SO 4(稀)FeSO 4+H 2S↑(不能用浓H 2SO 4或硝酸,因为H 2S 具有强还原性)——H 2S 是无色、有臭鸡蛋气味的有毒气体;能溶于水,密度比空气略大。
(2)硫化氢的化学性质A .可燃性:当22(H S)(O )21n n 时,2H 2S+O 2 点燃2S+2H 2O (H 2S 过量)当22(H S)(O )23n n ≤时,2H 2S+3O 2 点燃2SO 2+2H 2O (O 2过量) 当22(H S)(O )223n n 〈〈时,两种反应物全部反应完,而产物既有S 又有SO 2 B .强还原性:常见氧化剂Cl 2、Br 2、Fe 3+、HNO 3、KMnO 4等,甚至SO 2均可将H 2S 氧化。

硫元素及其化合物硫是一种非金属化学元素,化学符号S,原子序数16。
硫是氧族元素之一,属周期系VIA族,在元素周期表中位于第三周期。
相对原子质32.065。
通常单质硫是黄色的晶体,又称作硫磺。
硫单质的同素异形体有很多种,有斜方硫、单斜硫和弹性硫等。
硫元素在自然界中硫元素以硫化物、硫酸盐或单质硫形式存在。
硫是人体内蛋白质的重要组成元素,对人的生命活动具有重要意义。
硫主要用于肥料、火药、润滑剂、杀虫剂和抗真菌剂生产。
硫及含硫矿石燃烧生成的二氧化硫(S+O2==点燃==SO2)在空气中与水和氧结合形成亚硫酸,亚硫酸与空气中的氧气反应生成硫酸,从而造成硫酸型酸雨。
含量分布硫在自然界中分布较广,在地壳中含量为0.048%(按质量计)。
在自然界中硫的存在形式有游离态和化合态。
单质硫主要存在于火山周围的地域中。
以化合态存在的硫多为矿物,可分为硫化物矿和硫酸盐矿。
硫化物矿有黄铁矿(FeS2)、黄铜矿(CuFeS2)、方铅矿(PbS)、闪锌矿(ZnS)等。
硫酸盐矿有石膏(CaSO4·2H2O)、芒硝(Na2SO4·10H2O)、重晶石(BaSO4)、天青石(SrSO4)、矾石[(AlO)2SO4·9H2O]、明矾石[K2SO4·Al2(SO4)3·24H2O]等。
物理性质纯的硫呈浅黄色,质地柔软、轻,粉末有臭味。
硫不溶于水但溶于二硫化碳。
硫在所有的物态中(固态、液态和气态),硫都有不同的同素异形体,这些同素异形体的相互关系还没有被完全理解。
晶体的硫可以组成一个由八个原子组成的环:S8。
导热性和导电性都差。
性松脆,不溶于水。
无定形硫主要有弹性硫,是由熔态硫迅速倾倒在冰水中所得。
不稳定,可转变为晶状硫。
晶状硫能溶于有机溶剂如二硫化碳(而弹性硫只能部分溶解)、四氯化碳和苯。
化合价有4种,为-2(硫化氢)、+2(硫代硫酸钠)、+4(亚硫酸钠)和+6(硫酸)价。
第一电离能10.360电子伏特。
硫及硫的有关化合物知识点整理硫是一种常见的化学元素,其化学符号为S,原子序数为16,原子量为32.06 g/mol。
硫的原子结构是2s²2p⁶3s²3p⁴。
硫在自然界中以多种形式存在,如硫矿石、硫化物和酸等。
以下是硫及其化合物的一些重要知识点:1.硫的性质:-硫是一种黄绿色的非金属元素,具有特殊的气味。
-硫是一种固体,在常温下比较容易溶于有机溶剂。
-硫的熔点为115.21°C,沸点为444.67°C。
2.硫的化合物:-硫氧化物(SOx):硫和氧元素的化合物,包括二氧化硫(SO₂)和三氧化硫(SO₃)。
它们是大气中的主要污染物之一,也是酸雨的成分之一-硫化物(S²⁻):硫与其他元素形成的化合物,如硫化铁(FeS₂)和硫化氢(H₂S)。
硫化物具有特殊的气味,并且有着多种应用,如冶金、材料科学和生物化学等领域。
-硫酸盐(SO₄²⁻):硫酸(H₂SO₄)是硫酸盐的最常见形式之一、硫酸是一种重要的化学品,广泛用于工业生产和实验室中。
-硫醇(R-SH):硫与有机化合物形成的化合物,常见于蛋白质分子中。
硫醇具有特殊的气味,并且具有一些重要的生物活性。
3.硫和环境:-温室效应:硫气体和硫化物是温室气体之一,在大气中可以产生温室效应,对地球的气候变化产生一定影响。
4.硫的应用:-农业:硫是植物生长和发育所必需的微量元素之一、硫营养对植物的生长和产量具有重要影响,可通过施用硫肥来改善土壤中的硫含量。
-化学工业:硫及其化合物广泛应用于化学工业生产过程中,如制造硫酸、硫酸盐、硫醇、硫醚等重要化学品。
-燃料工业:硫是许多燃料中的主要成分之一,如煤炭和原油。
硫的含量会对燃料的质量和环境影响产生一定影响。
-药学:硫化物和硫代谢产物在药学中有重要的应用,如抗生素、抗癌药物和其他药物中的活性成分之一以上是硫及其化合物的一些重要知识点。
硫的化学性质及应用非常广泛,对环境和人类生活产生着重要影响。
1高中化学必修一3.1硫及其重要化合物-知识点1、黑火药中含有硫,纯净的硫一种黄色或淡黄色的固体,俗称硫黄。
硫很脆,容易研磨成粉末,不溶于水,微溶于酒精,易溶于二硫化碳。
2、硫的化学性质比较活泼,与氧气相似,容易与金属、其他非金属发生反应。
①硫与铁粉混合加热,S+Fe −→−∆ FeS ,②铜在硫蒸气中燃烧,S+2Cu −→−∆ Cu S ,③常温下硫与汞反应,S+Hg →HgS ,④硫在空气中燃烧,S+O 2 −−→−点燃SO 2,⑤硫与氢气加热生成硫化氢,S+H −→−∆H S 。
3、硫的常见化合态有:-2,+4,+6 ,硫的常见氧化物是SO 2和SO 3。
4、二氧化硫是无色、有刺激性气味的有毒气体,密度比空气大,易溶于水,通常情况下,1体积的水可溶解40 体积的二氧化硫。
溶于水的二氧化硫与水反应生成亚硫酸(不稳定的中强酸,易分解),是可逆反应,SO 2+H 2O ⇌H 2SO 3 。
5、二氧化硫有漂白作用,能漂白品红等有色物质。
它能与这些有色物质反应生成不稳定的无色物质,这种无色物质受热后容易分解,从而使有色物质恢复至原来的颜色。
(SO 2的漂白性是可逆的,但Cl 2的漂白性不可逆)。
二氧化硫还具有杀菌防腐作用,可用作食品加工的防腐剂。
6、SO 2是酸性氧化物,化学性质活泼。
①氧化性,SO +2H S →3S+2H O ;②还原性,2SO 2+O 2−−−−→←催化剂,加热2SO 3 。
将SO 2气体通入KIO 3淀粉溶液,溶液先变蓝后褪色,是因为KIO 3被SO 2还原成碘单质后,碘单质又继续被还原成碘离子。
7、SO 2与碱的反应类似于CO 2,SO 2不足时生成亚硫酸钙沉淀CaSO 3,SO 2过量时生成亚硫酸氢钙溶液Ca(HSO 3)2 。
8、SO 2与CO 2的鉴别。
SO 2:既能使品红溶液褪色,又能使澄清石灰水变浑浊;CO 2:不能使品红溶液褪色,但能使澄清石灰水变浑浊。
另外,SO 2具有还原性,而CO 2没有还原性,可用高锰酸钾溶液来除去CO 2气体中混有的SO 2。