鲎试剂灵敏度复核记录
- 格式:doc
- 大小:102.50 KB
- 文档页数:3


正文规范鲎试剂灵敏度复核的操作过程和要求,确保鲎试剂灵敏度复核结果的可靠性。
适用于质监处药理室对鲎试剂灵敏度的复核。
质监处药理室分析人员负责本规程的实施和完成相关记录。
USP版附录85;CP版附录Ⅺ E 。
细菌内毒素检查法:本法系利用从鲎的变形细胞中提取的试剂来检测或量化由革兰阴性菌产生的细菌内毒素,以判断供试品中细菌内毒素的含量是否符合规定的一种方法。
细菌内毒素的量用内毒素单位(EU)表示。
鲎试剂:是鲎变形细胞的溶出物经提取而成。
鲎试剂灵敏度:在本检查法规定的条件下能检测出内毒素标准溶液或供试品溶液中的最低内毒素浓度,用EU/ml表示。
细菌内毒素检查用水(BET水):系指与灵敏度为0.03EU/ml 或更高灵敏度的鲎试剂在37 1 C 条件下24小时不产生凝集反应的灭菌注射用水。
细菌内毒素标准品:USP细菌内毒素参考标准品(RSE)或已标定的细菌内毒素工作标准品(CSE)。
反应终点浓度:是指系列递减的内毒素浓度中最后一个呈现阳性结果的浓度。
一、试剂、材料与仪器设备试剂:鲎试剂批号、灵敏度、规格、生产商。
细菌内毒素检查用水(BET水) 批号、规格、生产商。
细菌内毒素标准品批号、效价、生产商。
材料及仪器设备:电热恒温水箱型号、设备编号。
电热鼓风干燥箱型号、设备编号。
漩涡混合器型号。
无热原试管规格:1075mm。
正文无热原玻璃瓶规格:25ml。
无热原玻璃吸管规格:1ml、2ml、5ml、10ml。
试管架、无热原封口膜、洗耳球、酒精棉球、砂轮片。
二、试验准备试验所用的容器、用具都必须经过处理,250C以上干烤至少1小时,以去除外源性内毒素。
试验操作过程应避免微生物的污染。
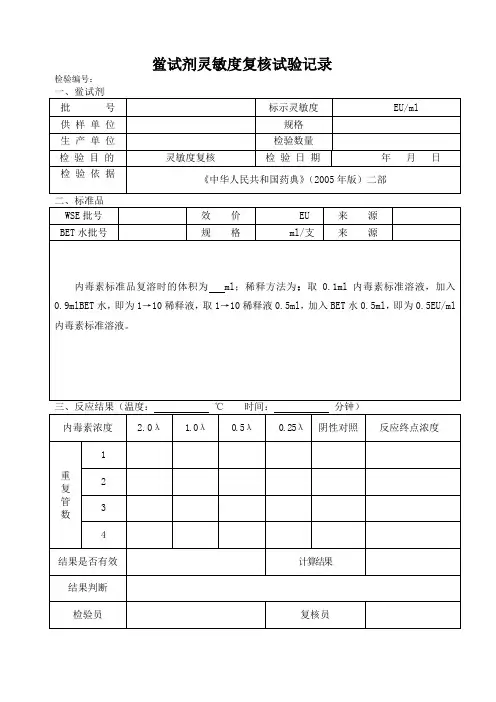
三、内毒素溶液配制细菌内毒素标准品系列溶液配制取RSE或CSE 1瓶,按照使用说明书加入规定量的细菌内毒素检查用水使溶,并用漩涡混合器间歇混匀30分钟,然后用细菌内毒素检查用水进一步稀释至2.0、、 0.5、 0.25四个浓度的内毒素标准溶液,每一步稀释应混匀至少30秒钟。
鲎试剂干扰试验检查记录
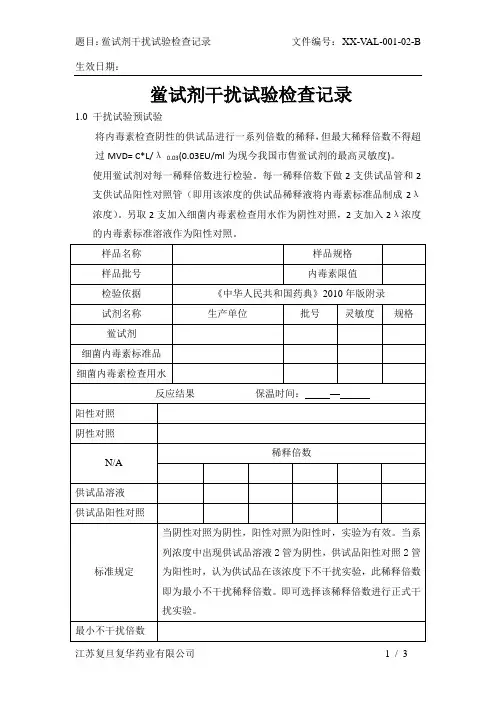
1.0 干扰试验预试验
将内毒素检查阴性的供试品进行一系列倍数的稀释,但最大稀释倍数不得超过MVD= C*L/λ0.03(0.03EU/ml为现今我国市售鲎试剂的最高灵敏度)。
使用鲎试剂对每一稀释倍数进行检验。
每一稀释倍数下做2支供试品管和2支供试品阳性对照管(即用该浓度的供试品稀释液将内毒素标准品制成2λ浓度)。
另取2支加入细菌内毒素检查用水作为阴性对照,2支加入2λ浓度的内毒素标准溶液作为阳性对照。
2.0 干扰试验
检验人:检验日期:复核人:复核日期:。

细菌内毒素检查记录(总3页)本页仅作为文档封面,使用时可以删除This document is for reference only-rar21year.March四川德阳食品药品检验所细菌内毒素检查记录(首页)总页分页检品编号:检验日期:检品名称:实验地点:一、标准规定的细菌内毒素限度(L)为:二、供试品溶液的制备:1、预试验确定的MVD为倍。
2、取本品 ml,加细菌内毒素检查用水 ml,摇匀,精密量取 ml,加细菌内毒素检查用水 ml,摇匀,即得。
三、试验用细菌内毒素溶液的制备:1、取一支细菌内毒素工作标准品,加入 ml细菌内毒素检查用水 ml,使溶解,得EU/ml的试验用细菌内毒素溶液。
2、取 ml( EU/ml),加入 ml细菌内毒素检查用水( EU/ml)3、取 ml( EU/ml),加入 ml细菌内毒素检查用水( EU/ml)4、取 ml( EU/ml),加入 ml细菌内毒素检查用水( EU/ml)5、取 ml( EU/ml),加入 ml细菌内毒素检查用水( EU/ml)6、取 ml( EU/ml),加入 ml细菌内毒素检查用水( EU/ml)四、供试品阳性对照溶液的制备:1、取 ml( EU/ml),加入 ml供试品溶液( EU/ml)2、取 ml( EU/ml),加入 ml供试品溶液( EU/ml)3、取 ml( EU/ml),加入 ml供试品溶液( EU/ml)4、取 ml( EU/ml),加入 ml供试品溶液( EU/ml)5、取 ml( EU/ml),加入 ml供试品溶液( EU/ml)6、取 ml( EU/ml),加入 ml供试品溶液( EU/ml)检验者:校对者:室负责人:四川德阳食品药品检验所细菌内毒素检查记录(附页)总页分页检品编号:检验日期:检品名称:实验地点:仪器设备:恒温箱(型号)保温温度:保温时间:自至结论:本品按《中国药典》2005年版二部附录XI E检验依据检验,结果检验者:校对者:室负责人:。

文件编号:版本:鲎试剂灵敏度复核试验作业指导书修订历史记录[至多存五版的历史修订记录]1.0 目的对细菌内毒素检查试验所用的鲎试剂的灵敏度进行复核。
2.0 职责质量与法规部负责本规程的起草,QC及相关人员执行本规程。
3.0 范围适用于本公司细菌内毒素检查法。
4.0 参考文件2010年版《中国药典》二部附录ⅪE细菌内毒素检查法2010年版《中国药品检验标准操作规范》细菌内毒素检查法《细菌内毒素检查法及其应用》第一版,气象出版社5.0 定义鲎试剂灵敏度复核试验:在细菌内毒素检查法规定的条件下,使鲎试剂产生凝集的内毒素的最低浓度即为鲎试剂的标示灵敏度(λ),用EU/ml表示。
当使用新批号的鲎试剂或试验条件发生了任何可能影响检验结果的改变时,应进行鲎试剂灵敏度复核试验。
反应终点浓度:指鲎试剂灵敏度复核试验中,系列递减的内毒素浓度中最后一个呈阳性结果的浓度。
6.0 设备/工具及物料6.1 设备/工具6.2 物料6.2.1 细菌内毒素工作标准品除另有规定外,使用由中国药品生物制品检定所统一发放的标准品。
6.2.2 细菌内毒素检查用水指内毒素含量小于0.015EU/ml(凝胶法)且对内毒素试验无干扰的灭菌注射用水。
6.2.3 鲎试剂规格一般选用0.25 EU/ml。
7.0 操作步骤7.1 提前30 min开启超净工作台,试验操作过程中不要开启风机,完毕后用75%乙醇擦拭超净工作台。
试验操作过程应防止微生物和细菌内毒素污染。
7.2 制备细菌内毒素标准溶液7.2.1 取细菌内毒素工作标准品1支,轻弹瓶壁使粉末落入瓶底,用砂轮在瓶颈上部划痕,用75%乙醇擦拭后启开,避免玻璃屑落入瓶内。
7.2.2 按照工作标准品说明书,加入细菌内毒素检查用水溶解。
封口膜封口,置漩涡混合器上混匀15 min后用细菌内毒素检查用水进行稀释,制成2.0 λ、1.0 λ、0.5 λ、0.25 λ四个浓度的内毒素标准溶液。
每稀释一步均应在漩涡混合器上混匀30 s。

细菌内毒素检查法1 目的该SOP用来判断供试品中细菌内毒素是否符合规定。
2适用范围该SOP适用于《中国兽药典》要求检查该项的药品和适合《中国兽药典》要求的其它品种的药品的细菌内毒素检查。
3职责进行该项检验的检验员应该按该SOP进行检验,检测室主任负责监督该SOP的正确执行。
4检验4.1 技术依据及原理本法系用鲎试剂与细菌内毒素产生凝集反应即内毒素在二价阳离子的参与下,作用于鲎血凝集酶系统而发生的一系列酶联反应,最后形成凝胶,以判断供试品中细菌内毒素的限量是否符合规定。
4.1.1 鲎试剂灵敏度复核试验项的目的不仅是考查鲎试剂和细菌内毒素工作标准品的效价是否准确,也是考查检验人员操作方法是否正确和实验条件是否符合规定。
因此要求每个实验室在将一批新的鲎试剂用于干扰试验或供试品细菌内毒素检查前应进行鲎试剂灵敏度复核试验。
4.1.2 供试品干扰试验项用于建立新品种细菌内毒素检查方法以及供试品的配方和工艺有变化,鲎试剂来源不同或供试品阳性对照结果呈阴性时确定供试品是否存在抑制或增强作用。
4.1.3检查法项为供试品细菌内毒素检查方法。
阴性对照、阳性对照和供试品阳性对照必须同时进行,否则试验结果无效。
4.2注意事项4.2.1实验前,须用肥皂洗手,用75%乙醇棉球消毒4.2.2实验时,须戴工作帽和口罩。
尤其在配制洗液和洗涤玻璃器皿时一定要戴手套、工作帽和口罩。
4.2.3试验应在洁净室或洁净工作台内进行。
4.2.4用移液管或刻度吸管等吸取样品时,须使用洗耳球,勿用嘴吸、吹,防止唾液溅入。
也可使用加样器等其它方法。
4.2.5 注意所用鲎试剂的批号、有效期、规格、灵敏度等。
4.2.6进行干扰实验时,标准对照和供试品阳性对照(含供试品的内毒素溶液)应同时进行。
4.2.7在进行灵敏度复核、干扰试验和供试品内毒素检查时,各个实验所要求的对照应同时进行,并在有效的条件下才能进行计算和判断。
4.3材料、仪器、试剂的准备及基本要求4.3.1天平供试品称量用,感量为0.1mg以下。


鲎试剂方法检测注射用阿昔洛韦中细菌内毒素Abstract Objectives To establish a method for test of bacterial endotoxin on aciclovir for injection Methods By interfere test,to study the inhibitive action of Aciclovir For Injection in bacterial endotoxins testResults The injection did not interfere with tachypleus amebocyte lysate in the concentration diluted to 0 8 mg·ml -1 Conclusion Bacterial Endotoxin test (gel-clot method) can be used as an alternative method for the rabbit pyrogen test for Aciclovir For InjectionKey Words Aciclovir for injection;Bacterial endotoxin;Interference test注射用阿昔洛韦为化学合成的一种广谱抗病毒药,临床主要用于免疫功能受损患者的粘膜和皮肤初发或复发的单纯疱疹病毒,水痘带状疱疹感染,免疫功能正常患者的带状疱疹和生殖器疱疹,单纯疱疹性脑炎,疱疹性结膜炎等。
《中国药典》2005年版规定的方法为热原检查法。
细菌内毒素检查法为替代热原检查法的一种检测方法,目前已被各国药典所采用。
为此,参照《中国药典》2005年版细菌内毒素检查法摘要[1]摘要,考察了注射用阿昔洛韦对细菌内毒素检查的干扰情况,为其建立细菌内毒素检查法提供实验依据。
1 实验材料ZH-2型旋涡混合器(天津药典标准仪器厂);DS1型恒温水浴箱(北京市医疗设备总厂);细菌内毒素标准品(中国药品生物制品检定所,批号20030829,每支8EU);细菌内毒素检查用水(海洋生物制品厂,批号20031020,每支2ml);鲎试剂(海洋生物制品厂,批号20040109,灵敏度0 25 EU·ml -1 ;湛江安度斯生物有限公司,批号20030824灵敏度0 25 EU·ml -1 );注射用阿昔洛韦(武汉生物化学制药公司,批号0408032、040911;武汉普生药业公司,批号041201)2 实验方法与结果2 1 细菌内毒素限值(L)的确定根据公式L=K·M-1,式中L为细菌内毒素限值;K为按规定的给药途径,人用每公斤体重每小时最大可接受的内毒素剂量,注射剂为5EU·Kg -1 ·h -1 、;M为本品每小时人用最大剂量,即M=15 mg·Kg -1 、·h -1 ;计算L=5/15=0 3EU·mg -1 。

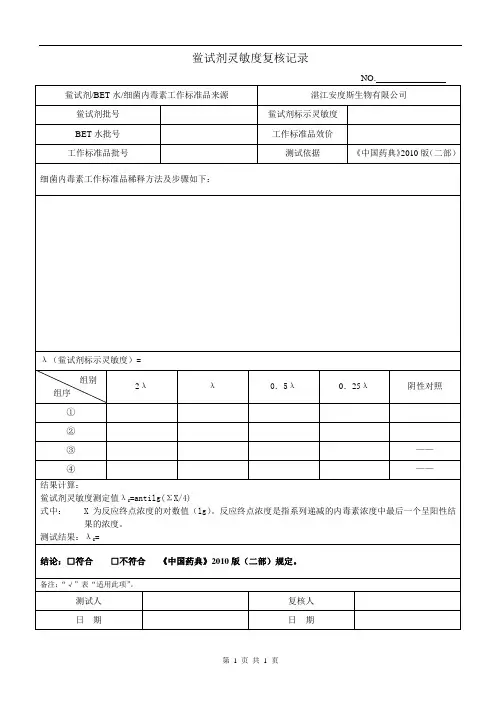
1目的建立细菌内毒素预试验操作规程,以指导检验人员的正确规范操作,为保证细菌内毒素检查凝胶法的准确性提供依据。
2适用范围适用于细菌内毒素检查法的“鲎试剂灵敏度复核试验”和“干扰试验”。
本规程参照《中国药典》2020年版四部-1143细菌内毒素检查法制定。
3职责进行细菌内毒素检查的操作人员严格按本规程进行操作。
4内容4.1基本原理4.1.1本法采用凝胶法,系通过鲎试剂与内毒素产生凝集反应的原理进行限度检测或半定量检测内毒素的方法。
4.1.2鲎试剂灵敏度复核试验:当使用新批号的鲎试剂或试验条件发生了任何可能影响检验结果的改变时,应进行鲎试剂灵敏度复核试验。
4.1.3干扰试验:当进行新药的内毒素检查试验前,或无内毒素检查项目的品种建立内毒素检查法时,须进行干扰试验;当鲎试剂、供试品的处方、生产工艺改变或试验环境中发生了任何有可能影响试验结果的变化时,须重新进行干扰试验。
4.1.4本试验操作过程应防止内毒素的污染。
4.1.5EU:内毒素单位,1EU与1个内毒素国际单位(IU)相当。
4.1.6λ:鲎试剂的标示灵敏度,单位:EU/ml。
4.1.7MVD:最大有效稀释倍数,指在试验中供试品溶液被允许达到稀释的最大倍数。
4.2材料准备4.2.1细菌内毒素工作标准品:应经细菌内毒素国家标准品为基准标定效价;4.2.2鲎试剂:当使用新批号前,按《细菌内毒素预试验SOP》进行灵敏度检查;4.2.3细菌内毒素检查用水(BET水):内毒素含量应<0.015EU/ml,且对内毒素试验无干扰作用;4.2.4供试品溶液:pH宜在6.0~8.0范围内,否则用已去除内毒素和干扰因子的酸、碱溶液或缓冲液调节。
4.3器具准备4.3.1移液枪、一次性除热源枪头(1000μL、200μL);4.3.2剪刀、砂轮片、试管架、除热源试管、医用胶布;4.3.3恒温培养箱(37℃±1℃)、旋涡混合器、洁净工作台。
4.4鲎试剂灵敏度复核试验4.4.1试验过程:4.4.1.1根据当批鲎试剂的标示灵敏度(λ),把细菌内毒素工作标准品用适量BET水充分溶解,避免产生气泡,在旋涡混合器上混匀15分钟。
细菌内毒素检查记录(总2页)--本页仅作为文档封面,使用时请直接删除即可----内页可以根据需求调整合适字体及大小--四川德阳食品药品检验所细菌内毒素检查记录(首页)总页分页检品编号:检验日期:检品名称:实验地点:一、标准规定的细菌内毒素限度(L)为:二、供试品溶液的制备:1、预试验确定的MVD为倍。
2、取本品 ml,加细菌内毒素检查用水 ml,摇匀,精密量取 ml,加细菌内毒素检查用水 ml,摇匀,即得。
三、试验用细菌内毒素溶液的制备:1、取一支细菌内毒素工作标准品,加入 ml细菌内毒素检查用水 ml,使溶解,得EU/ml的试验用细菌内毒素溶液。
2、取 ml( EU/ml),加入 ml细菌内毒素检查用水( EU/ml)3、取 ml( EU/ml),加入 ml细菌内毒素检查用水( EU/ml)4、取 ml( EU/ml),加入 ml细菌内毒素检查用水( EU/ml)5、取 ml( EU/ml),加入 ml细菌内毒素检查用水( EU/ml)6、取 ml( EU/ml),加入 ml细菌内毒素检查用水( EU/ml)四、供试品阳性对照溶液的制备:1、取 ml( EU/ml),加入 ml供试品溶液( EU/ml)2、取 ml( EU/ml),加入 ml供试品溶液( EU/ml)3、取 ml( EU/ml),加入 ml供试品溶液( EU/ml)4、取 ml( EU/ml),加入 ml供试品溶液( EU/ml)5、取 ml( EU/ml),加入 ml供试品溶液( EU/ml)6、取 ml( EU/ml),加入 ml供试品溶液( EU/ml)检验者:校对者:室负责人:四川德阳食品药品检验所细菌内毒素检查记录(附页)总页分页检品编号:检验日期:检品名称:实验地点:仪器设备:恒温箱(型号)保温温度:保温时间:自至结论:本品按《中国药典》2005年版二部附录XI E检验依据检验,结果检验者:校对者:室负责人:。
范围:鲎试剂职责:检验室对本规程的实施负责正文:1.内毒素标准溶液的制备1.1取细菌内毒素国家标准品(NSE)或内毒素工作标准品(WSE)一支,轻弹瓶壁,使粉末落入瓶底,再用砂轮在瓶颈上部轻轻划痕,75%酒精棉球擦拭后启开,防止玻璃屑落入瓶内。
1.2按标准品使用说明书用移液管加入规定量的细菌内毒素检查用水(BET)溶解其内容物,用封口膜将瓶口封严。
置旋涡混合器上混合15分钟,然后制备成所需浓度的细菌内毒素标准溶液即2.0λ、1.0λ、0.5λ、0.25λ(λ为所复核鲎试剂的标示灵敏度),每稀释一步均应在旋涡混合器上混合30秒。
若为NSE,可按其使用说明书将其稀释至规定浓度后分装并保存。
2.待复核鲎试剂的准备2.1在制备内毒素标准溶液的同时,取0.1ml/支的鲎试剂18支轻弹瓶壁,使粉末落入瓶底,用砂轮在瓶颈轻轻划痕,75%乙醇棉球擦拭后启开备用,防止玻璃屑落入瓶内,加入0.1mlBET水复溶,使内容物充分溶解,避免产生气泡。
2.2若待复核鲎试剂的规格不是0.1ml/支时,按标示量加入BET水复溶,将复溶后的鲎试剂溶液混匀后每0.1ml分配到10×75mm凝聚管中,要求至少分配18支管备用。
3.加样3.1将已充分溶解的待复核鲎试剂18支(管)放在试管架上,排成5列,其中4支(管)4列分别加入2.0λ、1.0λ、0.5λ、0.25λ的内毒素标准溶液;2支(管)1列分别加入BET水。
内毒素标准溶液和BET水的加样量均为0.1ml/支。
4.加样结束后,用封口膜封口,轻轻混匀,避免产生气泡,连同试管架放入37±1℃水浴或适宜恒温器中,试管架保持水平状态,保温60±2分钟,观察结果。
5.鲎试剂灵敏度复核如最大浓度2.0λ4管均为阳性,最低浓度0.25λ4管均为阴性,阴性对照为阴性,按下式计算反应终点浓度的几何平均值即为鲎试剂灵敏度的复核结果(λc)。
λc=lg- 1 (∑X/4)式中X为反应终点浓度的对数值(lg)。
标准品、鲎试剂操作规程目的:建立标准品、鲎试剂操作规程,指导检验员正确执行标准品、鲎试剂操作。
1.适用范围:适用于标准品、鲎试剂操作。
2.定义2.1标准品系以细菌内毒素国家标准品为基础标定其效价,用于试验中的鲎试剂灵敏度复核、干扰试验及各种阳性对照。
3.责任:QC人员。
4.规程4.1申购4.1.1标准品采购:按《对照品操作规程》中对照品申购程序,进行采购。
到药品检验所或中国生物制品检定所统一订购。
4.1.2鲎试剂采购:由管理员根据检验需要,填写申购单,注明:品名、规格、灵敏度、数量、购回日期。
交化验室主任核准后,交物料部采购。
4.2接收4.2.1物料部将鲎试剂与标准品购回后,管理员接通知,开具领料单。
4.2.2经化验室主任签字后,凭领料单到仓库领用。
4.2.3接收前,管理员仔细核对所领细菌内毒素工作标准品或鲎试剂的规格、数量、有效期和灵敏度,检查外包装、标签有无损坏或泄漏。
无误后,方可接收。
4.3贮存4.3.1接收的标准品与鲎试剂根据其特性存放在适宜的条件下,且根据批号、灵敏度分类摆放。
4.3.2管理员及时登记《标准品、鲎试剂接收、使用记录》。
4.4发放、使用4.4.1检验员根据检品需要,向管理员申请试验用量的标准品、鲎试剂。
4.4.2管理员在核实申请情况后,方可发放。
4.4.3领用后,检验员登记《标准品、鲎试剂接收、使用记录》,管理员签名确认。
4.4.4每批入库的鲎试剂必须按药典规定,进行灵敏度复核试验,符合规定后方可发放、使用。
4.4.5鲎试剂灵敏度复核4.4.5.1根据鲎试剂灵敏度的标示值(λ),将细菌内毒素工作标准品用细菌内毒素检查用水溶解,在漩涡混合器上混匀15分钟,然后制成2λ、λ、0.5λ、0.25λ四个浓度的内毒素标准溶液,每步混匀30秒。
4.4.5.2取复溶后的0.1ml/支规格的鲎试剂原安瓿18支,其中16管分别加入0.1ml不同浓度的内毒素标准溶液,每一个浓度平行做4管;另两管加入0.1ml细菌内毒素检查用水作为阴性对照。
河南省华隆生物技术有限公司质控中心鲎试剂干扰实验记录实验依据:_《细菌内毒素检测(凝胶法)标准操作规程》(G-SOP-QD-QC-002)供试品:名称编号送检部门细菌内毒素工作标准品:批号规格生产单位待检鲎试剂:批号灵敏度规格生产单位细菌内毒素检查用水:批号规格生产单位一、内毒素标准品稀释:(1)取 ml检查用水溶解标准品在漩涡混合器上混匀 min,为 E0(EU/ml);(2)取E0 ml+ ml检查用水在漩涡混合器上混匀30s,为E1 (EU/ml);(3)取E1 ml+ ml检查用水在漩涡混合器上混匀30s,为E2 (EU/ml);(4)取E2 ml+ ml检查用水在漩涡混合器上混匀30s,为E3 (EU/ml);(5)取E3 ml+ ml检查用水在漩涡混合器上混匀30s,为E4 (EU/ml);其中,E1~E4为2λ~0.25λ内毒素标准浓度二、供试品阳性液稀释:(1)取 ml供试品稀释液溶解内毒素标准品,并在混悬仪上混匀 min,得到溶液为 E0*(EU/ml);(2)取E0* ml+ ml供试品稀释液在漩涡混合器上混匀30s,为E1*(EU/ml);(3)取E1* ml+ ml供试品稀释液在漩涡混合器上混匀30s,为E2*(EU/ml);(4)取E2* ml+ ml供试品稀释液在漩涡混合器上混匀30s,为E3*(EU/ml);(5)取E3* ml+ ml供试品稀释液在漩涡混合器上混匀30s,为E4*(EU/ml);其中,E1*~E4*为供试品阳性标准浓度。
1 / 3溶液A:准备进行检查并且未检出内毒素的供试品溶液溶液B:干扰实验系列溶液C:鲎试剂标示灵敏度的对照系列溶液D:检查用水做的阴性对照放入℃水浴箱/生化培养箱中,保温 min,取出倒转180°观察结果。
三、结果:2 / 3四、计算:Es=Lg-1(∑Xs/4)=Et=Lg-1(∑Xt/4)=Xs为C溶液的反应终点浓度的对数值;Xt为B溶液的反应终点浓度的对数值;Es为C溶液的反应终点浓度的几何平均值;Et为B溶液的反应终点浓度的几何平均值;五、结论:备注:实验人员:实验日期:核对人员:核对日期:3 / 3。
细菌内毒素检测方法验证方案起草人起草日期审核人审核日期批准人批准日期西安力邦制药有限公司目的-------------------------------------------------------------------------范围-------------------------------------------------------------------------责任人----------------------------------------------------------------------内容-------------------------------------------------------------------------1.实验材料及用具-------------------------------------------------------2 实验准备----------------------------------------------------------------3.具体验证步骤----------------------------------------------------------3.1. 鲎试剂灵敏度复核------------------------------------------------3.2..干扰实验--------------------------------------------------------------3.3.供试品细菌内毒素检查--------------------------------------------4.验证结论--------------------------------------------------------------附:表1.鲎试剂灵敏度复核记录表2.干扰试验记录表3.细菌内毒素检查记录目的:为确保盐酸罗哌卡因一水合物细菌内毒素检测方法的专属性、灵敏度,保证检测结果可符合质量标准要求,特制定此方案。
文件名称File Name Record of Review for Limulus
Reagent Sensitivity
File Number
REC-SOP-C003059-01
-02
生效日期Effective Date 2018-10-18
有效期至
Expiry Date
2021-10-17
审批及颁发/APPROV AL & ISSUANCE
部门签名日期起草质量控制部
审核
质量控制部
质量保证部
批准质量负责人
颁发质量保证部
会审/COLLECTIVE REVIEW
部门签名日期部门签名日期/ / /
分发/DISTRIBUTION
Copy-1 Copy-2/
质量保证部质量控制部/
文件名称File Name Record of Review for Limulus
Reagent Sensitivity
File Number
REC-SOP-C003059-01
-02
生效日期Effective Date 2018-10-18
有效期至
Expiry Date
2021-10-17
变更历史/CHANGES
版本号修改简述提出人生效日期
01 由原文件RE-C003060《鲎试剂灵敏度复核记录》变
更而来;文件编码改变。
魏永红2017-06-01
02 增加所使用仪器及试剂的信息汪华2018-10-18 附:记录样张
REC-SOP-C003059-01-02
鲎试剂灵敏度复核记录
Record of Review for Limulus Reagent Sensitivity 起草人/日期审核人/日期批准人/日期执行日期
2018-10-18 制订依据SOP-C003059 《细菌内毒素检查法标准操作规程》
1 试剂鲎试剂批号:;规格: ml×支;
生产厂家:□湛江安度斯生物有限公司;□福州新北生化工业有限公司;
细菌内毒素检查用水批号:;规格: ml×支;内毒素含量: EU/ml;
生产厂家:□湛江安度斯生物有限公司;□福州新北生化工业有限公司;
细菌内毒素标准品批号:;规格:支/盒;效价:______EU/支;
生产厂家:□中国药品生物制品检定所;□;
2 仪器试管恒温仪型号:TAL-40D 编号:□QC-187 □QC-216 □QC-217
3 操作根据鲎试剂灵敏度标示值(λ)将细菌内毒素国家标准品或细菌内毒素工作标准品用细菌内毒素检查用水溶解,在旋涡混合器混匀15分钟,然后制成2.0λ、1.0λ、0.5λ、和0.25λ四个浓度的内毒素标准溶液。
每稀释一步均在旋涡混合器上混匀30秒钟,按检查法项试验,每一浓度平行做4支,同时用细菌内毒素检查用水做2支阴性对照管。
保温时间: ~
浓度
2.0λ 1.0λ0.5λ0.25λ阴性对照
管别
管 1
管 2
管 3
管 4
〈注:结果判断以+、-表示阳性、阴性〉
如最大浓度2.0λ管均为阳性,最低浓度0.25λ管均为阴性,阴性对照管均为阴性,按下式计算反应终点浓度的几何平均值,即为鲎试剂灵敏度的测定值(λc)。
计算公式:λc=lgˉ1(∑X/4)
=
=
X为反应终点浓度的对数值(lg)
当λc在0.5λ-2λ(包括0.5λ和2λ)时,方可用于细菌内毒素检查,并以标示灵敏度λ为该批鲎试剂的灵敏度。
4 结论:该批鲎试剂的灵敏度为 EU/ml。
检验人/日期:复核人/日期:。