酶抑制剂复合制剂的临床应用--从共识到实践
- 格式:ppt
- 大小:3.38 MB
- 文档页数:48

β-内酰胺类抗生素β内酰胺酶抑制剂复方制剂临床应用专家共识(2020年版)一、概述革兰阴性菌及少数革兰阳性菌对β-内酰胺类抗生素耐药的最重要机制是产生各种β-内酰胺酶。
β-内酰胺酶抑制剂能够抑制部分β-内酰胺酶,避免β-内酰胺类抗生素被水解而失活。
因此,β-内酰胺类抗生素/β-内酰胺酶抑制剂复方制剂(简称β-内酰胺酶抑制剂复方制剂)是临床治疗产β-内酰胺酶细菌感染的重要选择。
我国临床使用的β-内酰胺酶抑制剂复方制剂的种类和规格繁多,临床工作者对该类制剂的特点了解参差不齐,临床不合理使用问题比较突出。
二、主要β-内酰胺酶及产酶菌流行情况β-内酰胺酶是由细菌产生的,能水解β-内酰胺类抗生素的一大类酶。
β-内酰胺酶种类繁多,有多种分类方法,最主要的分类方法有两种:一、是根据β-内酰胺酶的底物、生化特性及是否被酶抑制剂所抑制的功能分类法(Bush分类法),其将β-内酰胺酶分为青霉素酶、广谱酶、超广谱β-内酰胺酶(ESBLs)、头孢菌素酶(AmpC酶)和碳青霉烯酶等;二、是根据β-内酰胺酶末端的氨基酸序列特征的分子生物学分类法(Ambler分类法),将β-内酰胺酶分为丝氨酸酶(包括A类、C类酶和D 类酶)及金属酶(B类酶)。
目前引用较多的是1995年Bush等基于上述二种方法建立的分类方法,2019年Bush等又将该分类表进一步完善和细化(表1)。
其中临床意义最大的是下列三类β-内酰胺酶:表1 常见β-内酰胺酶分类及特点,常见酶抑制剂抑酶活性1、ESBLs主要属2be\2br\2ber类酶,是由质粒介导的能水解青霉素类、头孢菌素及单环酰胺类等β-内酰胺类抗生素的β-内酰胺酶,其对碳青霉烯类和头霉素类水解能力弱。
ESBLs主要由肠杆菌科细菌产生,以肺炎克雷伯菌、大肠埃希菌、变形杆菌最为常见。
根据编码基因的同源性,ESBLs可分为TEM型、SHV型、CTX-M 型、OXA型和其他型共5大类型。
2、AmpC酶属C类酶,通常由染色体介导,可以被β-内酰胺类抗生素诱导。

β-内酰胺类抗生素β内酰胺酶抑制剂复方制剂临床应用专家共识(2020年版)一、概述革兰阴性菌及少数革兰阳性菌对β-内酰胺类抗生素耐药的最重要机制是产生各种β-内酰胺酶。
β-内酰胺酶抑制剂能够抑制部分β-内酰胺酶,避免β-内酰胺类抗生素被水解而失活。
因此,β-内酰胺类抗生素/β-内酰胺酶抑制剂复方制剂(简称β-内酰胺酶抑制剂复方制剂)是临床治疗产β-内酰胺酶细菌感染的重要选择。
我国临床使用的β-内酰胺酶抑制剂复方制剂的种类和规格繁多,临床工作者对该类制剂的特点了解参差不齐,临床不合理使用问题比较突出。
二、主要β-内酰胺酶及产酶菌流行情况β-内酰胺酶是由细菌产生的,能水解β-内酰胺类抗生素的一大类酶。
β-内酰胺酶种类繁多,有多种分类方法,最主要的分类方法有两种:一、是根据β-内酰胺酶的底物、生化特性及是否被酶抑制剂所抑制的功能分类法(Bush分类法),其将β-内酰胺酶分为青霉素酶、广谱酶、超广谱β-内酰胺酶(ESBLs)、头孢菌素酶(AmpC酶)和碳青霉烯酶等;二、是根据β-内酰胺酶末端的氨基酸序列特征的分子生物学分类法(Ambler 分类法),将β-内酰胺酶分为丝氨酸酶(包括A类、C类酶和D类酶)及金属酶(B类酶)。
目前引用较多的是1995年Bush等基于上述二种方法建立的分类方法,2019年Bush等又将该分类表进一步完善和细化(表1)。
其中临床意义最大的是下列三类β-内酰胺酶:表1常见β-内酰胺酶分类及特点,常见酶抑制剂抑酶活性1、ESBLs主要属2be\2br\2ber类酶,是由质粒介导的能水解青霉素类、头孢菌素及单环酰胺类等β-内酰胺类抗生素的β-内酰胺酶,其对碳青霉烯类和头霉素类水解能力弱。
ESBLs主要由肠杆菌科细菌产生,以肺炎克雷伯菌、大肠埃希菌、变形杆菌最为常见。
根据编码基因的同源性,ESBLs可分为TEM型、SHV型、CTX-M型、OXA型和其他型共5大类型。
2、AmpC酶属C类酶,通常由染色体介导,可以被β-内酰胺类抗生素诱导。

2022中国铜绿假单胞菌下呼吸道感染诊治专家共识(完整版)摘要铜绿假单胞菌是难治性下呼吸道感染最常见致病菌之一,由于其耐药严重和易形成生物被膜,特别是近10多年来碳青霉烯类耐药株的出现,使其治疗更为困难;同时新的治疗药物和治疗策略不断问世,有必要加以评估以指导临床合理应用。
中华医学会呼吸病学分会感染学组在《铜绿假单胞菌下呼吸道感染诊治专家共识(2014年版)》的基础上进行更新,并以临床诊治和预防的思路和技术为重点,以期为临床医生规范化诊治铜绿假单胞菌下呼吸道感染提供切实可行的参考。
铜绿假单胞菌(Pseudomonas aeruginosa,P.aeruginosa,PA)是临床常见的革兰阴性杆菌,在自然界广泛分布,可在人体皮肤表面分离到,还可污染医疗器械甚至消毒液,具有易定植、易变异和多耐药的特点。
PA 下呼吸道感染的种类主要包括肺炎、支气管扩张症(简称支扩)合并感染和慢性阻塞性肺疾病(简称慢阻肺)急性加重,由多重耐药PA(multidrug resistant P aeruginosa,MDR-PA)引起的下呼吸道感染病死率高,治疗困难。
中华医学会呼吸病学分会感染学组于2014年发表了“铜绿假单胞菌下呼吸道感染诊治专家共识”[1],对规范PA下呼吸道感染的诊断和治疗发挥了积极作用。
近年来,PA的流行病学、耐药情况不断发生变化,相关临床研究不断深入,新型抗菌药物研发上市,需要重新认识PA下呼吸道感染。
感染学组组织以呼吸与危重症医学为主的多学科专家对2014版共识加以修订,在病原检测、诊断、抗菌药物、耐药菌治疗策略、综合治疗以及感染预防控制方面进行了较大的更新,以期更好地指导临床实践。
一、PA的微生物学特点假单胞菌属为需氧革兰阴性杆菌,与不动杆菌属、黄杆菌属、嗜麦芽窄食单胞菌及洋葱伯克霍尔德菌等同属不发酵糖革兰阴性杆菌,是常见的条件致病菌,尤其是医院感染的主要病原菌之一。
PA是假单胞菌属的代表菌株,占所有假单胞菌属感染的70%以上。

2020版:β-内酰胺类抗生素/β-内酰胺酶抑制剂复方制剂临床应用专家共识(完整版)一、概述革兰阴性菌及少数革兰阳性菌对β-内酰胺类抗生素耐药的最重要机制是产生各种β-内酰胺酶。
β-内酰胺酶抑制剂能够抑制部分β-内酰胺酶,避免β-内酰胺类抗生素被水解而失活。
因此,β-内酰胺类抗生素/β-内酰胺酶抑制剂复方制剂(简称β-内酰胺酶抑制剂复方制剂)是临床治疗产β-内酰胺酶细菌感染的重要选择。
我国临床使用的β-内酰胺酶抑制剂复方制剂的种类和规格繁多,临床工作者对该类制剂的特点了解参差不齐,临床不合理使用问题比较突出。
本编写小组在2015年编写的《β-内酰胺类抗生素/β-内酰胺酶抑制剂合剂临床应用专家共识》[1],在指导和规范临床合理使用此类抗菌药物中发挥了重要作用。
随着细菌耐药性的变迁及多个新的酶抑制剂复方制剂应用于临床,为了进一步规范β-内酰胺酶抑制剂复方制剂的临床应用,延缓细菌对其耐药性的发生和发展,专家组特对共识进行了更新。
二、主要β-内酰胺酶及产酶菌流行情况β-内酰胺酶是由细菌产生的,能水解β-内酰胺类抗生素的一大类酶。
β-内酰胺酶种类繁多,有多种分类方法,最主要的分类方法有两种:一是根据β-内酰胺酶的底物、生化特性及是否被酶抑制剂所抑制的功能分类法(Bush分类法),其将β-内酰胺酶分为青霉素酶、广谱酶、超广谱β-内酰胺酶(ESBLs)、头孢菌素酶(AmpC酶)和碳青霉烯酶等;二是根据β-内酰胺酶末端的氨基酸序列特征的分子生物学分类法(Ambler分类法),将β-内酰胺酶分为丝氨酸酶(包括A类、C类酶和D类酶)及金属酶(B类酶)。
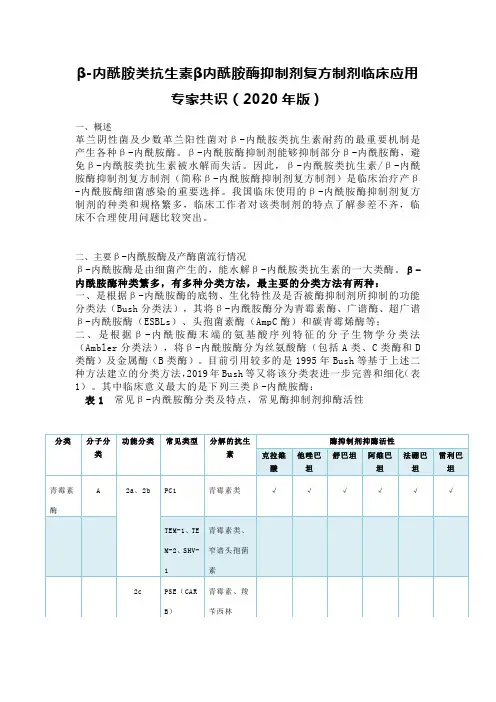
目前引用较多的是1995年Bush等[2]基于上述二种方法建立的分类方法,2019年Bush等[3]又将该分类表进一步完善和细化(表1)。
其中临床意义最大的是下列三类β-内酰胺酶:表1常见β-内酰胺酶分类及特点,常见酶抑制剂抑酶活性[3]1.ESBLs主要属2be\2br\2ber类酶,是由质粒介导的能水解青霉素类、头孢菌素及单环酰胺类等β-内酰胺类抗生素的β-内酰胺酶,其对碳青霉烯类和头霉素类水解能力弱。
β-内酰胺类抗生素β内酰胺酶抑制剂复方制剂临床应用专家共识(2020年版)一、概述革兰阴性菌及少数革兰阳性菌对β-内酰胺类抗生素耐药的最重要机制是产生各种β-内酰胺酶。
β-内酰胺酶抑制剂能够抑制部分β-内酰胺酶,避免β-内酰胺类抗生素被水解而失活。
因此,β-内酰胺类抗生素/β-内酰胺酶抑制剂复方制剂(简称β-内酰胺酶抑制剂复方制剂)是临床治疗产β-内酰胺酶细菌感染的重要选择。
我国临床使用的β-内酰胺酶抑制剂复方制剂的种类和规格繁多,临床工作者对该类制剂的特点了解参差不齐,临床不合理使用问题比较突出。
二、主要β-内酰胺酶及产酶菌流行情况β-内酰胺酶是由细菌产生的,能水解β-内酰胺类抗生素的一大类酶。
β-内酰胺酶种类繁多,有多种分类方法,最主要的分类方法有两种:一、是根据β-内酰胺酶的底物、生化特性及是否被酶抑制剂所抑制的功能分类法(Bush分类法),其将β-内酰胺酶分为青霉素酶、广谱酶、超广谱β-内酰胺酶(ESBLs)、头孢菌素酶(AmpC酶)和碳青霉烯酶等;二、是根据β-内酰胺酶末端的氨基酸序列特征的分子生物学分类法(Ambler分类法),将β-内酰胺酶分为丝氨酸酶(包括A类、C类酶和D 类酶)及金属酶(B类酶)。
目前引用较多的是1995年Bush等基于上述二种方法建立的分类方法,2019年Bush等又将该分类表进一步完善和细化(表1)。
其中临床意义最大的是下列三类β-内酰胺酶:表1 常见β-内酰胺酶分类及特点,常见酶抑制剂抑酶活性素及单环酰胺类等β-内酰胺类抗生素的β-内酰胺酶,其对碳青霉烯类和头霉素类水解能力弱。
ESBLs主要由肠杆菌科细菌产生,以肺炎克雷伯菌、大肠埃希菌、变形杆菌最为常见。
根据编码基因的同源性,ESBLs可分为TEM型、SHV型、CTX-M 型、OXA型和其他型共5大类型。
2、AmpC酶属C类酶,通常由染色体介导,可以被β-内酰胺类抗生素诱导。
部分由质粒介导,常呈持续高水平表达。

HMG—CoA还原酶抑制剂在调脂方面的临床应用3-羟基3-甲基戊二酰辅酶A还原酶抑制制(HMG—CoA)是一类新型调节血脂药物。
目前销售和使用的主要有5种:洛伐他汀、辛伐他汀、普伐他汀、氟伐他汀、阿托伐他汀。
本文就从其构数关系,几年来的临床应用情况作对照比较,最后它得出显著降低TC、LDL-C,中度降低TG,不同程度升高HDL—C,不良反应少,安全性好,且是一类临床疗效不错的调脂药。
维普资讯StatPamaetaoraVoNo520rihrcui1un1l1.06cJ8CR+P1R8例有效率6;B两组中位缓解期分别为5个oA、根茎3g水煎服可治疗胃炎、0,胃痛、胆型肝炎;治疗疗黄④疮肿毒:关鲜叶适量,烂外敷治疗疔疮肿毒“⑥治疗肾通岛;炎:祜族用通关藤茎91g配草血竭、果治肾炎;拉~5.草(月、个月.位生存期分别为9个月、4个月,有显著性差8中1均异,明消癌平注射液联合C表o外照射治疗晚期非小细胞肺癌其有效率、缓解期、生存期均明显高于单纯co外照射。
13能抑制胃癌细胞S一91的生长李茂全。
等人用.GC70止痛和戒毒作用:永向(国专利0t80,010—9发卢中101020—82)明了一种以乌骨藤作为主药的用于止痛、毒的中成药,配戒其不同浓度消癌平对S一91胃癌细胞的抑制率为10,GC700%5,9,9和1,空白对照差异明显。
其高浓度的92%15与抑制率与HC1(8)仿,物作用7P、9相药d后I52mgC。
1为mL。
同时运用昆明种小鼠胃癌细胞株移植后,用的消癌一采平为040608k一.腔内注射的肿瘤抑制率为.,.,.mlg腹5,3,1。
t验表明各用药剂量组的抗癌率与空白057检方为:骨藤1~2g徐长卿1~2g川芎8lg当归l乌30,0,6~2,4~1g延胡索1~2g茉莉花根1~22,乌35,仲8,60,8.g川~g杜1 ̄2g夏天无1~2g冰片0406。
该中成药系纯天82,82,.~.g然、本低的能止癌痛,成吸毒者使用后7d即戒毒瘾,不二次且成瘾,吸率低。

β-内酰胺类抗生素β 内酰胺酶抑制剂复方制剂临床应用专家共识( 2020 年版)一、概述革兰阴性菌及少数革兰阳性菌对β-内酰胺类抗生素耐药的最重要机制是产生各种β-内酰胺酶。
β-内酰胺酶抑制剂能够抑制部分β-内酰胺酶,避免β-内酰胺类抗生素被水解而失活。
因此,β-内酰胺类抗生素/β-内酰胺酶抑制剂复方制剂(简称β-内酰胺酶抑制剂复方制剂)是临床治疗产β-内酰胺酶细菌感染的重要选择。
我国临床使用的β-内酰胺酶抑制剂复方制剂的种类和规格繁多,临床工作者对该类制剂的特点了解参差不齐,临床不合理使用问题比较突出。
二、主要β-内酰胺酶及产酶菌流行情况β-内酰胺酶是由细菌产生的,能水解β-内酰胺类抗生素的一大类酶。
β-内酰胺酶种类繁多,有多种分类方法,最主要的分类方法有两种:一、是根据β-内酰胺酶的底物、生化特性及是否被酶抑制剂所抑制的功能分类法( Bush 分类法),其将β-内酰胺酶分为青霉素酶、广谱酶、超广谱β-内酰胺酶( ESBLs)、头孢菌素酶( AmpC 酶)和碳青霉烯酶等;二、是根据β-内酰胺酶末端的氨基酸序列特征的分子生物学分类法(Ambler 分类法),将β-内酰胺酶分为丝氨酸酶(包括 A 类、C 类酶和D 类酶)及金属酶( B 类酶)。
目前引用较多的是 1995 年 Bush 等基于上述二种方法建立的分类方法,2019 年Bush 等又将该分类表进一步完善和细化(表1)。
其中临床意义最大的是下列三类β-内酰胺酶:表 1 常见β-内酰胺酶分类及特点,常见酶抑制剂抑酶活性1、ESBLs 主要属 2be\2br\2ber 类酶,是由质粒介导的能水解青霉素类、头孢菌素及单环酰胺类等β-内酰胺类抗生素的β-内酰胺酶,其对碳青霉烯类和头霉素类水解能力弱。
ESBLs 主要由肠杆菌科细菌产生,以肺炎克雷伯菌、大肠埃希菌、变形杆菌最为常见。
根据编码基因的同源性,ESBLs 可分为 TEM 型、SHV 型、CTX-M 型、OXA 型和其他型共 5 大类型。

β-内酰胺类抗生素β内酰胺酶抑制剂复方制剂临床应用专家共识(2020年版)一、概述革兰阴性菌及少数革兰阳性菌对β-内酰胺类抗生素耐药的最重要机制是产生各种β-内酰胺酶。
β-内酰胺酶抑制剂能够抑制部分β-内酰胺酶,避免β-内酰胺类抗生素被水解而失活。
因此,β-内酰胺类抗生素/β-内酰胺酶抑制剂复方制剂(简称β-内酰胺酶抑制剂复方制剂)是临床治疗产β-内酰胺酶细菌感染的重要选择。
我国临床使用的β-内酰胺酶抑制剂复方制剂的种类和规格繁多,临床工作者对该类制剂的特点了解参差不齐,临床不合理使用问题比较突出。
二、主要β-内酰胺酶及产酶菌流行情况β-内酰胺酶是由细菌产生的,能水解β-内酰胺类抗生素的一大类酶。
β-内酰胺酶种类繁多,有多种分类方法,最主要的分类方法有两种:一、是根据β-内酰胺酶的底物、生化特性及是否被酶抑制剂所抑制的功能分类法(Bush分类法),其将β-内酰胺酶分为青霉素酶、广谱酶、超广谱β-内酰胺酶(ESBLs)、头孢菌素酶(AmpC酶)和碳青霉烯酶等;二、是根据β-内酰胺酶末端的氨基酸序列特征的分子生物学分类法(Ambler分类法),将β-内酰胺酶分为丝氨酸酶(包括A类、C类酶和D 类酶)及金属酶(B类酶)。
目前引用较多的是1995年Bush等基于上述二种方法建立的分类方法,2019年Bush等又将该分类表进一步完善和细化(表1)。
其中临床意义最大的是下列三类β-内酰胺酶:表1 常见β-内酰胺酶分类及特点,常见酶抑制剂抑酶活性1、ESBLs主要属2be\2br\2ber类酶,是由质粒介导的能水解青霉素类、头孢菌素及单环酰胺类等β-内酰胺类抗生素的β-内酰胺酶,其对碳青霉烯类和头霉素类水解能力弱。
ESBLs主要由肠杆菌科细菌产生,以肺炎克雷伯菌、大肠埃希菌、变形杆菌最为常见。
根据编码基因的同源性,ESBLs可分为TEM型、SHV型、CTX-M型、OXA型和其他型共5大类型。
2、AmpC酶属C类酶,通常由染色体介导,可以被β-内酰胺类抗生素诱导。



整合酶抑制剂临床应用专家共识(完整版)抗反转录病毒治疗(Antiretroviral therapy,ART)的出现和应用将艾滋病从一种致死性疾病转变为一种可以治疗但尚难以彻底治愈的慢性疾病。
ART是治疗艾滋病最重要的措施,目前共有7大类>50种抗反转录病毒药物(Antiretroviral drug,ARV)获得美国食品药品监督管理局(Food and drug administration,FDA)批准用于艾滋病临床治疗[1]。
随着ART在临床的广泛应用,HIV的耐药问题已成为影响疗效的重要原因。
奈韦拉平(NVP)和依非韦伦(EFV)等非核苷类反转录酶抑制剂(Non-nucleoside reverse transcriptase inhibitors,NNRTIs)曾是应用广泛的一线治疗药物,但近年来HIV对NNRTIs类药物的耐药率明显升高,部分地区甚至出现较高的传播性耐药,这使得基于NNRTIs的一线治疗方案受到巨大挑战[2]。
此外,不良反应也是影响ART疗效的重要因素。
因此,优化ART方案是近年来人们关注的焦点。
全新作用靶点的整合酶抑制剂(Integrase inhibitors,INIs)因其高效低毒,自上市后引起人们的广泛关注,其在临床广泛应用后表现出了良好的疗效和安全性,已成为国际艾滋病治疗指南中的首选推荐[3,4,5,6]。
INIs类药物已成为目前抗病毒治疗的核心药物,越来越多的INIs不断上市,为临床医师提供了更多选择。
目前,INIs尚未纳入我国免费抗病毒治疗药物目录,但临床上使用INIs的患者越来越多,为规范其在临床上的应用,中华医学会热带病与寄生虫学分会艾滋病学组和中华医学会感染病学分会艾滋病学组共同制订了"整合酶抑制剂临床应用专家共识"。
本共识为临床应用INIs提供参考,在具体的临床实践中,临床医师应结合患者具体情况合理选用,且应注意与国家免费抗病毒药物目录、《国家免费艾滋病抗病毒药物治疗手册》[7]、艾滋病诊疗指南[8]及相关政策间的衔接。
单片固定剂量复方制剂FDC在高血压治疗中的应用2024单片固定剂量复方制剂(FDC)是指将22种不同药理作用机制的药物活性成分以固定剂量组合成1片复合药物制剂的药物。
最新首版《单片固定剂量复方制剂在心血管疾病防控中应用的中国专家共识》[1]指出,与单药治疗相比,FDC具有提高治疗效益、减少药物不良反应、简化服药方式等优势。
与自由联合药物(FEC)相比,FDC能显著提高患者服药依从性、增加长期服药持续性、提高多重心血管危险因素控制达标率,从而使患者的心血管预后改善更显著。
诸多临床研究和实践已证实,由于FDC服药便利,医疗支出较低,与FEC 降压治疗相比,FDC的降压方案更能有效地提高患者服药依从性、改善血压控制水平,降低心血管疾病发生风险[1]。
本文仅对FDC在高血压治疗中的应用作以总结,以供临床参考。
01、厄贝沙坦氢氯曝嗪片厄贝沙坦氢氯嘎嗪片在控制血压水平方面具有独特优势[2]o可促进内皮细胞前列腺素及缓激肽释放,降低醛固酶水平及血管平滑肌细胞内的钙离子,从而降低血压[3]。
两药联合还可保护肾脏,协同降压,且药效平缓持久[4]。
临床治疗结果显示,厄贝沙坦氢氯曝嗪片效果显著,能有效控制血压水平,且不良反应较少[5];本药与非洛地平缓释片均不影响血液流变学指标,且安全性较高,但厄贝沙坦氢氯嘎嗪片更有利于控制血压水平,改善各生化指标水平,在高血压病情控制方面更具优势[6]。
用药方法:厄贝沙坦和氢氯曝嗪片(300mg∕12.5mg)口服1片,1次/d,空腹或进餐时使用,连续治疗4周评估疗效。
02氯沙坦钾氢氯嚷嗪片氯沙坦钾属于血管紧张素转换酶1受体(AT1)拮抗剂类降压药物;氢氯嘎嗪可利尿排钠,提升外周阻力血管对降压药物的敏感性。
二者联合应用发挥协调降压作用。
相关研究显示氯沙坦钾剂量为50mg/d时在24h内能够维持血压稳定,治疗3~6周后可以取得满意效果,降压持久,可以提升患者的依从性。
与氢氯曝嗪联合能够进一步控制血压,避免血尿酸、血钾异常,进而预防心血管事件。
最新抗菌药物在围手术期的预防应用指南围手术期是指从患者决定接受手术治疗开始,直到手术治疗结束后的一段时间。
在此期间,抗菌药物的合理使用对于预防手术部位感染(SSI)的发生具有重要意义。
本文将根据国内外相关指南和共识,结合临床实践,探讨。
一、抗菌药物预防应用的适应症1. 清洁手术:对于清洁手术,如甲状腺手术、乳腺手术、腹股沟疝修补术等,通常不需要预防性使用抗菌药物。
然而,对于一些高风险的清洁手术,如心脏手术、关节置换手术等,可根据手术部位、手术时间、患者健康状况等因素,考虑预防性使用抗菌药物。
2. 清洁-污染手术:对于清洁-污染手术,如胃肠道手术、胆道手术等,建议预防性使用抗菌药物。
手术部位可能存在潜在的污染,抗菌药物的使用有助于降低感染风险。
3. 污染手术:对于污染手术,如开放性骨折手术、烧伤手术等,应根据手术部位、手术时间、患者健康状况等因素,考虑预防性使用抗菌药物。
二、抗菌药物的选择1. 第一代头孢菌素:第一代头孢菌素(如头孢唑啉、头孢拉定等)具有广谱抗菌活性,适用于大多数清洁手术的预防性使用。
2. 第二代头孢菌素:第二代头孢菌素(如头孢呋辛、头孢替安等)具有更广的抗菌谱,适用于清洁-污染手术的预防性使用。
3. 第三代头孢菌素:第三代头孢菌素(如头孢曲松、头孢他啶等)具有更广的抗菌谱,适用于污染手术的预防性使用。
4. β-内酰胺酶抑制剂复合制剂:如头孢呋辛钠/克拉维酸钾、头孢他啶/阿维巴坦等,适用于对β-内酰胺类抗菌药物耐药的细菌感染。
5. 大环内酯类:如红霉素、克拉霉素等,适用于厌氧菌感染。
三、抗菌药物的给药时机和疗程1. 给药时机:抗菌药物应在手术切开皮肤前30分钟至1小时内给予,以确保手术部位达到有效浓度。
2. 疗程:清洁手术的预防性使用抗菌药物通常为24小时,清洁-污染手术为24-48小时,污染手术为48-72小时。
特殊情况下,可根据患者病情和药敏试验结果,适当延长预防用药时间。
四、抗菌药物预防应用的注意事项1. 严格掌握适应症,避免不必要的预防性使用抗菌药物。
整合酶抑制剂临床应用专家共识(全文)抗反转录病毒治疗(Antiretroviral therapy,ART)的出现和应用将艾滋病从一种致死性疾病转变为一种可以治疗但尚难以彻底治愈的慢性疾病。
ART是治疗艾滋病最重要的措施,目前共有7大类>50种抗反转录病毒药物(Antiretroviral drug,ARV)获得美国食品药品监督管理局(Food and drug administration,FDA)批准用于艾滋病临床治疗[1]。
随着ART 在临床的广泛应用,HIV的耐药问题已成为影响疗效的重要原因。
奈韦拉平(NVP)和依非韦伦(EFV)等非核苷类反转录酶抑制剂(Non-nucleoside reverse transcriptase inhibitors,NNRTIs)曾是应用广泛的一线治疗药物,但近年来HIV对NNRTIs类药物的耐药率明显升高,部分地区甚至出现较高的传播性耐药,这使得基于NNRTIs的一线治疗方案受到巨大挑战[2]。
此外,不良反应也是影响ART疗效的重要因素。
因此,优化ART方案是近年来人们关注的焦点。
全新作用靶点的整合酶抑制剂(Integrase inhibitors,INIs)因其高效低毒,自上市后引起人们的广泛关注,其在临床广泛应用后表现出了良好的疗效和安全性,已成为国际艾滋病治疗指南中的首选推荐[3,4,5,6]。
INIs 类药物已成为目前抗病毒治疗的核心药物,越来越多的INIs不断上市,为临床医师提供了更多选择。
目前,INIs尚未纳入我国免费抗病毒治疗药物目录,但临床上使用INIs的患者越来越多,为规范其在临床上的应用,中华医学会热带病与寄生虫学分会艾滋病学组和中华医学会感染病学分会艾滋病学组共同制订了"整合酶抑制剂临床应用专家共识"。
本共识为临床应用INIs提供参考,在具体的临床实践中,临床医师应结合患者具体情况合理选用,且应注意与国家免费抗病毒药物目录、《国家免费艾滋病抗病毒药物治疗手册》[7]、艾滋病诊疗指南[8]及相关政策间的衔接。