⊿rG T,P<0 反应自发进行 ⊿rG T,P =0 反应就是可逆得,处于平衡状态 ⊿rG T,P >0 反应不能自发进行
化学等温式
对于液相反应aA + bB ≒ gG+ hH
rG
rG
RT
ln
(CG'
(C
' A
/ C / C
)g )a
(C
' H
(C
' B
/ C )h / C )b
当体系处于平衡状态时, △rG = 0,则:
nA RT V
[ A]RT
PG
nG RT V
[G]RT
PB
nB RT V
[B]RT
PH
nH RT V
[H ]RT
Kp
( PG )g ( PH )h ( PA )a ( PB )b
[G]g[H ]h [ A]a[B]b
( RT )( ghab)
∴ Kp = Kc (RT) △n , △n = g+h - (a+b)。
例: 2H2 (g) +O2 (g) ≒2H2O (g)
873K-1273K时,生成水 得方向占优势
4273-5273K时,分解过 程占优势
4、1、2 化学平
衡
N2O4 (g) ≒ 2NO2 (g)
V
无色
棕红色
N2O4气体
V正
动态平衡
V正= V逆
≠0
V逆
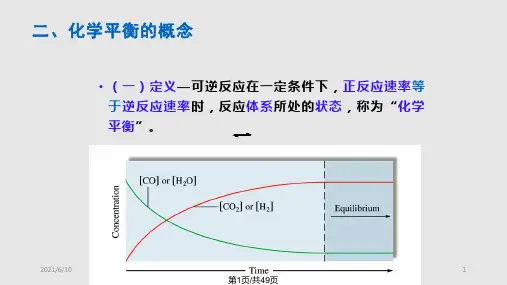
t 在可逆反应体系中,正反应与逆反应得速率相等时反应 物与生成物浓度不再随时间改变得状态,即动态平衡、
大学无机化学化学平衡
§4、1 化学反应得可逆性与化学平衡
4、1、1 化学反应得可逆性 4、1、2 化学平衡