乙烯氧气氧化法生产环氧乙烷反应器的选型与操作
- 格式:ppt
- 大小:991.50 KB
- 文档页数:15

第1篇一、前言本规程旨在规范乙烯制环氧乙烷的生产操作,确保生产过程安全、高效、稳定,降低生产成本,提高产品质量。
本规程适用于所有参与乙烯制环氧乙烷生产的相关人员。
二、原料及设备1. 原料:乙烯、氧气、银催化剂等。
2. 设备:乙烯储罐、氧气储罐、反应器、冷凝器、分离器、换热器、计量装置、安全装置等。
三、操作步骤1. 原料准备- 检查乙烯、氧气、银催化剂等原料的质量,确保符合生产要求。
- 将乙烯、氧气、银催化剂等原料按照比例混合均匀。
2. 设备检查- 检查反应器、冷凝器、分离器、换热器等设备的运行状态,确保设备正常。
- 检查计量装置、安全装置等辅助设备的可靠性。
3. 投料- 将混合好的原料投入反应器。
- 根据生产要求,调整反应器温度、压力等参数。
4. 反应- 在催化剂的作用下,乙烯与氧气发生催化氧化反应,生成环氧乙烷。
- 反应过程中,密切关注反应器内温度、压力、空速等参数,确保反应稳定进行。
5. 分离- 反应结束后,将反应混合物进入冷凝器进行冷凝。
- 冷凝后的混合物进入分离器进行分离,得到环氧乙烷和未反应的乙烯。
6. 纯化- 将分离得到的环氧乙烷进行纯化处理,去除杂质。
- 纯化后的环氧乙烷进入储罐储存。
7. 安全操作- 操作过程中,严格遵守安全操作规程,确保人身和设备安全。
- 定期检查设备,发现问题及时处理。
- 发现异常情况,立即停止生产,采取措施进行处理。
四、注意事项1. 温度控制:反应过程中,严格控制反应器温度,避免过高或过低影响产品质量。
2. 压力控制:反应过程中,严格控制反应器压力,避免过高或过低造成设备损坏。
3. 空速控制:反应过程中,严格控制空速,确保反应充分进行。
4. 催化剂管理:定期检查催化剂的性能,发现异常及时更换。
5. 环境保护:在生产过程中,严格控制废气、废水排放,确保符合环保要求。
五、总结乙烯制环氧乙烷操作规程是保证生产过程安全、高效、稳定的重要依据。
所有参与生产的人员应严格遵守本规程,确保生产顺利进行。


乙烯空气氧化法制备环氧乙烷的过程安全与操作风险分析乙烯空气氧化法是一种常用的制备环氧乙烷的方法。
在这个过程中,通过乙烯和空气的反应生成环氧乙烷。
然而,这个过程中存在一些安全风险和操作风险,需要我们加以分析和控制。
1. 原料安全风险分析乙烯是这个过程的主要原料,它是有毒可燃气体。
在储存和输送乙烯的过程中,存在泄漏的风险,这可能导致爆炸和中毒事故。
因此,必须确保乙烯的储存设施和输送管道的完整性和密封性。
同时,应加强监测和泄漏报警装置的安装,及时发现和处理泄漏事故。
空气是另一个主要原料,它是不可替代的氧气来源。
虽然空气一般不会导致火灾或爆炸,但在空气中含有一定的水分和杂质时,可能引起氧气富集而加剧火灾的危险。
因此,在使用空气前,应对其进行处理和净化,确保其纯度和干燥度。
2. 反应过程安全风险分析乙烯空气氧化反应是一个高温高压的过程,要求严格的控制条件。
因此,反应器的设计和选材非常重要。
反应器需具备耐高温、耐高压、耐腐蚀等特性,并且需要有可靠的温度和压力控制装置,以确保反应过程的安全稳定运行。
与此同时,反应过程中的反应物和产物流动也需要注意。
高温下乙烯和空气的反应速度较快,反应物和产物的流动速度较高,容易造成管道磨损、泄漏和堵塞等问题。
因此,需要选择耐腐蚀材料的管道和设备,并进行定期的检测和维护。
3. 产品处理安全风险分析环氧乙烷是一种易燃、易爆的化学品,需要注意其储存和处理。
首先,环氧乙烷的储存容器应具备防爆、防静电等特性,保证其储存过程的安全性。
其次,环氧乙烷的操作和使用应遵循严格的操作规程,防止泄露、溢出和接触火源等情况发生。
此外,还需要为环氧乙烷设置泄漏报警装置,并建立应急处置预案,以确保在发生事故时能迅速有效地进行处理。
4. 废物处理安全风险分析乙烯空气氧化反应产生的废水、废气等废物需要得到妥善处理。
废水中可能含有有机物和杂质,需要进行处理和净化,防止对环境造成污染。
废气中可能含有未反应的乙烯、环氧乙烷等有害物质,需要进行收集和处理,防止对大气造成污染。


乙烯環氧化製環氧乙烷低級烯烴的氣相氧化都屬非均相催化氧化範疇。
催化劑為毫米級或μ級微粒,它們分別用於固定床或流化床反應器。
環氧乙烷是乙烯工業衍生物中僅次於聚乙烯而占第二位元的重要有機化工產品。
它除部分用於製造非離子表面活性劑、氨基醇、乙二醇醚外,主要用來生產乙二醇,後者是製造聚酯樹脂的主要原料。
也大量用作抗凍劑。
1. 生產方法環氧乙烷有兩種生產方法:氯醇法和直接氧化法。
(1)氯醇法本法於1925年由美國聯碳公司(UCC)首先實現工業化。
生產過程包括二個基本反應:乙烯與次氯酸反應(俗稱次氯酸化)和氯乙醇脫氯化氫反應(俗稱環化或皂化)。
A次氯酸化反應主要副反應有:還有生成二氯二乙醚的副反應:次氯酸化反應溫度為40~60℃,C2H4∶Cl2=1.1~1.2∶1,即乙烯是過量的。
壓力對反應沒有影響,只需滿足克服系統阻力就行。
B氯乙醇的皂化(環化)反應副反應為:當有氧化鎂雜質存在時,還可能生成少量醛類:工業上除用Ca(OH)2作皂化劑外,還採用NaOH溶液。
操作中應將皂化劑緩慢加入氯乙醇中。
否則,在鹼性介質中生成的環氧乙烷會大量水解生成乙二醇。
皂化反應壓力為0.12MPa,溫度為102~105℃,在此條件下,可保證生成的環氧乙烷立即從液相逸出(環氧乙烷沸點10.7℃),避免環氧乙烷的水解。
本法可以採用低濃度乙烯(50%左右)為原料,乙烯單耗低、設備簡單、操作容易控製,有時還可聯產環氧丙烷。
但生產成本高(生產1噸產品,需消耗0.9噸乙烯、2噸氯氣和2噸石灰),產品只能用來生產表面活性劑。
氯氣和氫氧化鈣沒有進入產品分子中,而是變成工業廢渣,不僅浪費了氯氣和石灰資源,而且還會嚴重污染環境。
此外,氯氣、次氯酸和HCl等都會造成設備腐蝕和環境污染。
因此本法從20世紀50年代起,已被直接氧化法取代。
(2)直接氧化法本法於1938年也由美國聯碳公司開發成功。
由於受當時工業技術水準的限制,直至50年代才開始建造大型工業生產裝置。

乙烯空气氧化法制备环氧乙烷的反应过程模拟与优化研究环氧乙烷是一种重要的有机化工原料,广泛应用于涂料、胶粘剂、塑料等行业。
乙烯空气氧化法是制备环氧乙烷的主要工艺之一。
本文将对乙烯空气氧化法制备环氧乙烷的反应过程进行模拟与优化研究。
1. 反应原理乙烯空气氧化法制备环氧乙烷的反应原理是通过乙烯与空气中的氧气在催化剂的作用下发生氧化反应,生成环氧乙烷。
催化剂主要有银、过渡金属等。
2. 反应过程模拟为了更好地理解乙烯空气氧化法制备环氧乙烷的反应过程,可以利用计算机模拟方法对反应过程进行模拟和优化。
模拟方法主要有密度泛函理论、分子动力学模拟等。
2.1 密度泛函理论模拟密度泛函理论模拟方法基于量子力学理论,通过解析式计算反应物、产物以及中间过渡态的电子结构和能量,以及通过研究各个反应中间体的构型变化,来揭示反应机理和优化条件。
2.2 分子动力学模拟分子动力学模拟方法基于经典力学,通过求解分子间相互作用力,计算反应过程中的原子轨迹和能量变化。
可以模拟大分子体系,考虑溶剂效应等。
3. 反应过程优化反应过程优化的目标是提高环氧乙烷的产率和选择性,减少副产物的生成,降低能源消耗。
可以从以下几个方面进行优化研究。
3.1 催化剂设计催化剂的设计和优化是提高反应效率的重要手段。
可以通过改变催化剂的组成、晶体结构、表面形貌等因素来调控反应过程。
例如,利用纳米催化剂或拼接催化剂的设计,可以提高催化剂的活性和选择性。
3.2 反应条件优化反应条件的优化包括反应温度、压力、乙烯与空气的摩尔比等因素的选择。
通过合理调控反应条件,可以提高反应速率和产物选择性。
3.3 副产物的转化利用乙烯空气氧化法制备环氧乙烷的过程中会生成一些副产物,如醛类、酮类等。
可以研究副产物的转化反应,将其转化为有用的化合物,提高反应的经济性和环境友好性。
4. 结论通过乙烯空气氧化法制备环氧乙烷的反应过程模拟与优化研究,可以深入了解反应机理,提高反应效率和产物选择性。

乙烯空气氧化法制备环氧乙烷的反应机理与动力学研究环氧乙烷是一种重要的工业原料,在化工领域有着广泛的应用。
乙烯空气氧化法是一种常用的制备环氧乙烷的方法。
本文将对乙烯空气氧化法制备环氧乙烷的反应机理与动力学进行研究。
1. 乙烯空气氧化法简介乙烯空气氧化法是一种以乙烯和空气为原料,经过氧化反应生成环氧乙烷的方法。
该方法具有原料便宜、生产工艺简单等优点,在工业上得到了广泛应用。
2. 反应机理乙烯空气氧化法制备环氧乙烷的反应机理主要包括以下几个步骤:(1) 乙烯氧化为乙醛:在反应器中,乙烯与空气在过渡金属催化剂的作用下发生氧化反应,生成乙醛。
该氧化反应是一个重要的步骤,乙烯在催化剂表面吸附,并与氧分子反应生成乙醛。
(2) 乙醛与空气进一步氧化为乙酸:乙醛进一步与空气反应,氧化为乙酸。
这个过程是一个氧化反应,需要一定的温度和氧气的存在。
(3) 乙酸与乙烯发生酯化反应:经过氧化反应生成的乙酸与乙烯发生酯化反应,生成环氧乙烷。
该酯化反应需要催化剂的存在,并在一定的温度条件下进行。
3. 反应动力学研究反应动力学是研究化学反应速率随着温度、浓度等条件变化的规律。
乙烯空气氧化法制备环氧乙烷的反应动力学研究对于优化反应条件、提高产率和降低能耗具有重要的意义。
反应动力学研究中常用的方法包括测定反应速率常数、建立反应速率方程等。
通过实验测得的反应速率常数和反应条件之间的关系,可以进一步确定反应速率方程,揭示反应机理以及反应中的主要影响因素。
还可以通过改变反应温度、反应物浓度等条件进行反应动力学研究,从而得到反应速率随温度和浓度变化的规律。
4. 结论乙烯空气氧化法制备环氧乙烷是一种重要的工业制备方法。
通过对该方法的反应机理与动力学研究,可以更好地理解反应过程,优化反应条件,并提高产率。
反应机理研究表明,乙烯空气氧化法制备环氧乙烷的反应包括乙烯氧化为乙醛、乙醛进一步氧化为乙酸,以及乙酸与乙烯发生酯化反应生成环氧乙烷。
反应的动力学研究可以通过测定反应速率常数、建立反应速率方程等方法进行。

乙烯空气氧化法制备环氧乙烷的设备选型与优化环氧乙烷 (Ethylene Oxide, EO) 是一种重要的有机合成原料,广泛应用于化工、医药、农药和日化等领域。
乙烯空气氧化法是目前制备环氧乙烷的主要工艺路线,该方法通过将乙烯与空气催化反应,制得环氧乙烷。
本文将讨论乙烯空气氧化法制备环氧乙烷的设备选型与优化。
一、反应器选型乙烯空气氧化法制备环氧乙烷的反应器是整个过程中最关键的设备之一。
常用的反应器类型包括固定床反应器、流化床反应器和循环流化床反应器等。
1. 固定床反应器固定床反应器是最常见的反应器类型之一,其主要特点是结构简单、操作稳定,并且适应性广。
然而,乙烯空气氧化反应属于高度放热反应,固定床反应器存在热失控的风险。
此外,催化剂在操作过程中容易受到积碳和中毒,需要定期更新和再生,增加了生产成本。
2. 流化床反应器流化床反应器是另一种常见的反应器类型,其主要特点是具有良好的传热和传质性能,有利于催化剂的再生和控制反应温度。
然而,流化床反应器的操作复杂,催化剂的悬浮性需要进行良好的控制,以避免颗粒的沉积和外泄。
此外,流化床反应器对催化剂的选择也有较高的要求。
3. 循环流化床反应器循环流化床反应器是对传统流化床反应器的改进,可以有效地控制催化剂的循环和再生。
该反应器通过循环流化床内的气体进行催化剂的再生,避免了催化剂在操作过程中的积碳和中毒问题。
循环流化床反应器还具有较好的传热和传质性能,能够稳定控制反应温度。
二、适宜催化剂选择催化剂是乙烯空气氧化法制备环氧乙烷的关键组成部分,其催化性能直接影响反应效果和设备的稳定性。
常用的催化剂主要包括磷钼酸盐、银催化剂和铁催化剂等。
磷钼酸盐是一种常见而有效的催化剂,具有较高的催化活性和稳定性,适用于固定床反应器和流化床反应器。
银催化剂具有良好的选择性,可以提高环氧乙烷的产率和纯度,适用于固定床反应器和循环流化床反应器。
铁催化剂具有较好的耐热性和抗中毒性能,适用于循环流化床反应器。

四、乙烯环氧化制环氧乙烷低级烯烃的气相氧化都属非均相催化氧化范畴。
催化剂为毫米级或μ级微粒,它们分别用于固定床或流化床反应器。
烯烃气相氧化可制得很多有用的有机化合物,其中比较重要的有乙烯环氧化制环氧乙烷、丙烯氧化偶联制丙烯腈、丙烯环氧化制环氧丙烷以及丁烯氧化制顺丁烯二酸酐(俗称顺酐)等。
环氧乙烷是乙烯工业衍生物中仅次于聚乙烯而占第二位的重要有机化工产品。
它除部分用于制造非离子表面活性剂、氨基醇、乙二醇醚外,主要用来生产乙二醇,后者是制造聚酯树脂的主要原料。
也大量用作抗冻剂。
现在几乎所有的环氧乙烷都与乙二醇生产相结合在一起,大部或全部环氧乙烷用于生产乙二醇,少部分用于生产其它化工产品。
据预测,全世界环氧乙烷的生产能力2000年为1418.3万t/a。
中国1995年生产能力为69万t/a,2000年预测为89.0万t/a,低于需求量4~5万吨,因此在“九五”规划中仍需新建环氧乙烷生产装置。
1. 生产方法环氧乙烷有两种生产方法:氯醇法和直接氧化法。
(1)氯醇法本法于1925年由美国联碳公司(UCC)首先实现工业化。
生产过程包括二个基本反应:乙烯与次氯酸反应(俗称次氯酸化)和氯乙醇脱氯化氢反应(俗称环化或皂化)。
A次氯酸化反应主要副反应有:还有生成二氯二乙醚的副反应:次氯酸化反应温度为40~60℃,C2H4∶Cl2=1.1~1.2∶1,即乙烯是过量的。
压力对反应没有影响,只需满足克服系统阻力就行。
B氯乙醇的皂化(环化)反应副反应为:当有氧化镁杂质存在时,还可能生成少量醛类:工业上除用Ca(OH)2作皂化剂外,还采用NaOH溶液。
操作中应将皂化剂缓慢加入氯乙醇中。
否则,在碱性介质中生成的环氧乙烷会大量水解生成乙二醇。
皂化反应压力为0.12MPa,温度为102~105℃,在此条件下,可保证生成的环氧乙烷立即从液相逸出(环氧乙烷沸点10.7℃),避免环氧乙烷的水解。
本法可以采用低浓度乙烯(50%左右)为原料,乙烯单耗低、设备简单、操作容易控制,有时还可联产环氧丙烷。

反应工程课程设计设计题目:乙烯催化氧化制环氧乙烷的反应器设计专业名称:化学工程及工艺姓名:尹润田学号: 8系别:化学及化学工程系指导教师: 陈湘设计时间: 2012-5-28 至 2012-6-7目录设计任务书第一章绪论 (2)1.1反应过程分析 (2)1.2催化剂的选择 (2)1.3反应器的选择 (3)1.4反应条件的分析 (3)第二章工艺流程及说明 (4)2.1乙烯的氧化 (4)2.2环氧乙烷的吸收及解析 (6)第三章物料衡算 (8)3.1原料气的组成 (8)3.2物料衡算图及反应原理 (9)3.2反应器的物料衡算 (10)第四章热量衡算 (12)4.1 反应器的热量衡算 (12)4.2热量衡算 (14)第五章反应器的设计 (16)5.1催化剂的用量 (17)5.2确定氧化反应器的基本尺寸 (20)5.3床层压力降的计算 (20)5.4传热面积的核算 (20)5.5反应器塔径的确定 (22)5.6设备壁厚的计算 (24)5.7 附属设备的计算 (24)第六章设计结果汇总 (26)符号说明 (27)参考文献 (28)第一章绪论环氧乙烷(简称EO)是最简单也是最重要的环氧化合物,在常温下为气体,沸点10.5℃。
可以及水、醇、醚及大多数有机溶剂以任意比混合。
有毒,易自聚,尤其当有铁,酸,碱,醛等杂质或高温下更是如此,自聚时放出大量热,甚至发生爆炸,因此存放环氧乙烷的贮槽必须清洁,并保持在0℃以下。
环氧乙烷是以乙烯为原料产品中的第三大品种,仅次于聚乙烯和苯乙烯。
它的用途是制取生产聚酯树脂和聚酯纤维的单体、制备表面活性剂,此外还用于制备乙醇胺类、乙二醇醚类等。
1.1 过程分析工业上生产环氧乙烷最早采用的方法是氯醇法,该法分两步进行,第一步将乙烯和氯通入水中反应生成2-氯乙醇,2-氯乙醇水溶液浓度控制在6%-7%(质量);第二步使2-氯乙醇及Ca(OH)2反应,生成环氧乙烷。
该法的优点是对乙烯的浓度要求不高,反应条件较缓和,其主要缺点是要消耗大量氯气和石灰,反应介质有强腐蚀性,且有大量含氯化钙的污水要排放。
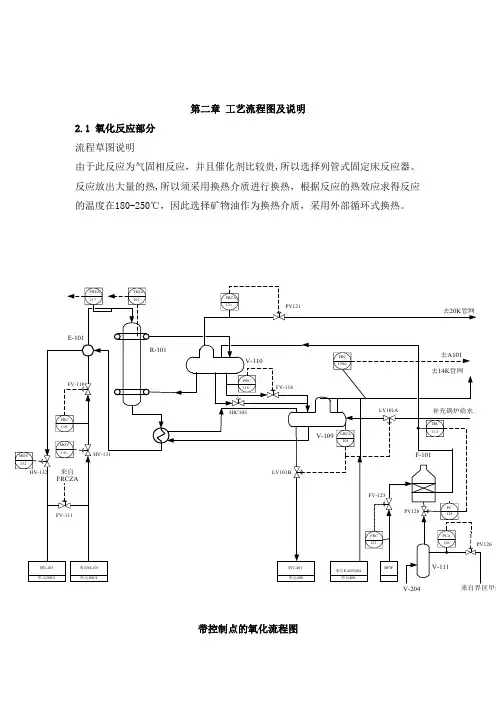
第二章工艺流程图及说明2.1 氧化反应部分流程草图说明由于此反应为气固相反应,并且催化剂比较贵,所以选择列管式固定床反应器。
反应放出大量的热,所以须采用换热介质进行换热,根据反应的热效应求得反应的温度在180-250℃,因此选择矿物油作为换热介质,采用外部循环式换热。
V-204带控制点的氧化流程图第三章 物料衡算由设计任务书已知数据如下:原料气的组成组分 42H C2CO2O 2N含量(mol%) 3.4 7.7 5.6 83.3原料进入反应器的温度为210°C反应温度为250°C 反应压力为1MPa 乙烯转化率为26.0%;选择性为65%;空速为5000h -1 年工作时间7200小时,年产量20000吨 反应产物分离后回收率为90%反应器内催化剂填充高度为管长95%,每根管长3米采用间接换热方式:导出液进口温度230°C ,出口温度235°C,导出液对管壁的给热系数为650W/m 2·K催化剂为球体,D=3mm,床层孔隙率为0.8在250°C ,1MPa 下反应气体导热系数为0.0304W/m 2K,粘度为4.26×10-5PaS,密度为7.17Kg/m 33.1 乙烯催化氧化制取环氧乙烷得物料衡算框图:其中:FF 新鲜原料气 MF 原料混合气 RP 反应混合气 SP 混合分离气 RC 循环气 P 产品环氧乙烷W 排空废气 SPC 未脱除二氧化碳的循环气 TC 脱除的二氧化碳 SRC 脱除二氧化碳的循环气3.2 反应原理乙烯和氧气在银催化剂上,于一定温度和压力下,直接氧化生产环氧乙烷,反应方程式可表为: (1)主反应:O H C O H C 4224221→+反应为放热反应,在250°C 时,每生成一摩尔环氧乙烷要放出25.19kcal 的热量。
(2)在主反应进行的同时,还发生其它副反应,其中主要是乙烯的燃烧反应。
乙烯制环氧乙烷工艺流程设计与催化剂评价一、引言近年来,环保意识的提高和对高附加值产品需求的增长,使得乙烯制环氧乙烷的工艺流程设计和催化剂评价成为研究的热点。
本文旨在探讨乙烯制环氧乙烷的工艺流程设计以及评价催化剂的方法和参数。
二、乙烯制环氧乙烷的工艺流程设计1. 原料准备乙烯作为乙烯制环氧乙烷的主要原料,需要通过适当的方法进行准备。
常见的方法包括乙烯气体的储存和净化,确保其纯度和稳定性。
2. 催化剂的选择对于乙烯制环氧乙烷的工艺流程,催化剂的选择是至关重要的。
常见的乙烯环氧化催化剂包括银系和铂系催化剂。
根据具体的工艺要求和经济评价,选择合适的催化剂对于工艺流程的设计至关重要。
3. 反应器设计反应器是乙烯制环氧乙烷工艺中的关键设备之一。
反应器的设计涉及到温度、压力、反应速率等多个参数的控制。
通过合理的反应器设计,可以提高反应效率和产率。
4. 分离与回收乙烯制环氧乙烷的工艺还需要考虑分离和回收产品的问题。
常见的分离技术包括蒸馏、吸附等方法。
通过合理的分离与回收设计,可以最大程度地提高产品的纯度和回收率,降低生产成本。
三、催化剂评价方法和参数1. 催化剂的催化活性评价催化剂的催化活性是衡量其性能的重要指标之一。
常见的评价方法包括反应速率、转化率等参数的测定。
同时,还可以通过对催化剂寿命的研究,评价其长期稳定性和使用寿命。
2. 催化剂的选择性评价催化剂的选择性是指其在反应中产生目标产品的能力。
通过评价催化剂的选择性,可以判断其用于乙烯制环氧乙烷工艺的适用性。
常见的评价方法包括目标产品的产率、副产物含量等参数的测定和分析。
3. 催化剂的耐性和抗毒性评价在实际生产中,催化剂可能会受到一些不良环境因素的影响,从而降低其催化活性和选择性。
对于乙烯制环氧乙烷工艺来说,常见的不良环境因素包括水、硫等物质的存在。
评价催化剂的耐性和抗毒性,可以帮助生产者选择更加稳定和高效的催化剂。
四、结论乙烯制环氧乙烷的工艺流程设计和催化剂评价是一个复杂而关键的课题。