分析用人基质质控血清水平II
- 格式:pdf
- 大小:227.09 KB
- 文档页数:4

临床实验室定义定义:根据ISO15189 “医学实验室质量管理”“目的是提供诊断、预防、治疗疾病信息,或为评价人类健康对源自人体物质进行生物学、微生物学、血清学、化学、免疫血液学、血液学、生物物理学、细胞学、病理学、或其它方面检查的机构,可以提供咨询服务”。
质量控制:ISO9000:2000,为“质量管理的一部分,致力于满足质量要求”。
校准定义:在规定条件下,为确定检测仪器(或检测系统)所指示的量值,与对应的由检测标准所复现的值之间关系的一组操作。
分析前阶段定义:医师选择检测项目提出检测申请单直至将检测标本送至实验室•临床灵敏度:指诊断试验检出阳性病人的百分率(真阳性率)•临床特异性:指诊断试验检查确定未患病者的阴性百分率(真阴性率)检测人员在这一阶段应起的作用:1、宣传和指导作用2、把关作用3、反馈作用4、参谋作用分析前阶段质量保证的三个特点:1、影响要素的非可控性2、质量缺陷的隐蔽性3、责任的难确定性习题:分析前阶段质量保证不包括A、正确选择项目B选定敏感度和特异度C、做好患者准备D、正确采集标本E、正确运送、保存标本下列哪个因素在定量测定中属于非生物性干扰因素A、营养 B 溶血C、年龄 D、运动E、生理节律变化某全血标本,在室温中放置了4小时方送检,这时可能引起下列何种变化:A、血钾降低、血糖增高 B血钾增高、血糖减低C、两者皆增高D、两者皆降低E、对结果无影响作临床生化定量测定,一般采取空腹血液标本,空腹时间以多少时间为宜:A、2小时左右B、4小时左右C、8小时左右D、12小时左右E、24小时左右用EDTA抗凝血作下列检验,影响检验结果最大的是:A、RBCB、HCTC、CaD、TPE、HBsAg下列何种物质红细胞中含量比血浆中低:A、CrB、LDHC、ASTD、HbE、Ca对真空采血管的评价,哪一种说法是不正确的:A、可控制采血量B、减少采血过程中的生物性污染C、减少溶血的发生D、操作方便,减少工作强度E即使不加添加剂,也可快速分离出血清进食高脂肪食物后可引起下列何种物质测定值大幅度增高A、BUNB、TGC、ALTD、GLUE、UA维生素C对某些试验的干扰作用主要是由于它的A、氧化性B、还原性C、改变了反应的pHD、与被测物的络合作用E、改变了被测物的空间结构肿瘤患者术后长期化疗,例行常规检查时,发现患者WBC、PLT降低,下列解释哪一种是正确的A、此治疗药物干扰了检测结果B、此结果不可靠C、此结果并非患者真实情况,无临床指导意义D此结果是真实的,有临床指导意义E、此检测结果反映了病情恶化正态分布:•以均值为中心、左右完全对称的钟型曲线•正态分布有两个参数,既均值u和标准差σ随机误差定义:测量结果与在重复性条件下,对同一被测量进行无限多次测量所得结果的平均值之差。

心肌酶谱测定在新生儿缺血缺氧性脑病早期诊断的临床意义摘要】目地了解新生儿缺血缺氧性脑病(HIE)发生时,心肌酶谱的变化以及对病情诊断、预后的评估。
方法对2009年-2012年期间住院的23例HIE患儿心肌酶谱的检测以及随时抽取的同期住院的非HIE患儿20例做为对照组。
结果①HIE患儿病情越重,心肌酶升高越显著,重度HIE组与对照组心肌酶有显著差异,P<0.01具有统计学意义。
②重症HIE对心肌损害程度严重,预后治疗较差。
结论血清酶水平测定对于病情的早期诊断,预后判断具有一定的参考价值。
【关键词】新生儿缺血缺氧性脑病心肌损害肌酸肌酶乳酸脱氢酶。
【中图分类号】R44 【文献标识码】A 【文章编号】2095-1752(2013)35-0255-01新生儿缺血缺氧性脑病(HIE)是指在围产期窒息而导致脑的缺氧缺血性损害。
临床出现一系列脑病表现。
严重的HIE可有脑瘫,认知障碍,癫痫等后遗症。
本症不仅严重威胁着新生儿的生命,并且是新生儿期后病残儿中最常见的病因之一。
血清酶学改变较为敏感对判定疾病的发展程度预后都有一定的指导意义。
一.临床资料1.1 2009-2012年我院收治的HIE住院患儿23例,其中男性17例,女性8例。
重度窒息15例,轻度窒息8例,其中伴羊水感染3例,低体重儿1例,重度黄疸1例。
对照组20例为新生儿上呼吸道感染,新生儿肺炎,新生儿黄疸患儿。
1.2 临床表现:轻度表现过度兴奋,如易激惹,对刺激反应过强,凝视,可出现过度通气和吞咽困难。
重度嗜睡,渐变迟钝,肌张力增强,惊厥和多脏器衰竭。
诊断标准及分度符合1996年杭州会议诊断标准。
(1)1.3 实验室检测方法采用迈瑞BS-200全自动生化分析仪测定,对AST、LDH、CK、CK-MB四项心肌酶指标进行测定。
质控品为分析用人基质质控血清,用5ml蒸馏水复溶。
心肌酶谱正常参考值:天冬氨酸转氨酶(AST) (0-40U/L),乳酸脱氢酶(LDH)(127-240 U/L),肌酸肌酶(CK)(40-200 U/L),肌酸肌酶同工酶MB(CK-MB)(0-10U/L)。
2性能指标
2.1外观和性状
2.1.1颜色性状
质控品正常水平和病理水平均为白色冻干粉末;复溶后正常水平为清澈透明浅黄色液体,病理水平为清澈透明黄色液体,均无沉淀、无悬浮物和絮状物。
2.1.2包装
分装瓶为棕色硬质玻璃瓶,盖有橡胶瓶内塞和塑料外盖;盒贴、瓶贴、标签标识应完整、清晰。
橡胶瓶内塞与玻璃配合后应无泄漏;塑料外盖应无明显划痕、崩缺。
2.2装量
质控品重量(含瓶重)应不少于10g。
2.3均一性
2.3.1瓶内均一性
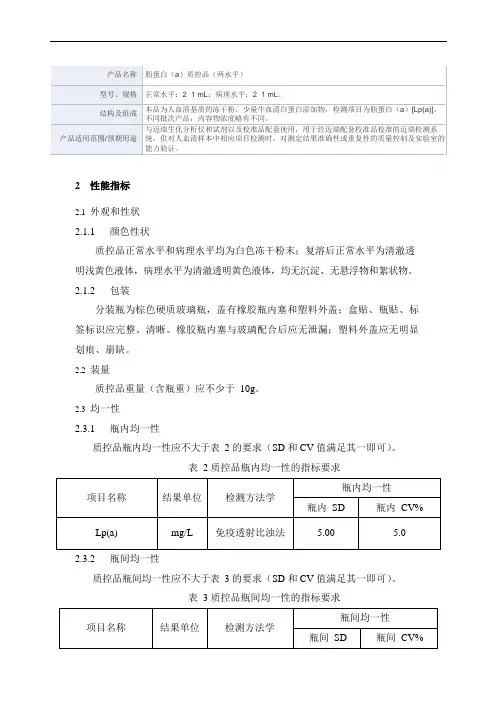
质控品瓶内均一性应不大于表2 的要求(SD 和CV 值满足其一即可)。
表 2 质控品瓶内均一性的指标要求
2.3.2瓶间均一性
质控品瓶间均一性应不大于表3 的要求(SD 和CV 值满足其一即可)。
表 3 质控品瓶间均一性的指标要求
2.4参考值及参考范围
每批质控品均应提供本批产品的参考值和参考范围表。
经迈瑞校准品校准的BS 系列生化分析仪及配套试剂对质控品进行测定,测定结果应在给定的参考范围内。
2.5生物安全性
使用国家权威管理机构认可的、且不低于我国法定用于血源筛查体外诊断试剂灵敏度的检测试剂对HBsAg、HIV 抗体、HCV 抗体、梅毒螺旋体TP 抗体检测应为阴性。

冻干质控血清冷冻保存对甲状腺激素测定的影响发表时间:2012-08-02T10:07:39.660Z 来源:《中外健康文摘》2012年第15期供稿作者:陈晖[导读] 统计学方法采用SPSS11.0统计软件分析处理数据,配对资料组间采用t检验,P<0.05为差异有统计学意义。
陈晖(广西壮族自治区江滨医院 530021)【中图分类号】R445.11【文献标识码】A【文章编号】1672-5085(2012)15-0129-01 【摘要】目的观察复溶后冰冻保存冻干质控血清对甲状腺激素测定结果的影响。
方法冻干质控血清复溶后,一部分即检测甲状腺激素,其余用离心管分装冰冻保存。
12周之后取出分装冰冻的质控血清复溶后检测甲状腺激素,统计两组数据,并分析结果。
结果冰冻前与冰冻后两组甲状腺激素数据比较无统计学意义(P>0.05)。
结论复溶后冻干质控血清冰冻保存对甲状腺激素测定尚有较好的稳定性。
【关键词】冻干质控血清冷冻保存甲状腺激素稳定性室内质量控制是临床实验室检验结果准确性的重要保证,是确定常规检测结果是否可靠、能否发出报告的依据。
质控血清是用来监测和评价实验室日常工作精密度和准确度的生物制品,而选择质量保证、使用方便的质控品,是实验室工作人员首先遇到的问题。
目前,国内大部分医院检验科使用的质控物均为进口冻干质控血清,价格比较昂贵,质控成本较高。
为此叶章发等[1]、郑希林等[2]、曾宇娟等[3]对冻干质控血清、液体质控血清复溶小包装冷冻保存后,观察不同保存期生化结果的稳定性,但对冻干质控血清免疫学方法测定结果的影响少有文献报道。
本文通过对冻干质控血清复溶后进行分装,然后冰冻保存,在冰冻保存前和冰冻保存后分别检测总三碘甲状腺原氨酸(TT3)、游离三碘甲状腺原氨酸(FT3)、总甲状腺素(TT4)、游离甲状腺素(FT4),以观察复溶后冰冻保存冻干质控血清对甲状腺激素测定结果的稳定性。
1 材料与方法 1.1 冻干质控血清英国朗道(RANDOX)公司生产的定值人基质多项免疫质控血清水平1 (批号为 740EC) 和水平3 (批号为 797EC)。

质控血清货号:HN1530 批号:887UN 包装:20×5ml 效期:1/2018准确量取5ml蒸馏水,小心复溶一瓶冻干质控血清。
注释:®:注册商标(1). 只适用于德国。
根据德国内科医生联邦议院的方针制订范围(中文说明已略,如需请另行参见英文说明)。
(2). 德国内科医生联邦议院官方认可的参考实验室测定的浓度值。
(3). DGKC:德国临床化学协会(4). IFCC:国际临床化学联盟(5). SCE:斯堪的纳维亚酶委员会使用说明本品为质控血清,又称人定值多项生化质控血清,为冻干品,用于临床准确性或者重复性质量控制。
朗道供应2种水平的质控血清。
赋值每一批质控血清都要送到参考实验室,根据国际参考标准进行赋值。
若没有国际参考标准,就使用参考方法。
朗道也将质控血清送到全世界3000多家实验室,然后将结果用相同的统计分析赋值。
质控范围值是平均值±2S.D.。
该结果非常准确可靠,实验室尽可放心使用。
准备1. 小心打开瓶盖,避免内容物的任何损失。
2. 在20-25℃的室温下,准确量取5ml蒸馏水复溶1瓶质控血清。
3. 盖上橡皮塞,拧紧瓶盖,使用前避光放置30分钟。
4. 轻轻旋转,确保内容物完全溶解。
5. 将小瓶倒置,确保所有的冻干物完全溶解。
6. 勿摇晃小瓶。
复溶后的血清既可以用于手工测试,也可以用于全自动生化分析仪。
该血清只能按照上述步骤复溶。
稳定性该血清自生产之日起,在4℃下保存可以稳定4年。
效期标在试剂盒的侧面。
该血清一旦复溶,在25℃下可以稳定24小时,在4℃下可以稳定7天,在-20℃至少可以稳定1个月(见受限情况)。
受限情况1、对于总酸性磷酸酶和前列腺酸性磷酸酶及醛缩酶来说,该血清每1ml应当加入1滴(25-30 l)0.7M的醋酸溶液。
其稳定作用可以使总和酸性磷酸酶在25℃下至少可以稳定2小时,在4℃下至少可以稳定2天,在-20℃下至少可以稳定1个月(只能冻融1次)。

定值多项质控血清适用范围:该产品与本公司生产的试剂盒配套使用,用于临床实验室内部的质量控制。
本产品所含项目为:白蛋白、总蛋白、胆汁酸、直接胆红素、总胆红素、肌酐、葡萄糖、尿素、尿酸、总胆固醇、甘油三酯、碱性磷酸酶、γ-谷氨酰转肽酶、胆碱酯酶、谷丙转氨酶、谷草转氨酶、肌酸激酶、α-羟丁酸脱氢酶、乳酸脱氢酶、α-淀粉酶、二氧化碳、钙、磷、镁、锌、铁。
1.1 包装规格见表1表1 包装规格1.2主要组成成分以人血清为基质的由正常/水平I与异常/水平II组成的冻干质控品。
主要组成见表2(其中水平I中各控制成分的浓度和活性通常在正常或参考值范围内,水平II中各控制成分的浓度和活性通常在病理或医学决定性水平范围内。
)表2主要组成成分注:不同批号质控品赋值有差异2.1 外观外包装盒应平整、无破损、文字和标识清晰;质控品为冻干粉,应密封、无泄漏;质控品复溶后应为黄色澄清透明液体,目测不得有沉淀及絮状悬浮物。
2.2 含水量冻干物水分含量:<5%。
2.3 赋值有效性测试待检质控品各个项目,测试结果均应落在标示值范围内。
2.4 瓶间精密度各项目的瓶间精密度不大于3%(其中天门冬氨酸氨基转移酶不大于5%;二氧化碳不大于5%;无机磷不大于8%)。
2.5 稳定性2.5.1 复溶稳定性复溶后质控品在2℃~8℃密封保存8h),复溶后质控品在2℃~8℃保存7天(CO2在生化分析仪上同时测试保存期末的质控品和新鲜的质控品,测试结果间的相对偏差不大于5%(其中总胆汁酸不大于3%;肌酐不大于4%;碱性磷酸酶不大于8%;锌不大于10%。
二氧化碳复溶后质控品在2℃~8℃密封保存8 h,在生化分析仪上同时测试保存期末的质控品和新鲜的质控品两个浓度水平,测试结果应不大于20%。
总胆红素、直接胆红素具有光敏性,建议血清避光保存,复溶后尽快使用。
)。
2.5.2 实时稳定性质控品在2℃~8℃储存条件下可保存36个月,在保存期末,同时测试到效期的质控品和-20℃保存的同批号质控品,测试结果间的相对偏差要求见下表。

AST检验原理试剂以国际临床化学联合会(IFCC)推荐⽅法为基础1样本中的AST催化L-天冬氨酸和a-氧化戌⼆酸氨基转换,⽣成草酰⼄酸和L-⾕氨酸2在NADH和苹果酸脱氢酶(MDH)存在下,草酰⼄酸被还原为L-苹果酸,NADH被氧化为NAD+,从⽽使340nm处的光吸收值下降。
通过监测340nm处光吸收值下降的速率,可以测定AST活⼒3样本中内源性丙酮酸的⼲扰可由试剂中LDH快速、完全地消除,不会对测定产⽣⼲扰。
临床意义AST⼴泛分布于⼈体各组织。
为细胞内酶,主要分布于细胞质及线粒体体机基质中。
在⼼、肝、⾻骼肌、肾和红细胞内有较⾼的浓度。
⾎清中酶活⼒最低。
红细胞中酶活⼒约为⾎清中得10倍,故轻度溶⾎对⾎清酶活性测定有⼀定影响。
这些组织的损伤或疾病,如⼼肌梗塞、病毒性肝炎、肝坏死、肝硬化和肌营养不良等症时,酶即从细胞内释放进⼊⾎液⽽引起⾎清或⾎浆中AST⽔平的升⾼。
储存条件及有效期在2-8℃避光、密封的储存条件下,试剂盒⾃⽣产之⽇起有效期为26个⽉。
样本要求1⾎清或⾎浆样本均不应溶⾎。
⾎浆样本只能采⽤肝素或EDTA抗凝。
2样本在2~8℃可稳定7天。
检验⽅法1试剂配制:在室温中,按照瓶签上标定的体积定量加⼊新鲜去离⼦⽔或蒸馏⽔,轻轻混匀⾄试剂完全溶解。
2测定条件:温度37°C 波长340nm 测定模式:速率法反应⽅向:吸光度下降的反应校准模式:两点定标注:两点定标:其中⼀点为实验⽤⽔,另⼀点为校准品3校准程序①校准品:复星长征临床化学校准⾎清为本试剂配套使⽤的校准品。
复星长征临床化学校准⾎清是以⼈与⼈源性物质为基础的含有26个不同组分、29个不同⽅法学定标值(校准浓度)的冻⼲校准⾎清。
临床化学校准⾎清中AST活性的计量学溯源性与校准浓度见相应批号临床化学校准⾎清的说明书。
②校准及校准频次的要求:正常情况下,应每周⾄少对测定进⾏⼀次校准。
当发⽣下列情况(试剂批号改变时、配套使⽤的仪器进⾏维修、保养或关键部件进⾏更换后、质控品的测定结果发⽣偏移或超出规定的范围等)应重新对测定进⾏校准后,再对患者样本进⾏检测。

室内质控评价指标依据室内质控评价指标主要依据以下几个方面:1.质控品的选择:质控品应当选用与人血清基质相同、分析物含量均匀的、瓶间变异小的、有明确靶值和允许范围的、稳定性好的质控品。
质控品的浓度应反映分析项目的决定水平,如医学决定水平、正常值参考范围的上下限值、临床治疗范围值、危急值等。
2.质控品的使用与保存:严格按质控品说明书操作和保存,不使用超过保质期的质控品;冻干质控品的复溶确保所用溶剂的质量和所加溶剂的量的准确性,复溶时应轻轻摇匀,使内容物完全溶解,切忌剧烈振摇,防止泡沫产生,复溶时间不得少于20分钟;质控品要在与患者标本同样测定条件下进行测定;每天至少做两水平以上质控品。
3.室内质控图的绘制:均数质控图:反映测定结果的精密度,用于判断日常测定结果是否在一致的精密度范围内。
该图的绘制,先求出质控血清在某一项目各天测定结果的均数和标准差,再计算均数±2s、均数±3s作为上、下警告线和失控线。
然后将各天测定的质控值点画在图上。
其中,超过上、下警告线的为警告,表示该测定批次的精密度较差;超过失控线的为失控,表示该测定结果已不可信,必须采取相应措施。
标准差质控图:反映测定结果的精密度是否随时间或不同批次而变化。
绘制时先求出某一项目各天测定结果的均数和标准差,以标准差为纵坐标绘制。
若各天的标准差落在±1s范围内,表示精密度良好;落在±2s范围内为警告;落在±3s范围为失控。
4.失控情况处理及原因分析:失控情况发生后应立即重测同一质控品(包括重新配制质控品),如结果在控则可判定前次测定中有随机误差,可继续测定患者标本。
如结果仍失控则应考虑存在系统误差,此时可采取下述措施:新开一瓶质控品,重测失控项目;新开另一批质控品,重测失控项目;进行仪器维护,重测失控项目;请专家帮助解决失控问题;重新校准,重测失控项目;认为有必要时,可更换试剂后重测失控项目。
失控原因的分析包括:试剂因素如更换试剂批号后未进行校准或试剂变质等;仪器因素如光源灯老化、滤光片老化、比色杯污染等;标准品因素如标准品损坏或丢失后未及时校准等;水质因素如去离子水不符合要求或蒸馏水被污染等;人为因素如操作不规范、加样错误等;环境因素如电压不稳、室温过高或过低等。
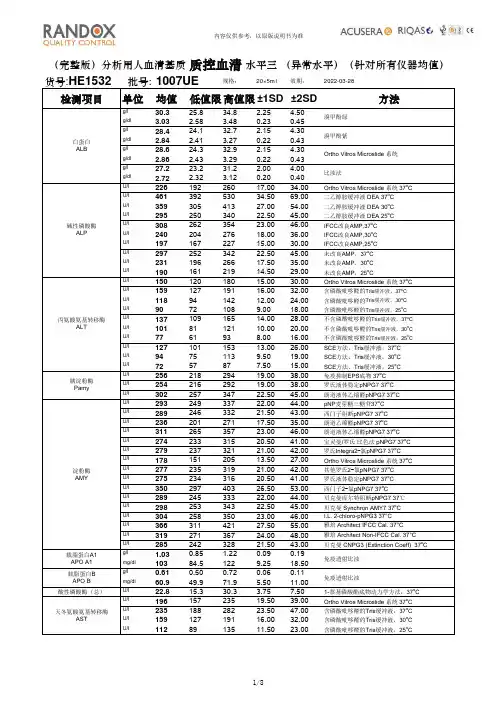
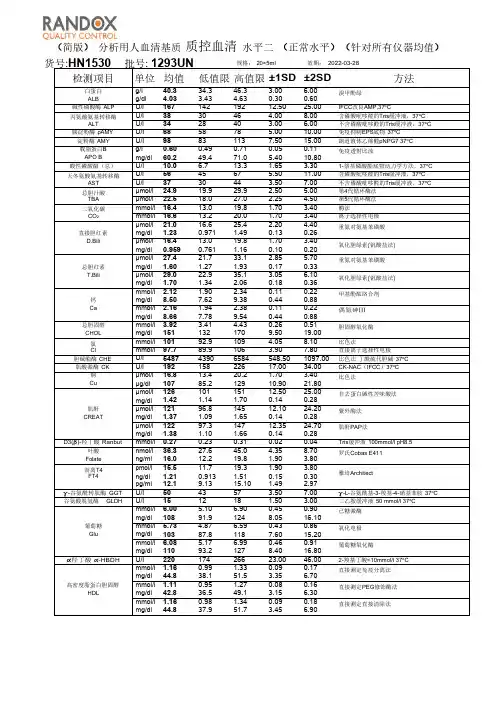
检测项目单位均值低值限高值限±1SD ±2SD方法白蛋白g/l 40.334.346.3 3.00 6.00溴甲酚绿ALBg/dl 4.03 3.43 4.630.300.60碱性磷酸酶ALP U/l 16714219212.5025.00IFCC 改良AMP,37o C丙氨酸氨基转移酶ALTU/l 383046 4.008.00含磷酸吡哆醛的Tris 缓冲液,37o C U/l 342840 3.00 6.00不含磷酸吡哆醛的Tris 缓冲液,37o C 胰淀粉酶pAMY U/I 685878 5.0010.00免疫抑制EPS 底物37o C淀粉酶AMY U/I 98831137.5015.00朗道液体乙缩醛pNPG737o C 载脂蛋白B g/l 0.600.490.710.050.11免疫透射比浊APO Bmg/dl 60.249.471.0 5.4010.80酸性磷酸酶(总)U/I 10.0 6.713.3 1.65 3.301-萘基磷酸酯底物动力学方法,37o C 天冬氨酸氨基转移酶ASTU/l 564567 5.5011.00含磷酸吡哆醛的Tris 缓冲液,37o C U/l 373044 3.507.00不含磷酸吡哆醛的Tris 缓冲液,37o C 总胆汁酸TBA μmol/l 24.919.929.9 2.50 5.00第4代循环酶法μmol/l 22.518.027.0 2.25 4.50第5代循环酶法二氧化碳CO 2mmol/l 16.413.019.8 1.70 3.40酶法mmol/l 16.613.220.0 1.70 3.40离子选择性电极μmol/l 21.016.625.4 2.20 4.40重氮对氨基苯磺酸直接胆红素mg/dl 1.230.971 1.490.130.26D.Biliμmol/l 16.413.019.8 1.70 3.40氧化胆绿素(钒酸盐法)mg/dl 0.9590.761 1.160.100.20μmol/l 27.421.733.1 2.85 5.70重氮对氨基苯磺酸总胆红素mg/dl 1.60 1.27 1.930.170.33T.Biliμmol/l 29.022.935.1 3.05 6.10氧化胆绿素(钒酸盐法)mg/dl 1.70 1.34 2.060.180.36mmol/l 2.12 1.90 2.340.110.22甲基酚酞络合剂钙mg/dl 8.507.629.380.440.88Ca mmol/l 2.16 1.94 2.380.110.22偶氮砷Ⅲmg/dl 8.667.789.540.440.88总胆固醇mmol/l 3.92 3.41 4.430.260.51胆固醇氧化酶CHOL mg/dl 1511321709.5019.00氯Clmmol/l 10192.9109 4.058.10比色法mmol/l 97.789.9106 3.907.80直接离子选择性电极胆碱酯酶CHE U/l 548743906584548.501097.00比色法丁酰硫代胆碱37o C 肌酸激酶CKU/l 19215822617.0034.00CK-NAC (IFCC )37o C 铜μmol/l 16.813.420.2 1.70 3.40比色法Cuμg/dl 10785.212910.9021.80μmol/l 12610115112.5025.00非去蛋白碱性苦味酸法mg/dl 1.42 1.14 1.700.140.28肌酐μmol/l 12196.814512.1024.20紫外酶法CREATmg/dl 1.37 1.09 1.650.140.28μmol/l 12297.314712.3524.70肌酐PAP 法mg/dl 1.38 1.10 1.660.140.28D3(β)-羟丁酸Ranbutmmol/l 0.270.230.310.020.04Tris 缓冲液100mmol/l pH8.5叶酸nmol/l 36.327.645.0 4.358.70罗氏Cobas E411Folateng/ml 16.012.219.8 1.90 3.80游离T4FT4pmol/l ng/dl pg/ml 15.51.2112.111.70.9139.1319.31.5115.10 1.900.151.49 3.800.302.97雅培Architectγ-谷氨酰转肽酶GGT U/I 504357 3.507.00γ-L-谷氨酰基-3-羧基-4-硝基苯胺37o C 谷氨酸脱氢酶GLDHU/I 151218 1.50 3.00三乙胺缓冲液50mmol/l 37o C mmol/l 6.00 5.10 6.900.450.90已糖激酶mg/dl 10891.91248.0516.10葡萄糖mmol/l 5.73 4.87 6.590.430.86氧化电极Glumg/dl 10387.81187.6015.20mmol/l 6.08 5.17 6.990.460.91葡萄糖氧化酶mg/dl 11093.21278.4016.80α羟丁酸α-HBDHU/I 22017426623.0046.002-羧基丁酸<10mmol/l 37o C mmol/l 1.160.99 1.330.090.17直接测定免疫分离法mg/dl 44.838.151.5 3.35 6.70高密度脂蛋白胆固醇mmol/l 1.110.95 1.270.080.16直接测定PEG 修饰酶法HDLmg/dl 42.836.549.1 3.15 6.30mmol/l 1.160.98 1.340.090.18直接测定直接清除法mg/dl 44.837.951.7 3.45 6.90TIPS :各位老师:RANDOX 人血清基质质控血清HN1530(正常值)和HE1532(异常值)针对不同厂家的生化分析仪和不同的分析方法给出了不同的靶值,篇幅所限如果在本靶值单中未能找到您需要的数据,您也可以联系您的产品供应商或公司本部,我们将竭诚为您服务。

质控血清靶值说明书【产品名称】通用名称:质控血清英文名称:Assayed Human Multi-sera【包装规格】货号:HEl532规格:20×5 ml批次:909UE效期:2021-01-28【预期用途】该类质控血清可用在多种型号的全自动生化分析仪上对临床化学分析项目进行准确度的评价。
【检验原理】质控血清分为两个水平,水平2和水平3。
我们为所列分析物提供两个水平范围的靶值和参考范围。
该产品为水平3。
【主要组成成份】试剂成分:人血清基质【储存条件及有效期】1.试剂的稳定性开封:冷冻贮存( 2-8℃)。
复溶血清25℃稳定8小时,4℃稳定7天,-20℃冻时至少稳定1个月(见局限性)。
未开封:冷冻贮存( 2-8℃)。
每个独立试剂瓶都可稳定保存到有效期。
2.有效期:四年【适合机型】雅培AEROSET®、Bayer ADVIA l650®、雅培Architect c8000/ei8200®、BAYER RA500/1000/2000/XT/OPERA®、Bayer Ciba 550 Express®、COBAS INTEGRA®、COBAS MIRA®、DADE DIMENSION®、HITACHI SERIES®、JOHNSON AND JOHNSON VITROS®、Konelab 20/30/60®、OLYMPUS AU400/500/600/800®、SYNCHRON CX4/5/7/9/LX20、VITALAB SELECTRA®等全自动生化分析仪。
【检验方法】质控血清处于冻干状态。
1. 在20℃至25℃,使用5 m1蒸馏水将每瓶冻干血清复溶。
密封使用前静置30分钟。
轻微搅动使内容物完全溶解。
避免形成泡沫。
不可摇动。
2. 参考独立分析仪实际应用的质控范围。
质控血清靶值说明书货号:HN1530 规格:20 x 5ml批号:1255UN 效期:2021-10-28【预期用途】该类质控血清可用在多种型号的全自动生化分析仪上对临床化学分析项目进行质量控制的评价。
【检验原理】质控血清分为两个水平,水平 2 和水平 3。
我们为所列分析物提供两个水平范围的靶值和参考范围。
该产品为水平 2。
【主要组成成份】试剂成分:人血清基质【储存条件及有效期】1. 试剂的稳定性开封:冷冻贮存( 2-8℃)。
复溶血清 25℃稳定 8 小时,4℃稳定 7 天,-20℃冻时至少稳定1 个月(见局限性)。
未开封:冷冻贮存( 2-8℃)。
每个独立试剂瓶都可稳定保存到有效期。
2. 有效期:四年。
【适合机型】雅培AEROSET®、Bayer ADVIA l650®、雅培Architect c8000/ei8200®、BAYERRA500/1000/2000/XT/OPERA®、Bayer Ciba 550 Express®、COBAS INTEGRA®、COBAS MIRA®、DADE DIMENSION®、HITACHI SERIES®、JOHNSON AND JOHNSON VITROS®、Konelab 20/30/60®、OLYMPUS AU400/500/600/800®、SYNCHRON CX4/5/7/9/LX20、VITALAB SELECTRA®等全自动生化分析仪。
【检验方法】质控血清处于冻干状态。
1. 在 20℃至 25℃,使用 5 m1 蒸馏水将每瓶冻干血清复溶。
密封使用前静置 30 分钟。
轻微搅动使内容物完全溶解。
避免形成泡沫。
不可摇动。
2. 参考独立分析仪实际应用的质控范围。
3. 冷冻任一未使用的原料。
重新使用前,将内容物完全混合。
【所需未提供的产品】容量吸管【赋值】提交给参考实验室的每批实验用人体血清根据国际参考标准进行赋值。
氨/乙醇质控水平1 : 包装规格 6 x 2 ml : 分类。
编号 EA1366氨/乙醇质控水平2 : 包装规格 6 x 2 ml : 分类。
编号 EA1367氨/乙醇质控水平3 : 包装规格 6 x 2 ml : 分类。
编号 EA1368水平分析物 1 2 3 单位氨 6.9 187 372 μmol/l乙醇0.55 1.55 2.73 g/l高值胆红素质控特征•l 总胆红素靶值接近290 μmol/l•用于监测儿科医学的胆红素水平•冻干品,稳定性强。
•牛基质•根据不同方法提供靶值和范围稳定性•未复溶+2 - 8°C 可稳定至有效期末•复溶后+2 - 8°C可稳定5天特征产品说明高值胆红素质控品 : 包装规格 10 x 3 ml : 分类。
货号BE454甘油质控品特征•冻干品,稳定性强•人基质产品稳定性•未复溶+2 - 8°C可稳定至有效期末•复溶后25°C时可稳定8小时,+2 - 8°C 可稳定7天,-20°C可稳定1个月产品说明甘油质控水平1 : 包装规格 3 x 5 ml : 分类。
货号 .GY1369葡萄糖-6-磷酸脱氢酶质控品特征•冻干品,稳定性强•人基质全血稳定性•+2 - 8°C 可稳定至有效期末•复溶后+2 - 8°C 可稳定5天产品说明葡萄糖-6-磷酸脱氢酶低含量质控品 : 包装规格 6 x 0.5 ml : 分类。
货号 .PD2617 葡萄糖-6-磷酸脱氢酶正常值质控品 : 包装规格 6 x 0.5 ml : 分类。
货号 .PD2618 脑脊液质控特征•包含10个分析物•冻干品,稳定性强•100%全人基质无动物添加成分•适用于大多数的临床分析仪•为常用仪器和方法提供靶值和参考范围稳定性•+2 - 8°C 稳定至有效期末•复溶后在+2 - 8°C可稳定5天,-20°C可稳定1个月。
质控血清靶值说明书【产品名称】通用名称:质控血清英文名称:Assayed Human Multi-sera【包装规格】货号:HNl530规格:20×5 ml批次:1282UN效期:2022-01-28【预期用途】该类质控血清可用在多种型号的全自动生化分析仪上对临床化学分析项目进行质量控制的评价。
【检验原理】质控血清分为两个水平,水平2和水平3。
我们为所列分析物提供两个水平范围的靶值和参考范围。
该产品为水平2。
【主要组成成份】试剂成分:人血清基质【储存条件及有效期】1. 试剂的稳定性开封:冷冻贮存( 2-8℃)。
复溶血清25℃稳定 8 小时,4℃稳定 7 天,-20℃冻时至少稳定 1 个月(见局限性)。
未开封:冷冻贮存( 2-8℃)。
每个独立试剂瓶都可稳定保存到有效期。
2. 有效期:四年。
【适合机型】雅培AEROSET®、Bayer ADVIA l650®、雅培Architect c8000/ei8200®、BAYER RA500/1000/2000/XT/OPERA®、Bayer Ciba 550 Express®、COBAS INTEGRA®、COBAS MIRA®、DADE DIMENSION®、HITACHI SERIES®、JOHNSON AND JOHNSON VITROS®、Konelab20/30/60®、OLYMPUS AU400/500/600/800®、SYNCHRON CX4/5/7/9/LX20、VITALAB SELECTRA®等全自动生化分析仪。
【检验方法】质控血清处于冻干状态。
1.在20℃至25℃,使用5 m1蒸馏水将每瓶冻干血清复溶。
密封使用前静置30分钟。
轻微搅动使内容物完全溶解。
避免形成泡沫。
不可摇动。
2.参考独立分析仪实际应用的质控范围。
R A N D X免疫分析专用质控品货号: IAS3114 包装: 5 x 2 ml批号: 1522EC 效期: 2017-04产品描述本品为免疫分析专用质控品,又称免疫特殊质控І,适用于临床化学体外诊断的免疫质控,用于监测免疫测定的正确度或重复度。
朗道供应3个浓度水平(水平1:IAS3113;水平2:IAS3114;水平3:IAS3115)。
安全预防措施和警告本产品仅用于体外诊断。
禁止用口吸。
按照实验室常规预防措施对试剂进行处理。
该质控品采用人基质血清,对所有捐献者的血清均进行了HIV(HIV1、HIV2)抗体、肝炎B表面抗原(HbsAg)和肝炎C病毒(HCV)抗体的测试,发现均呈阴性。
所采用的方法均经FDA认证。
然而,既然没有一种方法能够完全保证其没有传染物质,因此该质控品和所有的病人样品均应当按照能够传播疾病的样品小心处理。
保存和稳定性开瓶后,2~8℃保存。
复溶后的血清如果保存在原始容器,并且无污染,可在2~8℃保存5天,-20℃冷冻保存4周,只能冻融一次。
抗甲状腺球蛋白(Anti-TG)在2~8℃可稳定3天,C肽、类胰岛素一号增长因子(IGF-1)、降钙素原(PCT)在2~8℃可稳定1天,骨钙素在2~8℃可稳定4小时。
甲状旁腺素(PTH)复溶后如果2~8℃保存,要在4小时内检测;若-20℃以下保存,则须在2周内检测。
每次使用只吸取所需用量,剩余的样品不可返回原瓶。
未开瓶,2~8 ℃可保存至效期末。
复溶后的血清在受到细菌污染后,会导致许多组分稳定性的下降, 应该将该瓶样品抛弃,重新复溶一瓶新的血清。
使用说明该免疫分析专用质控品Ⅰ为冻干粉。
1.小心打开瓶盖,往瓶中加入2 ml蒸馏水,在15~25 ℃的条件下复溶,盖上瓶盖,放置30分钟。
轻轻翻转瓶子,确保内容物完全溶解,不要振荡,避免气泡的产生。
2.参照各个分析仪的质控说明。
3.冷藏未使用的材料,再次使用前,确保样品充分混合均匀。
需要自备的材料移液管,蒸馏水赋值每一批质控血清都要送到大量的参考实验室,这些实验室通过独特的统计分析方法得到一个结果进行赋值。